
ONDANSETRON KALCEKS 2mg/ml SOLUÇÃO INJETÁVEL E SOLUÇÃO PARA PERFUSÃO
Pergunte a um médico sobre a prescrição de ONDANSETRON KALCEKS 2mg/ml SOLUÇÃO INJETÁVEL E SOLUÇÃO PARA PERFUSÃO

Como usar ONDANSETRON KALCEKS 2mg/ml SOLUÇÃO INJETÁVEL E SOLUÇÃO PARA PERFUSÃO
Introdução
Prospecto: informação para o utilizador
Ondansetrón Kalceks 2mg/ml solução injectável e para perfusão EFG
Leia todo o prospecto atentamente antes de começar a usar este medicamento, porque contém informações importantes para si.
- Conserva este prospecto, porque pode ter que voltar a lê-lo.
- Se tiver alguma dúvida, consulte o seu médico, farmacêutico ou enfermeiro.
- Este medicamento foi prescrito apenas para si, e não deve dá-lo a outras pessoas, mesmo que tenham os mesmos sintomas que si, porque pode prejudicá-las.
- Se experimentar efeitos adversos, consulte o seu médico, farmacêutico ou enfermeiro, mesmo que se trate de efeitos adversos que não aparecem neste prospecto. Ver secção 4.
Conteúdo do prospecto
- O que é Ondansetrón Kalceks e para que é utilizado
- O que necessita saber antes de que lhe administrem Ondansetrón Kalceks
- Como usar Ondansetrón Kalceks
- Possíveis efeitos adversos
- Conservação de Ondansetrón Kalceks
- Conteúdo do envase e informação adicional
1. O que é Ondansetrón Kalceks e para que é utilizado
Ondansetrón Kalceks contém um fármaco chamado ondansetrón. Este pertence a um grupo de medicamentos denominados antieméticos que aliviam as náuseas e os vómitos.
Adultos
O ondansetrón é usado para o tratamento de náuseas e vómitos causados pela quimioterapia e pela radioterapia e para a prevenção e o tratamento das náuseas e vómitos pós-operatórios.
Crianças e adolescentes
O ondansetrón é usado para o tratamento de náuseas e vómitos causados pela quimioterapia em crianças maiores de 6 meses e em adolescentes.
O ondansetrón é usado para prevenir e tratar as náuseas e os vómitos posteriores a uma intervenção cirúrgica em crianças maiores de 1 mês de idade e em adolescentes.
2. O que necessita saber antes de que lhe administrem Ondansetrón Kalceks
Não lhe devem administrar Ondansetrón Kalceks se:
- é alérgico ao ondansetrón ou a algum dos outros componentes deste medicamento (incluídos na secção 6);
- está a usar apomorfina (para tratar a doença de Parkinson).
Não devem administrar-lhe este medicamento se alguma das condições acima for aplicável a si. Se não tiver a certeza, consulte o seu médico ou enfermeiro antes de que lhe administrem este medicamento.
Advertências e precauções
Consulte o seu médico ou enfermeiro antes de que lhe administrem este medicamento se:
- tiver sintomas de reação alérgica, como picazón, dificuldade para respirar ou inchação da face, lábios, garganta ou língua;
- alguma vez foi alérgico a outros medicamentos para as náuseas e os vómitos (por exemplo, granisetrona ou palonosetrona);
- tiver problemas cardíacos; podem ocorrer alterações temporárias no electrocardiograma (ECG);
- utilizar medicamentos para tratar os distúrbios do ritmo cardíaco (antiarrítmicos) ou medicamentos que reduzem a pressão arterial e a frequência cardíaca em repouso (betabloqueantes);
- está constipado ou tem uma doença intestinal que pode provocar constipação;
- tiver problemas hepáticos ou usar algum medicamento que possa ser prejudicial para o fígado (medicamentos de quimioterapia hepatotóxicos). Nesses casos, será monitorizado de perto como funciona o fígado, especialmente em crianças e adolescentes;
- fez uma análise de sangue para verificar os valores hepáticos (o ondansetrón pode afetar os resultados);
- tiver alterações com os níveis de sais no sangue, como o potássio e o magnésio;
- vai ser submetido a uma operação de amígdalas. Nesse caso, deve ser monitorizado cuidadosamente.
Se não tiver a certeza de que alguma das condições acima for aplicável a si, consulte o seu médico ou enfermeiro antes de usar este medicamento.
Outros medicamentos e Ondansetrón Kalceks
Informa o seu médico ou enfermeiro se está a usar, usou recentemente ou possa ter que usar qualquer outro medicamento.
Em particular, informa o seu médico ou enfermeiro se está a tomar algum dos seguintes medicamentos:
- apomorfina (ver Não lhe devem administrar Ondansetrón Kalceks);
- carbamazepina ou fenitoína (usados para tratar a epilepsia);
- rifampicina (usada para tratar as infecções como a tuberculose);
- tramadol (analgésico);
- medicamentos usados para tratar a depressão e/ou a ansiedade:
- ISRS (inibidores seletivos da recaptação de serotonina), como a fluoxetina, paroxetina, sertralina, fluvoxamina, citalopram, escitalopram;
- IRSN (inibidores da recaptação de serotonina e noradrenalina) como a venlafaxina ou a duloxetina.
Quando é administrado juntamente com medicamentos para certas doenças cardíacas, podem ocorrer alterações no seu electrocardiograma (ECG). O uso simultâneo de medicamentos que danificam o coração (por exemplo, antraciclinas (como a doxorrubicina, daunorrubicina) ou trastuzumab), antibióticos (como a eritromicina), antifúngicos (como o cetoconazol), antiarrítmicos (como a amiodarona) e betabloqueantes (como a atenolol ou timolol)) pode aumentar o risco de distúrbios do ritmo cardíaco.
Gravidez, lactação e fertilidade
Se está grávida ou em período de lactação, acredita que possa estar grávida ou tem intenção de engravidar, consulte o seu médico antes de usar este medicamento.
Gravidez
Não deve usar este medicamento durante o primeiro trimestre da gravidez. Isto deve-se a que este medicamento pode aumentar ligeiramente o risco de que um bebê nasça com lábio leporino e/ou palato fendido (aberturas ou fendas no lábio superior e/ou no palato). Se já está grávida, acredita que possa estar grávida ou tem intenção de engravidar, consulte o seu médico ou farmacêutico antes de usar este medicamento.
Mulheres com possibilidade de engravidar
Se é uma mulher em idade fértil, será aconselhada a usar contraceptivos seguros.
Lactação
A lactação deve ser interrompida antes do tratamento com o ondansetrón.
Fertilidade
O ondansetrón não tem efeito algum sobre a fertilidade.
Condução e uso de máquinas
O ondansetrón tem muito pouca ou praticamente nenhuma influência sobre a capacidade para conduzir e utilizar máquinas.
Ondansetrón Kalceks contém sódio
Este medicamento contém 3,52 mg de sódio (componente principal do sal de mesa/para cozinhar) em cada ml de solução. Isto equivale a 0,18% da ingestão diária máxima de sódio recomendada para um adulto.
3. Como usar Ondansetrón Kalceks
O ondansetrón será administrado por um médico ou enfermeiro como injeção ou perfusão lentas em uma veia ou como injeção em um músculo.
O ondansetrón também está disponível em formas de dosificação adequadas para a administração oral, o que permite ajustar a dose de forma individual. No entanto, este medicamento está concebido para ser administrado apenas em uma veia ou em um músculo.
A dose que lhe foi prescrita dependerá do tratamento que está a seguir.
Adultos
Para prevenir as náuseas e os vómitos da quimioterapia ou da radioterapia
- No dia da quimioterapia ou da radioterapia
O ondansetrón deve ser administrado imediatamente antes da quimioterapia ou da radioterapia. A dose habitual em adultos é de 8 mg, administrada mediante injeção lenta em uma veia ou músculo, ou por perfusão lenta em uma veia.
- Nos dias seguintes
Depois do tratamento inicial, o seu médico pode prescrever-lhe o ondansetrón para que o tome por via oral. Siga as instruções do prospecto correspondente, conforme necessário. Tome sempre o ondansetrón exatamente como lhe foi indicado pelo seu médico.
Se necessário, a dose pode ser aumentada até 32 mg por dia.
Para prevenir e tratar as náuseas e os vómitos após uma operação
A dose habitual para adultos é de 4 mg, administrados mediante injeção lenta em uma veia ou músculo.
População pediátrica
Para prevenir as náuseas e os vómitos da quimioterapia em crianças de 6 meses e em adolescentes
Em crianças, este medicamento é administrado lentamente em uma veia (intravenoso), imediatamente antes da quimioterapia (dose recomendada: 5 mg/m2 ou 0,15 mg/kg). A dose intravenosa não deve exceder 8 mg. A dose oral pode ser iniciada 12 horas mais tarde. Este tratamento pode ser continuado durante um máximo de 5 dias após a quimioterapia. A dose oral é calculada com base no peso corporal ou na superfície corporal. A dose total diária não deve ultrapassar a dose de adultos de 32 mg.
Para prevenir e tratar as náuseas e os vómitos após uma operação em crianças a partir da idade de 1 mês e em adolescentes
Em crianças, a dose oral é calculada com base no peso corporal ou na superfície corporal. A dose total diária não deve ultrapassar a dose de adultos de 32 mg. A dose é administrada como injeção intravenosa lenta antes, durante ou após a indução da anestesia.
Pessoas idosas (maiores de 65 anos)
O ondansetrón é bem tolerado em pacientes com mais de 65 anos.
Náuseas e vómitos induzidos pela quimioterapia e pela radioterapia
Em pacientes de 65 anos ou mais, todas as doses intravenosas devem ser diluídas e administradas mediante perfusão durante 15 minutos. Se for necessário repetir as doses, estas devem ser administradas com um intervalo mínimo de 4 horas entre elas.
Em pacientes de 65 a 74 anos, a dose inicial é de 8 mg ou 16 mg. Em pacientes maiores de 75 anos, a dose inicial não deve ultrapassar 8 mg.
Para prevenir e tratar as náuseas e os vómitos após uma operação
Há pouca experiência em pessoas idosas.
Pacientes com problemas hepáticos
Em pacientes com problemas hepáticos moderados ou graves, a dose diária total não deve ultrapassar 8 mg.
Pacientes com problemas renais
Não é necessário ajustar a dose, a frequência da dose ou a via de administração.
Se receber mais Ondansetrón Kalceks do que deve
O seu médico ou enfermeiro serão os responsáveis por administrar este medicamento a si ou ao seu filho, por isso é pouco provável que si ou o seu filho recebam demasiada quantidade. Se acredita que si ou o seu filho receberam demasiado ou se esqueceram de uma dose, diga-o ao seu médico ou enfermeiro.
Podem ocorrer os seguintes sintomas: alterações visuais, constipação severa, pressão arterial baixa e batimentos cardíacos lentos.
Se tiver alguma outra dúvida sobre o uso deste medicamento, pergunte ao seu médico, farmacêutico ou enfermeiro.
4. Possíveis efeitos adversos
Como todos os medicamentos, este medicamento pode causar efeitos adversos, embora nem todas as pessoas os sofram.
O perfil de reações adversas em crianças e adolescentes é semelhante ao observado em adultos.
Reações alérgicas graves.Estas raramente ocorrem em pessoas que usam ondansetrón. As queixas incluem:
- Erupção cutânea elevada e com picazón (urticária)
- Inchação, às vezes da face ou da boca (angioedema) com dificuldade para respirar
- Perda breve de consciência
Entre em contacto com um médico imediatamente se experimentar algum destes sintomas. Interrompa o uso deste medicamento.
Efeitos adversosmuito frequentes(podem afetar mais de 1 de cada 10 doentes)
- Dor de cabeça
Efeitos adversos frequentes(podem afetar até 1 de cada 10 doentes)
- Sensação de calor ou rubor
- Constipação
- Sofocos
- Irritação no local da injeção (após a injeção em uma veia)
Efeitos secundários pouco frequentes(podem afetar até 1 de cada 100 doentes)
- Convulsões
- Movimentos musculares involuntários ou espasmos
- Batimentos irregulares ou lentos do coração
- Dor torácica
- Pressão arterial baixa
- Hipo
- Aumento das enzimas hepáticas
Efeitos adversos raros(podem afetar até 1 de cada 1.000 doentes)
- Alterações do ritmo cardíaco (que às vezes provocam uma perda repentina de consciência)
- Tontura
- Visão borrosa transitoria ou alterações visuais
Efeitos secundários muito raros(podem afetar até 1 de cada 10.000 doentes)
- Erupção generalizada com bolhas e descamação da pele em grande parte da superfície corporal (necrólise epidérmica tóxica)
- Perda transitoria da visão
Frequência não conhecida(não pode ser estimada a partir dos dados disponíveis)
- Secura da boca
- Isquemia miocárdica (os sinais incluem: dor repentina no peito ou opressão no peito)
Comunicação de efeitos adversos
Se experimentar algum tipo de efeito adverso, consulte o seu médico, farmacêutico ou enfermeiro, mesmo que se trate de possíveis efeitos adversos que não aparecem neste prospecto. Também pode comunicá-los directamente através do Sistema Español de Farmacovigilância de Medicamentos de Uso Humano: www.notificaRAM.es. Mediante a comunicação de efeitos adversos, você pode contribuir para fornecer mais informações sobre a segurança deste medicamento.
5. Conservação de Ondansetrón Kalceks
Mantenha este medicamento fora da vista e do alcance das crianças.
Este medicamento não requer nenhumatemperatura especial de conservação.
Conserva as ampolas no embalagem exterior para protegê-las da luz.
Depois de abrir a ampola
Use imediatamente após a abertura da ampola.
Período de validade após a diluição
A estabilidade química e física em uso foi demonstrada durante 7 dias a 25 °C e de 2 a 8 °C.
Do ponto de vista microbiológico, a solução diluída deve ser usada imediatamente. Se não for usada imediatamente, os tempos de armazenamento em uso e as condições prévias ao uso são responsabilidade do utilizador e normalmente não devem ser superiores a 24 horas a uma temperatura de 2 a 8 °C, a menos que a diluição tenha sido feita em condições assépticas controladas e validadas.
Não use este medicamento após a data de validade que aparece na etiqueta da ampola e na caixa após CAD. A data de validade é o último dia do mês que se indica.
Os medicamentos não devem ser jogados fora pelo esgoto ou na lixeira. Pergunte ao seu farmacêutico como se livrar dos medicamentos que já não precisa. Dessa forma, você ajudará a proteger o meio ambiente.
6. Conteúdo do envase e informação adicional
Composição de Ondansetrón Kalceks
? O princípio ativo é o ondansetrón.
Cada ml de solução contém ondansetrón hidrocloruro dihidrato, equivalente a 2 mg de ondansetrón.
Cada ampola com 2 ml de solução contém ondansetrón hidrocloruro dihidrato, equivalente a 4 mg de ondansetrón.
Cada ampola com 4 ml de solução contém ondansetrón hidrocloruro dihidrato, equivalente a 8 mg de ondansetrón.
? Os demais componentes são cloreto de sódio, ácido cítrico monohidrato, citrato sódico dihidrato, água para preparações injetáveis.
Aspecto do produto e conteúdo do envase
Solução transparente e incolor, sem partículas visíveis.
Volúmenes de 2 ml ou 4 ml de solução em ampolas de vidro transparentes com um ponto de corte.
As ampolas são colocadas em uma bandeja. As bandejas são envasadas em uma caixa de cartão.
Tamanhos de envases:
5, 10 ou 25 ampolas
Pode ser que apenas alguns tamanhos de envases sejam comercializados.
Título da autorização de comercializaçãoe responsável pela fabricação
AS KALCEKS
Krustpils iela 71E,
Riga, LV‑1057,
Letônia
Tel.: +371 67083320
E‑mail: [email protected]
Pode solicitar mais informações sobre este medicamento dirigindo-se ao representante local do título da autorização de comercialização
Grindeks Kalceks España, S.L.
c/ José Abascal, 58 2º dcha
28003 Madrid
Espanha
Este medicamento está autorizado nos estados membros do Espaço Econômico Europeu e no Reino Unido (Irlanda do Norte) com os seguintes nomes:
Letônia: Ondansetron Kalceks 2 mg/ml šķīdums injekcijām/infūzijām
Áustria, Bulgária, Croácia, República Checa, Dinamarca, Estônia, Finlândia, Alemanha, Hungria, Islândia, Lituânia, Noruega, Eslováquia, Suécia: Ondansetron Kalceks
Bélgica: Ondansetron Kalceks 2 mg/ml, solution injectable/pour perfusion
Ondansetron Kalceks 2 mg/ml, oplossing voor injectie/infusie
Ondansetron Kalceks 2 mg/ml, Injektions-/Infusionslösung
Grécia: ONDANSETRON/KALCEKS
Reino Unido (Irlanda do Norte), Irlanda: Ondansetron 2 mg/ml solution for injection/infusion
Itália: Ondansetrone Kalceks
Países Baixos: Ondansetron Kalceks 2 mg/ml, oplossing voor injectie/infusie
Polônia: ONDANSETRON KALCEKS
Romênia: Ondansetron Kalceks 2 mg/ml soluție injectabilă/perfuzabilă
Eslovênia: Ondansetron Kalceks 2 mg/ml raztopina za injiciranje/infundiranje
Espanha: Ondansetrón Kalceks 2 mg/ml solução injetável e para perfusão EFG
Data da última revisão deste prospecto: Fevereiro 2022.
A informação detalhada deste medicamento está disponível na página web da Agência Espanhola de Medicamentos e Produtos Sanitários (AEMPS) (http://www.aemps.gob.es/).
?------------------------------------------------------------------------------------------------------------------------
Esta informação está destinada unicamente a profissionais do setor sanitário:
Consulte a Ficha técnica ou Resumo das Características do Produto para obter mais detalhes sobre este medicamento.
Sobredosagem
Sintomas e sinais
A experiência de sobredosagem por ondansetrón é limitada, mas no caso de sobredosagem acidental podem ocorrer os seguintes sintomas de intoxicação: alterações visuais, constipação grave, hipotensão e um episódio vasovagal com bloqueio AV transitorio de segundo grau. Em todos os casos, as reações experimentadas se resolveram completamente. O ondansetrón prolonga o intervalo QT com uma tendência dose-dependente.
População pediátrica
Foram notificados casos em crianças com síndrome serotoninérgica após uma sobredosagem oral acidental de ondansetrón (ingestão excessiva estimada de 4 mg/kg) em lactentes e crianças de 12 meses a 2 anos.
Tratamento
Não há um antídoto específico para o ondansetrón, por isso, nos casos de suspeita de sobredosagem, será fornecido o tratamento sintomático e de suporte que for apropriado. Recomenda-se uma monitorização do ECG. Um tratamento adicional deve seguir as recomendações clínicas indicadas ou as recomendações do Instituto Nacional de Toxicologia, se estiverem disponíveis.
Não se recomenda a administração de ipecacuana para tratar a sobredosagem, pois não é provável que os pacientes respondam, devido à ação antiemética do próprio ondansetrón.
Incompatibilidades
Este medicamento não deve ser administrado na mesma seringa, ou no mesmo equipamento de perfusão que qualquer outro medicamento.
Este medicamento não deve ser misturado com outros, exceto com os mencionados a seguir.
Instruções de uso, eliminação e outras manipulações
Para uso único.
O medicamento deve ser inspecionado visualmente antes de seu uso. O medicamento não deve ser utilizado se apresentar sinais visíveis de deterioração (p. ex., partículas ou mudança de cor).
Este medicamento não deve ser esterilizado em autoclave.
Somente pode ser misturado com as seguintes soluções para perfusão intravenosa:
- solução de cloreto de sódio 9 mg/ml (0,9%);
- solução de glicose 50 mg/ml (5%);
- solução de manitol 100 mg/ml (10%);
- solução de Ringer;
- solução de cloreto potássico 3 mg/ml (0,3%) e de cloreto de sódio 9 mg/ml (0,9%);
- solução de cloreto potássico 3 mg/ml (0,3%) e de 50 mg/ml (5%);
- solução de Ringer lactada.
Este medicamento demonstrou ser compatível com seringas de polipropileno (PP), frascos de vidro tipo I, bolsas para perfusão de polietileno (PE), cloreto de polivinilo (PVC) e acetato de etilo e vinilo (EVA), assim como com tubos de PVC e PE quando está diluído com as soluções para infusão acima mencionadas. Foi observado que este medicamento é compatível com seringas de PP.
Compatibilidade com outros medicamentos
O ondansetrón pode ser administrado por perfusão intravenosa (a 1 mg/hora). Os seguintes medicamentos podem ser administrados por perfusão intravenosa através de um dispositivo em Y para concentrações de ondansetrón de 16 a 160 microgramas/ml (p. ex., 8 mg/500 ml e 8 mg/50 ml, respectivamente).
- Cisplatino
- 5-Fluorouracilo
- Carboplatino
- Etopósido
- Ceftazidima
- Ciclofosfamida
- Doxorrubicina
- Dexametasona
Instruções para a abertura da ampola
- Mantenha a ampola com o ponto de cor para cima. Se restar alguma solução na parte superior da ampola, bata suavemente com o dedo para que toda a solução desça para a parte inferior da ampola.
- Use ambas as mãos para abri-la e, enquanto segura a parte inferior da ampola com uma mão, use a outra para quebrar a parte superior da ampola em direção oposta ao ponto de cor (ver as imagens a seguir).
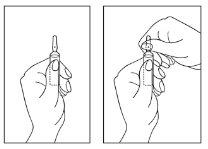
A eliminação do medicamento não utilizado e de todos os materiais que tenham estado em contato com ele será realizada de acordo com a normativa local.
- País de registo
- Substância ativa
- Requer receita médicaSim
- Fabricante
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a ONDANSETRON KALCEKS 2mg/ml SOLUÇÃO INJETÁVEL E SOLUÇÃO PARA PERFUSÃOForma farmacêutica: INJETÁVEL, 2 mg/mLSubstância ativa: ondansetronFabricante: Accord Healthcare S.L.U.Requer receita médicaForma farmacêutica: COMPRIMIDO ORODISPERSÍVEL / LIOTAB, 4 mgSubstância ativa: ondansetronFabricante: Aristo Pharma Iberia S.L.Requer receita médicaForma farmacêutica: COMPRIMIDO ORODISPERSÍVEL/LIOTAB, 8 mgSubstância ativa: ondansetronFabricante: Aristo Pharma Iberia S.L.Requer receita médica
Alternativas a ONDANSETRON KALCEKS 2mg/ml SOLUÇÃO INJETÁVEL E SOLUÇÃO PARA PERFUSÃO noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a ONDANSETRON KALCEKS 2mg/ml SOLUÇÃO INJETÁVEL E SOLUÇÃO PARA PERFUSÃO em Polónia
Alternativa a ONDANSETRON KALCEKS 2mg/ml SOLUÇÃO INJETÁVEL E SOLUÇÃO PARA PERFUSÃO em Ukraine
Médicos online para ONDANSETRON KALCEKS 2mg/ml SOLUÇÃO INJETÁVEL E SOLUÇÃO PARA PERFUSÃO
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de ONDANSETRON KALCEKS 2mg/ml SOLUÇÃO INJETÁVEL E SOLUÇÃO PARA PERFUSÃO – sujeita a avaliação médica e regras locais.














