OKEDI 75 mg pó e solvente para suspensão injetável de libertação prolongada

Pergunte a um médico sobre a prescrição de OKEDI 75 mg pó e solvente para suspensão injetável de libertação prolongada

Como usar OKEDI 75 mg pó e solvente para suspensão injetável de libertação prolongada
Introdução
Prospecto: informação para o utilizador
OKEDI 75 mg pó e solvente para suspensão injetável de libertação prolongada
risperidona
Leia todo o prospecto atentamente antes de começar a usar este medicamento, porque contém informações importantes para si.
- Conserva este prospecto, porque pode ter que voltar a lê-lo.
- Se tiver alguma dúvida, consulte o seu médico ou farmacêutico.
- Este medicamento foi prescrito apenas para si, e não deve dá-lo a outras pessoas, mesmo que tenham os mesmos sintomas que si, porque pode prejudicá-las.
- Se experimentar efeitos adversos, consulte o seu médico ou farmacêutico, mesmo que se trate de efeitos adversos que não aparecem neste prospecto. Ver secção 4.
Conteúdo do prospecto
- O que é OKEDI e para que é utilizado
- O que precisa saber antes de começar a usar OKEDI
- Como usar OKEDI
- Posíveis efeitos adversos
- Conservação de OKEDI
- Conteúdo do envase e informações adicionais
1. O que é OKEDI e para que é utilizado
OKEDI contém o princípio ativo risperidona, que pertence ao grupo de medicamentos denominados «antipsicóticos».
OKEDI é utilizado em pacientes adultos para tratar a esquizofrenia, um distúrbio no qual se podem ver, ouvir ou sentir coisas que não estão lá, acreditar coisas que não são verdadeiras ou sentir-se inusualmente desconfiado ou confundido.
OKEDI está indicado para pacientes que mostraram tolerabilidade e eficácia a risperidona oral (p. ex., comprimidos).
OKEDI pode ajudar a aliviar os sintomas da doença e evitar que reapareçam.
2. O que precisa saber antes de começar a usar OKEDI
Não use OKEDI:
- Se é alérgico (hipersensibilidade) a risperidona ou a algum dos outros componentes deste medicamento (incluídos na secção 6).
Advertências e precauções
Consulte o seu médico ou farmacêutico antes de começar a usar OKEDI se:
- Tém problemas de coração. Entre os exemplos incluem-se ritmo cardíaco irregular, se é propenso a ter tensão arterial baixa ou se utiliza medicamentos para a tensão arterial. OKEDI pode causar tensão arterial baixa. É possível que seja necessário ajustar a dose.
- Sabe que tem algum fator que o faria mais propenso a sofrer um acidente vascular cerebral, tal como tensão arterial alta, distúrbio cardiovascular ou problemas nos vasos sanguíneos do cérebro.
- Alguma vez apresentou movimentos involuntários da língua, boca e face.
- Alguma vez teve uma afecção cujos sintomas incluem temperatura alta, rigidez muscular, suor ou nível de consciência reduzido (também conhecido como síndrome neuroléptico maligno).
- Tém doença de Parkinson.
- Tém demência.
- Sabe que teve anteriormente concentrações baixas de glóbulos brancos (que pode ter sido causada por outros medicamentos ou não).
- É diabético.
- Tém epilepsia.
- É homem e alguma vez teve uma ereção prolongada ou dolorosa.
- Tém problemas para controlar a temperatura corporal ou sente um calor excessivo.
- Tém problemas renais.
- Tém problemas hepáticos.
- Tém uma concentração anormalmente elevada da hormona prolactina no sangue ou um tumor, que possivelmente dependa da prolactina.
- Si ou alguém da sua família tem antecedentes de coágulos sanguíneos, já que os antipsicóticos se têm associado à formação de coágulos sanguíneos.
Se não tem certeza de que as opções anteriores se aplicam ao seu caso, consulte o seu médico ou farmacêutico antes de começar a usar risperidona oral ou OKEDI.
Durante o tratamento
Com muito rara frequência nos pacientes que tomam risperidona se têm observado cifras perigosamente baixas de um tipo de glóbulo branco necessário para combater infecções no sangue. Por isso, é possível que o médico precise controlar os seus recuentos de glóbulos brancos antes e durante o tratamento.
Embora anteriormente tenha tolerado risperidona oral, em raras ocasiões se produzem reações alérgicas após receber injeções de OKEDI. Solicite assistência médica de imediato se tiver erupção, inchaço da garganta, picazón ou problemas respiratórios, já que podem ser sinais de uma reação alérgica grave.
OKEDI pode causar aumento de peso. O aumento de peso significativo pode afetar negativamente a saúde. O médico deve pesá-lo periodicamente.
Nos pacientes que utilizam OKEDI se tem observado diabetes mellitus ou o agravamento da diabetes mellitus preexistente. Por isso, o médico deve fazer controles para detectar sinais de níveis altos de açúcar no sangue. Nos pacientes com diabetes mellitus preexistente, se devem controlar periodicamente as concentrações de glicose no sangue.
OKEDI normalmente aumenta as concentrações de uma hormona denominada «prolactina». Isso pode causar efeitos adversos, tais como distúrbios menstruais ou problemas de fertilidade nas mulheres, e inflamação das mamas nos homens (ver secção 4, «Posíveis efeitos adversos»). Em caso de que se apresentem estes efeitos adversos, se recomenda avaliar a concentração de prolactina no sangue.
Durante uma cirurgia ocular por opacidade do cristalino (cataratas), podem surgir problemas que podem causar dano ocular. Se planeia realizar-se uma cirurgia ocular, certifique-se de avisar o seu oftalmologista de que está usando este medicamento.
Crianças e adolescentes
Não administre este medicamento a crianças e adolescentes menores de 18 anos.
Outros medicamentos e OKEDI
Informa o seu médico ou farmacêutico se está tomando, tomou recentemente ou pudesse ter que tomar qualquer outro medicamento.
É especialmente importante que fale com o seu médico ou farmacêutico se está tomando algum dos seguintes:
- Medicamentos que actuam sobre o cérebro, por exemplo, para tranquilizar-se (benzodiazepinas) ou alguns medicamentos para a dor (opiáceos), para a alergia (alguns antihistamínicos), já que OKEDI pode aumentar o efeito sedante de todos eles.
- Medicamentos que podem modificar a actividade eléctrica do coração, tais como medicamentos para tratar a malária, problemas do ritmo cardíaco, alergias (antihistamínicos), alguns antidepressivos ou outros medicamentos para problemas mentais.
- Medicamentos que retardam o latido cardíaco.
- Medicamentos que geram uma baixa concentração de potássio no sangue (tais como determinados diuréticos).
- Medicamentos para tratar o aumento da tensão arterial. OKEDI pode reduzir a tensão arterial.
- Medicamentos para a doença de Parkinson (como levodopa).
- Medicamentos que incrementam a actividade do sistema nervoso central (psicoestimulantes, como metilfenidato).
- Diuréticos empregados para tratar problemas cardíacos ou inchaço de partes do corpo devido à acumulação de um excesso de líquido (p. ex., furosemida ou clorotiazida). OKEDI, em monoterapia ou combinado com furosemida, pode aumentar o risco de acidente vascular cerebral ou morte em pessoas de idade avançada com demência.
Os seguintes medicamentos podem reduzir o efeito de risperidona:
- Rifampicina (medicamento para tratar algumas infecções).
- Carbamazepina, fenitoína (medicamentos para a epilepsia).
- Fenobarbital.
Se começa a tomar estes medicamentos ou deixa de tomá-los, é possível que precise de uma dose diferente de risperidona.
Os seguintes medicamentos podem aumentar o efeito de risperidona:
- Quinidina (se utiliza para determinados tipos de cardiopatias).
- Antidepressivos (como paroxetina, fluoxetina, antidepressivos tricíclicos).
- Medicamentos conhecidos como betabloqueantes (se usam para tratar a tensão arterial alta).
- Fenotiazinas (como os medicamentos usados para tratar a psicose ou para tranquilizar-se).
- Cimetidina, ranitidina (bloqueantes da acidez estomacal).
- Itraconazol e ketoconazol (medicamentos para tratar infecções por fungos).
- Determinados medicamentos para o tratamento do VIH/SIDA, como ritonavir.
- Verapamilo, que se usa para tratar a tensão arterial alta e/ou a alteração do ritmo cardíaco.
- Sertralina e fluvoxamina, medicamentos para tratar a depressão e outros distúrbios psiquiátricos.
Se começa a tomar estes medicamentos ou deixa de tomá-los, é possível que precise de uma dose diferente de risperidona.
Se não tem certeza de que as opções anteriores se aplicam ao seu caso, consulte o seu médico ou farmacêutico antes de começar a usar OKEDI.
Uso de OKEDI com alimentos, bebidas e álcool
Deve evitar o consumo de álcool quando utilizar OKEDI.
Gravidez, lactação e fertilidade
- Se está grávida ou em período de lactação, acredita que possa estar grávida ou tem intenção de ficar grávida, consulte o seu médico ou farmacêutico antes de utilizar este medicamento. O seu médico decidirá se pode usá-lo.
- Os sintomas a seguir podem aparecer em recém-nascidos de mães que têm utilizado risperidona durante o último trimestre (últimos três meses de gravidez): tremores, rigidez muscular e/ou fraqueza, sonolência, agitação, problemas respiratórios e dificuldade na alimentação. Se o seu bebê apresenta algum destes sintomas, é possível que precise consultar o médico.
- OKEDI pode aumentar as concentrações de uma hormona denominada «prolactina» que pode afetar a fertilidade (ver secção 4, «Posíveis efeitos adversos»).
Condução e uso de máquinas
Durante o tratamento com OKEDI podem aparecer tonturas, cansaço e problemas visuais. Não conduza nem use nenhuma ferramenta ou máquina sem antes consultar o seu médico.
3. Como usar OKEDI
Um profissional de saúde lhe administrará OKEDI mediante injeção intramuscular no braço ou no glúteo cada 28 dias. As injeções devem ser alternadas entre o lado direito e o esquerdo.
A dose recomendada é de 75 mg cada 28 dias, mas pode ser necessária uma dose maior de 100 mg cada 28 dias. O médico decidirá qual a dose de OKEDI indicada para si.
Se atualmente recebe tratamento com outros antipsicóticos distintos de risperidona, mas anteriormente utilizou risperidona, deve começar a tomar risperidona oral pelo menos 6 dias antes de começar o tratamento com OKEDI.
Se nunca tomou nenhuma forma de risperidona, deve começar a tomar risperidona por via oral pelo menos 14 dias antes de começar o tratamento com OKEDI. O seu médico determinará a duração do período de administração de risperidona por via oral.
Se tem problemas renais
Não se recomenda o uso de OKEDI em pacientes com insuficiência renal de moderada a grave.
Se usa mais OKEDI do que deve
- Consulte um médico de imediato.
- Em caso de sobredose, é possível que se sinta sonolento ou cansado, que tenha movimentos corporais anormais, problemas para permanecer de pé e caminhar, que tenha tonturas devido à tensão arterial baixa, ou que tenha batimentos cardíacos anormais ou crises convulsivas.
Se interrompe o tratamento com OKEDI
Perderá os efeitos do medicamento. Não deve interromper o tratamento com este medicamento a menos que se lo indique o seu médico, porque os sintomas podem reaparecer.
É importante que não falte às consultas que tem uma vez cada 28 dias quando se supõe que deve receber as injeções deste medicamento. Se não puder ir a uma consulta, certifique-se de avisar o médico de imediato para concertar outra data em que possa ir a administrar-se a injeção.
Se tiver alguma outra dúvida sobre o uso deste medicamento, pergunte ao seu médico ou farmacêutico.
4. Efeitos adversos possíveis
Tal como todos os medicamentos, este medicamento pode produzir efeitos adversos, embora nem todas as pessoas os sofram.
Consulte um médico ou dirija-se imediatamente ao serviço de urgências mais próximo se apresentar o seguinte efeito adverso pouco frequente (pode afetar até 1 em cada 100 pessoas):
- Apresenta discinesia tardia (movimentos involuntários ou tiques no rosto, língua ou outras partes do corpo que não consegue controlar).
Consulte um médico ou dirija-se imediatamente ao serviço de urgências mais próximo se apresentar algum dos seguintes efeitos adversos raros (podem afetar até 1 em cada 1000 pessoas):
- Apresenta coágulos sanguíneos nas veias, especialmente nas pernas (os sintomas incluem inchaço, dor e vermelhidão nas pernas), que podem deslocar-se pelos vasos sanguíneos para os pulmões e causar dor torácica e dificuldade para respirar.
- Apresenta febre, rigidez muscular, suor ou nível de consciência reduzido (um transtorno conhecido como "síndrome neuroléptico maligno").
- É do sexo masculino e tem uma ereção prolongada ou dolorosa, o que é conhecido como priapismo.
- Apresenta uma reação alérgica grave caracterizada por febre; inchaço da boca, face, lábio ou língua; dificuldade para respirar; coceira; erupção cutânea ou descida da tensão arterial (reação anafiláctica ou angioedema). Embora anteriormente tenha tolerado risperidona oral, em raras ocasiões aparecem reações alérgicas após receber injeções de OKEDI.
- A urina é de cor escura ou marrom, ou diminuiu notoriamente a quantidade de urina junto com fraqueza muscular ou dificuldade para mover os braços e as pernas. Podem ser sinais de rabdomiólise (dano rápido dos músculos).
- Apresenta fraqueza ou tontura, febre, calafrios ou feridas na boca. Podem ser sinais de uma cifra muito baixa de granulócitos (um tipo de glóbulo branco que ajuda a combater as infecções).
Também podem aparecer estes outros efeitos adversos:
Efeitos adversos muito frequentes (podem afetar mais de 1 em cada 10 pessoas):
- Dificuldade para conciliar o sono ou permanecer dormido.
- Parkinsonismo: transtornos do movimento que podem incluir movimentos lentos ou deteriorados, sensação de rigidez ou tensão muscular e, por vezes, até uma sensação de que os movimentos "se paralisam" e depois se pode voltar a mover. Outros sinais incluem marcha lenta arrastada, tremor em repouso, salivação aumentada ou babeio, e perda de expressão no rosto.
- Dor de cabeça.
Efeitos adversos frequentes (podem afetar até 1 em cada 10 pessoas):
- Pneumonia (infecção pulmonar), bronquite (infecção das principais vias aéreas dos pulmões), infecção sinusal, infecção do trato urinário, infecção de ouvido, gripe, sintomas pseudogripais, dor de garganta, tosse, congestão nasal, febre, infecção ocular ou conjuntivite.
- Aumento das concentrações de uma hormona denominada "prolactina" que se detecta em um exame de sangue. Os sintomas de concentrações altas de prolactina são pouco frequentes e nos homens podem incluir inchaço das mamas, dificuldade para ter ou manter ereções e diminuição do desejo sexual. Nas mulheres podem incluir secreção de leite das mamas, transtornos menstruais, ausência de períodos menstruais, ausência de ovulação, problemas de fertilidade.
- Aumento de peso, aumento ou diminuição do apetite.
- Transtorno do sono, irritabilidade, depressão, ansiedade, sentir-se adormecido ou estar menos alerta.
- Distonia (contracção involuntária dos músculos que geram movimentos repetitivos lentos ou posturas anormais), discinesia (outro transtorno que afeta os movimentos musculares involuntários, incluindo movimentos repetitivos, espásticos ou de torção, ou tiques).
- Tremor (agitação), espasmos musculares, dor óssea ou muscular, dor de costas, dor articular, quedas.
- Visão borrosa.
- Incontinência urinária (perda involuntária de urina).
- Frequência cardíaca rápida, tensão arterial alta, falta de ar.
- Dor abdominal, molestia abdominal, vômitos, náuseas, tontura, constipação, diarreia, dispepsia, boca seca, dor dental.
- Erupção, vermelhidão cutânea, reação na zona de injeção (que inclui molestia, dor, vermelhidão ou inchaço), inchaço do corpo, dos braços ou das pernas, dor torácica, falta de energia e força, fadiga, dor.
Efeitos adversos pouco frequentes (podem afetar até 1 em cada 100 pessoas):
- Infecção de bexiga, amigdalite, infecção por fungos das unhas, infecção das camadas mais profundas da pele, infecção viral, inflamação da pele causada por ácaros.
- Redução ou aumento dos glóbulos brancos no sangue, diminuição das plaquetas (células sanguíneas que ajudam a deter as hemorragias), anemia ou hematocrito diminuído (redução dos glóbulos vermelhos), creatina-fosfoquinase no sangue elevada, enzimas hepáticas no sangue elevadas.
- Tensão arterial baixa, descida da tensão arterial após levantar-se, vermelhidão da pele, isquemia cerebral (fluxo sanguíneo insuficiente ao cérebro).
- Diabetes, açúcar no sangue elevado, beber água em excesso, colesterol no sangue elevado, perda de peso, anorexia, triglicéridos (gordura) no sangue elevados.
- Mania (ânimo eufórico), confusão, libido diminuída, nervosismo, pesadelos.
- Desmaios, convulsão (crises epilépticas), sensação de que tudo gira (vertigem), zumbido, dor de ouvidos.
- Necessidade imperiosa e incessante de mover partes do corpo, transtorno do equilíbrio, coordenação anormal, atenção deficiente, problemas com a fala, perda ou alteração do sentido do gosto, sensação reduzida da pele ao dor e ao tato, sensação de formigamento, picadas ou entorpecimento da pele.
- Frequência cardíaca irregular e, por vezes, rápida, frequência cardíaca lenta, eletrocardiograma anormal (exame que mede a atividade elétrica dos batimentos cardíacos), palpitações (sensação de aleteo ou pulsões no peito), interrupção da condução entre as partes superior e inferior do coração.
- Congestão das vias respiratórias, sibilância (som áspero/sibilante durante a respiração), hemorragias nasais.
- Postura anormal, rigidez articular, inchaço articular, fraqueza muscular, dor de pescoço, marcha anormal, sede, sentir-se mal, molestia no peito ou molestia geral, sentir-se decaído.
- Irritação ou infecção estomacal ou intestinal, incontinência fecal, dificuldade para engolir, excesso de gases ou flatulência, micção frequente, incapacidade de urinar, dor ao urinar.
- Ausência de períodos menstruais ou outros problemas com o ciclo menstrual, secreção de leite das mamas, disfunção sexual, dor ou molestia nas mamas, secreção vaginal, disfunção erétil, transtorno da ejaculação, desenvolvimento de mamas em homens.
- Urticária, espessamento da pele, transtorno cutâneo, coceira intensa da pele, perda de cabelo, eczema (zonas da pele que se inflamam, picam, racham e estão ásperas), pele seca, mudança de cor da pele, acne, dermatite seborreica (pele vermelha, escamosa, gordurosa, com coceira e inflamada), lesão da pele.
- Hipersensibilidade dos olhos à luz, olho seco, aumento do lacrimejo.
- Reação alérgica, calafrios.
Efeitos adversos raros (podem afetar até 1 em cada 1000 pessoas):
- Infecção.
- Secreção inadequada da hormona que controla o volume urinário, consumo perigosamente excessivo de água, excesso de açúcar na urina, baixo açúcar no sangue, insulina (hormona que controla as concentrações de açúcar no sangue) no sangue elevada.
- Ausência de resposta a estimulação, catatonia (não se mover nem responder enquanto está desperto), nível de consciência diminuído, sonambulismo, transtorno da alimentação relacionado com o sono, dificuldade para respirar durante o sono (apneia do sono), respiração superficial rápida, infecção pulmonar causada pela inalação de alimentos nas vias respiratórias, congestão pulmonar, transtorno das vias respiratórias, transtorno da voz, sons pulmonares crepitantes, ausência de emoção, incapacidade de alcançar o orgasmo.
- Problemas nos vasos sanguíneos do cérebro, coma por diabetes não controlada, tremor involuntário da cabeça.
- Glaucoma (aumento da pressão intraocular), problemas com o movimento dos olhos, giro dos olhos, crosta/inflamação no canto palpebral, problemas oculares durante a cirurgia de catarata.
- Inflamação do pâncreas, obstrução dos intestinos.
- Língua inchada, lábios rachados, caspa, icterícia (cor amarela da pele e dos olhos), endurecimento da pele.
- Aumento de tamanho da mama, congestão mamária (mamas duras, inchadas e dolorosas por excessiva produção de leite materno).
- Temperatura corporal baixa, sensação de frio nos braços e pernas.
- Sintomas de abstinência de fármacos (também em recém-nascidos).
Efeitos adversos muito raros (podem afetar até 1 em cada 10 000 pessoas):
- Complicações potencialmente mortais da diabetes não controlada.
- Ausência de movimento muscular intestinal que causa obstrução.
Frequência não conhecida: não pode ser estimada a partir dos dados disponíveis
- Erupção grave ou potencialmente mortal com bolhas e descamação da pele que pode começar ao redor da boca, nariz, olhos, genitais e estender-se a outras zonas do corpo (Síndrome de Stevens Johnson ou necrólise epidérmica tóxica).
Comunicação de efeitos adversos
Se experimentar qualquer tipo de efeito adverso, consulte o seu médico ou farmacêutico, mesmo que se trate de possíveis efeitos adversos que não aparecem neste prospecto. Também pode comunicá-los diretamente através do sistema nacional de notificação incluído no Apêndice V. Mediante a comunicação de efeitos adversos, você pode contribuir para fornecer mais informações sobre a segurança deste medicamento.
5. Conservação de OKEDI
Mantenha este medicamento fora da vista e do alcance das crianças.
Não utilize este medicamento após a data de validade que aparece na caixa, nos sobres de alumínio ou nas etiquetas das seringas após (CAD). A data de validade é o último dia do mês que se indica.
Conservar a uma temperatura inferior a 30 °C. Conservar no embalagem original para protegê-lo da umidade.
Utilize OKEDI imediatamente após a reconstituição.
Os medicamentos não devem ser jogados nos deságues ou na lixeira. Pergunte ao seu farmacêutico como se livrar dos recipientes e dos medicamentos que já não precisa. Desta forma, ajudará a proteger o meio ambiente.
6. Conteúdo do envase e informação adicional
Composição de OKEDI
O princípio ativo é risperidona.
Apenas a seringa de pó contém o princípio ativo. Uma vez reconstituído, a quantidade de risperidona administrada é de 75 mg.
Os outros componentes são:
Seringa precargada de pó: poli(D,L-lactida-co-glicolida).
Seringa precargada de dissolvente: dimetilsulfóxido.
Aspecto do produto e conteúdo do envase
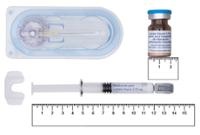
Cada caixa do kit de OKEDI pó e dissolvente para suspensão injetável de liberação prolongada contém:
- Um saco de alumínio com uma seringa precargada que contém pó (dentro do pó se encontra o princípio ativo, risperidona) e um sobre de dessecante de gel de sílica. Trata-se de pó solto de cor branca a esbranquiçada.
- Um saco de alumínio com uma seringa precargada que contém o dissolvente e um sobre de dessecante de gel de sílica. A seringa precargada de dissolvente contém uma solução transparente e tem asas de sujeição VERMELHAS.
- Uma agulha estéril de 2 polegadas (0,90 × 51 mm [calibre 20G]) para injeção intramuscular com protetor de segurança para administração nos glúteos.
- Uma agulha estéril de 1 polegada (0,80 × 25 mm [calibre 21G]) para injeção intramuscular com protetor de segurança para administração nos músculos deltoides.
Título da autorização de comercialização e responsável pela fabricação
Laboratórios Farmacêuticos Rovi, S.A.
Julián Camarillo, 35
28037 Madrid
Espanha
Podem solicitar mais informações sobre este medicamento dirigindo-se ao representante local do titular da autorização de comercialização:
Bélgica Laboratórios Farmacêuticos Rovi, S.A. Julián Camarillo, 35 28037 Madrid Espanha Tel: +34 91 375 62 30 | Lituânia Laboratórios Farmacêuticos Rovi, S.A. Julián Camarillo, 35 28037 Madrid Espanha Tel: +34 91 375 62 30 |
?????? Laboratórios Farmacêuticos Rovi, S.A. Julián Camarillo, 35 28037 Madrid ??????? Te?.: +34 91 375 62 30 | Luxemburgo Laboratórios Farmacêuticos Rovi, S.A. Julián Camarillo, 35 28037 Madrid Espanha Tel: +34 91 375 62 30 |
República Checa Laboratórios Farmacêuticos Rovi, S.A. Julián Camarillo, 35 28037 Madrid Espanha Tel: +34 91 375 62 30 | Hungria Laboratórios Farmacêuticos Rovi, S.A. Julián Camarillo, 35 28037 Madrid Espanha Tel: +34 91 375 62 30 |
Dinamarca Laboratórios Farmacêuticos Rovi, S.A. Julián Camarillo, 35 28037 Madrid Espanha Tlf: +34 91 375 62 30 | Malta Laboratórios Farmacêuticos Rovi, S.A. Julián Camarillo, 35 28037 Madrid Espanha Tel: +34 91 375 62 30 |
Alemanha Rovi GmbH Rudolf-Diesel-Ring 6 83607 Holzkirchen Tel: +49 8024 4782955 | Países Baixos Laboratórios Farmacêuticos Rovi, S.A. Julián Camarillo, 35 28037 Madrid Espanha Tel: +34 91 375 62 30 |
Estônia Laboratórios Farmacêuticos Rovi, S.A. Julián Camarillo, 35 28037 Madrid Espanha Tel: +34 91 375 62 30 | Noruega Laboratórios Farmacêuticos Rovi, S.A. Julián Camarillo, 35 28037 Madrid Espanha Tlf: +34 91 375 62 30 |
Grécia BIANEΞ Α.Ε. Οδ?ς Βαρυμπ?μπης 8, 14671 Ν. Ερυθρα?α, Κηφισι? Tηλ. 210 8009111 | Áustria Rovi GmbH Rudolf-Diesel-Ring 6 83607 Holzkirchen Alemanha Tel: +43 664 1340471 |
Espanha Laboratórios Farmacêuticos Rovi, S.A. Julián Camarillo, 35 28037 Madrid Tel: +34 91 375 62 30 | Polônia Laboratórios Farmacêuticos Rovi, S.A. Julián Camarillo, 35 28037 Madrid Espanha Tel: +34 91 375 62 30 |
França ROVI 24, Rue Du Drac 38180 Seyssins Tél: +33 (0)4 76 968 969 | Portugal Laboratórios Farmacêuticos Rovi, S.A. Julián Camarillo, 35 28037 Madrid Espanha Tel: +34 91 375 62 30 |
Croácia Laboratórios Farmacêuticos Rovi, S.A. Julián Camarillo, 35 28037 Madrid Espanha Tel: +34 91 375 62 30 Irlanda Laboratórios Farmacêuticos Rovi, S.A. Julián Camarillo, 35 28037 Madrid Espanha Tel: +34 91 375 62 30 | Romênia Laboratórios Farmacêuticos Rovi, S.A. Julián Camarillo, 35 28037 Madrid Espanha Tel: +34 91 375 62 30 Eslovênia Laboratórios Farmacêuticos Rovi, S.A. Julián Camarillo, 35 28037 Madrid Espanha Tel: +34 91 375 62 30 |
Islândia Laboratórios Farmacêuticos Rovi, S.A. Julián Camarillo, 35 28037 Madrid Espanha Sími: +34 91 375 62 30 | República Eslovaca Laboratórios Farmacêuticos Rovi, S.A. Julián Camarillo, 35 28037 Madrid Espanha Tel: +34 91 375 62 30 |
Espanha Laboratórios Farmacêuticos Rovi, S.A. Julián Camarillo, 35 28037 Madrid Tel: +34 91 375 62 30 | Polônia Laboratórios Farmacêuticos Rovi, S.A. Julián Camarillo, 35 28037 Madrid Espanha Tel: +34 91 375 62 30 |
Itália Rovi Biotech, S.R.L. Viale Achille Papa, 30 20149 Milano Tel: +39 02 366 877 10 | Finlândia Laboratórios Farmacêuticos Rovi, S.A. Julián Camarillo, 35 28037 Madrid Espanha Puh/Tel: +34 91 375 62 30 |
Chipre Laboratórios Farmacêuticos Rovi, S.A. Julián Camarillo, 35 28037 Madrid Espanha Tηλ: +34 91 375 62 30 | Suécia Laboratórios Farmacêuticos Rovi, S.A. Julián Camarillo, 35 28037 Madrid Espanha Tel: +34 91 375 62 30 |
Letônia Laboratórios Farmacêuticos Rovi, S.A. Julián Camarillo, 35 28037 Madrid Espanha Tel: +34 91 375 62 30 | Reino Unido (Irlanda do Norte) Rovi Biotech Limited Davis House 4th Floor Suite 425 Robert Street Croydon CR0 1QQ - UK Tel: + 44 (0) 203 642 06 77 |
Data da última revisão deste prospecto: Maio 2023.
Esta informação está destinada apenas a profissionais de saúde
INSTRUÇÕES PARA PROFISSIONAIS DE SAÚDE
OKEDI 75 mg pó e dissolvente para suspensão injetável de liberação prolongada
Informação importante
Para garantir a administração correta de OKEDI, é necessário prestar suma atenção a estas instruções de uso passo a passo.
Use os componentes fornecidos
Os componentes incluídos na caixa do kit estão projetados especificamente para serem usados com OKEDI. OKEDI deve ser reconstituído apenas com o dissolvente fornecido na caixa do kit.
Não substituaNENHUM componente da caixa do kit.
Administre a dose imediatamente após a reconstituição. Apenas para uso intramuscular após a reconstituição.
Administração correta
Deve ser administrado todo o conteúdo da seringa reconstituída para garantir a administração da dose de OKEDI indicada.
Dispositivo de uso único
- VERIFIQUE O CONTEÚDO
Sobre uma superfície limpa, abra os sacos e descarte o dessecante.
A caixa do kit de OKEDI contém o seguinte:
- Um saco de alumínio com uma seringa precargada de OKEDI, com um pistão do êmbolo BRANCO e asas de sujeição BRANCAS. A seringa está marcada com .
- Um saco de alumínio com DISOLVENTE para a seringa precargada de OKEDI, com um pistão do êmbolo TRANSPARENTE e asas de sujeição VERMELHAS. A seringa está marcada com
- Duas agulhas para administração (calibre 21, 1 polegada para músculos deltoides [cápsula de fechamento verde] e calibre 20, 2 polegadas para glúteos [cápsula de fechamento amarela]).
Deseche o kit se algum dos componentes estiver danificado.
Em caso de que observe alguma partícula estranha e/ou variação no aspecto físico, não administre OKEDI.
1.1 Inspeccione a seringa de dissolvente
ASEGURE-SE de que o conteúdo da seringa de DISOLVENTE flua normalmente como um líquido.
O dissolvente congela abaixo de 19ºC.
Se estiver congelado ou parcialmente congelado, antes de continuar, permita que se descongele colocando-o em contato com as mãos ou deixando-o à temperatura ambiente até que volte a fluir como um líquido.
1.2 Desprenda o pó da seringa
DÊ GOLPES leves na seringa de OKEDI para desprender qualquer possível tampão de pó perto da cápsula de fechamento.
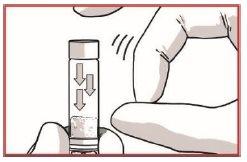
- CONECTE AS SERINGAS
2.1 Retire as cápsulas de fechamento das seringas em posição vertical
Sustente ambas as seringas em posição vertical para evitar a perda de produto.
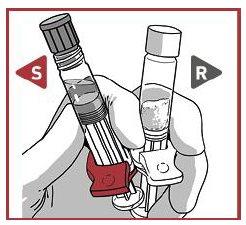
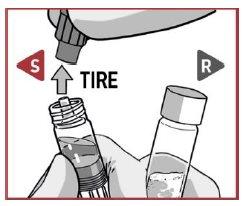
TIRE da cápsula de fechamento para retirá-la da seringa de dissolvente.
GIRE a cápsula de fechamento e TIRE dela para retirá-la da seringa de pó.
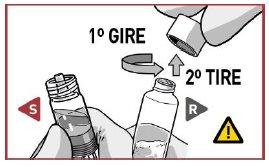
2.2 Conecte as seringas
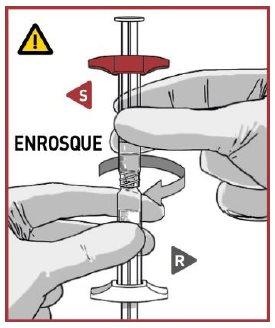
Coloque a seringa de dissolvente S que tem as asas de sujeição de cor ENCIMA da seringa de pó R, ou incline-a levemente ao conectá-las.
ENROSQUE as seringas entre si até que sinta uma leve resistência.
ASEGURE-SE de que a seringa de pó R esteja em posição vertical para evitar a perda de produto.
- MISTURE O CONTEÚDO
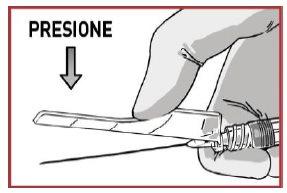
DETENHA-SE E LEIA ESTA SEÇÃO ANTES DE COMEÇAR OU É POSSÍVEL QUE RECONSTITUA O MEDICAMENTO INCORRETAMENTE.
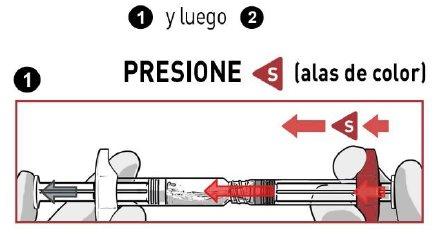
- PRESIONE VIGOROSAMENTE o conteúdo de dissolvente dentro da seringa de pó.
- NÃO ESPERE até que o pó se umedecia e comece a misturar o conteúdo RÁPIDAMENTE, pressionando os êmbolos de maneira RÁPIDA e alternada cerca de 100 vezes (2 vezes em 1 segundo, aproximadamente 1 minuto).
- ASEGURE-SE de que o medicamento passe de uma seringa para a outra para que se misture corretamente: o medicamento é viscoso e deverá fazer força quando pressionar os pistões dos êmbolos.
Misturepressionando pelo menos 100 vezesde maneira alternada
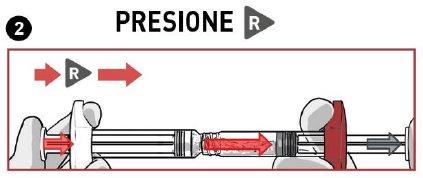

ASEGURE-SE de que o medicamento passe de uma seringa para a outra
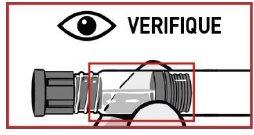
Quando o medicamento está misturado corretamente, o aspecto será uma suspensão uniforme de cor esbranquiçada a amarelada e consistência espessa.

Uma vez que se tenha reconstituído, prepare imediatamente a seringa de injeção para administrá-la para evitar a perda de homogeneidade.
- PREPARE A SERINGA DE INJEÇÃO
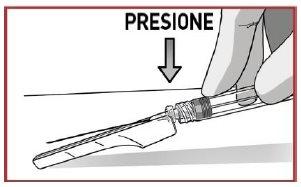
4.1 Transfira o medicamento
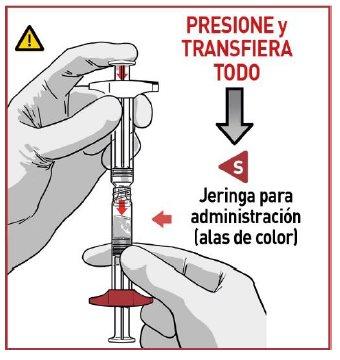
Exerça uma pressão descendente sobre o pistão do êmbolo Re transfira todo o conteúdo para a seringa Sque tem as asas de sujeição de cor.
ASEGURE-SE de que se tenha transferido todo o conteúdo.
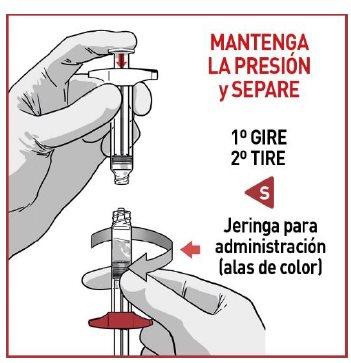
4.2 Separe as seringas
Uma vez que se tenha transferido todo o medicamento, separe ambas as seringas desenroscando-as.
OKEDI deve ser administrado imediatamente para evitar a perda de homogeneidade.
4.3 Coloque a agulha estéril com o protetor de segurança
Escolha a agulha correta:
- Deltoides: calibre 21G, 1 polegada para o músculo deltoides (cápsula de fechamento verde).
- Glúteos: calibre 20G, 2 polegadas para os glúteos (cápsula de fechamento amarela).
Coloque-a girando no sentido horário. Não aperte excessivamente.
4.4 Extraia o ar excedente
Retire o protetor da agulha e extraia o excesso de ar (somente as bolhas grandes) do cilindro da seringa.
NÃO expulse nenhuma gota de medicamento
Se observar medicamento na ponta da agulha, tire do êmbolo levemente para trás para evitar que se derrame medicamento.

- ADMINISTRE E DESECHE
5.1 Injete o medicamento
Introduza a agulha totalmente dentro do músculo. NÃO ADMINISTRE A INJEÇÃO POR NENHUMA OUTRA VIA.
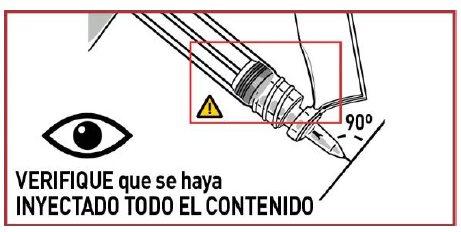
MEDICAMENTO ESPESO, INJETE-LO LENTAMENTE E DE FORMA CONSTANTE. ASEGURE-SE DE INJETAR-LO TODO.
- O tempo de injeção é mais longo do que o habitual devido à viscosidade do medicamento.
- Espere alguns segundos antes de retirar a agulha.
- Evite a injeção acidental em um vaso sanguíneo.
5.2 Deseche o medicamento
Cubra a agulha exercendo pressão sobre o protetor da agulha com o dedo ou uma superfície plana, e desça-a imediatamente em um recipiente para objetos pontiagudos seguro.
|
|

Quanto custa o OKEDI 75 mg pó e solvente para suspensão injetável de libertação prolongada em Espanha em 2025?
O preço médio do OKEDI 75 mg pó e solvente para suspensão injetável de libertação prolongada em dezembro de 2025 é de cerca de 539.57 EUR. Os valores podem variar consoante a região, a farmácia e a necessidade de receita. Confirme sempre com uma farmácia local ou fonte online para obter informações atualizadas.
- País de registo
- Preço médio em farmácia539.57 EUR
- Substância ativa
- Requer receita médicaSim
- Fabricante
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a OKEDI 75 mg pó e solvente para suspensão injetável de libertação prolongadaForma farmacêutica: COMPRIMIDO, 1 mgSubstância ativa: risperidoneFabricante: Neuraxpharm Spain S.L.Requer receita médicaForma farmacêutica: COMPRIMIDO, 3 mgSubstância ativa: risperidoneFabricante: Neuraxpharm Spain S.L.Requer receita médicaForma farmacêutica: COMPRIMIDO, 6 mgSubstância ativa: risperidoneFabricante: Neuraxpharm Spain S.L.Requer receita médica
Alternativas a OKEDI 75 mg pó e solvente para suspensão injetável de libertação prolongada noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a OKEDI 75 mg pó e solvente para suspensão injetável de libertação prolongada em Polónia
Alternativa a OKEDI 75 mg pó e solvente para suspensão injetável de libertação prolongada em Ukraine
Médicos online para OKEDI 75 mg pó e solvente para suspensão injetável de libertação prolongada
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de OKEDI 75 mg pó e solvente para suspensão injetável de libertação prolongada – sujeita a avaliação médica e regras locais.