ICATIBANTO FRESENIUS 30 mg Solução injetável em seringa pré-carregada

Pergunte a um médico sobre a prescrição de ICATIBANTO FRESENIUS 30 mg Solução injetável em seringa pré-carregada

Como usar ICATIBANTO FRESENIUS 30 mg Solução injetável em seringa pré-carregada
Introdução
Prospecto: informação para o utilizador
Icatibanto Fresenius 30 mg solução injetável em seringa pré-carregada EFG
Leia todo o prospecto atentamente antes de começar a usar este medicamento, porque contém informações importantes para si.
- Conserva este prospecto, porque pode ter que voltar a lê-lo.
- Se tiver alguma dúvida, consulte o seu médico ou farmacêutico.
- Este medicamento foi prescrito apenas para si, e não deve dá-lo a outras pessoas, mesmo que tenham os mesmos sintomas que si, porque pode prejudicá-las.
- Se experimentar efeitos adversos, consulte o seu médico ou farmacêutico, mesmo que se trate de efeitos adversos que não aparecem neste prospecto. Ver seção 4.
Conteúdo do prospecto
- O que é Icatibanto Fresenius e para que é utilizado
- O que necessita saber antes de começar a usar Icatibanto Fresenius
- Como usar Icatibanto Fresenius
- Posíveis efeitos adversos
5 Conservação de Icatibanto Fresenius
- Conteúdo do envase e informações adicionais
1. O que é Icatibanto Fresenius e para que é utilizado
Este medicamento contém o princípio ativo icatibanto.
Icatibanto é utilizado para o tratamento dos sintomas do angioedema hereditário (AEH) em adultos, adolescentes e crianças maiores de 2 anos.
No AEH, aumentam as concentrações de uma substância presente no sangue chamada bradicinina, o que produz sintomas como inchaço, dor, náuseas e diarreia.
Icatibanto bloqueia a atividade da bradicinina e, portanto, freia a progressão dos sintomas de uma crise de AEH.
2. O que necessita saber antes de começar a usar Icatibanto Fresenius
Não use Icatibanto Fresenius
- se é alérgico a icatibanto, ou a algum dos outros componentes deste medicamento (incluídos na seção 6).
Advertências e precauções
Consulte o seu médico antes de começar a usar Icatibanto Fresenius:
- se sofre de angina de peito (diminuição do fluxo de sangue que chega ao coração)
- se sofreu recentemente um acidente vascular cerebral
Os efeitos adversos relacionados com Icatibanto são semelhantes aos sintomas da sua própria doença. Consulte imediatamente com o seu médico se nota que os sintomas da crise se agravam após a administração de Icatibanto.
Além disso:
- Si ou o seu cuidador devem aprender a técnica de administração de injeções subcutâneas (sob a pele) antes de autoadministrar ou de que o seu cuidador lhe administre Icatibanto.
- Imediatamente após autoadministrar Icatibanto ou de que o seu cuidador lhe administre enquanto experimenta uma crise laríngea (obstrução da via aérea superior), deve procurar atenção médica em uma instituição médica.
- Se os seus sintomas não se resolvem após uma injeção de Icatibanto autoadministrada ou administrada pelo seu cuidador, deve consultar o médico sobre a administração de injeções adicionais de Icatibanto. Em pacientes adultos, podem ser administradas até 2 injeções adicionais no prazo de 24 horas.
Crianças e adolescentes
Não se recomenda o uso de Icatibanto em crianças menores de 2 anos ou que pesem menos de 12 kg porque não foi estudado nestes pacientes.
Outros medicamentos e Icatibanto Fresenius
Informa ao seu médico se está a tomar, tomou recentemente ou possa ter que tomar qualquer outro medicamento.
Não se conhecem interações de Icatibanto com outros medicamentos. Se está a tomar algum medicamento que seja um inibidor da enzima de conversão da angiotensina (IECA) (por exemplo: captopril, enalapril, ramipril, quinapril, lisinopril) para reduzir a pressão arterial ou por qualquer outro motivo, informe o seu médico antes de utilizar Icatibanto.
Gravidez e lactação
Se está grávida ou em período de lactação, acredita que possa estar grávida ou tem intenção de engravidar, consulte o seu médico antes de começar a usar este medicamento.
Se se encontra em período de lactação, não deve amamentar o seu filho durante as 12 horas seguintes à última administração de Icatibanto.
C
Não conduza nem maneje máquinas se se sentir cansado ou mareado como consequência da crise de AEH ou após utilizar Icatibanto Fresenius.
I
Este medicamento contém menos de 23 miligramas (1 mmol) de sódio por dose, pelo que se considera essencialmente “isento de sódio”.
3. Como usar Icatibanto Fresenius
Siga exatamente as instruções de administração deste medicamento indicadas pelo seu médico.
Em caso de dúvida, consulte novamente o seu médico.
Se nunca se lhe administrou Icatibanto previamente, a primeira dose sempre deve ser injetada por pessoal médico ou de enfermagem. O médico dar-lhe-á alta quando considerar seguro que se vá para casa. Após analisar com o seu médico ou enfermeiro, e após aprender a técnica para injeções subcutâneas (sob a pele), si mesmo ou a pessoa que o atende podem administrar-lhe Icatibanto se tiver uma crise de AEH. É importante injetar Icatibanto por via subcutânea (sob a pele) assim que advertir uma crise de angioedema. O pessoal sanitário ensinar-lhe-á a si e a quem o atende o modo de injetar Icatibanto de forma segura, seguindo as instruções do prospecto.
Quando e com que frequência deve usar Icatibanto Fresenius?
O seu médico determinou a dose exata de Icatibanto e dir-lhe-á com que frequência deve utilizá-lo.
- A dose recomendada de Icatibanto é de uma injeção (3 ml, 30 mg) administrada por via subcutânea (debaixo da pele) assim que si advertir a crise de angioedema (por exemplo, com aumento do inchaço cutâneo, sobretudo na face e no pescoço, ou aumento da dor abdominal).
- Se não notar uma melhoria dos sintomas, após seis horas, deve procurar aconselhamento médico sobre a administração de injeções adicionais de Icatibanto. Em adultos, podem ser administradas até 2 injeções adicionais no prazo de 24 horas.
- Não deve receber mais de 3 injeções num período de 24 horas e se necessitar de mais de 8 injeções num mês, deve procurar aconselhamento médico.
Crianças e adolescentes de 2 a 17 anos
- A dose recomendada de Icatibanto é de uma injeção de 1 ml até um máximo de 3 ml em função do peso corporal por via subcutânea (sob a pele) assim que apresente sintomas de uma crise de angioedema (por exemplo, um aumento do inchaço cutâneo, sobretudo na face e no pescoço, ou aumento da dor abdominal).
- Consulte a seção das instruções de uso para ver a dose que deve injetar.
- Se não tiver certeza sobre a dose que deve injetar, consulte o seu médico, farmacêutico ou enfermeiro.
-.
Icatibanto Fresenius é administrado mediante injeção subcutânea (debaixo da pele). Cada seringa deve ser usada apenas uma vez.
Icatibanto Fresenius é injetado com uma agulha curta no tecido gordo situado debaixo da pele do abdômen (barriga). Se tiver alguma outra dúvida sobre o uso deste medicamento, pergunte ao seu médico ou farmacêutico.
As seguintes instruções passo a passo estão previstas para
- autoadministração (adultos)
- administração por parte de um cuidador ou um profissional de saúde para adultos, adolescentes ou crianças maiores de 2 anos (que pesem 12 kg como mínimo).
As instruções incluem os seguintes passos principais:
- Informação geral
2a) Preparação da seringa para crianças e adolescentes (2-17 anos) que pesem 65 kg ou menos
2b) Preparação da seringa e da agulha para a injeção (todos os pacientes)
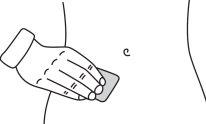
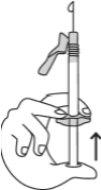
- Preparação do local da injeção
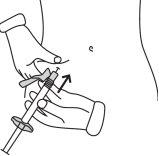
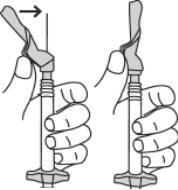
- Injeção da solução
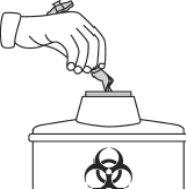
- Eliminação dos materiais da injeção
Instruções passo a passo para a injeção
| |||||||||||||||
| |||||||||||||||
2a)Preparação da seringa para crianças e adolescentes (2-17 anos) que pesem 65 kg ou menos: | |||||||||||||||
Informação importante para profissionais de saúde e cuidadores: Quando a dose é inferior a 30 mg (3 ml), é necessário o seguinte equipamento para extrair a dose adequada (ver informação a seguir):
O volume de injeção necessário em ml deve ser preparado numa seringa graduada de 3 ml vazia (ver tabela a seguir).Tabela 1: Pauta posológica para crianças e adolescentes
Os pacientes que pesem mais de 65 kgusarão todo o conteúdo da seringa pré-carregada (3 ml).
Se não tiver certeza sobre o volume de solução que deve extrair, consulte o seu médico, farmacêutico ou enfermeiro
Evite tocar os extremos do conector e as pontas das seringas, para prevenir a contaminação
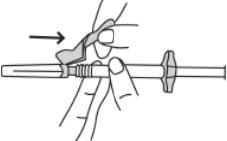
Transferir a solução de icatibanto para a seringa graduada
| |||||||||||||||
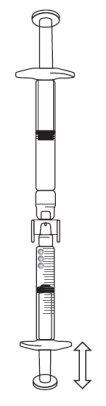
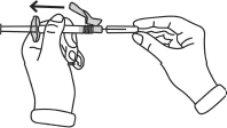
Se houver ar na seringa graduada:
| |||||||||||||||
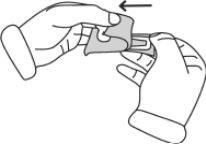
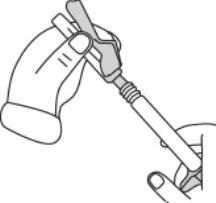
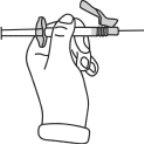
2b) Preparação da seringa e da agulha para a injeção: Todos os pacientes (adultos, adolescentes e crianças) | |||||||||||||||
| |||||||||||||||
| |||||||||||||||
| |||||||||||||||
| |||||||||||||||
| |||||||||||||||
| |||||||||||||||
| |||||||||||||||
| |||||||||||||||
|
4. Posíveis efeitos adversos
Como todos os medicamentos, este medicamento pode produzir efeitos adversos, embora nem todas as pessoas os sofram. Quase todos os pacientes que recebem Icatibanto notam uma reação no local da injeção (como irritação cutânea, inflamação, dor, prurido, erupção cutânea e ardor). Estes efeitos são geralmente leves e melhoram sem necessidade de qualquer tratamento adicional.
Muito frequentes (podem afetar mais de 1 de cada 10 pessoas):
Reações adicionais no local da injeção (sensação de pressão, hematoma, diminuição da sensibilidade e/ou entorpecimento, aumento da erupção cutânea com picazón e calor).
Frequentes (podem afetar até 1 de cada 10 pessoas):
Náuseas
Dor de cabeça
Tontura
Febre
Prurido
Erupção
Verdade cutânea
Provas de função hepática anormais
Frequência não conhecida (não pode ser estimada a partir dos dados disponíveis):
Urticárias (urticária)
Informe ao seu médico imediatamente se observar que os sintomas da crise se agravam após ter recebido Icatibanto.
Se experimentar efeitos adversos, consulte o seu médico, mesmo que se trate de efeitos adversos que não aparecem neste prospecto.
Comunicação de efeitos adversos
Se experimentar qualquer tipo de efeito adverso, consulte o seu médico ou farmacêutico, mesmo que se trate de possíveis efeitos adversos que não aparecem neste prospecto. Também pode comunicá-los diretamente através do Sistema Espanhol de Farmacovigilância de Medicamentos de Uso Humano: www.notificaRAM.es
Ao comunicar efeitos adversos, você pode contribuir para fornecer mais informações sobre a segurança deste medicamento.
5. Conservação de Icatibanto Fresenius
Mantenha este medicamento fora da vista e do alcance das crianças.
Não utilize este medicamento após a data de validade que aparece no envase de cartão e na seringa pré-carregada após “VAL”. A data de validade é o último dia do mês que se indica.
Não conserve a uma temperatura superior a 30ºC. Não congele.
Utilize imediatamente após abrir e apenas em envases que não estejam danificados. Para uso único.
Não utilize este medicamento se observar que o envase da seringa ou da agulha está danificado ou se observar sinais visíveis de deterioração; por exemplo, se a solução está turva, se contém partículas flutuantes ou se o cor da solução mudou.
Os medicamentos não devem ser jogados nos esgotos nem na lixeira. Pergunte ao seu farmacêutico como se livrar dos envases e dos medicamentos que já não precisa. Dessa forma, ajudará a proteger o meio ambiente.
6. Conteúdo do envase e informação adicional
Composição de Icatibanto Fresenius
O princípio ativo é icatibanto. Cada seringa pré-carregada contém 30 miligramas de icatibanto (na forma de acetato). Cada ml de solução contém 10 mg de icatibanto. Os outros componentes são cloreto de sódio, ácido acético glacial, hidróxido de sódio e água para preparações injetáveis.
Aspecto do produto e conteúdo do envase
Icatibanto Fresenius apresenta-se como solução injetável transparente e incolor em uma seringa pré-carregada.
3 ml de solução em uma seringa pré-carregada de 3 ml (vidro de tipo I) com tampão do êmbolo (bromobutilo recoberto com polímero de fluorocarbono). Na caixa é fornecida uma agulha hipodérmica de segurança (25 G; 16 mm).
Envase unitário de uma seringa pré-carregada com uma agulha ou em envase múltiplo de três seringas pré-carregadas com três agulhas de segurança.
Pode ser que apenas alguns tamanhos de envases sejam comercializados.
Título da autorização de comercialização
Fresenius Kabi España, S.A.U.
Torre Mapfre-Vila Olímpica
C/Marina 16-18
08005 Barcelona
Espanha
Responsável pela fabricação
Fresenius Kabi Austria GmbH
Hafnerstraße 36
8055 Graz
Áustria
Este medicamento está autorizado nos estados membros do Espaço Económico Europeue no Reino Unido (Irlanda do Norte)com os seguintes nomes:
Nome do estado membro | Nome do medicamento |
Áustria | Icatibant Fresenius 30 mg Injektionslösung in einer Fertigspritze |
Bélgica | Icatibant Fresenius 30 mg oplossing voor injectie in een voorgevulde spuit, solution injectable en seringue pré-remplie, Injektionslösung in einer Fertigspritze |
Croácia | Ikatibant Fresenius 30 mg otopina za injekciju u napunjenoj štrcaljki |
República Checa | Icatibant Fresenius |
Dinamarca | Icatibant Fresenius |
Estónia | Icatibant Fresenius |
Finlândia | Icatibant Fresenius 30 mg injektioneste, liuos, esitäytetty ruisku |
França | ICATIBANT FRESENIUS 30 mg, solution injectable en seringue préremplie |
Alemanha | Icatibant Fresenius 30 mg Injektionslösung in einer Fertigspritze |
Hungria | Icatibant Fresenius 30 mg oldatos injekció eloretöltött fecskendoben |
Irlanda | Icatibant 30 mg solution for injection in pre-filled syringe |
Itália | Icatibant Fresenius |
Letónia | Icatibant Fresenius 30 mg šķidums injekcijām pilnšļirce |
Lituânia | Icatibant Fresenius 30 mg injekcinis tirpalas užpildytame švirkšte |
Países Baixos | Icatibant Fresenius 30 mg, oplossing voor injectie in een voorgevulde spuit |
Noruega | Icatibant Fresenius |
Polónia | Icatibant Fresenius |
Portugal | Icatibant Fresenius |
Eslováquia | Icatibant Fresenius 30 mg |
Espanha | Icatibanto Fresenius 30 mg solução injetável em seringa pré-carregada EFG |
Suécia | Icatibant Fresenius 30 mg injektionsvätska, lösning i förfylld spruta |
Reino Unido (Irlanda do Norte) | Icatibant 30 mg solution for injection in pre-filled syringe |
Data da última revisão deste prospecto: Abril2022
A informação detalhada deste medicamento está disponível na página web da Agência Espanhola de Medicamentos e Produtos Sanitários (AEMPS), http://www.aemps.gob.es/
- País de registo
- Substância ativa
- Requer receita médicaSim
- Fabricante
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a ICATIBANTO FRESENIUS 30 mg Solução injetável em seringa pré-carregadaForma farmacêutica: INJETÁVEL, 30 mgSubstância ativa: icatibantRequer receita médicaForma farmacêutica: INJETÁVEL, 30 mgSubstância ativa: icatibantFabricante: Accord Healthcare S.L.U.Requer receita médicaForma farmacêutica: INJETÁVEL, 30 mgSubstância ativa: icatibantFabricante: Laboratoire AguettantRequer receita médica
Alternativas a ICATIBANTO FRESENIUS 30 mg Solução injetável em seringa pré-carregada noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a ICATIBANTO FRESENIUS 30 mg Solução injetável em seringa pré-carregada em Polónia
Alternativa a ICATIBANTO FRESENIUS 30 mg Solução injetável em seringa pré-carregada em Ukraine
Médicos online para ICATIBANTO FRESENIUS 30 mg Solução injetável em seringa pré-carregada
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de ICATIBANTO FRESENIUS 30 mg Solução injetável em seringa pré-carregada – sujeita a avaliação médica e regras locais.




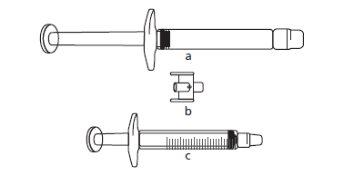 Seringa graduada de 3 ml
Seringa graduada de 3 ml

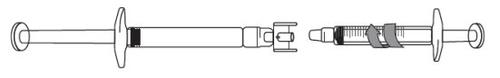
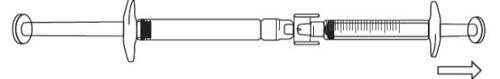
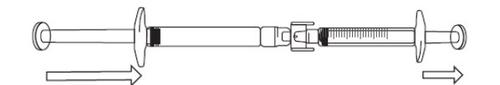 Para iniciar a transferência da solução de icatibanto, empurre o êmbolo da seringa pré-carregada (no extremo esquerdo da imagem que aparece a seguir).
Para iniciar a transferência da solução de icatibanto, empurre o êmbolo da seringa pré-carregada (no extremo esquerdo da imagem que aparece a seguir).