Como usar BELKYRA 10 mg/ml SOLUÇÃO INJETÁVEL
Introdução
Prospecto: informação para o utilizador
BELKYRA 10mg/ml solução injetável
ácido desoxicolico
Leia todo o prospecto atentamente antes de começar a usar o medicamento, porque contém informações importantes para si.
- Conserva este prospecto, porque pode ter que voltar a lê-lo.
- Se tiver alguma dúvida, consulte o seu médico, farmacêutico ou enfermeiro.
- Se experimentar efeitos adversos, consulte o seu médico, farmacêutico ou enfermeiro, mesmo que se trate de efeitos adversos que não aparecem neste prospecto. Ver secção 4.
Conteúdo do prospecto
- O que é BELKYRA e para que é utilizado
- O que precisa saber antes de começar a usar BELKYRA
- Como usar BELKYRA
- Possíveis efeitos adversos
- Conservação de BELKYRA
- Conteúdo do envase e informação adicional
1. O que é BELKYRA e para que é utilizado
Belkyra contém o princípio ativo denominado ácido desoxicolico. O organismo produz ácido desoxicolico de forma natural para ajudar a digerir as gorduras.
Este medicamento é usado em adultos para o tratamento da gordura submentoniana (gordura não desejada debaixo da barbilla) quando a sua presença tem um impacto psicológico importante no paciente.
Belkyra contém uma versão não humana e não animal de ácido desoxicolico, que é idêntica ao ácido desoxicolico produzido de forma natural. Belkyra é um medicamento injetável administrado pelo seu médico.
2. O que precisa saber antes de começar a usar BELKYRA
Não use BELKYRA:
- Se é alérgico ao ácido desoxicolico ou a algum dos outros componentes deste medicamento (incluídos na secção 6).
- Se tem uma infecção na zona da barbilla ou do pescoço onde se deve injetar o medicamento.
Advertências e precauções
Consulte o seu médico, farmacêutico ou enfermeiro antes de começar a usar Belkyra. O seu médico ou enfermeiro verificarão o seu estado de saúde antes de cada tratamento. Informe o seu médico ou enfermeiro de qualquer doença que sofra antes de cada tratamento.
O seu médico ou enfermeiro prestarão especial atenção à zona em torno do seu pescoço, porque devem ser tomadas medidas de precaução em caso de presença de qualquer doença ou cirurgia prévia (p. ex., cicatrizes, lipoaspiração, dificuldade para engolir, aumento da glândula tiróidea ou das glândulas linfáticas).
- Pode ocorrer uma lesão temporária do nervo da mandíbula, o que pode dar origem a uma sorriso assimétrica ou a fraqueza dos músculos faciais.
- Pode ocorrer um dano nos tecidos ao redor da zona tratada (ou seja, erosão cutânea, ulceração, necrose). Isso pode causar cicatrização. Se ocorrer ulceração ou necrose, nunca deve voltar a receber um tratamento com Belkyra novamente (ver secção 4).
- Pode ocorrer infecção ao redor da área de tratamento e pode requerer tratamento médico adicional. Se ocorrer vermelhidão ou dor, consulte o seu médico, farmacêutico ou enfermeiro.
Não se deve usar Belkyra se padece obesidade ou um transtorno dismórfico corporal (percepção distorcida da sua própria imagem).
Crianças e adolescentes
Este medicamento não está indicado para uso em crianças e adolescentes.
Outros medicamentos e BELKYRA
Informe o seu médico ou enfermeiro se está a tomar, tomou recentemente ou pode ter que tomar qualquer outro medicamento.
Gravidez e amamentação
Não se conhecem os efeitos deste medicamento em mulheres grávidas ou em período de amamentação. Por precaução, não se recomenda o uso de Belkyra durante a gravidez.
Se está grávida ou em período de amamentação, acredita que possa estar grávida ou tem intenção de ficar grávida, consulte o seu médico ou enfermeiro antes de utilizar este medicamento.
Condução e uso de máquinas
Não se espera que Belkyra afete a capacidade do paciente para conduzir ou utilizar máquinas.
BELKYRA contém sódio
Este medicamento contém 4,23 mg de sódio (principal componente do sal de cozinha/mesa) em cada ml. Isso equivale a 0,2 % da ingestão diária máxima de sódio recomendada para um adulto.
3. Como usar BELKYRA
Como é administrado BELKYRA
Belkyra é administrado diretamente debaixo da pele (“via subcutânea”) por um médico, ou nos países em que a normativa o permita, por um profissional de saúde sob a supervisão de um médico. Belkyra será injetado em pequenas quantidades em vários pontos da zona de tratamento, que é o tecido gordo diretamente debaixo da pele na zona situada debaixo da barbilla.
O seu médico pode tomar algumas medidas para aliviar a dor antes e depois da injeção.
Dose
O seu médico decidirá a quantidade de Belkyra administrada.
Serão administradas várias injeções por sessão de tratamento. O número total de injeções e as sessões de tratamento necessárias para alcançar uma resposta satisfatória dependerão das suas necessidades individuais e serão decididos pelo seu médico. O tratamento pode ser repetido várias vezes, mas não devem ser ultrapassadas as 6 sessões de tratamento, sendo normalmente suficientes entre 2 e 4 sessões. O tempo transcorrido entre sessões de tratamento deve ser de pelo menos 4 semanas.
Se lhe foi administrado mais BELKYRA do que o deve
Se lhe foi administrado mais Belkyra do que o recomendado, podem aumentar os efeitos adversos locais (ver secção 4). Neste caso, consulte o seu médico ou enfermeiro.
No final deste prospecto, é fornecida mais informação sobre o uso e a manipulação pelo médico ou profissional de saúde..
Se tiver alguma outra dúvida sobre o uso deste medicamento, pergunte ao seu médico ou enfermeiro.
4. Possíveis efeitos adversos
Como todos os medicamentos, este medicamento pode produzir efeitos adversos, embora nem todas as pessoas os sofram.
- Pode ocorrer uma lesão temporária do nervo da mandíbula, o que pode dar origem a uma sorriso assimétrica ou a fraqueza dos músculos faciais.
- Pode ocorrer um dano nos tecidos ao redor da zona tratada (ou seja, erosão cutânea, ulceração, necrose). Isso pode causar cicatrização.
Se experimentar algum dos efeitos adversos mencionados anteriormente, informe o seu médico ou enfermeiro imediatamente.
A seguir, é incluída uma lista de efeitos adversosobservados com as frequências seguintes:
Muito frequentes(podem afetar mais de 1 de cada 10 pessoas):
- Reações no local da injeção:
- dor
- retenção de líquidos no tecido (edema) e inchação
- sintomas de sensibilidade (parestesia): perda de sensibilidade, menor sensibilidade, entorpecimento, formigamento, sensibilidade incomum
- zona pequena e redonda de dureza localizada (nódulo)
- hematomas
- rigidez ou engrossamento do tecido (induração)
- vermelhidão da pele (eritema)
- coceira
Frequentes(podem afetar até 1 de cada 10 pessoas):
- Reações no local da injeção:
- hemorragia
- molestias
- calor
- mudança da cor da pele
- Lesão do nervo situado ao redor da mandíbula
- Tensão na pele
- Dificuldade para engolir (disfagia)
- Náuseas
- Dor de cabeça
Pouco frequentes(podem afetar até 1 de cada 100 pessoas):
- Sabor estranho na boca (disgeusia)
- Dificuldade para falar (disfonía)
- Reações no local da injeção:
- perda de cabelo (alopecia)
- urticária
- lesões cutâneas (úlceras)
- reação alérgica (hipersensibilidade)
- cicatriz
Frequência não conhecida(não pode ser estimada a partir dos dados disponíveis)
- Sensação reduzida ou anormal na área da boca (p. ex. lábio, língua) (hipoestesia oral, parestesia oral).
- Reação no local de injeção (ver “Advertências e precauções”):
- diminuição da sensibilidade ao toque ou sensação alterada na bochecha.
- danos nos tecidos e morte celular (necrose) ao redor da zona tratada.
- Infecção incluindo vermelhidão, inchação ou dor (celulite) ou um acúmulo de pus (abscesso)
- lesão dos vasos sanguíneos se for injetado acidentalmente em uma artéria ou veia.
A maioria dos efeitos adversos observados melhorou durante o período de 4 semanas entre tratamentos. No entanto, algumas dessas reações no local da injeção podem prolongar-se por mais tempo.
Comunicação de efeitos adversos
Se experimentar algum tipo de efeito adverso, consulte o seu médico ou enfermeiro, mesmo que se trate de efeitos adversos que não aparecem neste prospecto. Também pode comunicá-los diretamente através do Sistema Espanhol de Farmacovigilância de medicamentos de Uso Humano: https://www.notificaram.es. Mediante a comunicação de efeitos adversos, você pode contribuir para fornecer mais informações sobre a segurança deste medicamento.
5. Conservação de BELKYRA
Mantenha este medicamento fora da vista e do alcance das crianças.
Não utilize este medicamento após a data de validade que aparece na etiqueta e na caixa após “CAD/EXP”. A data de validade é o último dia do mês que se indica.
Este medicamento não requer condições especiais de conservação. Recomenda-se utilizar a solução injetável imediatamente após a sua abertura.
Não use este medicamento se observar partículas visíveis.
6. Conteúdo do envase e informação adicional
Composição de BELKYRA
- O princípio ativo é ácido desoxicolico.
1 ml de solução injetável contém 10 mg de ácido desoxicolico. 1 frasco com 2 ml contém 20 mg de ácido desoxicolico.
- Os outros componentes são água para preparações injetáveis, cloreto de sódio, hidróxido de sódio (para dissolução e ajustar o pH), ácido clorídrico (para ajustar o pH) e hidrogenofosfato de disódio anidro.
Aspecto de BELKYRA e conteúdo do envase
Belkyra é uma solução para injeção transparente, incolor e estéril.
Tamanho do envase:
Uma caixa com 4 frascos (vidro tipo I com um fecho de borracha de clorobutilo, selo de alumínio e tampa abatível de polipropileno).
Cada frasco contém 2 ml de solução injetável.
Titular da autorização de comercialização e responsável pela fabricação
Titular da autorização de comercialização
AbbVie Spain, S.L.U.
Avenida de Burgos 91,
28050 Madrid
Espanha
Responsável pela fabricação
Almac Pharma Services, Ltd.
Seagoe Industrial Estate,
Portadown,
Craigavon,
County Armagh, BT63 5QD
Reino Unido
Allergan Pharmaceuticals International Ltd.
Clonshaugh Business & Technology Park,
Dublin 17,
D17 E400,
Irlanda
Data da última revisão deste prospecto:
Abril 2023
A informação detalhada e atualizada deste medicamento está disponível na página Web da Agência Espanhola de Medicamentos e Produtos Sanitários (AEMPS) http://www.aemps.gob.es/
--------------------------------------------------------------------------------------------------------------------
Esta informação está destinada apenas a médicos ou profissionais de saúde:
Deve-se rever visualmente a solução injetável antes do seu uso. Devem ser utilizadas apenas soluções transparentes, incolores e sem partículas visíveis.
Posologia
O volume total injetado e o número de sessões de tratamento devem ser adaptados aos objetivos de tratamento e à distribuição da gordura submentoniana de cada paciente individual.
Injetar 0,2 ml (2 mg) por ponto de injeção, com 1 cm de distância. Não se deve ultrapassar a dose máxima de 10 ml (100 mg, equivalente a 50 injeções) em uma sessão de tratamento.
Pode ser realizado um máximo de 6 sessões de tratamento, embora a maior parte dos pacientes apresente melhoria entre as sessões 2 e 4 do tratamento. O intervalo de tempo entre sessões de tratamento deve ser de pelo menos 4 semanas.
Para maior comodidade do paciente durante as injeções, podem ser administrados analgésicos orais ou AINEs, anestesia local tópica e/ou injetável (ex., lidocaína) e/ou aplicar frio com bolsas de gel congelado na zona de injeção, a critério do profissional de saúde.
Forma de administração
O produto está indicado apenas para administração subcutânea.
Belkyra é fornecido em frascos de uso único e prontos para uso. Inverta devagar o frasco várias vezes antes do seu uso e não o dilua.
Belkyra deve ser preparado para injeção da seguinte forma:
- Retire a tampa a pressão do frasco e limpe o fecho perfurável do frasco com um antiséptico. Não use se o frasco, o selo ou a tampa estiverem danificados.
- Coloque uma agulha estéril de grande calibre em uma seringa estéril descartável de 1 ml.
- Introduza a agulha estéril de grande calibre no fecho do frasco e extraia 1 ml de Belkyra na seringa de 1 ml.
- Troque a agulha de grande calibre por uma agulha de 30 G (ou inferior) de 12-13 mm. Expulse as bolhas de ar da seringa antes de injetar o produto na gordura subcutânea.
- Para extrair o conteúdo restante do frasco, repita os passos 3 e 4.
Apenas devem administrar Belkyra médicos com formação, experiência no tratamento e conhecimentos adequados da anatomia submentoniana. Nos países em que a normativa o permita, os profissionais de saúde com formação adequada podem administrar Belkyra sob a supervisão de um médico. O uso seguro e eficaz de Belkyra depende da seleção de pacientes adequada, o que inclui conhecer os antecedentes do paciente de intervenções anteriores e a possibilidade de que essas tenham alterado a anatomia cervical superficial. Deve-se ter especial precaução ao utilizar Belkyra em pacientes com excessiva laxidade cutânea, bandas platismais proeminentes ou outras condições em que uma redução da gordura submentoniana possa produzir resultados não desejados.
Introduza a agulha perpendicularmente à pele para injetar Belkyra.
A colocação da agulha em relação à mandíbula é muito importante, pois reduz a possibilidade de lesão do nervo marginal mandibular, uma ramo motora do nervo facial. Esta lesão no nervo se apresenta como uma sorriso assimétrica devido à paresia dos músculos depressores do lábio.
Para evitar a lesão do nervo marginal mandibular:
- Não injete acima do bordo inferior da mandíbula.
- Não injete em uma região definida por uma linha de 1-1,5 cm por debaixo do bordo inferior (desde o ângulo da mandíbula ao mentão).
- Injete Belkyra apenas dentro da zona de tratamento com gordura submentoniana objetivo (ver figuras 1 e 3).
Figura1. Evite a zona do nervo marginal mandibular
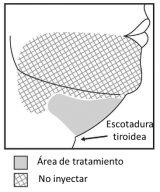
Evite injetar no músculo platisma. Antes de cada sessão de tratamento, palpe a zona submentoniana para garantir a presença de suficiente gordura submentoniana e para identificar a gordura subcutânea entre a derme e o músculo platisma (gordura pré-platisma) na zona de tratamento diana (figura 2).
Figura 2. Vista sagital da zona platismal
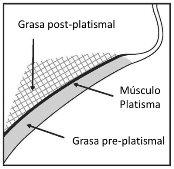
Marque a zona de tratamento planejada com um lápis cirúrgico e utilize uma plantilha de marcação de 1 cm2 para marcar os pontos de injeção (figuras 2 e 3).
Figura 3. Zona de tratamento e padrão de injeção
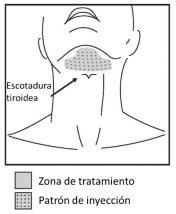
Não injete Belkyra fora dos parâmetros definidos.
Cada frasco é para um paciente único. Após o seu uso, elimine o medicamento não utilizado.
- País de registo
- Substância ativa
- Requer receita médicaSim
- Fabricante
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a BELKYRA 10 mg/ml SOLUÇÃO INJETÁVELForma farmacêutica: COMPRIMIDO, 1 mgSubstância ativa: finasterideFabricante: Industrial Farmaceutica Cantabria S.A.Requer receita médicaForma farmacêutica: SOLUÇÃO PARA USO TÓPICO, 2,275 mg/mlSubstância ativa: finasterideFabricante: Industrial Farmaceutica Cantabria S.A.Requer receita médicaForma farmacêutica: SOLUÇÃO PARA USO TÓPICO, 50 mg/mlSubstância ativa: minoxidilFabricante: Mibe Pharma Espana S.L.Não requer receita médica
Alternativas a BELKYRA 10 mg/ml SOLUÇÃO INJETÁVEL noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a BELKYRA 10 mg/ml SOLUÇÃO INJETÁVEL em Poland
Alternativa a BELKYRA 10 mg/ml SOLUÇÃO INJETÁVEL em Ukraine
Médicos online para BELKYRA 10 mg/ml SOLUÇÃO INJETÁVEL
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de BELKYRA 10 mg/ml SOLUÇÃO INJETÁVEL – sujeita a avaliação médica e regras locais.