Como usar Zivafert
folheto para o doente
Folheto incluído na embalagem: informação para o doente
Zivafert, 5000 UI
pó e solvente para solução injetável
Gonadotropina coriônica
Este medicamento está sujeito a monitorização adicional. Isso permitirá a identificação rápida de novas informações sobre a segurança.
O utilizador do medicamento também pode ajudar, relatando quaisquer efeitos adversos que ocorram após a administração do medicamento. Para saber como relatar efeitos adversos, consulte o ponto 4.
Deve ler atentamente o conteúdo do folheto antes de tomar o medicamento, pois contém informações importantes para o doente.
- Deve guardar este folheto para poder relê-lo se necessário.
- Em caso de dúvidas, deve consultar o médico ou farmacêutico.
- Este medicamento foi prescrito especificamente para si. Não o deve dar a outros. O medicamento pode prejudicar outra pessoa, mesmo que os sintomas da sua doença sejam os mesmos.
- Se o doente apresentar algum efeito adverso, incluindo quaisquer efeitos adversos não listados neste folheto, deve informar o médico ou farmacêutico.
Consulte o ponto 4.
efeitos adversos não listados neste folheto, deve informar o médico ou farmacêutico.
Consulte o ponto 4.
- Neste folheto, o medicamento Zivafert 5000 UI pó e solvente para solução injetável é designado por Zivafert.
Sumário do folheto
- 1. O que é o medicamento Zivafert e para que é utilizado
- 2. Informações importantes antes de tomar o medicamento Zivafert
- 3. Como tomar o medicamento Zivafert
- 4. Efeitos adversos possíveis
- 5. Como conservar o medicamento Zivafert
- 6. Conteúdo da embalagem e outras informações
1. O que é o medicamento Zivafert e para que é utilizado
O que é o medicamento Zivafert:
O medicamento Zivafert contém gonadotropina coriônica humana altamente purificada, um hormônio obtido
da urina humana, pertencente à família das "gonadotropinas", que são hormônios naturais
responsáveis pela reprodução e fertilidade.
Quando utilizar o medicamento Zivafert:
O medicamento Zivafert é utilizado para:
- auxiliar o desenvolvimento e amadurecimento de vários folículos (cada um contendo um óvulo) em mulheres submetidas a técnicas de reprodução assistida (procedimento que pode ajudar a engravidar), como a "fertilização in vitro”;
- auxiliar a liberação do óvulo do ovário (indução da ovulação) em mulheres que não podem produzir óvulos (""falta de ovulação") ou mulheres que produzem muito poucos óvulos (""oligo-ovulação").
Este medicamento deve ser utilizado sob supervisão médica, a menos que o médico prescreva de outra forma.
2. Informações importantes antes de tomar o medicamento Zivafert
Quando não utilizar o medicamento Zivafert:
- se o doente tiver alergia à gonadotropina coriônica humana ou a qualquer outro componente deste medicamento (listados no ponto 6);
- se o doente tiver doenças não tratadas da tireoide, pituitária ou supra-renal;
- se o doente tiver cancro do ovário, útero ou mama;
- se o doente tiver uma condição que impeça a gravidez normal, como insuficiência ovariana, falta de útero, menopausa prematura, obstrução das trompas de Falópio ou outras anormalidades dos órgãos genitais;
- se o doente tiver apresentado hemorragia vaginal inexplicada recentemente.
Deve informar o médico ou farmacêutico se o doente tiver algum dos estados acima, pois este medicamento pode não ser adequado para o doente.
Precauções e advertências
Antes de iniciar o tratamento, o médico deve verificar se os órgãos genitais do doente estão
normais.
Antes de iniciar o tratamento com o medicamento Zivafert, deve discutir com o médico se o doente tiver ou tiver tido algum dos seguintes estados:
- anormalidades dos órgãos genitais;
- doenças crônicas (como diabetes, doenças cardiovasculares, etc.);
- complicações vasculares (ou seja, aumento do risco de trombose, história de trombose no doente ou na família do doente, excesso de peso).
Exames médicos
Até 10 dias após a administração do medicamento Zivafert, o teste de gravidez pode dar um resultado falso positivo.
Durante o tratamento com o medicamento Zivafert, podem ocorrer:
Síndrome de hiperestimulação ovariana
O tratamento com hormônios gonadotrópicos, como o medicamento Zivafert, pode causar síndrome
de hiperestimulação ovariana. É uma doença grave, na qual os ovários são estimulados excessivamente,
e os folículos em desenvolvimento atingem um tamanho excessivo. Em casos raros, a síndrome de hiperestimulação ovariana grave pode ser uma ameaça à vida. Por isso, é muito importante que o doente permaneça sob supervisão médica. O médico realizará um exame de ultrassom (USG) dos ovários para verificar os efeitos do tratamento. Também pode recomendar o controle dos níveis de hormônios no sangue (consulte também o ponto 4).
Na síndrome de hiperestimulação ovariana, ocorre uma acumulação rápida de líquidos na cavidade abdominal e no tórax. Também podem se formar coágulos sanguíneos. Deve procurar imediatamente um médico se:
- apresentar inchaço abdominal e dores abdominais significativas;
- apresentar náuseas;
- apresentar vômitos;
- apresentar um aumento rápido de peso devido à acumulação de líquidos;
- apresentar diarreia;
- apresentar redução da produção de urina;
- apresentar problemas respiratórios.
Torção ovariana
A torção ovariana é uma condição na qual o ovário se torce, o que pode levar à interrupção do suprimento sanguíneo para o ovário.
Antes de iniciar o tratamento com este medicamento, deve informar o médico se:
- o doente já teve síndrome de hiperestimulação ovariana;
- o doente está grávida ou suspeita que possa estar grávida;
- o doente já teve uma operação abdominal;
- o doente já teve torção ovariana;
- o doente já teve cistos ovarianos ou ováricos.
Trombose sanguínea (trombose)
A gravidez aumenta o risco de formação de trombos sanguíneos.
Se o doente tiver fatores de risco para a formação de trombos sanguíneos (por exemplo, excesso de peso ou trombose na família do doente), o risco de formação de trombos sanguíneos em um vaso sanguíneo pode aumentar durante o tratamento com a técnica de fertilização in vitro.
A formação de trombos sanguíneos pode estar associada a doenças graves, como:
- embolia pulmonar (embolia pulmonar);
- acidente vascular cerebral;
- infarto do miocárdio;
- redução do fluxo sanguíneo para os órgãos vitais, o que pode levar à lesão dos órgãos;
- redução do fluxo sanguíneo (trombose venosa profunda) para os braços ou pernas, o que pode levar à amputação do braço ou perna.
Gravidez múltipla, defeitos congênitos, aborto ou complicações da gravidez
As gravidezes que ocorrem após o tratamento com o medicamento Zivafert são mais frequentemente gravidezes gêmeas ou múltiplas.
As gravidezes múltiplas estão associadas a um risco aumentado para a mãe e o feto durante o período perinatal.
Em mulheres em tratamento para infertilidade, há um risco ligeiramente aumentado de aborto ou gravidez ectópica (gravidez fora do útero). Por isso, o médico deve realizar um exame de ultrassom precoce para excluir a possibilidade de gravidez ectópica. O nascimento múltiplo é mais provável se o doente estiver tomando outros medicamentos que estimulam a ovulação (por exemplo, hMG).
Não se sabe se a técnica de fertilização in vitrocausa defeitos congênitos ou certos tumores dos órgãos genitais.
Crianças e adolescentes
O medicamento Zivafert não é indicado para uso em crianças e adolescentes.
Medicamento Zivafert e outros medicamentos
Deve informar o médico ou farmacêutico sobre todos os medicamentos que o doente está tomando atualmente ou recentemente, bem como sobre os medicamentos que o doente planeja tomar, incluindo todos os medicamentos disponíveis sem prescrição. Isso é especialmente importante se o doente estiver tomando medicamentos que:
- estimulam a ovulação (por exemplo, hMG);
- contêm cortisona, especialmente em doses altas.
Gravidez e amamentação
Não deve tomar o medicamento Zivafert se estiver grávida ou amamentando. Se o doente suspeitar que possa estar grávida, deve consultar o médico antes de tomar este medicamento.
Condução de veículos e operação de máquinas
O medicamento Zivafert não afeta a capacidade de conduzir veículos ou operar máquinas.
Medicamento Zivafert contém sódio
Este medicamento contém menos de 1 mmol de sódio (23 mg) por injeção, ou seja, o medicamento é considerado "livre de sódio".
3. Como tomar o medicamento Zivafert
O medicamento Zivafert é um pó que deve ser dissolvido em líquido (solvente) antes de ser administrado; é
administrado por injeção subcutânea ou intramuscular. A solução é obtida misturando o solvente com o pó e deve ser utilizada imediatamente após a preparação.
Este medicamento deve ser sempre utilizado de acordo com as recomendações do médico. Em caso de dúvidas, deve consultar o médico ou farmacêutico.
Método de administração
Como administrar o medicamento Zivafert:
O medicamento Zivafert é administrado por injeção subcutânea ou intramuscular.
Cada frasco deve ser utilizado apenas uma vez, e a injeção deve ser administrada imediatamente após a preparação da solução.
A dose recomendada de medicamento Zivafert é de 5 000 UI ou 10 000 UI. O medicamento deve ser administrado dentro de 24-48 horas após a obtenção da estimulação óptima do crescimento dos folículos.
Após aconselhamento e treinamento adequados, o médico pode recomendar que o doente administre o medicamento Zivafert sozinho.
Antes da primeira administração do medicamento sozinho, o médico:
- explicará como preparar a dose correta do medicamento;
- mostrará como preparar a solução para injeção;
- mostrará os locais possíveis para a injeção;
- permitirá que o doente pratique a administração da injeção subcutânea.
Antes de administrar o medicamento Zivafert sozinho, deve ler atentamente as instruções abaixo.
Como preparar a solução do medicamento Zivafert a partir de 1 frasco de pó:
A solução deve ser preparada imediatamente antes da injeção. Cada frasco é destinado a um uso único.
O medicamento Zivafert só pode ser preparado com o solvente fornecido na embalagem, de acordo com as seguintes instruções:
Passo 1
Lavar as mãos antes de preparar a solução. Utilizar uma superfície limpa para preparar a solução. É importante que as mãos e os objetos utilizados estejam o mais limpos possível.
Passo 2
Colocar os seguintes objetos em uma superfície limpa:
- dois algodões embebidos em álcool (não incluídos no kit);
- um frasco contendo o pó do medicamento Zivafert;
- um solvente em uma seringa-ampola;
- uma agulha longa para reconstituição e injeção intramuscular;
- uma agulha curta para injeção subcutânea.
Passo 3
- Remover apenas a tampa da seringa-ampola.
- Colocar a agulha para reconstituição (agulha longa) com a tampa de proteção na seringa e verificar se a agulha está bem encaixada para evitar vazamento da solução. Se ocorrer vazamento, tente ajustar a agulha, girando-a ligeiramente.
- Colocar a seringa cuidadosamente em uma superfície limpa.
- Evitar tocar a agulha.
Passo 4
- Remover a tampa colorida de plástico do frasco do medicamento Zivafert, pressionando-a suavemente para cima.
- Limpar a parte superior de borracha do frasco com um algodão embebido em álcool e deixar secar.
Passo 5
- Pegar a seringa, remover a tampa de proteção da agulha e perfurar a agulha através do centro de borracha da parte superior do frasco do medicamento Zivafert.
- Pressionar firmemente o êmbolo e injetar lentamente o solvente no frasco com o pó para injetar toda a solução no frasco com o pó.
- NÃO AGITE, gire suavemente o frasco nas mãos até que o pó seja completamente dissolvido, evitando a formação de espuma.
Passo 6
Após a dissolução do pó (o que geralmente ocorre imediatamente), retire lentamente a solução para a seringa, como descrito abaixo:
- Deixar a agulha inserida, virar o frasco de cabeça para baixo.
- Certificar-se de que a ponta da agulha está abaixo do nível do líquido.
- Puxar suavemente o êmbolo para retirar toda a solução do medicamento Zivafert para a seringa.
- Verificar se a solução reconstituída é transparente e incolor.
Preparação de doses maiores utilizando mais de 1 frasco de pó:
Se o médico prescrever uma dose maior de medicamento - 10 000 UI, isso pode ser alcançado usando dois
frascos de pó e uma seringa-ampola com solvente.
Ao preparar 2 frascos do medicamento Zivafert, no final do passo 3 acima, retire o conteúdo reconstituído do primeiro frasco para a seringa e injete lentamente no segundo frasco.
Repita os passos 4 a 6 para o segundo frasco.
A solução deve ser transparente e incolor.
Injeção intramuscular:
No caso de injeção intramuscular, o médico ou enfermeiro preparará e, em seguida, administrará o medicamento Zivafert no quadril ou nádega.
Injeção subcutânea:
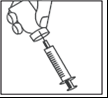
- Quando a seringa contiver a dose correta, colocar a tampa de proteção da agulha longa. Remover a agulha longa da seringa e substituí-la pela agulha curta para injeção subcutânea com a tampa de proteção colocada. Verificar se a agulha está bem encaixada e pressionar firmemente a agulha curta no cilindro da seringa e, em seguida, girá-la ligeiramente para garantir que esteja completamente encaixada, para evitar vazamento da solução.
- Remover a tampa de proteção da agulha. Segurar a seringa com a agulha apontando para cima e bater suavemente na lateral da seringa para fazer com que quaisquer bolhas de ar subam.
- Pressionar o êmbolo até que uma gota de líquido apareça na ponta da agulha.
- NÃO USE a solução se contiver quaisquer partículas ou estiver turva.
- O médico ou enfermeiro aconselhará sobre o local do corpo para administrar o medicamento. Os locais típicos são os quadris ou a área abdominal (abaixo do umbigo).
- Limpar o local da injeção com um algodão embebido em álcool.
- Segurar firmemente a pele. Com a outra mão, inserir a agulha com um movimento firme em um ângulo de 45° ou 90°.
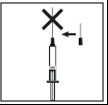
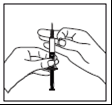
Local da injeção:
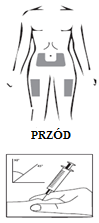
Injeção da solução:
- A solução deve ser injetada sob a pele de acordo com as recomendações do médico.
- Não injetar a solução diretamente na veia.
- Pressionar lentamente o êmbolo para que a solução seja injetada corretamente e os tecidos da pele não sejam danificados.
Dedique o tempo necessário para injetar o volume prescrito da solução.
Remoção da agulha:
- Retirar rapidamente a seringa e pressionar o local da injeção.
- Massagear suavemente o local da injeção - enquanto mantém a pressão - para ajudar a distribuir a solução do medicamento Zivafert e aliviar o desconforto.
Remoção de todos os itens usados:
Após a injeção, todos os objetos usados, incluindo agulhas e seringas vazias, devem ser descartados em um recipiente apropriado. Qualquer solução não utilizada ou resíduos devem ser eliminados de acordo com as regulamentações locais.
Uso de dose maior do que a recomendada do medicamento Zivafert
Os efeitos de superdose do medicamento Zivafert não são conhecidos, no entanto, pode-se esperar a ocorrência de síndrome de hiperestimulação ovariana (consulte "Efeitos adversos possíveis"). Se uma dose maior do que a recomendada do medicamento Zivafert for administrada, deve-se entrar em contato com o médico ou farmacêutico.
Omissão da administração do medicamento Zivafert
Se o doente esquecer de administrar uma dose do medicamento Zivafert, deve entrar em contato com o médico imediatamente.
Interrupção do tratamento com o medicamento Zivafert
Se o doente não pretende continuar tomando o medicamento, deve consultar o médico.
Em caso de dúvidas adicionais sobre o uso deste medicamento, deve consultar o médico ou farmacêutico.
4. Efeitos adversos possíveis
Como qualquer medicamento, este medicamento pode causar efeitos adversos, embora não todos os doentes os apresentem.
Em caso de ocorrência de algum dos seguintes efeitos adversos graves, deve interromper o tratamento com o medicamento Zivafert e procurar imediatamente um médico - pode ser necessária assistência médica de emergência:
- Estimulação ovariana excessiva leve ou moderada (síndrome de hiperestimulação ovariana), que se manifesta como aumento do tamanho dos ovários, cistos ovarianos, dor abdominal com vômitos e náuseas (consulte também o ponto 2. "Síndrome de hiperestimulação ovariana"). É um efeito adverso comum (pode ocorrer em até 1 em cada 10 doentes).
- Estimulação ovariana excessiva grave caracterizada por dor na parte inferior do abdômen (pélvis), náuseas, vômitos, aumento de peso, acumulação de líquidos na cavidade abdominal ou tórax (derrame pleural). É um efeito adverso incomum (pode ocorrer em até 1 em cada 100 doentes).
- Ruptura de cisto ovariano (como uma complicação rara da síndrome de hiperestimulação ovariana grave, pode ocorrer em até 1 em cada 1 000 doentes).
- Formação de coágulos sanguíneos nos vasos sanguíneos (eventos tromboembólicos), como uma complicação da síndrome de hiperestimulação ovariana. É um efeito adverso raro (pode ocorrer em até 1 em cada 1 000 doentes).
- Reações alérgicas graves generalizadas, que podem incluir: inchaço do rosto, olhos, lábios, garganta ou língua, dificuldade para respirar, respiração sibilante, erupção cutânea. É um efeito adverso raro (pode ocorrer em até 1 em cada 1 000 doentes).
Outros efeitos adversos:
Efeitos adversos comuns(podem ocorrer em até 1 em cada 10 doentes):
- reação no local da injeção, que pode incluir vermelhidão, equimose, inchaço, coceira ou dor no local da injeção;
- inchaço;
- mudanças de humor;
- dor de cabeça;
- dor nas mamas.
Efeitos adversos incomuns(podem ocorrer em até 1 em cada 100 doentes):
- ansiedade (agitação);
- fadiga.
Efeitos adversos raros(podem ocorrer em até 1 em cada 1 000 doentes):
- inchaço na pele profunda, frequentemente com urticária;
- erupções cutâneas generalizadas.
Se ocorrer algum dos efeitos adversos raros listados acima, deve procurar imediatamente um médico, que avaliará se é necessário interromper o tratamento com o medicamento Zivafert ou procurar atendimento médico de emergência.
Notificação de efeitos adversos
Se ocorrer algum efeito adverso, incluindo quaisquer efeitos adversos não listados neste folheto, deve informar o médico ou farmacêutico. Os efeitos adversos podem ser notificados diretamente ao Departamento de Monitoramento de Efeitos Adversos de Medicamentos do Ministério da Saúde:
Rua X, nº Y, 1000-000 Lisboa,
Telefone: +351 21 123 4567,
Fax: +351 21 123 4568,
Sítio da internet: https://www.infomed.pt .
Os efeitos adversos também podem ser notificados ao titular da autorização de comercialização.
A notificação de efeitos adversos permitirá a coleta de mais informações sobre a segurança do medicamento.
5. Como conservar o medicamento Zivafert
O medicamento deve ser conservado em local não visível e inacessível a crianças.
Não conservar a uma temperatura superior a 25°C. Conservar o frasco e a seringa-ampola com solvente na embalagem exterior para proteger da luz.
A solução deve ser utilizada imediatamente após a preparação.
Não utilize este medicamento após o prazo de validade impresso na caixa, frasco, seringa-ampola com solvente após: VAL. Se a data de validade for indicada como mês/ano, o prazo de validade é o último dia do mês indicado.
Não utilize este medicamento se verificar que a solução não é transparente (turva ou contém partículas visíveis). Após a reconstituição, a solução deve ser transparente e incolor.
Os medicamentos não devem ser jogados na canalização. Deve perguntar ao farmacêutico como eliminar os medicamentos que não são mais necessários. Essa ação ajudará a proteger o meio ambiente.
6. Conteúdo da embalagem e outras informações
O que contém o medicamento Zivafert
- O princípio ativo do medicamento é a gonadotropina coriônica humana.
- Os outros componentes são:
- frasco de pó: lactose monoidratada;
- seringa-ampola com solvente (solução de cloreto de sódio a 0,9%): água para injeção, cloreto de sódio.
Cada frasco contém: gonadotropina coriônica humana 5000 UI, obtida da urina humana.
Como é o medicamento Zivafert e que conteúdo tem a embalagem
O medicamento Zivafert é apresentado como:
Pó em frasco: pó liofilizado branco ou quase branco.
Solvente em seringa-ampola (solução de cloreto de sódio a 0,9%): solução transparente e incolor.
Uma embalagem única contém:
Um suporte de plástico contendo o pó em frasco de vidro tipo I, fechado com uma tampa de borracha de bromobutilo com uma tampa de alumínio do tipo flip-off.
1 ml de solvente em seringa-ampola de vidro tipo I com uma tampa de borracha de clorobutilo (que também serve como êmbolo) e 1 agulha para injeção intramuscular e 1 agulha para injeção subcutânea.
A embalagem coletiva (10+10) contém 10 suportes de plástico, como descrito acima.
Nem todos os tamanhos de embalagem podem estar disponíveis.
Titular da autorização de comercialização e fabricante
Titular da autorização de comercialização:
IBSA Farmaceutici Italia s.r.l.
Via Martiri di Cefalonia 2
26900 Lodi
Itália
[email protected]
Importador:
IBSA Farmaceutici Italia srl
Via Martiri di Cefalonia 2
26900 Lodi
Itália
Este medicamento está autorizado para comercialização nos países membros da Área Econômica Europeia sob as seguintes denominações:
AT:
Zivafert
DK:
Gonasi Set
CZ:
Zivafert
EL:
Zivafert
ES:
Gonasi Kit
FI:
Gonasi Set
FR:
GONADOTROPHINE CHORIONIQUE IBSA
HU:
Zivafert Kit
NL:
Gonasi
NO:
Gonasi Set
PL:
Zivafert
SE:
Gonasi Set
SK:
Gonasi Kit
Data da última atualização do folheto:janeiro de 2025
- País de registo
- Substância ativa
- Requer receita médicaSim
- ImportadorIBSA Farmaceutici Italia S.r.l.
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a ZivafertForma farmacêutica: Pó, 1500 UISubstância ativa: chorionic gonadotrophinFabricante: Ferring GmbHRequer receita médicaForma farmacêutica: Pó, 5000 UISubstância ativa: chorionic gonadotrophinFabricante: Ferring GmbHRequer receita médicaForma farmacêutica: Pó, 75 UISubstância ativa: urofollitropinRequer receita médica
Alternativas a Zivafert noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a Zivafert em Ukraine
Alternativa a Zivafert em Spain
Médicos online para Zivafert
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de Zivafert – sujeita a avaliação médica e regras locais.