
Como usar Mirelez
Folheto informativo: informação para o utilizador
Myrelez, 60 mg, solução injectável em seringa pré-cheia
Myrelez, 90 mg, solução injectável em seringa pré-cheia
Myrelez, 120 mg, solução injectável em seringa pré-cheia
Lanreotida
Deve ler atentamente o conteúdo do folheto antes de tomar o medicamento, pois contém informações importantes para o paciente.
- Deve guardar este folheto para poder relê-lo se necessário.
- Em caso de dúvidas, deve consultar o médico, farmacêutico ou enfermeiro.
- Este medicamento foi prescrito especificamente para si. Não o deve dar a outros. O medicamento pode ser prejudicial a outra pessoa, mesmo que os sintomas da sua doença sejam os mesmos.
- Se o paciente apresentar algum efeito não desejado, incluindo quaisquer efeitos não desejados não mencionados neste folheto, deve informar o médico, farmacêutico ou enfermeiro. Ver ponto 4.
Índice do folheto
- 1. O que é o medicamento Myrelez e para que é utilizado
- 2. Informações importantes antes de tomar o medicamento Myrelez
- 3. Como tomar o medicamento Myrelez
- 4. Efeitos não desejados
- 5. Como conservar o medicamento Myrelez
- 6. Conteúdo do pacote e outras informações
1. O que é o medicamento Myrelez e para que é utilizado
O medicamento Myrelez contém a substância ativa lanreotida, que pertence a um grupo de medicamentos chamados hormônios inibidores do crescimento. É semelhante a outra substância (hormônio) chamada somatostatina.
Lanreotida causa uma redução na atividade de hormônios como o GH (hormônio do crescimento) e o fator de crescimento semelhante à insulina (IGF-1) e inibe a libertação de alguns hormônios do trato gastrointestinal e a secreção intestinal. Também tem um efeito sobre alguns tipos avançados de tumores (chamados tumores neuroendócrinos) que ocorrem no trato gastrointestinal e no pâncreas, através da inibição ou retardamento do seu crescimento.
Para que é utilizado o medicamento Myrelez:
- no tratamento de pacientes com acromegalia (uma condição em que o corpo produz demasiado hormônio do crescimento);
- no alívio dos sintomas como ondas de calor e diarreia, que podem ocorrer em pacientes com tumores neuroendócrinos (tumores NET);
- no tratamento e inibição do crescimento de alguns tumores avançados que ocorrem no trato gastrointestinal e no pâncreas, chamados tumores neuroendócrinos gastroenteropancreáticos (GEP-NET) - quando não podem ser removidos cirurgicamente.
2. Informações importantes antes de tomar o medicamento Myrelez
Quando não tomar o medicamento Myrelez:
- se o paciente tiver alergia (hipersensibilidade) à lanreotida, somatostatina ou medicamentos da mesma classe (análogos da somatostatina), ou a qualquer um dos outros componentes do medicamento (listados no ponto 6).
Precauções e advertências
Antes de começar a tomar o medicamento Myrelez, deve discutir com o médico, farmacêutico ou enfermeiro:
- se o paciente tiver diabetes, pois a lanreotida pode causar flutuações nos níveis de açúcar no sangue. Durante o tratamento com o medicamento Myrelez, o médico pode recomendar a verificação dos níveis de açúcar no sangue e, possivelmente, alterar o esquema de tratamento da diabetes;
- se o paciente tiver cálculos biliares, pois o medicamento Myrelez pode favorecer a formação de cálculos na vesícula biliar. Nesse caso, é recomendável realizar exames periódicos. Se ocorrerem complicações de cálculos biliares, o médico pode decidir interromper o tratamento com a lanreotida.
- se o paciente tiver distúrbios da tireoide, pois a lanreotida pode afetar ligeiramente a função da tireoide;
- se o paciente tiver distúrbios cardíacos, pois durante o tratamento com o medicamento Myrelez pode ocorrer bradicardia sinusal (batimento cardíaco lento). Em pacientes com bradicardia, deve-se ter cuidado ao iniciar o tratamento com o medicamento Myrelez.
Se o paciente apresentar algum dos estados mencionados acima, antes de iniciar o tratamento com o medicamento Myrelez, deve discutir com o médico ou farmacêutico.
Crianças
Não se recomenda o uso do medicamento Myrelez em crianças.
Myrelez e outros medicamentos
Deve informar o médico ou farmacêutico sobre todos os medicamentos que está a tomar atualmente ou recentemente, bem como sobre os medicamentos que planeia tomar.
Deve ter cuidado especial ao tomar os seguintes medicamentos:
- ciclosporina(medicamento que reduz a resposta do sistema imunológico e é usado, por exemplo, após transplantação ou em caso de doença autoimune);
- bromocriptina(agonista dos receptores da dopamina, usado no tratamento de tumores da hipófise e doença de Parkinson ou para inibir a lactação);
- medicamentos que causam bradicardia(medicamentos que reduzem a frequência cardíaca, como os beta-bloqueadores).
O médico pode considerar a necessidade de ajustar a dosagem desses medicamentos.
Gravidez e amamentação
Se a paciente estiver grávida ou a amamentar, suspeitar que possa estar grávida ou planejar ter um filho, deve consultar o médico ou farmacêutico antes de tomar este medicamento.
Nestes casos, o medicamento Myrelez só será utilizado se houver uma necessidade clara.
Condução de veículos e operação de máquinas
É pouco provável que o medicamento Myrelez afete a capacidade de conduzir veículos ou operar máquinas, mas durante o tratamento com o medicamento Myrelez podem ocorrer efeitos não desejados como tontura. Se ocorrerem tais sintomas, deve-se ter cuidado ao conduzir veículos ou operar máquinas.
3. Como tomar o medicamento Myrelez
Este medicamento deve ser sempre tomado de acordo com as recomendações do médico ou farmacêutico. Em caso de dúvida, deve consultar o médico ou farmacêutico.
Dosagem recomendada
Tratamento da acromegalia
A dosagem recomendada é de uma injeção do medicamento a cada 28 dias. A dosagem do medicamento a ser injetada será escolhida pelo médico entre as três forças do medicamento Myrelez (60, 90, 120 mg).
Se for obtida a resposta desejada, o médico pode recomendar a alteração da frequência de administração das injeções do medicamento Myrelez 120 mg para uma injeção a cada 42 ou 56 dias. Qualquer alteração da dosagem dependerá dos sintomas e da resposta do paciente ao tratamento.
O médico também decidirá sobre a duração do tratamento.
Alívio dos sintomas (como ondas de calor e diarreia) associados a tumores neuroendócrinos
A dosagem recomendada é de uma injeção do medicamento a cada 28 dias. A dosagem do medicamento a ser injetada será escolhida pelo médico entre as três forças do medicamento Myrelez (60, 90, 120 mg).
Se for obtida a resposta desejada, o médico pode recomendar a alteração da frequência de administração das injeções do medicamento Myrelez 120 mg para uma injeção a cada 42 ou 56 dias.
O médico também decidirá sobre a duração do tratamento.
Tratamento de tumores avançados que ocorrem no trato gastrointestinal e no pâncreas, chamados tumores neuroendócrinos gastroenteropancreáticos (GEP-NET). O medicamento é utilizado quando esses tumores não podem ser removidos cirurgicamente
A dosagem recomendada é de 120 mg a cada 28 dias. O médico decidirá sobre a duração do tratamento com o medicamento Myrelez para inibir o tumor.
Método de administração
O medicamento Myrelez deve ser administrado por injeção subcutânea profunda.
Se a injeção for realizada por um profissional de saúde ou por uma pessoa treinada (membro da família ou amigo), a injeção deve ser administrada no quadrante superior externo da nádega.
Se a injeção for autoadministrada, após treinamento adequado, a injeção deve ser administrada na parte superior externa da coxa.
A decisão sobre a autoadministração ou administração por outra pessoa treinada é tomada pelo médico.
INSTRUÇÕES DE MANUSEIO
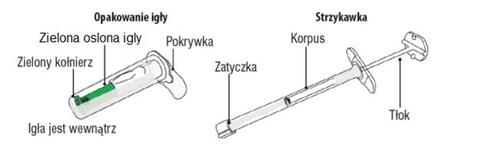
A. Conteúdo da caixa
Abaixo está descrito o procedimento para realizar a injeção do medicamento Myrelez.
Deve ler atentamente as instruções antes de realizar a injeção
O conteúdo da seringa é uma fase semi-sólida com aparência gelatinosa, propriedades adesivas e cor branca a amarelo-clara. A solução supersaturada também pode conter microbolhas, que podem desaparecer durante a injeção. Essas diferenças são normais e não afetam a qualidade do produto.
B. Antes de começar
B1. Retirar o medicamento Myrelez da geladeira 30 minutos antes de realizar a injeção. O saco laminado deve ser aberto imediatamente antes da injeção.
B2. Antes de abrir o saco, deve verificar a integridade do pacote e a data de validade do medicamento.
A data de validade está impressa no saco e na caixa. – Não deve usar o medicamento após o término da validade ou se o saco estiver danificado.
B3. Antes de começar, deve lavar as mãos com sabão e enxugá-las.
B4. Certificar-se de que a superfície para preparar a injeção está limpa.
B5. Escolher o local da injeção – os locais estão descritos abaixo
B6. Deve lembrar de limpar o local da injeção.
B7. Abrir o saco e retirar a seringa.
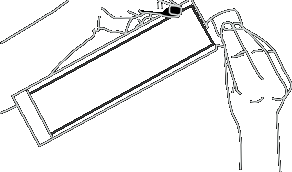
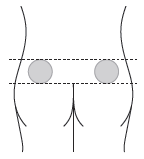
Para injeção em outra pessoa: deve
injetar no quadrante superior externo da
nádega.
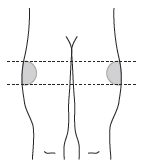
Para autoinjeção: deve
injetar na parte superior externa da coxa.
O local da injeção do medicamento Myrelez deve ser alterado a cada administração, injetando alternadamente de um lado e de outro.
C. Preparação da seringa
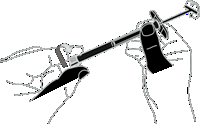
C1: Remover a tampa da seringa
Segurar firmemente o corpo da
seringa (não o êmbolo).
Com a outra mão, remover a tampa, girando-a.
C2: Abrir o pacote da agulha.
Segurar o pacote da agulha
e puxar a tampa.
Atenção: Não deve tocar na extremidade aberta
do pacote da agulha. Ela deve permanecer
limpa.
C3: Inserir a extremidade da seringa no pacote da agulha aberto.
Segurar o pacote da agulha com
uma mão.
Com a outra mão, segurar firmemente o corpo
da seringa (não o êmbolo)e girar até que
a conexão entre a seringa e a agulha esteja
totalmente bloqueada.


O bloqueio total da conexão ocorre quando não for mais possível girar.
Importante: Deve apertar firmemente a seringa,
para evitar que o medicamento vaze.
C4: Retirar a agulha do pacote
Segurar o corpo da seringa
(não o êmbolo).
Retirar a agulha diretamente do pacote sem girá-la
ou torcê-la, para garantir que a seringa esteja bem conectada
à agulha segura.
Atenção: A partir deste estágio, a agulha está parcialmente
exposta.
NUNCA DEVE TOCAR OU TENTAR ABRIR A
PROTEÇÃO VERDE DA AGULHA .
A PROTEÇÃO VERDE DA AGULHA NÃO é uma tampa removível ou um estojo para a agulha.
A PROTEÇÃO VERDE DA AGULHA é ativada automaticamente durante a injeção.
A PROTEÇÃO VERDE DA AGULHA cobre automaticamente a agulha e bloqueia-a após a injeção.
A PROTEÇÃO VERDE DA AGULHA é um mecanismo de segurança automático.
D. Realização da injeção


D1: Posicionar a seringa
Os locais para realizar as injeções estão descritos na parte B.
Puxar a pele ao redor do local da injeção com o polegar e o dedo indicador, para que fique esticada e plana.
Com a outra mão, segurar a parte inferior do
corpo da seringa (não o êmbolo).
Posicionar a seringa em um ângulo de 90° em relação à pele.
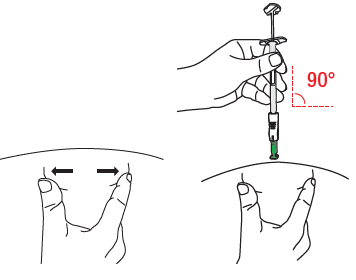
D2: Inserir a agulha
Sem criar um dobra na pele ou apertar
a pele no local da injeção,
empurrar firmemente a agulha até a pele.
Ocorrerá o recuo da proteção verde da agulha
e a ativação do mecanismo de segurança.
Continuar até que apenas o colarinho verde da proteção da agulhaseja visível.
Não deveempurrar o êmbolo neste estágio. Na próxima etapa, por favor, segure a seringa nesta posição.
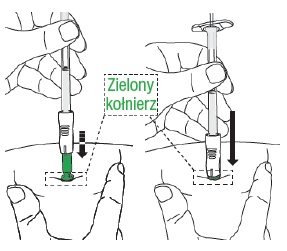
D3: Empurrar o êmbolo da seringa
Mover a mão da pele para o êmbolo.
Devagarempurrar o êmbolo, até que sua
extremidade toque o corpo da seringa
(é mais fácil empurrar o êmbolo com a mão dominante).
Isso deve levar cerca de 20 segundos.
E. Retirar e descartar a seringa
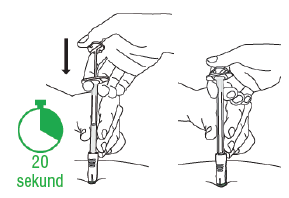
E1: Retirar da pele
Levantar a seringa para cima
e afastá-la do corpo do paciente.
A proteção verde da agulha cobre a agulha.
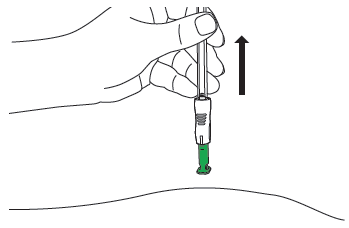
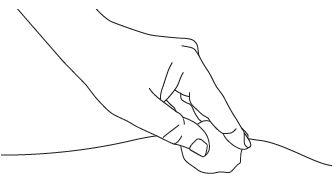
E2: Pressionar suavemente
Pressionar suavemente o local da injeção com um
algodão seco ou gaze estéril, para evitar sangramento.
Após a administração do medicamento, não devefriccionar ou massagear o local da injeção.
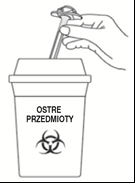
E3: Descartar
A seringa usada e a agulha devem ser descartadas
de acordo com as regulamentações locais ou
instruções do médico.
As agulhas não são reutilizáveis.
Não devedescartar a seringa ou a agulha no lixo doméstico.
Uso de dose maior do que a recomendada do medicamento Myrelez
Se ocorrer a injeção de uma dose maior do que a recomendada do medicamento Myrelez, deve informar o médico.
Se ocorrer a injeção de uma dose maior do que a recomendada do medicamento Myrelez, existe o risco de ocorrência de efeitos não desejados adicionais ou mais intensos (ver ponto 4. Efeitos não desejados).
Omissão da administração do medicamento Myrelez
Se o paciente perceber que omitiu uma injeção, deve entrar em contato com o seu médico, que fornecerá informações sobre o prazo para a próxima administração do medicamento. Não deve autoadministrar injeções adicionais para compensar a dose omitida sem discutir com o médico.
Interrupção do tratamento com o medicamento Myrelez
A omissão de mais de uma dose ou a interrupção prematura do tratamento com o medicamento Myrelez pode afetar a eficácia da terapia. Deve consultar o médico antes de interromper o tratamento com o medicamento.
Em caso de dúvidas adicionais sobre o uso deste medicamento, deve consultar o médico ou farmacêutico.
4. Efeitos não desejados
Como qualquer medicamento, este medicamento pode causar efeitos não desejados, embora não ocorram em todos.
Se o paciente apresentar algum dos seguintes efeitos não desejados, deve entrar em contato imediatamente com o médico:
- aumento da sede ou fadiga e secura na boca. Isso pode indicar que o paciente tem níveis elevados de açúcar no sangue ou está desenvolvendo diabetes;
- fome, tremores, suor excessivo ou confusão - podem ser sintomas de baixos níveis de açúcar no sangue. Esses efeitos não desejados são comuns, podem ocorrer em 1 de cada 10 pessoas.
Deve entrar em contato imediatamente com o médico se o paciente notar:
- vermelhidão ou inchaço no rosto, erupções ou rash,
- pressão no peito, falta de ar ou respiração sibilante,
- tontura, que pode ser causada por uma queda na pressão arterial. Esses efeitos não desejados podem ser sintomas de uma reação alérgica. A frequência de ocorrência desses efeitos não desejados não é conhecida; não pode ser estimada com base nos dados disponíveis.
Outros efeitos não desejados
Se o paciente apresentar algum dos seguintes efeitos não desejados, deve informar o médico ou farmacêutico.
Os efeitos não desejados mais comuns que podem ocorrer durante o tratamento com o medicamento Myrelez incluem distúrbios do trato gastrointestinal, distúrbios da vesícula biliar e reações no local da injeção. Abaixo estão listados os efeitos não desejados relacionados ao uso do medicamento Myrelez, incluindo a frequência de ocorrência.
Muito comuns: podem ocorrer em mais de 1 de cada 10 pacientes tratados:
- diarreia, fezes soltas, dor abdominal
- cálculos biliares e distúrbios da vesícula biliar, podem ocorrer dor abdominal forte e súbita, febre alta, icterícia (amarelamento da pele e olhos), calafrios, perda de apetite, coceira na pele.
Comuns: podem ocorrer em 1 de cada 10 pessoas:
- perda de peso,
- falta de energia,
- batimento cardíaco lento,
- sentimento de fadiga intensa,
- diminuição do apetite,
- fraqueza geral,
- excesso de gordura nas fezes,
- tontura e dor de cabeça,
- perda de cabelo ou menor crescimento do cabelo no corpo,
- dor muscular, nos tendões, ligamentos e ossos,
- reações no local da injeção, como dor ou endurecimento da pele,
- anomalias nos exames de função hepática e pancreática e alterações nos níveis de açúcar no sangue,
- náuseas, vômitos, constipação, flatulência ou desconforto abdominal, dispepsia,
- alargamento dos ductos biliares (aumento dos ductos biliares entre o fígado e a vesícula biliar e o intestino). Pode ocorrer dor abdominal, náuseas, icterícia e febre.
Não muito comuns: podem ocorrer em 1 de cada 100 pessoas:
- ondas de calor,
- dificuldade para dormir,
- alteração da cor das fezes,
- alterações nos níveis de sódio e fosfatase alcalina nos exames de sangue.
Frequência desconhecida: a frequência não pode ser estimada com base nos dados disponíveis:
- dor abdominal súbita e intensa - pode ser um sintoma de pancreatite,
- abscesso no local da injeção, que pode parecer cheio de líquido quando pressionado (vermelhidão, dor, calor e inchaço, podem estar associados à febre),
- colecistite (inflamação da vesícula biliar) - podem ocorrer sintomas de dor abdominal forte e súbita, febre alta, calafrios, perda de apetite, náuseas, vômitos e icterícia,
- dor abdominal na parte superior direita, febre, calafrios, icterícia, náuseas, vômitos, fezes escuras, urina escura, fadiga - podem ser sintomas de inflamação dos ductos biliares (colangite).
Como a lanreotida pode causar flutuações nos níveis de açúcar no sangue, o médico pode recomendar a verificação regular dos níveis de açúcar no sangue, especialmente no início do tratamento.
Da mesma forma, devido à possibilidade de ocorrência de distúrbios da vesícula biliar durante o tratamento com o medicamento Myrelez, o médico pode recomendar a verificação regular da vesícula biliar no início do tratamento e, subsequentemente, em intervalos de tempo determinados.
Se ocorrer algum dos efeitos não desejados mencionados acima, deve informar o médico ou farmacêutico
Notificação de efeitos não desejados
Se ocorrerem algum dos efeitos não desejados, incluindo quaisquer efeitos não desejados não mencionados neste folheto, deve informar o médico, farmacêutico ou enfermeiro. Os efeitos não desejados podem ser notificados diretamente ao Departamento de Monitoramento de Efeitos Não Desejados de Produtos Farmacêuticos da Agência Reguladora de Produtos Farmacêuticos, Dispositivos Médicos e Produtos Biocidas: Al. Jerozolimskie 181C, 02-222 Varsóvia
Tel.: +48 22 49 21 301
Fax: +48 22 49 21 309
Sítio na Internet: https://smz.ezdrowie.gov.pl
Os efeitos não desejados também podem ser notificados ao responsável pelo produto.
A notificação de efeitos não desejados permitirá a coleta de mais informações sobre a segurança do medicamento.
5. Como conservar o medicamento Myrelez
O medicamento deve ser conservado em um local não visível e inacessível às crianças.
Não use este medicamento após a data de validade impressa na caixa e na etiqueta após "Data de validade (EXP)". A data de validade refere-se ao último dia do mês indicado.
Após a abertura do saco de proteção de alumínio, o medicamento deve ser administrado imediatamente.
O medicamento Myrelez deve ser conservado na geladeira a uma temperatura entre 2°C e 8°C, no pacote original, para proteger da luz.
Após a retirada da geladeira, o produto pode ser armazenado em temperatura ambiente (below 40°C) por um período máximo de 72 horas, desde que o medicamento tenha sido armazenado em temperatura ambiente por um período total não superior a 72 horas.
Cada seringa é embalada individualmente.
Os medicamentos não devem ser descartados no sistema de esgoto ou em recipientes de lixo doméstico. Deve perguntar ao farmacêutico como descartar os medicamentos que não são mais necessários. Esse procedimento ajudará a proteger o meio ambiente.
6. Conteúdo do pacote e outras informações
O que contém o medicamento Myrelez
- A substância ativa é a lanreotida (em doses de 60 mg, 90 mg ou 120 mg)
- Outros componentes: água para injeção, ácido acético glacial (para ajustar o pH)
Como é o medicamento Myrelez e que conteúdo tem o pacote
Myrelez é uma solução injetável viscosa em uma seringa de plástico transparente com capacidade de 0,5 ml, com um dispositivo de segurança para a agulha. Tem uma consistência semi-sólida e cor branca a amarelo-clara.
Cada seringa é embalada em um saco de alumínio e uma caixa de cartão.
Tamanhos do pacote:
1 caixa contendo uma seringa de 0,5 ml com uma agulha segura (1,2 mm x 20 mm),
embaladas juntas.
1 pacote coletivo com 3 caixas, cada uma contendo uma seringa de 0,5 ml com uma agulha segura (1,2 mm x 20 mm) embaladas juntas.
Nem todos os tamanhos de pacote podem estar disponíveis no mercado.
Responsável pelo produto e fabricante
Responsável pelo produto:
Amdipharm Limited
3 Burlington Road
Dublin 4
Irlanda
e-mail: [email protected]
Amdipharm Limited faz parte do grupo ADVANZ PHARMA.
Fabricante:
Pharmathen S.A.
Dervenakion 6
Pallini Attiki, 15351
Grécia
Pharmathen International S.A.
Industrial Park Sapes
Rodopi Prefecture, Block No 5
Rodopi 69300
Grécia
Este medicamento é autorizado para comercialização nos países membros da Área Econômica Europeia sob os seguintes nomes:
Alemanha
Mytolac 60mg Injektionslösung in einer Fertigspritze
Mytolac 90mg Injektionslösung in einer Fertigspritze
Mytolac 120mg Injektionslösung in einer Fertigspritze
Áustria
Mytolac 60mg Injektionslösung in einer Fertigspritze
Mytolac 90mg Injektionslösung in einer Fertigspritze
Mytolac 120mg Injektionslösung in einer Fertigspritze
Bélgica
Mytolac 60mg solution injectable en seringue préremplie
Mytolac 90mg solution injectable en seringue préremplie
Mytolac 120mg solution injectable en seringue préremplie
Chipre
Mytolente
Dinamarca
Myrelez 60mg injektionsvæske, opløsning i fyldt injektionssprøjte
Myrelez 90mg injektionsvæske, opløsning i fyldt injektionssprøjte
Myrelez 120mg, injektionsvæske, opløsning i fyldt injektionssprøjte
Eslováquia
Mytolente 60 mg injekčný roztok naplnený v injekčnej striekačke
Mytolente 90 mg injekčný roztok naplnený v injekčnej striekačke
Mytolente 120 mg injekčný roztok naplnený v injekčnej striekačke
Espanha
Myrelez 60mg Solucion inyectable en jeringa precargada
Myrelez 90mg Solucion inyectable en jeringa precargada
Myrelez 120mg Solucion inyectable en jeringa precargada
Estônia
Myrelez
Finlândia
Myrelez 60mg injektioneste, liuos esitäytetyssä ruiskussa
Myrelez 90mg injektioneste, liuos esitäytetyssä ruiskussa
Myrelez 120mg injektioneste, liuos esitäytetyssä ruiskussa
França
Myrelez L.P. 60mg solution injectable à libération prolongée en seringue préremplie
Myrelez L.P. 90mg solution injectable à libération prolongée en seringue préremplie
Myrelez L.P. 120mg solution injectable à libération prolongée en seringue préremplie
Grécia
Myrelez 60mg ενέσιμο διάλυμα σε προγεμισμένη σύριγγα
Myrelez 90mg ενέσιμο διάλυμα σε προγεμισμένη σύριγγα
Myrelez 120mg ενέσιμο διάλυμα σε προγεμισμένη σύριγγα
Hungria
Mytolac 60mg oldatos injekció előretöltött fecskendőben
Mytolac 90mg oldatos injekció előretöltött fecskendőben
Mytolac 120mg oldatos injekció előretöltött fecskendőben
Irlanda
Myrelez 60mg solution for injection in a prefilled syringe
Myrelez 90mg solution for injection in a prefilled syringe
Myrelez 120mg solution for injection in a prefilled syringe
Itália
Myrelez
Letônia
Myrelez 60mg šķīdums injekcijām pilnšļircē
Myrelez 90mg šķīdums injekcijām pilnšļircē
Myrelez 120mg šķīdums injekcijām pilnšļircē
Lituânia
Myrelez 60mg injekcinis tirpalas užpildytame švirkšte
Myrelez 90mg injekcinis tirpalas užpildytame švirkšte
Myrelez 120mg injekcinis tirpalas užpildytame švirkšte
Países Baixos
Mytolac 60mg oplossing voor injectie in een voorgevulde spuit
Mytolac 90mg oplossing voor injectie in een voorgevulde spuit
Mytolac 120mg oplossing voor injectie in een voorgevulde spuit
Noruega
Myrelez 60mg injeksjonsvæske, oppløsning i ferdigfylt sprøyte
Myrelez 90mg injeksjonsvæske, oppløsning i ferdigfylt sprøyte
Myrelez 120mg injeksjonsvæske, oppløsning i ferdigfylt sprøyte
Polônia
Myrelez
Portugal
Mytolac 60mg solução injetável em seringa pré-cheia
Mytolac 90mg solução injetável em seringa pré-cheia
Mytolac 120mg solução injetável em seringa pré-cheia
Reino Unido
Myrelez 60mg solution for injection in a prefilled syringe
Myrelez 90mg solution for injection in a prefilled syringe
Myrelez 120mg solution for injection in a prefilled syringe
República Tcheca
Mytolente 60 mg injekčný roztok naplnený v injekčnej striekačke
Mytolente 90 mg injekčný roztok naplnený v injekčnej striekačke
Mytolente 120 mg injekčný roztok naplnený v injekčnej striekačke
Romênia
Mytolac 60mg soluţie injectabilă în seringă preumplută
Mytolac 90mg soluţie injectabilă în seringă preumplută
Mytolac 120mg soluţie injectabilă în seringă preumplută
Data da última atualização do folheto: 16-05-2025
- País de registo
- Substância ativa
- Requer receita médicaSim
- Fabricante
- ImportadorPharmathen International S.A. Pharmathen S.A.
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a MirelezForma farmacêutica: Solução, 60 mgSubstância ativa: lanreotideRequer receita médicaForma farmacêutica: Solução, 90 mgSubstância ativa: lanreotideRequer receita médicaForma farmacêutica: Solução, 120 mgSubstância ativa: lanreotideRequer receita médica
Alternativas a Mirelez noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a Mirelez em Espanha
Médicos online para Mirelez
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de Mirelez – sujeita a avaliação médica e regras locais.







