
Midrane

Pergunte a um médico sobre a prescrição de Midrane

Como usar Midrane
Folheto informativo para o paciente
Mydrane, (0,2 mg + 3,1 mg + 10 mg)/ml, solução para injeção
Tropicamida + Cloridrato de fenilefrina + Cloridrato de lidocaína monohidratado
Deve ler atentamente o conteúdo do folheto antes de tomar o medicamento, pois contém informações importantes para o paciente.
- Deve guardar este folheto, para que possa relê-lo se necessário.
- Em caso de dúvidas, deve consultar um médico, farmacêutico ou enfermeira.
- Se o paciente apresentar algum efeito não desejado, incluindo qualquer efeito não desejado não listado neste folheto, deve informar o médico, farmacêutico ou enfermeira. Ver ponto 4.
Índice do folheto
- 1. O que é Mydrane e para que é utilizado
- 2. Informações importantes antes de tomar o medicamento Mydrane
- 3. Como tomar Mydrane
- 4. Efeitos não desejados
- 5. Como armazenar Mydrane
- 6. Conteúdo da embalagem e outras informações
1. O que é Mydrane e para que é utilizado
O que é Mydrane
Este medicamento é uma solução que é injetada no olho.
Contém três substâncias ativas:
- tropicamida, que pertence a um grupo de medicamentos que bloqueiam a transmissão de impulsos nervosos, conhecidos como medicamentos anticolinérgicos,
- fenilefrina (na forma de cloridrato de fenilefrina), que pertence a um grupo de medicamentos que imitam o efeito de impulsos nervosos (medicamentos alfa-simpaticomiméticos),
- lidocaína (na forma de cloridrato de lidocaína monohidratado), que pertence a uma classe de medicamentos conhecidos como anestésicos locais do tipo amida.
Para que é utilizado este medicamento
Medicamento para uso exclusivo em adultos.
É administrado por um cirurgião oftalmologista por injeção no olho no início da operação de catarata
(opacidade do cristalino) para dilatar a pupila do olho (midríase) e para obter
anestesia do olho durante a operação.
2. Informações importantes antes de tomar o medicamento Mydrane
Quando não usar Mydrane:
- se o paciente for alérgico à tropicamida, cloridrato de fenilefrina e (ou) cloridrato de lidocaína monohidratado ou a qualquer um dos outros componentes deste medicamento (listados no ponto 6),
- se o paciente for alérgico a anestésicos locais do tipo amida,
- se o paciente for alérgico a derivados da atropina.
Advertências e precauções
O medicamento Mydrane não é recomendado:
- em operações de catarata combinadas com certos tipos de operações oculares (vitrektomia),
- se a câmara anterior do olho for rasa,
- se o paciente tiver história de aumento agudo da pressão intraocular (glaucoma agudo com ângulo de filtração estreito).
Deve consultar um médico, especialmente se o paciente tiver:
- hipertensão arterial (pressão alta),
- espessamento das paredes das artérias (aterosclerose),
- qualquer doença cardíaca, especialmente se afetar a frequência cardíaca,
- contraindicações para medicamentos que aumentam a pressão arterial (aminas pressoras) e são administrados por via sistêmica,
- hipertireoidismo,
- distúrbios da próstata,
- epilepsia (convulsões),
- qualquer doença hepática ou problema renal,
- qualquer problema respiratório,
- perda de função muscular e fraqueza muscular (miastenia).
Mydrane e outros medicamentos
Deve informar o médico ou farmacêutico sobre todos os medicamentos que o paciente está tomando
atualmente ou recentemente, bem como sobre os medicamentos que o paciente planeja tomar.
Gravidez, amamentação e fertilidade
Não deve usar este medicamento:
- durante a gravidez,
- durante a amamentação. Se a paciente estiver grávida ou amamentando, achar que pode estar grávida ou planejar ter um filho, deve consultar um médico ou farmacêutico antes de usar este medicamento.
Condução de veículos e operação de máquinas
O medicamento Mydrane tem um efeito moderado na capacidade de conduzir veículos e operar máquinas.
Não deve conduzir veículos e (ou) operar máquinas, até que a visão normal seja restaurada.
Mydrane contém sódio
O medicamento contém menos de 1 mmol de sódio (23 mg) por dose, ou seja, o medicamento é considerado "livre de sódio".
3. Como tomar Mydrane
O paciente deve receber este medicamento apenas se, durante o exame pré-operatório,
for obtida uma dilatação suficiente da pupila após a aplicação de gotas oculares dilatadoras padrão.
Posologia e modo de administração
- A injeção do medicamento Mydrane será realizada por um cirurgião oftalmologista, sob anestesia local, no início da operação de catarata.
- A dose recomendada é de 0,2 ml da solução em uma única injeção. Não deve ser administrada uma dose adicional, pois não foi demonstrado um efeito adicional significativo e foi observada uma perda aumentada de células endoteliais.
- A mesma dose é utilizada para adultos e idosos.
Uso de dose maior do que a recomendada ou menor do que a recomendada do medicamento Mydrane
O medicamento será administrado por um cirurgião oftalmologista. É pouco provável que o paciente sofra uma superdose.
A superdose pode causar uma perda aumentada de células endoteliais da córnea (células da camada de revestimento da superfície posterior da córnea).
Em caso de dúvidas sobre a administração deste medicamento, deve consultar um médico, farmacêutico ou enfermeira.
4. Efeitos não desejados
Como qualquer medicamento, este medicamento pode causar efeitos não desejados, embora não todos os pacientes os experimentem.
As complicações mais graves conhecidas que ocorrem durante ou após a operação de catarata:
Não muito frequentes: podem afetar até 1 pessoa em 100
- lesão do cristalino (ruptura da cápsula posterior),
- edema da retina (edema cistóide da mácula). Nesse caso, deve procurar um médico imediatamente.
Outros efeitos não desejados:
Não muito frequentes: podem afetar até 1 pessoa em 100
- dor de cabeça,
- edema da córnea (ceratite), aumento da pressão intraocular, vermelhidão do olho (hiperemia do olho),
- hipertensão arterial (pressão alta).
Notificação de efeitos não desejados
Se ocorrerem algum efeito não desejado, incluindo qualquer efeito não desejado não listado neste folheto,
deve informar o médico, farmacêutico ou enfermeira. Os efeitos não desejados podem ser notificados diretamente ao Departamento de Monitoramento de Efeitos Não Desejados de Medicamentos do Instituto de Regulação de Medicamentos,
Rua Jerozolimskie 181C, 02-222 Varsóvia,
Sítio da internet: https://smz.ezdrowie.gov.pl
Os efeitos não desejados também podem ser notificados ao responsável pelo medicamento.
A notificação de efeitos não desejados pode ajudar a coletar mais informações sobre a segurança do medicamento.
5. Como armazenar o medicamento Mydrane
O medicamento deve ser armazenado em um local seguro e inacessível a crianças.
Não deve usar este medicamento após a data de validade impressa na caixa, bliste e ampola.
A data de validade é o último dia do mês indicado.
Não há recomendações especiais para o armazenamento do medicamento.
Apenas para uso único. O medicamento deve ser usado imediatamente após a abertura da ampola.
Os medicamentos não devem ser jogados na canalização ou em recipientes de lixo doméstico. Deve perguntar ao farmacêutico como descartar os medicamentos que não são mais necessários. Essa ação ajudará a proteger o meio ambiente.
6. Conteúdo da embalagem e outras informações
O que contém o medicamento Mydrane
- Em cada dose de 0,2 ml, as substâncias ativas são: tropicamida 0,04 mg, cloridrato de fenilefrina 0,62 mg e cloridrato de lidocaína monohidratado 2 mg, o que corresponde a 0,2 mg de tropicamida, 3,1 mg de cloridrato de fenilefrina e 10 mg de cloridrato de lidocaína monohidratado por ml.
- Os outros componentes são: cloreto de sódio, fosfato dissódico dodecahidratado, fosfato dissódico dihidratado, edetato dissódico e água para injeção.
Como é o medicamento Mydrane e o que contém a embalagem
Mydrane é uma solução para injeção transparente, ligeiramente amarelada
e praticamente livre de partículas visíveis, fornecida em uma ampola de vidro marrom de 1 ml. Cada ampola estéril contém 0,6 ml da solução para injeção e é embalada individualmente
ou com uma agulha estéril com filtro de 5 microns em um bliste de papel/PVC selado.
Cada caixa contém 20 ou 100 ampolas estéreis com agulhas estéreis com filtro de 5 microns, separadamente ou no mesmo bliste. As agulhas com filtro de 5 microns devem ser usadas apenas para retirar o conteúdo da ampola. Todos os componentes são para uso único.
Nem todos os tamanhos de embalagem podem estar disponíveis.
Responsável e fabricante
Responsável:
FRANÇA
Este medicamento é autorizado para comercialização nos países membros da Área Econômica Europeia sob os seguintes nomes:
Áustria, Bélgica, Bulgária, Chipre, República Tcheca, Alemanha, Dinamarca, Grécia, Finlândia, França, Croácia,
Islândia, Itália, Luxemburgo, Países Baixos, Polônia, Portugal, Romênia, Suécia, Eslovênia, Eslováquia,
Reino Unido ........................................................................................................................... Mydrane
Irlanda, Espanha.........................................................................................................................Fydrane
Noruega .......................................................................................................................................Mydane
Data da última atualização do folheto: 06-09-2023
Informações detalhadas sobre este medicamento podem ser encontradas no sítio da internet do Instituto de Regulação de Medicamentos:
www.urpl.gov.pl
---------------------------------------------------------------------------------------------------------------------------
Informações destinadas apenas ao pessoal médico especializado:
Incompatibilidades farmacêuticas
Não foram descritas incompatibilidades com produtos frequentemente usados durante a operação de catarata na literatura ou durante os estudos clínicos. Isso também foi confirmado para os materiais viscoelásticos comumente usados por meio de um estudo de interações farmacêuticas.
Advertência
Não use se o bliste estiver danificado ou rasgado. Abrir apenas em condições assépticas.
Garante-se que o conteúdo do bliste não aberto é estéril.
Como preparar e administrar Mydrane
Solução para injeção para uso único em um olho, apenas para administração na câmara anterior do olho.
O medicamento Mydrane deve ser administrado por injeção na câmara anterior do olho (injeção intracamerular) por um cirurgião oftalmologista em condições assépticas recomendadas para a operação de catarata.
Antes da injeção intracamerular, a solução deve ser verificada visualmente e deve ser usada apenas se for uma solução clara, ligeiramente amarelada
e praticamente livre de partículas visíveis.
A dose recomendada é de 0,2 ml de Mydrane; não deve ser administrada uma dose adicional, pois não foi demonstrado um efeito adicional significativo e foi observada uma perda aumentada de células endoteliais.
Este produto deve ser usado imediatamente após a abertura da ampola e não deve ser reutilizado para o segundo olho ou outro paciente.
Apenas no caso do conjunto (ou seja, bliste contendo ampola e agulha): colar a etiqueta do bliste na documentação do paciente.
Para preparar o medicamento Mydrane para administração na câmara anterior do olho, deve seguir as seguintes instruções: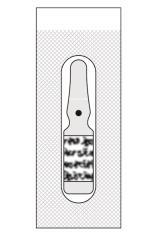 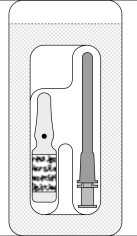  | |
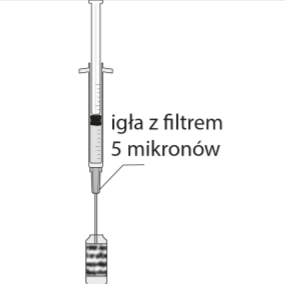 |
|
Após o uso, deve descartar o resto da solução preparada. Não deve armazenar o resto da solução para uso posterior. 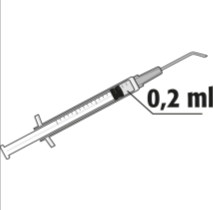 | |
Todos os resíduos do medicamento ou seus descartes devem ser eliminados de acordo com as regulamentações locais. As agulhas usadas devem ser descartadas em um recipiente para resíduos médicos perfurantes.
- País de registo
- Substância ativa
- Requer receita médicaSim
- Fabricante
- ImportadorDelpharm Tours Laboratoires Thea
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a MidraneForma farmacêutica: Gotas, 10 mg/mlSubstância ativa: atropineFabricante: Warszawskie Zakłady Farmaceutyczne POLFA S.A.Requer receita médicaForma farmacêutica: Gotas, 10 mg/mlSubstância ativa: cyclopentolateForma farmacêutica: Gotas, 100 mcg/mlSubstância ativa: atropineFabricante: Jadran-Galenski laboratorij d.d.Requer receita médica
Alternativas a Midrane noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a Midrane em Ucrania
Alternativa a Midrane em España
Médicos online para Midrane
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de Midrane – sujeita a avaliação médica e regras locais.














