
Biotaksim

Pergunte a um médico sobre a prescrição de Biotaksim

Como usar Biotaksim
Folheto informativo para o utilizador
BIOTAKSYM, 1 g, pó de cefotaxima para solução injectável ou infusão
BIOTAKSYM, 2 g, pó de cefotaxima para solução injectável ou infusão
Cefotaxima
Deve ler atentamente o conteúdo do folheto antes de tomar o medicamento, pois contém informações importantes para o doente.
- Deve guardar este folheto para poder reler-lo se necessário.
- Em caso de dúvidas, deve consultar o médico ou a enfermeira.
- Este medicamento foi prescrito especificamente para si. Não o deve dar a outros. O medicamento pode prejudicar outras pessoas, mesmo que os sintomas da sua doença sejam os mesmos.
- Se o doente apresentar algum efeito secundário, incluindo quaisquer efeitos secundários não mencionados neste folheto, deve informar o médico ou a enfermeira. Ver ponto 4.
Índice do folheto
- 1. O que é o Biotaksym e para que é utilizado
- 2. Informações importantes antes de tomar o medicamento Biotaksym
- 3. Como tomar Biotaksym
- 4. Efeitos secundários possíveis
- 5. Como conservar Biotaksym
- 6. Conteúdo da embalagem e outras informações
1. O que é o Biotaksym e para que é utilizado
O Biotaksym contém um antibiótico cefalosporínico de terceira geração - a cefotaxima.
O medicamento, após dissolução e diluição adequada, é administrado por via intramuscular ou intravenosa
(por injeção ou infusão).
A cefotaxima é utilizada:
- no tratamento de infecções graves causadas por bactérias sensíveis:
- infecções das vias respiratórias inferiores, incluindo pneumonia;
- infecções do trato urinário;
- infecções da pelve;
- septicemia;
- infecções da pele e tecidos moles;
- infecções intra-abdominais, incluindo peritonite;
- infecções ósseas e articulares;
- infecções do sistema nervoso central, incluindo meningite;
- na prevenção de infecções pós-operatórias.
2. Informações importantes antes de tomar o medicamento Biotaksym
Quando não tomar o medicamento Biotaksym:
- se o doente for alérgico à cefotaxima ou a outras cefalosporinas;
- se o doente estiver a tomar penicilinas, devido ao risco de reação cruzada (ver ponto: "Biotaksym e outros medicamentos");
- se o doente já apresentou uma reação grave de pele ou descamação da pele, bolhas ou úlceras na boca após a administração de cefotaxima ou outras cefalosporinas;
- com lidocaína:
- em doentes alérgicos à lidocaína ou a outros anestésicos locais da classe das amidas;
- por via intravenosa;
- em lactentes com menos de 30 meses;
- em doentes com insuficiência cardíaca grave ou bloqueio cardíaco (sem marca-passo).
Precauções e advertências
Antes de iniciar o tratamento com o medicamento Biotaksym, deve discutir com o médico ou a enfermeira.
- Se o doente for alérgico, especialmente a cefalosporinas e penicilinas (e outros antibióticos beta-lactâmicos); deve ter especial cuidado, pois as pessoas alérgicas à penicilina podem também ser alérgicas às cefalosporinas (chamada alergia cruzada). Existe o risco de uma reação alérgica grave. Se ocorrer uma reação alérgica, deve interromper a administração da cefotaxima e, se necessário, iniciar o tratamento adequado. No tratamento de uma reação alérgica grave, pode ser necessário administrar adrenalina e outros medicamentos para choque (medicamentos para manter a circulação, corticosteroides e medicamentos antihistamínicos).
- Em relação à administração de cefotaxima, foram relatados casos de reações cutâneas graves, incluindo síndrome de Stevens-Johnson, necrólise epidérmica tóxica, reação medicamentosa com eosinofilia e sintomas gerais (síndrome DRESS), erupção cutânea aguda generalizada pustulosa (AGEP). Deve interromper a administração da cefotaxima e procurar imediatamente um médico se ocorrer algum dos sintomas relacionados com essas reações cutâneas graves, descritos no ponto 4.
- Se o doente tiver disfunção renal, o médico pode solicitar a monitorização da função renal e, se necessário, reduzir a dose do medicamento.
- Se o doente apresentar sintomas neurológicos, como alterações da consciência, movimentos anormais e convulsões, deve procurar um médico antes de continuar o tratamento.
- Se a cefotaxima for administrada por um período prolongado, assim como no caso de outros antibióticos, as cepas inicialmente sensíveis podem tornar-se resistentes, e pode ocorrer um aumento de bactérias da família Enterococcus spp. O médico pode solicitar a realização de um antibiograma.
- Se o doente apresentar diarreia relacionada com a administração do medicamento, deve procurar um médico, que solicitará as medidas adequadas. Raramente, durante ou após o tratamento com antibióticos, pode ocorrer colite pseudomembranosa, caracterizada por diarreia. A colite pode ter um curso leve ou grave. A forma leve geralmente desaparece após a interrupção do medicamento. Em casos mais graves, o médico pode solicitar a administração de metronidazol ou vancomicina. Não deve tomar medicamentos que reduzam a peristalse ou que tenham efeito constipante.
- Se o doente já teve colite no passado, especialmente colite do cólon.
- Se o doente estiver a tomar o medicamento por mais de 7 dias, o médico pode solicitar a monitorização da contagem de glóbulos brancos e da função hepática.
Crianças
Em crianças com menos de 2 meses de idade, o medicamento deve ser administrado exclusivamente por via intravenosa.
Biotaksym e outros medicamentos
Deve informar o médico sobre todos os medicamentos que está a tomar atualmente ou recentemente,
e também sobre os medicamentos que planeia tomar.
Deve ter cuidado ao administrar cefotaxima em conjunto com:
- substâncias com atividade bacteriostática (por exemplo, tetraciclina, eritromicina, clorafenicol, sulfonamidas) - podem reduzir a atividade antibacteriana da cefotaxima;
- antibióticos aminoglicosídicos (por exemplo, estreptomicina) e diuréticos potentes (por exemplo, furosemida) - podem aumentar o efeito prejudicial na função renal;
- probenecida - aumenta a concentração de cefotaxima no sangue e prolonga a sua ação.
Efeito sobre os resultados dos exames laboratoriais
A administração de cefotaxima pode causar:
- resultado falso positivo nos testes de redução para detecção de glicose na urina;
- resultado falso positivo no teste de Coombs.
Gravidez e amamentação
Se a paciente estiver grávida ou a amamentar, suspeitar que pode estar grávida ou planeia ter
um filho, deve consultar o médico ou o farmacêutico antes de tomar este medicamento.
Gravidez
A segurança da administração de cefotaxima em mulheres grávidas não foi estabelecida. Portanto, a cefotaxima
não deve ser administrada durante a gravidez, a menos que os benefícios previstos superem o risco.
Amamentação
A cefotaxima passa para o leite materno. Não se pode excluir o efeito sobre a flora intestinal fisiológica
dos recém-nascidos amamentados, o que pode levar a diarreia, colonização por fungos semelhantes a leveduras. Em recém-nascidos, também pode ocorrer uma reação alérgica.
Deve discutir com o médico se deve parar de amamentar ou interromper o tratamento, considerando o benefício da amamentação para o bebê e o benefício do tratamento para a mãe.
Condução de veículos e utilização de máquinas
Não há evidências de que a cefotaxima afete diretamente a capacidade de conduzir veículos ou utilizar máquinas. Doses elevadas de cefotaxima, especialmente em doentes com insuficiência renal, podem causar alterações da consciência, movimentos anormais e convulsões. Nesses casos, não deve conduzir veículos ou utilizar máquinas.
Biotaksym contém sódio
O medicamento contém 48 mg de sódio (principal componente do sal de cozinha) por grama. Isso corresponde a 2,4% da dose diária máxima recomendada de sódio na dieta para adultos.
Deve ser considerado em doentes com função renal reduzida e em doentes que controlam a ingestão de sódio na dieta.
Preparação do medicamento para administração - ver ponto: "Informações destinadas exclusivamente ao pessoal médico" no final do folheto. Ao calcular o conteúdo total de sódio na solução diluída preparada, deve considerar o sódio proveniente do diluente. Para obter informações precisas sobre o conteúdo de sódio na solução utilizada para diluir o medicamento, deve consultar o folheto do paciente do diluente utilizado.
3. Como tomar Biotaksym
Este medicamento deve ser sempre tomado de acordo com as recomendações do médico. Em caso de dúvida, deve consultar o médico.
A posologia e a via de administração são determinadas pelo médico com base na gravidade e tipo de infecção, idade, peso corporal e função renal do doente.
As instruções detalhadas de posologia e administração, bem como a preparação do medicamento para administração, estão no final do folheto, no ponto "Informações destinadas exclusivamente ao pessoal médico".
Administração de uma dose maior do que a recomendada de Biotaksym
Se o doente suspeitar que recebeu uma dose maior do que a recomendada de Biotaksym, deve informar o médico. A superdose pode ocorrer especialmente em doentes com insuficiência renal. Pode ocorrer convulsões, tremores e coma. Nesses casos, deve interromper a administração do medicamento e iniciar o tratamento adequado. A hemodiálise é um método que remove o medicamento do organismo.
Omissão da administração de Biotaksym
Se o doente suspeitar que omitiu uma dose de Biotaksym, deve informar o médico o mais rápido possível.
4. Efeitos secundários possíveis
Como qualquer medicamento, este medicamento pode causar efeitos secundários, embora não em todos os doentes.
Abaixo estão listados os efeitos secundários e a frequência com que ocorrem.
Deve interromper imediatamente a administração da cefotaxima e informar o médicose o doente notar a ocorrência de algum dos seguintes sintomas:
- manchas vermelhas, não elevadas, em forma de alvo ou redondas no tronco, frequentemente com bolhas ou descamação da pele, úlceras na boca, garganta, nariz, genitálias e olhos. Essas reações cutâneas graves podem ser precedidas por febre e sintomas semelhantes aos da gripe (síndrome de Stevens-Johnson ou necrólise epidérmica tóxica).
- Erupção cutânea generalizada, febre alta e linfonodos aumentados (síndrome DRESS ou síndrome de hipersensibilidade ao medicamento).
- Erupção cutânea vermelha e escamosa, generalizada, com nódulos sob a pele e bolhas, acompanhada de febre. Os sintomas geralmente aparecem no início do tratamento (erupção cutânea aguda generalizada pustulosa).
Muito frequentes (ocorrem em mais de 1 em 10 doentes):
- dor no local da injeção após administração intramuscular.
Frequentes (ocorrem em 1 a 10 de cada 1.000 doentes):
- diminuição do número de glóbulos brancos, aumento do número de eosinófilos (tipo de glóbulos brancos), diminuição do número de plaquetas, reação de Herxheimer (sintomas que aparecem dentro de algumas semanas após o início do tratamento da borreliose, como erupção cutânea, prurido, febre, leucopenia, dificuldade respiratória, dores articulares),
- convulsões,
- diarreia,
- aumento da atividade das enzimas hepáticas (ALAT, AspAT, LDH, GGTP, fosfatase alcalina) e (ou) aumento da bilirrubina,
- erupção cutânea, prurido, urticária,
- disfunção renal e (ou) aumento da creatinina (durante a administração com aminoglicosídios),
- febre, reações inflamatórias no local da injeção, incluindo flebite ou tromboflebite.
Frequência desconhecida (não pode ser estimada com base nos dados disponíveis):
- infecções, diminuição do número de neutrófilos (tipo de glóbulos brancos), incluindo formas graves (neutropenia), anemia hemolítica,
- reações anafiláticas, angioedema, broncoespasmo, choque anafilático,
- dor de cabeça e tontura, encefalopatia (por exemplo, alterações da consciência, movimentos anormais),
- arritmia causada por infusão rápida por cateter venoso central,
- náuseas, vômitos, dor abdominal,
- colite pseudomembranosa, hepatite (por vezes com icterícia), nefrite intersticial, reações sistémicas à lidocaína após administração intramuscular (se a solução contiver lidocaína).
Notificação de efeitos secundários
Se ocorrerem algum efeito secundário, incluindo quaisquer efeitos secundários não mencionados neste folheto, deve informar o médico, farmacêutico ou enfermeira. Os efeitos secundários podem ser notificados diretamente ao Departamento de Monitorização de Efeitos Secundários de Medicamentos da Agência Nacional de Medicamentos e Produtos de Saúde
Al. Jerozolimskie 181C
02-222 Warszawa
Tel.: + 48 22 49 21 301
Fax: + 48 22 49 21 309
Site da Internet: https://smz.ezdrowie.gov.pl
Os efeitos secundários também podem ser notificados ao titular da autorização de comercialização.
A notificação de efeitos secundários permite reunir mais informações sobre a segurança do medicamento.
5. Como conservar Biotaksym
O medicamento deve ser conservado a uma temperatura de até 25 °C. Proteger da luz.
A solução preparada pode ser conservada por 24 horas no refrigerador, a uma temperatura entre 2 °C e 8 °C.
Recomenda-se preparar as soluções imediatamente antes da administração.
O medicamento deve ser conservado fora do alcance e da vista das crianças.
Não deve tomar este medicamento após o prazo de validade impresso na embalagem. O prazo de validade é o último dia do mês indicado.
A menção "EXP" na embalagem indica o prazo de validade, e "Lot" indica o número do lote.
Os medicamentos não devem ser jogados na canalização ou nos contentores de lixo doméstico. Deve perguntar ao farmacêutico como eliminar os medicamentos que já não são necessários. Essa ação ajudará a proteger o meio ambiente.
6. Conteúdo da embalagem e outras informações
O que contém o Biotaksym
- O princípio ativo do medicamento é a cefotaxima. Cada frasco contém 1 g ou 2 g de cefotaxima na forma de cefotaxima sódica. O medicamento não contém substâncias auxiliares.
Como é o Biotaksym e que embalagem contém
O medicamento tem a forma de pó branco ou ligeiramente amarelado, higroscópico.
O Biotaksym é destinado à preparação de soluções injectáveis ou para infusão.
O frasco de vidro é fechado com um rolha de borracha e protegido por uma tampa de alumínio ou uma tampa de alumínio com capuz, em uma caixa de cartão.
A embalagem contém 1 ou 10 frascos.
Nem todos os tamanhos de embalagem podem estar disponíveis.
Titular da autorização de comercialização e fabricante
Titular da autorização de comercialização
Zakłady Farmaceutyczne POLPHARMA S.A.
ul. Pelplińska 19, 83-200 Starogard Gdański
tel. + 48 22 364 61 01
Fabricante
Zakłady Farmaceutyczne POLPHARMA S.A.
ul. Pelplińska 19, 83-200 Starogard Gdański
Zakłady Farmaceutyczne POLPHARMA S.A.
Divisão de Produção em Duchnice
ul. Ożarowska 28/30, 05-850 Ożarów Mazowiecki
Data da última atualização do folheto:abril de 2024
-----------------------------------------------------------------------------------------------------------------
Informações destinadas exclusivamente ao pessoal médico
BIOTAKSYM, 1 g, pó para solução injectável ou infusão
BIOTAKSYM, 2 g, pó para solução injectável ou infusão
Cefotaxima
Posologia
Adultos e crianças com mais de 12 anos
Em infecções leves a moderadas, a dose é de 1 g a cada 12 horas.
Em infecções graves, a dose diária pode ser aumentada para 12 g em 3 ou 4 doses divididas.
As doses diárias de até 6 g devem ser divididas em pelo menos duas doses, administradas a cada 12 horas. Doses diárias maiores devem ser divididas em pelo menos 3 ou 4 doses, administradas a cada 8 ou 6 horas.
As diretrizes de posologia estão apresentadas na tabela abaixo.
| Tipo de infecção | Dose única de cefotaxima | Intervalo entre doses | Dose diária de cefotaxima |
| Infecção típica, quando se confirma ou se suspeita que o microrganismo é sensível | 1 g | 12 horas | 2 g |
| Infecções em que se confirma ou se suspeita que há vários microrganismos com sensibilidade alta ou moderada | 2 g | 12 horas | 4 g |
| Infecções bacterianas não esclarecidas, em que não foi possível localizar o local da infecção e o estado do doente é crítico | 2 a 3 g | 8 horas 6 horas | 6 a 9 g 8 a 12 g |
Lactentes e crianças com menos de 12 anos
Em lactentes e crianças com menos de 12 anos, a dose é de 50 a 150 mg/kg de peso corporal por dia de cefotaxima, em 2 ou 4 doses divididas.
Em infecções muito graves, especialmente ameaçadoras da vida, pode ser necessário aumentar a dose diária de cefotaxima para 200 mg/kg de peso corporal por dia, em doses divididas.
Crianças com menos de 2 meses de idade devem receber o medicamento exclusivamente por via intravenosa.
Recém-nascidos prematuros e a termo
Não deve exceder a dose de 50 mg/kg de peso corporal por dia de cefotaxima, em 2 a 4 doses divididas.
Em infecções graves e ameaçadoras da vida, pode ser necessário aumentar a dose diária de 150 a 200 mg/kg de peso corporal por dia, em doses divididas.
Em tais casos, a posologia recomendada está apresentada na tabela abaixo.
Doença de Lyme
Doença de Lyme não complicada: dose única de 1 g de cefotaxima por via intramuscular. Antes de iniciar o tratamento com cefotaxima, deve realizar exames para garantir que não há infecção simultânea por sífilis.
| Idade da criança | Dose diária de cefotaxima |
| De 0 a 7 dias de vida | 50 mg/kg de peso corporal a cada 12 horas por via intravenosa |
| De 8 dias a 1 mês de vida | 50 mg/kg de peso corporal a cada 8 horas por via intravenosa |
Prevenção de infecções pós-operatórias
Deve administrar uma dose única de 1 g de cefotaxima 30 a 90 minutos antes da cirurgia.
Dependendo do risco de infecção, pode ser necessário continuar a administração do medicamento após a cirurgia.
Posologia em doentes com insuficiência renal
A redução da dose do medicamento é necessária apenas em casos de insuficiência renal grave (clearance de creatinina menor que 5 ml/min, concentração de creatinina no sangue 751 micromol/l). Após a administração da dose inicial de 1 g, a dose diária deve ser reduzida pela metade, sem alterar a frequência de administração do medicamento, por exemplo, a dose de 1 g a cada 12 horas deve ser reduzida para 500 mg a cada 12 horas, a dose de 1 g a cada 8 horas deve ser reduzida para 500 mg a cada 8 horas, a dose de 2 g a cada 8 horas deve ser reduzida para 1 g a cada 8 horas, etc.
Em alguns doentes, pode ser necessário um ajuste adicional da dose, dependendo do curso da infecção e do estado geral do doente.
Via de administração
O medicamento, após dissolução adequada, é administrado por via intravenosa em injeção de 3 a 5 minutos ou por via intramuscular - profundamente no quadrante superior externo do músculo glúteo maior ou na parte lateral da coxa. O medicamento pode ser administrado por infusão intravenosa.
Método de perfuração do frasco
Deve perfurar a tampa com uma agulha e injetar no frasco a quantidade recomendada de solvente. Para perfurar a tampa, deve usar uma agulha com diâmetro não superior a 0,8 mm (21 G na escala Gauge [G]). A agulha deve ser inserida no campo central da tampa, sob um ângulo de 90°, de acordo com o esquema abaixo:
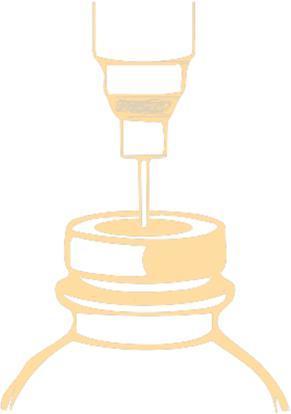
Após adicionar o solvente ao frasco, deve agitá-lo até que o medicamento se dissolva, o que geralmente ocorre em 1 a 2 minutos. Antes de administrar o medicamento, deve verificar se a solução está clara e não contém partículas insolúveis. A solução do medicamento pode ser incolor ou ligeiramente amarelada.
Preparação das soluções para injeção e infusão
| Conteúdo de antibiótico no frasco | Volume do solvente | ||
| Injeção intramuscular | Injeção intravenosa | Infusão intravenosa | |
| 1 g | 4 ml | 10 ml | 50-100 ml |
| 2 g | 10 ml | 50-100 ml | |
Injeção intramuscular
O medicamento deve ser administrado por via intramuscular após dissolução em água para injeção ou solução a 1% de lidocaína. Não deve administrar por via intravenosa a solução do medicamento com lidocaína.
Injeção intravenosa(de 3 a 5 minutos)
O conteúdo do frasco é dissolvido em água para injeção no volume dependente da dose, como apresentado na tabela acima.
Infusão intravenosa(de 20 a 60 minutos)
Para preparar soluções para infusão intravenosa, o pó é dissolvido em água para injeção (como para injeções intravenosas). A solução resultante deve ser então diluída em um dos seguintes solventes:
- solução a 0,9% de cloreto de sódio,
- solução a 5% de glicose,
- solução a 5% de glicose com solução a 0,45% de cloreto de sódio,
- solução a 5% de glicose com solução a 0,2% de cloreto de sódio,
- solução de Ringer com lactato,
- solução de lactato de sódio para injeção (M/6). Não se recomenda o uso de soluções de infusão que contenham bicarbonato de sódio, pois a cefotaxima é instável nessas soluções.
A cefotaxima e os aminoglicosídios não devem ser misturados na mesma seringa ou solução de infusão.
Se for necessário administrar esses medicamentos simultaneamente, devem ser injetados em locais diferentes do corpo.
- País de registo
- Substância ativa
- Requer receita médicaNão
- Fabricante
- ImportadorZakłady Farmaceutyczne POLPHARMA S.A. Zakłady Farmaceutyczne POLPHARMA S.A. Oddział Produkcyjny w Duchnicach
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a BiotaksimForma farmacêutica: Pó, 1 gSubstância ativa: cefotaximeFabricante: Zakłady Farmaceutyczne POLPHARMA S.A. Zakłady Farmaceutyczne POLPHARMA S.A. Oddział Produkcyjny w DuchnicachNão requer receita médicaForma farmacêutica: Pó, 1 gSubstância ativa: cefotaximeNão requer receita médicaForma farmacêutica: Pó, 2 gSubstância ativa: cefotaximeNão requer receita médica
Alternativas a Biotaksim noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a Biotaksim em Ukraine
Alternativa a Biotaksim em Espanha
Médicos online para Biotaksim
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de Biotaksim – sujeita a avaliação médica e regras locais.














