SANDOSTATIN LAR 20 mg PROSZEK I ROZPUSZCZALNIK DO PRZYGOTOWANIA ZAWIESINY DO WSTRZYKIWAŃ


Jak stosować SANDOSTATIN LAR 20 mg PROSZEK I ROZPUSZCZALNIK DO PRZYGOTOWANIA ZAWIESINY DO WSTRZYKIWAŃ
Wprowadzenie
Charakterystyka produktu leczniczego: informacje dla pacjenta
SANDOSTATIN LAR 20 mg proszek i rozpuszczalnik do sporządzania zawiesiny do wstrzykiwań
oktreotyda
Przed rozpoczęciem stosowania tego leku przeczytaj uważnie całą tę ulotkę, ponieważ zawiera ona ważne informacje dla Ciebie.
- Zachowaj tę ulotkę, ponieważ może być konieczne ponowne przeczytanie jej.
- Jeśli masz jakieś wątpliwości, skonsultuj się z lekarzem, farmaceutą lub pielęgniarką.
- Ten lek został przepisany wyłącznie dla Ciebie, nie wolno go przekazywać innym osobom, nawet jeśli mają takie same objawy, ponieważ może im to zaszkodzić.
- Jeśli doświadczasz działań niepożądanych, skonsultuj się z lekarzem, farmaceutą lub pielęgniarką, nawet jeśli są to działania niepożądane, które nie są wymienione w tej ulotce. Patrz rozdział 4.
Zawartość ulotki
- Co to jest Sandostatin LAR i w jakim celu się go stosuje
- Informacje niezbędne przed rozpoczęciem stosowania Sandostatin LAR
- Jak stosować Sandostatin LAR
- Możliwe działania niepożądane
- Przechowywanie Sandostatin LAR
- Zawartość opakowania i dodatkowe informacje
1. Co to jest Sandostatin LAR i w jakim celu się go stosuje
Sandostatin LAR to związek syntetyczny pochodny somatostatyny. Somatostatyna występuje naturalnie w organizmie ludzkim, gdzie hamuje uwalnianie niektórych hormonów, takich jak hormon wzrostu. Zalety Sandostatin LAR w porównaniu z somatostatyną polegają na tym, że jest bardziej potężny i jego działanie jest dłuższe.
Sandostatin LAR stosuje się
- w leczeniu akromegali,
Akromegalia to choroba, w której organizm wytwarza zbyt dużo hormonu wzrostu. Zwykle hormon wzrostu kontroluje wzrost tkanek, narządów i kości. Nadmiar hormonu wzrostu powoduje zwiększenie rozmiaru kości i tkanek, szczególnie w rękach i stopach. Sandostatin LAR znacznie redukuje objawy akromegali, w tym bóle głowy, nadmierne pocenie się, drętwienie rąk i stóp, zmęczenie i bóle stawów. W większości przypadków nadmiar hormonu wzrostu jest spowodowany przez zwiększenie rozmiaru przysadki mózgowej (gruczolak przysadki); leczenie Sandostatin LAR może zmniejszyć rozmiar gruczolaka.
Sandostatin LAR stosuje się w leczeniu osób z akromegalią:
- gdy inne rodzaje leczenia akromegali (chirurgia lub radioterapia) nie są odpowiednie lub nie działały prawidłowo;
- po radioterapii, w celu pokrycia okresu czasu, aż radioterapia będzie w pełni skuteczna.
- w celu złagodzenia objawów związanych z nadmierną produkcją niektórych hormonów i innych substancji pokrewnych w żołądku, jelitach lub trzustce.
Nadmierna produkcja niektórych hormonów i innych substancji naturalnych może być spowodowana przez niektóre rzadkie zaburzenia żołądka, jelit lub trzustki. To zaburza naturalny balans hormonalny i powoduje szereg objawów, takich jak uderzenia gorąca, biegunka, niskie ciśnienie krwi, wysypka skórna i utrata masy ciała. Leczenie Sandostatin LAR pomaga kontrolować te objawy.
- w leczeniu guzów neuroendokrynnych zlokalizowanych w jelitach (np. w wyrostku robaczkowym, jelitach cienkich lub grubych)
Guzami neuroendokrynnymi są rzadkie guzy, które mogą wystąpić w różnych częściach ciała. Sandostatin LAR stosuje się również w celu kontrolowania wzrostu tych guzów, gdy są zlokalizowane w jelitach (np. w wyrostku robaczkowym, jelitach cienkich lub grubych)
- w leczeniu guzów przysadki, które wytwarzają zbyt dużo hormonu stymulującego tarczycę (TSH).
Nadmiar hormonu stymulującego tarczycę (TSH) powoduje nadczynność tarczycy. Sandostatin LAR stosuje się w leczeniu osób z guzami przysadki, które wytwarzają zbyt dużo hormonu stymulującego tarczycę (TSH):
- gdy inne rodzaje leczenia (chirurgia lub radioterapia) nie są odpowiednie lub nie działały;
po radioterapii, w celu pokrycia okresu czasu, aż radioterapia będzie w pełni skuteczna.
2. Informacje niezbędne przed rozpoczęciem stosowania Sandostatin LAR
Przestrzegaj wszystkich wskazówek, które otrzymałeś od lekarza. Mogą one być różne od informacji zawartych w tej ulotce.
Przeczytaj następujące wskazówki przed zastosowaniem Sandostatin LAR.
- jeśli jesteś uczulony na oktreotydę lub na którykolwiek z pozostałych składników tego leku (wymienionych w rozdziale 6).
Ostrzeżenia i środki ostrożności
Skonsultuj się z lekarzem przed rozpoczęciem stosowania Sandostatin LAR:
- jeśli wiesz, że masz obecnie kamienie w pęcherzyku żółciowym lub miałeś je w przeszłości lub masz jakieś powikłania, takie jak gorączka, dreszcze, ból brzucha lub zażółcenie skóry i oczu; poinformuj lekarza, ponieważ długotrwałe stosowanie Sandostatin LAR może powodować tworzenie się kamieni żółciowych. Lekarz może chcieć regularnie kontrolować twój pęcherzyk żółciowy.
- jeśli wiesz, że masz cukrzycę, ponieważ Sandostatin LAR może wpływać na poziom cukru we krwi. Jeśli jesteś cukrzykiem, powinieneś regularnie kontrolować poziom cukru we krwi.
- jeśli masz historię niedoboru witaminy B12, lekarz może kontrolować poziom B12 okresowo.
Badania i kontrole
Jeśli otrzymujesz leczenie Sandostatin LAR przez dłuższy okres czasu, lekarz może regularnie kontrolować Twoją czynność tarczycy.
Lekarz będzie kontrolować czynność Twojego wątroby.
Lekarz będzie mógł sprawdzić funkcjonowanie Twoich enzymów trzustkowych.
Dzieci
Istnieje niewiele doświadczenia w stosowaniu Sandostatin LAR u dzieci.
Stosowanie Sandostatin LAR z innymi lekami
Poinformuj lekarza lub farmaceutę, jeśli stosujesz, stosowałeś niedawno lub możesz potrzebować stosować inne leki.
Zwykle możesz kontynuować stosowanie innych leków podczas leczenia Sandostatin LAR. Jednakże, stwierdzono, że niektóre leki, takie jak cymetydyna, cyklosporyna, bromokryptyna, chinidyna i terfenadyna, mogą być wpływane przez Sandostatin LAR.
Jeśli stosujesz lek na kontrolowanie ciśnienia krwi (np. beta-bloker lub antagonistę kanałów wapniowych) lub środek na kontrolowanie równowagi płynów i elektrolitów, lekarz może potrzebować dostosować dawkę.
Jeśli jesteś cukrzykiem, lekarz może potrzebować dostosować Twoją dawkę insuliny.
Jeśli będziesz otrzymywał leczenie lutem (177Lu) oksodotreotydą, radiofarmaceutykiem, lekarz może przerwać i/lub dostosować leczenie Sandostatin LAR na krótki okres czasu.
Ciąża i laktacja
Jeśli jesteś w ciąży lub w okresie karmienia piersią, podejrzewasz, że możesz być w ciąży lub planujesz ciążę, skonsultuj się z lekarzem przed zastosowaniem tego leku.
Należy stosować Sandostatin LAR w czasie ciąży tylko w przypadku, gdy jest to absolutnie konieczne.
Kobiety w wieku rozrodczym powinny stosować skuteczną antykoncepcję podczas leczenia.
Nie wolno karmić piersią podczas leczenia Sandostatin LAR. Nie wiadomo, czy Sandostatin LAR przenika do mleka matki.
Jazda i obsługa maszyn
Sandostatin LAR nie ma wpływu lub ma niewielki wpływ na zdolność prowadzenia pojazdów lub obsługi maszyn. Jednakże, niektóre z tych działań niepożądanych, które możesz doświadczyć podczas leczenia Sandostatin LAR, takie jak bóle głowy i zmęczenie, mogą obniżyć Twoją zdolność do bezpiecznej jazdy i obsługi maszyn.
Sandostatin zawiera sód
Ten lek zawiera mniej niż 1 mmol sodu (23 mg) na fiolkę; jest to ilość nieistotna z punktu widzenia diety.
3. Jak stosować Sandostatin LAR
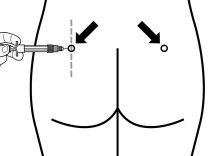
Sandostatin LAR powinien być zawsze podawany jako wstrzyknięcie domięśniowe w mięśnie pośladków. Przy powtarzającym się podawaniu, należy używać prawego i lewego pośladka na przemian.
Jeśli zażyjesz zbyt dużo Sandostatin LAR
Nie zgłoszono żadnych groźnych dla życia reakcji niepożądanych po przedawkowaniu Sandostatin LAR.
Objawy przedawkowania to: uderzenia gorąca, częste oddawanie moczu, zmęczenie, depresja, lęk i brak koncentracji.
Jeśli podejrzewasz, że zażyłeś zbyt dużo Sandostatin LAR i masz któryś z tych objawów, poinformuj lekarza natychmiast. Możesz również skontaktować się z Centrum Informacji Toksykologicznej, tel. 91 562 0420.
Jeśli zapomnisz zażyć Sandostatin LAR
Jeśli zapomnisz o wstrzyknięciu, zaleca się, abyś otrzymał wstrzyknięcie tak szybko, jak się o tym pamiętasz, a następnie kontynuował normalny schemat leczenia. Nie spowoduje to żadnej szkody, jeśli otrzymasz dawkę kilka dni później, ale objawy mogą tymczasowo powrócić do momentu, aż wrócisz do normalnego schematu leczenia.
Jeśli przerwiesz leczenie Sandostatin LAR
Jeśli przerwiesz leczenie Sandostatin LAR, Twoje objawy mogą powrócić. Dlatego nie przerywaj leczenia Sandostatin LAR, chyba że zaleci to lekarz.
Jeśli masz jakieś inne wątpliwości dotyczące stosowania tego leku, skonsultuj się z lekarzem, pielęgniarką lub farmaceutą.
4. Możliwe działania niepożądane
Podobnie jak wszystkie leki, ten lek może powodować działania niepożądane, chociaż nie wszystkie osoby je doświadczają.
Niektóre reakcje niepożądane mogą być poważne. Poinformuj lekarza natychmiast, jeśli doświadczasz któregokolwiek z następujących:
Bardzo częste(mogą wystąpić u więcej niż 1 na 10 osób):
- Kamienie żółciowe, które mogą powodować nagły ból pleców.
- Zbyt wysoki poziom cukru we krwi.
Częste(mogą wystąpić u do 1 na 10 osób):
- Obniżona aktywność tarczycy (niedoczynność tarczycy), która może powodować zmiany w rytmie serca, apetycie lub wadze; zmęczenie, uczucie zimna, lub obrzęk w przedniej części szyi.
- Zmiany w badaniach czynności tarczycy.
- Zapalenie pęcherzyka żółciowego (kolecytitis); objawy mogą obejmować ból w górnej prawej części brzucha, gorączkę, nudności, zażółcenie skóry i oczu (żółtaczka).
- Zbyt niski poziom cukru we krwi.
- Zaburzenia tolerancji glukozy.
- Wolne bicie serca.
Rzadkie(mogą wystąpić u do 1 na 100 osób):
- Pragnienie, niska eliminacja moczu, ciemny kolor moczu, sucha, czerwona skóra.
- Szybkie bicie serca.
Pozostałe poważne reakcje niepożądane
- Reakcje nadwrażliwości (alergiczne) w tym pokrzywka na skórze.
- Rodzaj reakcji alergicznej (anafilaksja) który może powodować trudności w połykaniu lub oddychaniu, obrzęk i mrowienie, możliwe z obniżeniem ciśnienia krwi i zawrotami głowy lub utratą przytomności.
- Zapalenie trzustki (pankreatitis); objawy mogą obejmować nagły ból w górnej części brzucha, nudności, wymioty, biegunkę.
- Zapalenie wątroby (hepatitis); objawy mogą obejmować zażółcenie skóry i oczu (żółtaczka), nudności, wymioty, utratę apetytu, ogólne uczucie niepokoju, swędzenie, lekko zabarwiony mocz.
- Nieregularne bicie serca.
- Niski poziom płytek krwi; może to powodować zwiększone krwawienie lub pojawianie się siniaków.
Poinformuj lekarza natychmiast, jeśli zauważysz którykolwiek z powyższych działań niepożądanych.
Pozostałe działania niepożądane:
Poinformuj lekarza, farmaceutę lub pielęgniarkę, jeśli zauważysz którykolwiek z następujących działań niepożądanych. Zwykle są one łagodne i mają tendencję do zaniku wraz z postępem leczenia.
Bardzo częste(mogą wystąpić u więcej niż 1 na 10 osób):
- Biegunka.
- Ból brzucha.
- Nudności.
- Zaparcie.
- Wzdęcia (gazy).
- Bóle głowy.
- Ból w miejscu wstrzyknięcia.
Częste(mogą wystąpić u do 1 na 10 osób):
- Niepokój żołądka po jedzeniu (dyspepsja).
- Wymioty.
- Uczucie pełności żołądka.
- Luźne stolce.
- Zmiana koloru stolca.
- Zawroty głowy.
- Utrata apetytu.
- Zmiany w badaniach czynności wątroby.
- Wypadanie włosów.
- Trudności w oddychaniu.
- Słabość.
Jeśli doświadczasz jakiegokolwiek działania niepożądanego, skonsultuj się z lekarzem, pielęgniarką lub farmaceutą.
Zgłaszanie działań niepożądanych
Jeśli doświadczasz jakiegokolwiek działania niepożądanego, skonsultuj się z lekarzem lub farmaceutą, nawet jeśli są to działania niepożądane, które nie są wymienione w tej ulotce. Możesz również zgłosić je bezpośrednio do Systemu Hiszpańskiej Farmakowigilancji Leków Stosowanych u Ludzi: http://www.notificaram.es. Przez zgłaszanie działań niepożądanych, możesz przyczynić się do zapewnienia większej ilości informacji na temat bezpieczeństwa tego leku.
5. Przechowywanie Sandostatin LAR
Przechowuj ten lek poza zasięgiem dzieci.
Przechowuj w oryginalnym opakowaniu, aby chronić go przed światłem.
Przechowuj w lodówce (między 2°C a 8°C). Nie zamrażaj.
Sandostatin LAR może być przechowywany poniżej 25°C w dniu wstrzyknięcia.
Nie przechowuj Sandostatin LAR po jego rozcieńczeniu (należy go użyć natychmiast).
Nie używaj tego leku po upływie terminu ważności, który jest podany na opakowaniu po CAD. Termin ważności jest ostatnim dniem miesiąca, który jest podany.
Nie używaj tego leku, jeśli zauważysz obecność cząstek lub zmianę koloru.
Leków nie wolno wylewać do kanalizacji ani wyrzucać do śmieci. Opakowania i leki, których nie potrzebujesz, powinieneś zwrócić do punktu zbiórki SIGRE w aptece. W razie wątpliwości, skonsultuj się z farmaceutą, jak usunąć opakowania i leki, których nie potrzebujesz. Dzięki temu, pomożesz chronić środowisko.
6. Zawartość opakowania i dodatkowe informacje
Skład Sandostatin LAR
- Substancją czynną jest oktreotyd.
Fiolka zawiera 20 mg oktreotydu (w postaci octreotydu octanu).
- Pozostałe składniki to:
W proszku (fiolka): poli(DL-kwas mlekowy-co-glikolowy), mannitol (E421).
W rozpuszczalniku (strzykawka przedładowana): karboksymetyloceluloza sodowa, mannitol (E421), poloksamer 188, woda do wstrzykiwań
Wygląd Sandostatin LAR i zawartość opakowania
Opakowania jednostkowe zawierające fiolkę szklaną 6 ml z korkiem gumowym (bromobutylowym), zamkniętą za pomocą zatyczki aluminiowej, zawierającą proszek do wstrzykiwań i strzykawkę przedładowaną szklaną bezbarwną 3 ml z przednim korkiem i tłokiem (guma chlorobutylowa) z 2 ml rozpuszczalnika, wspólnie opakowane w blister zamknięty z adapterem do fiolki i igłą do wstrzykiwań ochronnych.
Opakowania wielokrotnego użytku składające się z trzech opakowań jednostkowych, z których każde zawiera: fiolkę szklaną 6 ml z korkiem gumowym (bromobutylowym), zamkniętą za pomocą zatyczki aluminiowej, zawierającą proszek do wstrzykiwań i strzykawkę przedładowaną szklaną bezbarwną 3 ml z przednim korkiem i tłokiem (guma chlorobutylowa) z 2 ml rozpuszczalnika, wspólnie opakowane w blister zamknięty z adapterem do fiolki i igłą do wstrzykiwań ochronnych.
Możliwe, że będą dostępne tylko niektóre rozmiary opakowań.
Posiadacz pozwolenia na dopuszczenie do obrotu
Novartis Farmacéutica, S.A.
Gran Vía de les Corts Catalanes, 764
08013 Barcelona
Odpowiedzialny za wytwarzanie
Novartis Farmacéutica, S.A.
Gran Vía de les Corts Catalanes, 764
08013 Barcelona
Novartis Pharma GmbH
Jakov-Lind-Straße 5, Top 3.05 1020 Wien Austria
Novartis Pharma NV
Medialaan 40/Bus 1, 1800 Vilvoorde, (Belgia).
Novartis Healthcare A/S
Edvard Thomsens vej 14, DK-2300 Copenhagen S, (Dania).
Novartis Finland Oy
Metsänneidonkuja 10, 02130 Espoo, (Finlandia)
Novartis Pharma SAS
8-10 rue Henri Sainte-Claire Deville, 92500 Rueil-Malmaison (Francja)
Novartis Pharma GmbH
Roonstrasse 25, 90429 Nürnberg, (Niemcy).
Novartis Pharma GmbH
Sophie-Germain-Strasse 10, 90443 Nürnberg (Niemcy).
Novartis Farma-Produtos Farmacéuticos, SA
Avenida Professor Doutor Cavaco Silva nº10E, Taguspark, 2740-255 Porto Salvo, (Portugalia).
Novartis Farma S.p.A.
Via Provinciale Schito 131, 80058 Torre Annunziata, NA , (Włochy).
Novartis Farma S.p.A.
Viale Luigi Sturzo 43, 20154 - Mediolan (MI) (Włochy)
Novartis Sverige AB
Torshamnsgatan 48, 164 40 Kista (Szwecja)
Novartis (Hellas) S.A.
12th km National Road Athinon-Lamia 14451 Metamorphosis Attiki, (Grecja).
Novartis Pharma B.V.
Haaksbergweg 16, 1101 BX Amsterdam (Holandia).
Novartis Poland Sp. z o.o.
15 Marynarska Street, 02-674 Warszawa (Polska).
Novartis Hungária Kft.
Vasút u.13, 2040 Budaörs (Węgry).
Abbot Biologicals B.V.
Veerweg, 12. 8121 AA Olst (Holandia)
Ten lek jest dopuszczony do obrotu w państwach członkowskich Europejskiego Obszaru Gospodarczego pod następującymi nazwami:
Austria, Belgia, Bułgaria, Chorwacja, Cypr, Czechy, Dania, Estonia, Finlandia, Francja, Grecja, Hiszpania, Holandia, Irlandia, Islandia, Litwa, Łotwa, Luksemburg, Malta, Niemcy, Norwegia, Polska, Portugalia, Rumunia, Słowacja, Słowenia, Szwecja, Węgry, Włochy | Sandostatin LAR |
Belgia, Luksemburg, Holandia | Sandostatine LAR |
Francja | Sandostatine L.P. |
Włochy, Portugalia | Sandostatina LAR |
Data ostatniej aktualizacji tego prospektu:12/2023
Pozostałe źródła informacji
Szczegółowe i aktualne informacje o tym leku są dostępne na stronie internetowej Hiszpańskiej Agencji Leków i Produktów Sanitarnych (AEMPS) http://www.aemps.gob.es/
Informacje te są przeznaczone wyłącznie dla profesjonalistów sektora zdrowia:
Jak stosować Sandostatin LAR
Akromegalia
Zalecane jest rozpoczęcie leczenia od podania 20 mg Sandostatin LAR w odstępach 4-tygodniowych przez 3 miesiące. Pacjenci leczeni Sandostatinem s.c. mogą rozpocząć leczenie Sandostatinem LAR w dniu następującym po ostatniej dawce Sandostatinu s.c.. Następne dostosowanie dawki powinno opierać się na stężeniach hormonu wzrostu (GH) i czynnika wzrostu 1 typu insulina/somatomedyna C (IGF-1) oraz objawach klinicznych.
Dla pacjentów, u których objawy kliniczne i parametry biochemiczne (GH; IGF-1) nie są w pełni kontrolowane w ciągu 3 miesięcy (stężenia GH nadal powyżej 2,5 mikrogramów/l), można zwiększyć dawkę do 30 mg co 4 tygodnie. Jeśli po 3 miesiącach GH, IGF-1 i/lub objawy nie są odpowiednio kontrolowane przy dawce 30 mg, dawkę można zwiększyć do 40 mg co 4 tygodnie.
Dla pacjentów z stężeniami GH poniżej 1 mikrograma/l i z normalizowanymi stężeniami IGF-1 we krwi, u których większość odwracalnych objawów akromegali zniknęła po 3 miesiącach leczenia dawką 20 mg, można podawać 10 mg Sandostatin LAR co 4 tygodnie. Jednak szczególnie w tej grupie pacjentów zalecane jest ścisłe monitorowanie stężeń GH i IGF-1 oraz objawów przy tej niskiej dawce Sandostatin LAR.
Dla pacjentów leczonych ustaloną dawką Sandostatin LAR, ocenę GH i IGF-1 należy przeprowadzać co 6 miesięcy.
Guzy endokrynne gastroenteropancreatic
- Leczenie pacjentów z objawami związanymi z guzami neuroendokrynnymi gastroenteropancreatic
Zalecane jest rozpoczęcie leczenia od podania 20 mg Sandostatin LAR w odstępach 4-tygodniowych. Pacjenci leczeni Sandostatinem s.c. powinni kontynuować leczenie dotychczasową dawką przez 2 tygodnie po pierwszym wstrzyknięciu Sandostatin LAR.
Dla pacjentów, u których objawy i markery biologiczne są dobrze kontrolowane po 3 miesiącach leczenia, można zmniejszyć dawkę do 10 mg Sandostatin LAR co 4 tygodnie.
Dla pacjentów, u których objawy są tylko częściowo kontrolowane po 3 miesiącach leczenia, można zwiększyć dawkę do 30 mg Sandostatin LAR co 4 tygodnie.
W dniach, w których mogą nasilić się objawy związane z guzami gastroenteropancreatic podczas leczenia Sandostatin LAR, zalecane jest dodatkowe podanie Sandostatinu s.c. w dawce stosowanej przed leczeniem Sandostatinem LAR. Może to nastąpić głównie w pierwszych 2 miesiącach leczenia, aż do osiągnięcia stężeń terapeutycznych oktreotydu.
- Leczenie pacjentów z zaawansowanymi guzami neuroendokrynnymi jelita lub nieznanego pochodzenia, w których wykluczono miejsca pochodzenia niebędące jelitem
Zalecana dawka Sandostatin LAR wynosi 30 mg podawane co 4 tygodnie. Leczenie Sandostatinem LAR w celu kontroli guza powinno być kontynuowane w przypadku braku progresji guza.
Leczenie gruczolaków wydzielających TSH
Leczenie Sandostatinem LAR powinno być rozpoczęte od dawki 20 mg w odstępach 4-tygodniowych przez 3 miesiące, zanim zostanie rozważone dostosowanie dawki. Następnie dawkę dostosowuje się na podstawie TSH i odpowiedzi hormonalnej tarczycy.
Instrukcje przygotowania i wstrzyknięcia domięśniowego Sandostatin LAR
TYLKO DO WSTRZYKNIĘĆ DOMIĘŚNIOWYCH
Składniki zestawu do wstrzyknięcia:
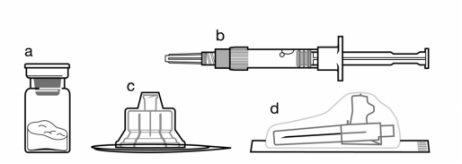
- Fiolka zawierająca proszek Sandostatin LAR
- Strzykawka przedładowana zawierająca rozpuszczalnik do rekonstytucji
- Adapter do fiolki do rekonstytucji leku
- Igła do wstrzyknięć ochronnych
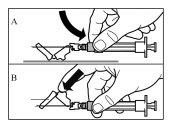
Postępuj zgodnie z poniższymi instrukcjami, aby zapewnić rekonstytucję Sandostatin LAR przed wstrzyknięciem domięśniowym
Istnieją trzy krytyczne etapy w procesie rekonstytucji Sandostatin LAR. Jeśli nie zostaną one wykonane prawidłowo, może to spowodować, że lek nie zostanie podany prawidłowo.
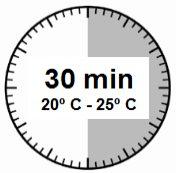
- Zestaw do wstrzyknięcia musi osiągnąć temperaturę pokojową. Wyjmij zestaw do wstrzyknięcia z lodówki i pozostaw go na temperaturze pokojowej przez co najmniej 30 minut przed rekonstytucją, ale nie dłużej niż 24 godziny.
- Po dodaniu roztworu rozpuszczalnika, pozostaw fiolkę na 5 minut aby upewnić się, że proszek jest całkowicie nasączony.
- Po nasączeniu, wstrząśnij fiolką umiarkowaniew kierunku poziomym przez co najmniej 30 sekund aż do utworzenia jednorodnej zawiesiny. Zawiesina Sandostatin LAR powinna być przygotowana bezpośrednioprzed podaniem.
Sandostatin LAR powinien być podawany tylko przez doświadczonego pracownika służby zdrowia.
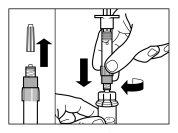
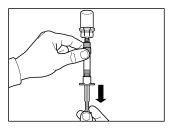
| KROK 1
UWAGA: jest niezwykle ważne, aby rozpocząć proces rekonstytucji tylko po tym, jak zestaw do wstrzyknięcia osiągnął temperaturę pokojową. Pozostaw zestaw do wstrzyknięcia na temperaturze pokojowej przez co najmniej 30 minut przed rekonstytucją, ale nie dłużej niż 24 godziny. Uwaga: Zestaw do wstrzyknięcia może być ponownie schłodzony, jeśli jest to konieczne. |
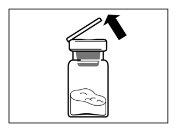
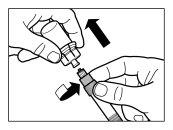
| KROK 2
|
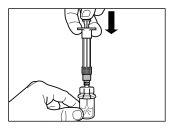
| KROK 3
|
| |
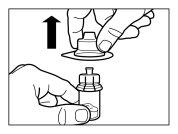
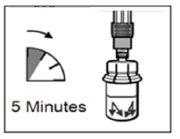
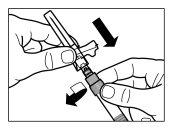
| KROK 4 UWAGA: jest niezwykle ważne, aby pozostawić fiolkę na 5 minut, aby upewnić się, że rozpuszczalnik całkowicie nasączył proszek. Uwaga: normalne jest, że tłok przesunie się w górę, ponieważ może wystąpić nadciśnienie w fiolce.
|
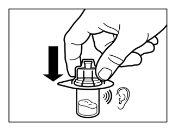
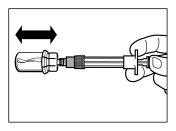
| KROK 5
UWAGA:Trzymaj tłok naciskany i wstrząśnij fiolką umiarkowaniew kierunku poziomym przez co najmniej 30 sekund, aby proszek był całkowicie zawiesiony w rozpuszczalniku (jednorodna zawiesina o konsystencji mlecznej). Powtórz wstrząsanie umiarkowane przez kolejne 30 sekund, jeśli proszek nie jest całkowicie zawiesiony. |
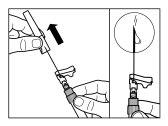
| KROK 6
|
| |
| KROK 7
|
| KROK 8
|
| KROK 9
|
- Kraj rejestracji
- Substancja czynna
- Wymaga receptyTak
- Producent
- Te informacje mają charakter wyłącznie poglądowy i nie stanowią porady medycznej. Przed zastosowaniem jakiegokolwiek leku zawsze skonsultuj się z lekarzem. Oladoctor nie ponosi odpowiedzialności za decyzje medyczne podjęte na podstawie tych treści.
- Zamienniki SANDOSTATIN LAR 20 mg PROSZEK I ROZPUSZCZALNIK DO PRZYGOTOWANIA ZAWIESINY DO WSTRZYKIWAŃPostać farmaceutyczna: ROZTWÓR DO WSTRZYKIWAŃ, Octreotyd 100 mikrogramów/mlSubstancja czynna: octreotideProducent: Gp Pharm S.A.Wymaga receptyPostać farmaceutyczna: ROZTWÓR DO WSTRZYKIWAŃ, Octreotyd 500 mikrogramów/mlSubstancja czynna: octreotideProducent: Gp Pharm S.A.Wymaga receptyPostać farmaceutyczna: ROZTWÓR DO WSTRZYKIWAŃ, 200 mikrogramów/mlSubstancja czynna: octreotideProducent: Gp Pharm S.A.Wymaga recepty
Odpowiedniki SANDOSTATIN LAR 20 mg PROSZEK I ROZPUSZCZALNIK DO PRZYGOTOWANIA ZAWIESINY DO WSTRZYKIWAŃ w innych krajach
Najlepsze odpowiedniki z tą samą substancją czynną i działaniem terapeutycznym.
Odpowiednik SANDOSTATIN LAR 20 mg PROSZEK I ROZPUSZCZALNIK DO PRZYGOTOWANIA ZAWIESINY DO WSTRZYKIWAŃ – Polska
Odpowiednik SANDOSTATIN LAR 20 mg PROSZEK I ROZPUSZCZALNIK DO PRZYGOTOWANIA ZAWIESINY DO WSTRZYKIWAŃ – Ukraina
Lekarze online w sprawie SANDOSTATIN LAR 20 mg PROSZEK I ROZPUSZCZALNIK DO PRZYGOTOWANIA ZAWIESINY DO WSTRZYKIWAŃ
Konsultacja w sprawie dawkowania, działań niepożądanych, interakcji, przeciwwskazań i odnowienia recepty na SANDOSTATIN LAR 20 mg PROSZEK I ROZPUSZCZALNIK DO PRZYGOTOWANIA ZAWIESINY DO WSTRZYKIWAŃ – decyzja należy do lekarza, zgodnie z lokalnymi przepisami.