AMBIRIX SUSPENSION INYECTABLE EN JERINGA PRECARGADA

Cómo usar AMBIRIX SUSPENSION INYECTABLE EN JERINGA PRECARGADA
Traducción generada por IA
Este contenido ha sido traducido automáticamente y se ofrece solo con fines informativos. No sustituye la consulta con un profesional sanitario.
Ver originalContenido del prospecto
Introducción
Prospecto: información para el usuario
Ambirix, suspensión inyectable en jeringa precargada
Vacuna (HAB) (adsorbida) antihepatitis A (inactivada) y antihepatitis B (ADNr)
Lea todo el prospecto detenidamente antes de que usted/su hijo empiece a recibir esta vacuna,porque contiene información importante para usted.
- Conserve este prospecto, ya que puede tener que volver a leerlo.
- Si tiene alguna duda, consulte a su médico, farmacéutico o enfermero.
- Esta vacuna se le ha recetado solamente a usted/su hijo, y no debe dársela a otras personas.
- Si usted/su hijo experimenta efectos adversos, consulte a su médico, farmacéutico o enfermero, incluso si se trata de efectos adversos que no aparecen en este prospecto. Ver sección 4.
Este prospecto se ha escrito asumiendo que la persona que recibe la vacuna es la que lo está leyendo. Sin embargo, la vacuna se puede administrar a niños y adolescentes de modo que puede que usted lo esté leyendo por su hijo.
Contenido del prospecto
- Qué es Ambirix y para qué se utiliza
- Qué necesita saber antes de recibir Ambirix
- Cómo administrar Ambirix
- Posibles efectos adversos
- Conservación de Ambirix
- Contenido del envase e información adicional
1. Qué es Ambirix y para qué se utiliza
Ambirix es una vacuna utilizada en lactantes, niños y jóvenes a partir de 1 año de edad y hasta los 15 años inclusive. Se utiliza para prevenir dos enfermedades: la hepatitis A y la hepatitis B.
- Hepatitis A:La infección por el virus de la hepatitis A puede causar inflamación del hígado. El virus se adquiere a partir de alimentos o bebidas que contienen el virus. Sin embargo, a veces se adquiere por otros medios, tales como nadando en aguas residuales o a partir de otra persona infectada. El virus se halla presente en fluidos corporales tales como las heces, el suero o la saliva.
Los síntomas comienzan entre las 3 y las 6 semanas después de la infección. Algunas personas pueden tener náuseas, fiebre y dolores. Después de varios días pueden sentirse muy cansadas, tener la orina oscura, la cara pálida y la piel o los ojos amarillentos (ictericia). La gravedad y el tipo de síntomas pueden variar. Es posible que los niños pequeños no sufran todos los síntomas. La mayoría de los niños se recupera completamente de la enfermedad aunque, por lo general, es lo suficientemente grave como para hacer que los niños estén enfermos durante aproximadamente un mes.
- Hepatitis B:La infección por el virus de la hepatitis B puede causar inflamación del hígado. El virus se adquiere normalmente a partir de otra persona infectada. Se encuentra en fluidos corporales tales como la sangre, el semen, las secreciones vaginales o la saliva (esputo).
Es posible que no se observen síntomas durante las 6 semanas o los 6 meses después de la infección. Las personas que han sido infectadas no siempre se sienten o parecen enfermas. Algunas personas pueden tener náuseas, fiebre y dolores. Sin embargo, otras pueden llegar a estar muy enfermas. Pueden estar muy cansadas, tener la orina oscura, la cara pálida y la piel o los ojos amarillentos (ictericia). Es posible que algunas personas necesiten acudir a un hospital.
La mayoría de los adultos se recupera completamente de la enfermedad, aunque algunas personas (particularmente los niños) que no hayan tenido síntomas pueden permanecer infectadas. A estas personas se les conoce como “portadoras” de la hepatitis B y pueden continuar infectando a otras personas a lo largo de su vida. Además, los portadores están en riesgo de padecer problemas graves del hígado, tales como hígado dañado (cirrosis) o cáncer de hígado.
Cómo funciona Ambirix
- Ambirix ayuda a que el organismo produzca su propia protección (anticuerpos) frente a estas enfermedades. La vacuna no contiene virus vivos (ver sección 6 para el contenido de la vacuna) y, por lo tanto, no puede producir infecciones por el virus de la hepatitis A o B.
- Al igual que con todas las vacunas, algunas personas no responden igual de bien a una vacuna que otras.
- Puede que Ambirix no le proteja de la enfermedad si ya ha adquirido el virus de la hepatitis A o B.
- Ambirix sólo puede ayudar a protegerle frente a infecciones por el virus de la hepatitis A o B. No puede proteger frente a otras infecciones que puedan afectar al hígado, incluso aunque esas infecciones tengan signos parecidos a aquellos causados por el virus de la hepatitis A o B.
2. Qué necesita saber antes de recibir Ambirix
Ambirix no se debe administrar si:
- es alérgico a Ambirix o a alguno de los demás componentes de esta vacuna (incluidos en la sección 6). Los signos de una reacción alérgica pueden incluir erupción de la piel con picor, dificultad para respirar e hinchazón de su cara o lengua
- ha tenido anteriormente una reacción alérgica a cualquier vacuna frente a la hepatitis A o hepatitis B
- tiene una infección grave con fiebre elevada. La vacuna se puede administrar una vez que se haya recuperado. Una infección de poca importancia, como un resfriado, no debería ser un problema para la vacunación, aunque consulte primero a su médico.
Ambirix no se debe administrar si se encuentra en cualquiera de las circunstancias anteriores. Si no está seguro, consulte a su médico, farmacéutico o enfermero antes de recibir Ambirix.
Advertencias y precauciones
Consulte a su médico, farmacéutico o enfermero antes de recibir Ambirix si:
- necesita estar completamente protegido frente a la infección de hepatitis A y B en los próximos 6 meses (puede que su médico le recomiende una vacuna diferente)
- tiene algún problema hemorrágico o le aparece cardenales con facilidad (la inyección se puede administrar justo debajo de la piel en lugar de en un músculo para reducir el sangrado o la aparición de cardenales)
- tiene problemas del sistema inmune (tales como los debidos a una enfermedad, tratamiento farmacológico o diálisis), puede que la vacuna no funcione completamente. Esto significa que puede que no esté protegido frente a uno o ambos virus de la hepatitis A y B. Su médico le realizará análisis de sangre para comprobar si se necesitan más inyecciones para ayudarle a estar mejor protegido
- se ha desmayado en anteriores ocasiones o durante una inyección previa, para prevenirlo en caso de que ocurra de nuevo. Antes o después de cualquier inyección, podría producirse un desmayo (especialmente en los adolescentes).
Si se encuentra en cualquiera de las circunstancias anteriores (o no está seguro), consulte a su médico, farmacéutico o enfermero antes de recibir Ambirix.
Otros medicamentosy Ambirix
Informe a su médico si está utilizando, ha utilizado recientemente o pudiera tener que utilizar cualquier otro medicamento o vacuna. Esto incluye a los medicamentos adquiridos sin receta y a los medicamentos a base de plantas. Pregunte a su médico, farmacéutico o enfermero si tiene alguna duda.
A pesar de que esté tomando medicamentos que afectan a la respuesta inmunológica de su cuerpo, puede recibir Ambirix si así se considera necesario. Sin embargo, puede que la vacuna no funcione completamente. Esto significa que puede que no esté protegido frente a uno o ambos virus de la hepatitis A y B. Su médico le realizará análisis de sangre para determinar si se necesitan más inyecciones para ayudarle a que esté mejor protegido.
Puede que sea necesario administrar Ambirix al mismo tiempo que otras vacunas frente a sarampión, parotiditis, rubéola, difteria, tétanos, tos ferina (pertussis), poliomielitis, Haemophilus influenzaetipo b o algunos tipos de tratamientos para las infecciones del hígado denominados “inmunoglobulinas”. Su médico se asegurará de que las vacunas se le inyectan en diferentes partes de su cuerpo.
Embarazo, lactancia y fertilidad
Si está embarazada o en periodo de lactancia, cree que podría estar embarazada o tiene intención de quedarse embarazada, consulte a su médico, farmacéutico o enfermero antes de recibir esta vacuna. Ambirix no se administra habitualmente a mujeres que están embarazadas o en periodo de lactancia.
Conducción y uso de máquinas
Puede que se sienta somnoliento o mareado después de recibir Ambirix. Si esto ocurre, no conduzca ni monte en bicicleta ni use herramientas o máquinas.
Ambirix contiene neomicina y sodio
Esta vacuna contiene neomicina (un antibiótico). Ambirix no debe administrarse si es alérgico a la neomicina.
Esta vacuna contiene menos de 1 mmol de sodio (23 mg) por dosis; esto es, esencialmente “exento de sodio”.
3. Cómo administrar Ambirix
Cómo se administra la inyección
- El médico o enfermero administrará Ambirix como una inyección en un músculo, normalmente en la parte superior del brazo.
- Ellos tendrán cuidado de que Ambirix no se administre en una vena.
- En niños muy pequeños, la inyección puede administrarse en el músculo del muslo.
Cuánto se administra
- Recibirá normalmente un total de dos inyecciones. Cada una se administra en una visita independiente.
- Las inyecciones se administrarán dentro de un periodo de 12 meses:
- La primera inyección - en una fecha acordada con su médico.
- La segunda inyección - entre 6 y 12 meses después de la primera inyección.
Su médico le aconsejará sobre la necesidad de dosis adicionales y futuras dosis de recuerdo.
Si no recibe una dosis
- Si no recibe la segunda inyección, hable con su médico para fijar otra visita tan pronto como sea posible.
- Asegúrese de que termina la serie completa de dos inyecciones. En caso contrario, puede que no esté protegido frente a las enfermedades.
4. Posibles efectos adversos
Al igual que todos los medicamentos, esta vacuna puede producir efectos adversos, aunque no todas las personas los sufran.
Efectos adversos graves
- Informe a su médico inmediatamente si nota cualquiera de los siguientes efectos adversos graves (puede que necesite tratamiento médico urgente):reacciones anafilácticas y alérgicas: los signos pueden incluir una erupción cutánea con picor o ampollas, hinchazón de los ojos y de la cara, dificultad para respirar o tragar, bajada repentina de la presión sanguínea y pérdida del conocimiento.
Informe a su médico inmediatamente si nota cualquiera de los efectos adversos graves enumerados arriba.
Los efectos adversos ocurridos durante los ensayos clínicos con Ambirix fueron los siguientes:
Muy frecuentes(pueden ocurrir en más de 1 de cada 10 dosis de la vacuna): dolor de cabeza, pérdida del apetito, sensación de cansancio o irritabilidad, dolor y enrojecimiento en el lugar en el que se administró la inyección.
Frecuentes(pueden ocurrir en hasta 1 de cada 10 dosis de la vacuna): fiebre, sensación de somnolencia, problemas de estómago y digestivos, hinchazón en el lugar en el que se administró la inyección.
Los efectos adversos adicionales comunicados durante los ensayos clínicos con vacunas combinadas frente a la hepatitis A y hepatitis B muy similares a ésta, incluyen:
Frecuentes(pueden ocurrir en hasta 1 de cada 10 dosis de la vacuna): malestar general, diarrea, náuseas, reacción en el lugar en el que se administró la inyección.
Poco frecuentes(pueden ocurrir en hasta 1 de cada 100 dosis de la vacuna): sensación de mareo, dolor de estómago, vómitos, infecciones de las vías respiratorias superiores, dolor muscular (mialgia).
Raros(pueden ocurrir en hasta 1 de cada 1.000 dosis de la vacuna): presión sanguínea baja, dolor articular (artralgia), picor (prurito), erupción cutánea, hormigueo (parestesia), hinchazón de glándulas del cuello, axilas e ingles (linfadenopatía), síntomas gripales, tales como temperatura elevada, dolor de garganta, moqueo, tos y escalofríos.
Muy raros(pueden ocurrir en hasta 1 de cada 10.000 dosis de la vacuna): habones (urticaria).
Contacte con su médico si tiene efectos adversos similares.
Los efectos adversos ocurridos durante el uso rutinario de Ambirix, fueron los siguientes:desmayo, pérdida de la sensibilidad de la piel al dolor o al tacto (hipoestesia).
Los efectos adversos adicionales ocurridos durante el uso rutinario de vacunas combinadas o individuales frente a la hepatitis A y hepatitis B muy similares a ésta, fueron los siguientes:esclerosis múltiple, hinchazón de la médula espinal (mielitis), resultados de los análisis anormales en relación al hígado, hinchazón o infección del cerebro (encefalitis), inflamación de algunos vasos sanguíneos (vasculitis), una enfermedad degenerativa del cerebro (encefalopatía), hinchazón de la cara, la boca y la garganta (edema angioneurótico), dolor de cabeza intenso con rigidez de cuello y sensibilidad a la luz (meningitis), una inflamación temporal de los nervios que causa dolor, debilidad y parálisis en los brazos y las piernas y a menudo progresa al pecho y la cara (síndrome de Guillain-Barré), convulsiones o ataques, inflamación de los nervios (neuritis), enfermedad de los nervios de los ojos (neuritis óptica), entumecimiento o debilidad de los brazos y las piernas (neuropatía), dolor inmediato en el lugar de la inyección, escozor y sensación de ardor, parálisis, párpado colgante y músculos caídos en un lado de la cara (parálisis facial), enfermedad que afecta principalmente a las articulaciones con dolor e hinchazón (artritis) debilidad muscular, bultos de color púrpura o púrpura rojizo en la piel (liquen plano), erupciones de la piel graves (eritema multiforme), reducción de las plaquetas sanguíneas, lo que incrementa el riesgo de sangrado o aparición de cardenales (trombocitopenia), manchas de color púrpura o marrón rojizo visibles a través de la piel (púrpura trombocitopénica).
Comunicación de efectos adversos
Si experimenta cualquier tipo de efecto adverso, consulte a su médico o farmacéutico, incluso si se trata de posibles efectos adversos que no aparecen en este prospecto. También puede comunicarlos directamente a través del sistema nacional de notificación incluido en el Apéndice V. Mediante la comunicación de efectos adversos usted puede contribuir a proporcionar más información sobre la seguridad de este medicamento.
5. Conservación de Ambirix
Mantener esta vacuna fuera de la vista y del alcance de los niños.
No utilice esta vacuna después de la fecha de caducidad que aparece en el envase. La fecha de caducidad es el último día del mes que se indica.
Conservar en nevera (entre 2 ºC y 8 ºC). No congelar. La congelación destruye la vacuna.
Conservar en el embalaje original para protegerlo de la luz.
Los medicamentos no se deben tirar por los desagües ni a la basura. Pregunte a su farmacéutico cómo deshacerse de los envases y de los medicamentos que ya no necesita. De esta forma, ayudará a proteger el medio ambiente.
6. Contenido del envase e información adicional
Composición de Ambirix
- Los principios activos son:
- Virus de la hepatitis A (inactivados)1,2 720 Unidades ELISA
- Antígeno de superficie de la hepatitis B3,4 20 microgramos
1Producido en células diploides humanas (MRC-5)
2Adsorbido en hidróxido hidratado de aluminio 0,05 miligramos Al3+
3Producido por la tecnología del ADN recombinante en células de levadura (Saccharomyces cerevisiae)
4Adsorbido en fosfato de aluminio 0,4 miligramos Al3+
- Los demás componentes de Ambirix son: cloruro de sodio y agua para preparaciones inyectables.
Aspecto del productoy contenido del envase
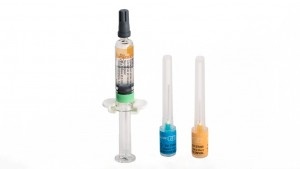
Ambirix es un líquido blanco y ligeramente lechoso.
Ambirix está disponible en jeringa precargada de 1 dosis con o sin agujas separadas, tamaños de envases de 1, 10 y 50 .
Puede que solamente estén comercializados algunos tamaños de envases.
Titular de la autorización de comercialización y responsable de la fabricación
GlaxoSmithKline Biologicals s.a.
Rue de l’Institut 89
B-1330 Rixensart
Bélgica
Pueden solicitar más información respecto a este medicamento dirigiéndose al representante local del titular de la autorización de comercialización:
België/Belgique/Belgien GlaxoSmithKline Pharmaceuticals SA/NV Tél/Tel: + 32 10 85 52 00 | Lietuva GlaxoSmithKline Biologicals SA Tel. + 370 80000334 |
???????? GlaxoSmithKline Biologicals SA ???.: + 359 80018205 | Luxembourg/Luxemburg GlaxoSmithKline Pharmaceuticals SA/NV Tél/Tel: + 32 10 85 52 00 |
Ceská republika GlaxoSmithKline s.r.o. Tel: + 420 2 22 00 11 11 | Magyarország GlaxoSmithKline Biologicals SA Tel.: + 36 80088309 |
Danmark GlaxoSmithKline Pharma A/S Tlf: + 45 36 35 91 00 | Malta GlaxoSmithKline Biologicals SA Tel: + 356 80065004 |
Deutschland GlaxoSmithKline GmbH & Co. KG Tel: + 49 (0)89 360448701 | Nederland GlaxoSmithKline BV Tel: + 31 (0)33 2081100 |
Eesti GlaxoSmithKline Biologicals SA Tel: + 372 8002640 | Norge GlaxoSmithKline AS Tlf: + 47 22 70 20 00 |
Ελλ?δα GlaxoSmithKline Μονοπρ?σωπη A.E.B.E. Tηλ: + 30 210 68 82 100 | Österreich GlaxoSmithKline Pharma GmbH. Tel: + 43 (0)1 97075-0 |
España GlaxoSmithKline, S.A. Tel: + 34 900 202 700 | Polska GSK Services Sp. z o.o. Tel.: + 48 (22) 576 9000 |
France Laboratoire GlaxoSmithKline Tél: + 33 (0) 1 39 17 84 44 Hrvatska GlaxoSmithKline Biologicals SA Tel.: + 385 800787089 | Portugal Smith Kline & French Portuguesa - Produtos Farmacêuticos, Lda. Tel: + 351 21 412 95 00 România GlaxoSmithKline Biologicals SA Tel: + 40 800672524 |
Ireland GlaxoSmithKline (Ireland) Ltd Tel: + 353 (0)1 495 5000 | Slovenija GlaxoSmithKline Biologicals SA Tel: + 386 80688869 |
Ísland Vistor hf. Sími: + 354 535 7000 | Slovenskárepublika GlaxoSmithKline Biologicals SA Tel: + 421 800500589 |
Italia GlaxoSmithKline S.p.A. Tel: + 39 (0)45 7741 111 | Suomi/Finland GlaxoSmithKline Oy Puh/Tel: + 358 (0)10 30 30 30 |
Κ?προς GlaxoSmithKline Biologicals SA Τηλ: + 357 80070017 | Sverige GlaxoSmithKline AB Tel: + 46 (0)8 638 93 00 |
Latvija GlaxoSmithKline Biologicals SA Tel: + 371 80205045 | United Kingdom(Northern Ireland) GlaxoSmithKline Biologicals SA Tel: + 44 (0)800 221441 |
Fecha de la última revisión de este prospecto:
Otras fuentes de información
La información detallada de este medicamento está disponible en la página web de la Agencia Europea de Medicamentos: http://www.ema.europa.eu, y en la página web de la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) (http://www.aemps.gob.es/).
---------------------------------------------------------------------------------------------------------------------
Esta información está destinada únicamente a profesionales sanitarios:
Durante el almacenamiento se puede observar un depósito fino de color blanco con una capa translúcida e incolora por encima.
Se debe resuspender la vacuna antes de su uso. Una vez resuspendida, la vacuna tendrá una apariencia blanca, turbia y uniforme.
Resuspensión de la vacuna para obtener una suspensión blanca, turbia y uniforme
Se debe resuspender la vacuna siguiendo los pasos que se indican a continuación.
- Sujetar la jeringa boca arriba con la mano cerrada.
- Agitar la jeringa volteándola boca abajo y nuevamente boca arriba.
- Repetir esta acción de forma vigorosa durante, por lo menos, 15 segundos.
- Inspeccionar de nuevo la vacuna:
- Si la vacuna se muestra como una suspensión blanca, turbia y uniforme, está lista para ser usada (no debe tener una apariencia translúcida).
- Si la vacuna todavía no se muestra como una suspensión blanca, turbia y uniforme, voltearla boca abajo y nuevamente boca arriba durante, por lo menos, otros 15 segundos y a continuación inspeccionar de nuevo.
Antes de la administración, la vacuna se debe inspeccionar visualmente para observar si tiene alguna partícula extraña y/o apariencia física anormal. En caso de observar cualquiera de estas circunstancias, no administrar la vacuna.
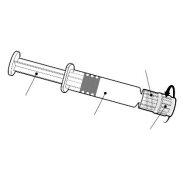
Instrucciones para la jeringa precargada tras la resuspensión
| Sostenga la jeringa por el cuerpo, no por el émbolo. Desenrosque el tapón de la jeringa girándola en sentido contrario a las agujas del reloj. | |
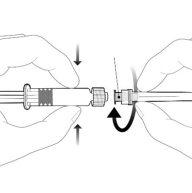
| Para insertar la aguja, conecte la base al adaptador luer-locky gírelo un cuarto de vuelta en el sentido de las agujas del reloj hasta que sienta que se bloquea. No saque el émbolo de la jeringa del cuerpo. Si esto ocurre, no administre la vacuna. |
Eliminación de residuos
La eliminación del medicamento no utilizado y de todos los materiales que hayan estado en contacto con él se realizará de acuerdo con la normativa local.
- País de registro
- Principio activo
- Requiere recetaSí
- Fabricante
- Esta información es de carácter general y no sustituye la consulta con un profesional sanitario.
- Alternativas a AMBIRIX SUSPENSION INYECTABLE EN JERINGA PRECARGADAForma farmacéutica: INYECTABLE, DesconocidaPrincipio activo: combinationsFabricante: Glaxosmithkline BiologicalsRequiere recetaForma farmacéutica: INYECTABLE, DescpnocidaPrincipio activo: combinationsFabricante: Glaxosmithkline BiologicalsRequiere recetaForma farmacéutica: INYECTABLE, DescpnocidaPrincipio activo: combinationsFabricante: Glaxosmithkline BiologicalsRequiere receta
Médicos online para AMBIRIX SUSPENSION INYECTABLE EN JERINGA PRECARGADA
Comenta la dosis, los posibles efectos secundarios, interacciones, contraindicaciones o la revisión de receta de AMBIRIX SUSPENSION INYECTABLE EN JERINGA PRECARGADA, sujeto a valoración médica y a la normativa local.
Preguntas frecuentes