

Octaplex

Zapytaj lekarza o receptę na Octaplex

Jak stosować Octaplex
ULOTKA DOŁĄCZONA DO OPAKOWANIA: INFORMACJA DLA UŻYTKOWNIKA
Octaplex, 500 j.m., proszek i rozpuszczalnik do sporządzania roztworu do infuzji
Zespół protrombiny ludzkiej
Octaplex, 1000 j.m., proszek i rozpuszczalnik do sporządzania roztworu do infuzji
Zespół protrombiny ludzkiej
Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje ważne dla pacjenta.
- Należy zachować tę ulotkę, aby w razie potrzeby móc ją ponownie przeczytać.
- W razie jakichkolwiek wątpliwości należy zwrócić się do lekarza, farmaceuty lub pielęgniarki.
- Lek ten przepisano ściśle określonej osobie. Nie należy go przekazywać innym. Lek może zaszkodzić innej osobie, nawet jeśli objawy jej choroby są takie same.
- Jeśli u pacjenta wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie objawy niepożądane niewymienione w tej ulotce, należy powiedzieć o tym lekarzowi, farmaceucie lub pielęgniarce. Patrz punkt 4.
Spis treści ulotki:
- 1. Co to jest lek Octaplex i w jakim celu się go stosuje
- 2. Informacje ważne przed zastosowaniem leku Octaplex
- 3. Jak stosować lek Octaplex
- 4. Możliwe działania niepożądane
- 5. Jak przechowywać lek Octaplex
- 6. Zawartość opakowania i inne informacje
1. CO TO JEST LEK OCTAPLEX I W JAKIM CELU SIĘ GO STOSUJE
Octaplex należy do grupy leków nazywanych czynnikami krzepnięcia. Zawiera zależne od witaminy
K ludzkie czynniki krzepnięcia II, VII, IX i X.
Octaplex jest stosowany w celu leczenia krwawień i zapobieganiu krwawieniom:
- spowodowanym leczeniem antagonistami witaminy K (takimi jak warfaryna). Te leki blokują działanie witaminy K i powodują niedobór czynników krzepnięcia zależnych od witaminy K. Octaplex jest stosowany gdy wymagane jest szybkie wyrównanie niedoboru;
- u pacjentów urodzonych z niedoborem czynników krzepnięcia II i X zależnych od witaminy K. Podawany jest, gdy oczyszczony produkt danego czynnika krzepnięcia nie jest dostępny.
2. INFORMACJE WAŻNE PRZED ZASTOSOWANIEM LEKU OCTAPLEX
Kiedy nie stosować leku Octaplex:
- jeśli pacjent ma uczulenie na którykolwiek ze składników tego leku (wymienionych w punkcie 6),
- jeśli u pacjenta występuje alergia na heparynę lub kiedykolwiek w przeszłości występował spadek poziomu płytek krwi po heparynie.
- jeśli u pacjenta występuje niedobór IgA z obecnością przeciwciał przeciwko IgA.
Ostrzeżenia i środki ostrożności
- Powinno się zasięgnąć rady specjalisty mającego doświadczenie w leczeniu zaburzeń krzepnięcia podczas otrzymywania leku Octaplex.
- U pacjentów z nabytym niedoborem czynników krzepnięcia zależnych od witaminy K (na przykład wywołanym leczeniem antagonistami witaminy K), Octaplex powinien być zastosowany jedynie kiedy niezbędna jest szybka korekta poziomu kompleksu protrombiny, tak jak w przypadku dużych krwawień lub nagłych zabiegów operacyjnych. W innych przypadkach zmniejszenie dawki antagonistów witaminy K i/lub podanie witaminy K jest zwykle wystarczające.
- Pacjenci leczeni antagonistami witaminy K (takimi jak warfaryna) mogą mieć zwiększone ryzyko powstawania zakrzepów. W takim przypadku leczenie lekiem Octaplex może zwiększyć ryzyko.
- We wrodzonym niedoborze danego czynnika krzepnięcia zależnego od witaminy K, powinno się zastosować określony produkt tego czynnika krzepnięcia jeżeli jest dostępny.
- W przypadku pojawienia się reakcji alergicznej lub anafilaktycznej infuzję należy natychmiast wstrzymać i zastosować odpowiednie leczenie.
- Występuje ryzyko zakrzepicy lub zespołu rozsianego wykrzepiania śródnaczyniowego (poważne schorzenie polegające na tworzeniu zakrzepów w całym organizmie) u pacjentów otrzymujących lek Octaplex (zwłaszcza gdy jest otrzymywany regularnie). Pacjenci otrzymujący zespół protrombiny ludzkiej powinni być ściśle obserwowani pod względem objawów i symptomów zespołu rozsianego wykrzepiania śródnaczyniowego i zakrzepicy. Jest to zwłaszcza istotne u pacjentów z chorobą niedokrwienną serca w wywiadzie, chorobą wątroby, u pacjentów oczekujących na zabieg operacyjny oraz gdy Octaplex jest podawany małym dzieciom.
- Nie ma dostępnych danych odnośnie zastosowania Octaplex w przypadku krwawienia okołoporodowego związanego z niedoborem witaminy K u noworodków.
Bezpieczeństwo wirusowe
- W przypadku produktów leczniczych otrzymywanych z ludzkiej krwi lub osocza stosuje się odpowiednie metody zapobiegające przenoszeniu zakażeń na pacjentów. Obejmują one ścisłą selekcję dawców krwi i osocza w celu wyeliminowania zakażonych nosicieli oraz badanie poszczególnych donacji i puli osocza w kierunku specyficznych markerów wirusowych. Wytwórcy tych produktów również włączają do procesu wytwarzania odpowiednie metody mające na celu inaktywację lub usunięcie wirusów. Pomimo tego, w przypadku podawania produktów otrzymywanych z ludzkiej krwi lub osocza, możliwość przeniesienia czynnika zakaźnego nie może być całkowicie wykluczona. Dotyczy to także zakażeń wywołanych nieznanym lub nowym wirusem lub innych rodzajów zakażeń. Zastosowane metody uważane są za skuteczne wobec wirusów otoczkowych takich jak wirus ludzkiego niedoboru odporności (HIV), wirus zapalenia wątroby typu B (HBV) i wirus zapalenia wątroby typu C (HCV). Zastosowane metody mogą mieć ograniczoną skuteczność wobec wirusów bezotoczkowych takich jak wirus zapalenia wątroby typu A (HAV) lub parwowirus B19. Parwowirus B19 może być niebezpieczny dla kobiet w ciąży (zakażenie płodu) i dla pacjentów z niedoborami odporności lub chorych na pewny rodzaj niedokrwistości (np. w niedokrwistości sierpowatokrwinkowej lub niedokrwistości hemolitycznej). Zaleca się zapisywanie nazwy i numeru serii produktu w przypadku każdorazowego podawania Octaplex w celu powiązania z zastosowaną serią.
- Wskazane są odpowiednie szczepienia (przeciwko wirusowemu zapaleniu wątroby typu A i B) w przypadku regularnego/powtarzanego podawania produktów kompleksu protrombiny otrzymywanego z ludzkiego osocza.
Dzieci i młodzież
Dane dotyczące stosowania leku Octaplex u dzieci i młodzieży nie są dostępne.
Lek Octaplex a inne leki
Leku Octaplex nie wolno mieszać z innymi produktami leczniczymi.
Octaplex neutralizuje efekt leczenia antagonistami witaminy K, ale nie są znane interakcje z innymi
produktami leczniczymi .
Octaplex może wpływać na wyniki testów krzepnięcia, które są zależne od heparyny.
Należy powiedzieć lekarzowi lub farmaceucie o wszystkich lekach przyjmowanych przez pacjenta
obecnie lub ostatnio, a także o lekach, które pacjent planuje przyjmować.
Ciąża i karmienie piersią
Octaplex powinien być stosowany w trakcie ciąży i karmienia piersią jedynie jeżeli jest ściśle
wskazany. Przed zastosowaniem produktu należy poradzić się lekarza lub farmaceuty.
Prowadzenie pojazdów i obsługiwanie maszyn
Nie jest znany wpływ leku Octaplex na zdolność prowadzenia pojazdów mechanicznych
i obsługiwania urządzeń mechanicznych w ruchu.
Ważne informacje o niektórych składnikach leku Octaplex
- Heparyna może spowodować reakcje alergiczne i spadek liczby komórek krwi odpowiedzialnych za krzepnięcie krwi. Pacjenci ze znanymi w przeszłości wywołanymi heparyną reakcjami alergicznymi powinni unikać stosowania leków zawierających heparynę.
- Lek zawiera 75-125 mg (fiolka 500 j.m.) lub 150-250 mg (fiolka 1000 j.m.) sodu (głównego składnika soli kuchennej) w każdej fiolce. Odpowiada to 3,8-6,3% lub 7,5-12,5% maksymalnej zalecanej dobowej dawki sodu w diecie u osób dorosłych.
3. JAK STOSOWAĆ LEK OCTAPLEX
Leczenie lekiem Octaplex powinno być rozpoczęte pod nadzorem lekarza specjalisty w leczeniu
zaburzeń krzepnięcia.
- Po pierwsze proszek należy rozpuścić w wodzie do wstrzykiwań.
- Następnie roztwór powinien być podany do żyły (droga dożylna).
Dawka otrzymywanego leku Octaplex oraz czas trwania leczenia zależą od:
- nasilenia choroby;
- miejsca krwawienia, jego nasilenia i
- stanu ogólnego pacjenta.
Zastosowanie większej niż zalecana dawki leku Octaplex
W przypadku przedawkowania wzrasta ryzyko
- rozwoju powikłań zakrzepowych (takich jak zawał serca i zakrzepica w żyłach lub płucach),
- rozsianego wykrzepiania śródnaczyniowego (poważnego schorzenia polegającego na występowaniu zakrzepów w całym organizmie).
4. MOŻLIWE DZIAŁANIA NIEPOŻĄDANE
Jak każdy lek, lek ten może powodować działania niepożądane, chociaż nie u każdego one wystąpią.
Często (mogą wystąpić u nie więcej niż 1 na 10 osób)
Zakrzepy w naczyniach krwionośnych.
Niezbyt często (mogą wystąpić u nie więcej niż 1 na 100 osób)
Lęki, wzrost ciśnienia tętniczego, objawy przypominające astmę oskrzelową, krwioplucie, krwawienie
z nosa, pieczenie w miejscu iniekcji, zakrzepy w urządzeniu.
Rzadko (mogą wystąpić u nie więcej niż 1 na 1000 osób)
Mogą wystąpić reakcje typu alergicznego. Rzadko obserwuje się tymczasowy wzrost wyników prób
wątrobowych (transaminaz).
U pacjentów leczonych lekiem Octaplex w terapii zastępczej mogą powstać przeciwciała
neutralizujące (inhibitory) przeciw któremukolwiek z zawartych czynników krzepnięcia. W przypadku
pojawienia się tych inhibitorów leczenie substytucyjne nie będzie wysoce skuteczne.
Bardzo rzadko (mogą wystąpić u nie więcej niż 1 na 10 000 osób)
Obserwowano przypadki wzrostu temperatury ciała (gorączki).
Występuje ryzyko powstawania zakrzepów po podaniu tego leku.
Częstość nieznana (częstość nie może być określona na podstawie dostępnych danych)
Ciężkie reakcje alergiczne i wstrząs, nadwrażliwość, drżenie, niewydolność serca, przyspieszenie akcji
serca, zaburzenia krążenia krwi, spadek ciśnienia krwi, niewydolność oddechowa, zaburzenia
oddychania, nudności, pokrzywka, wysypka, dreszcze.
Heparyna zawarta w preparacie może spowodować nagły spadek liczby płytek we krwi. Jest to reakcja
alergiczna nazywana "wywołaną heparyną trombocytopenią typu II". W rzadkich przypadkach ten
spadek liczby płytek może wystąpić 6-14 dni po rozpoczęciu leczenia u pacjentów bez wcześniejszej
nadwrażliwości na heparynę. U pacjentów ze znaną nadwrażliwością na heparynę zmiana ta może
wystąpić w ciągu kilku godzin po rozpoczęciu leczenia.
Należy niezwłocznie przerwać leczenie preparatem Octaplex u pacjentów wykazujących taką reakcję
alergiczną. Pacjentom tym nie wolno podawać w przyszłości produktów leczniczych zawierających
heparynę.
Informacje odnośnie bezpieczeństwa wirusowego, patrz punkt 2.
Zgłaszanie działań niepożądanych
Jeśli wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie objawy niepożądane niewymienione
w tej ulotce, należy powiedzieć o tym lekarzowi, farmaceucie lub pielęgniarce. Działania niepożądane
można zgłaszać bezpośrednio do Departamentu Monitorowania Niepożądanych Działań Produktów
Leczniczych Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów
Biobójczych,
Al. Jerozolimskie 181C, 02-222 Warszawa,
tel.: + 48 22 49 21 301, faks: + 48 22 49 21 309
e-mail: [email protected].
Dzięki zgłaszaniu działań niepożądanych można będzie zgromadzić więcej informacji na temat
bezpieczeństwa stosowania leku.
5. JAK PRZECHOWYWAĆ LEK OCTAPLEX
Lek należy przechowywać w miejscu niewidocznym i niedostępnym dla dzieci.
Nie stosować tego leku po upływie terminu ważności zamieszczonego na opakowaniu. Termin
ważności oznacza ostatni dzień podanego miesiąca.
Nie przechowywać w temperaturze powyżej 25˚C. Nie zamrażać. Przechowywać w oryginalnym
opakowaniu w celu ochrony przed światłem.
Proszek należy rozpuszczać tylko bezpośrednio przed wstrzyknięciem. Wykazano stabilność roztworu
przez okres do 8 godzin w temperaturze 25°C. Jednak w celu uniknięcia zanieczyszczenia roztwór
należy zużyć natychmiast i tylko jednorazowo.
6. ZAWARTOŚĆ OPAKOWANIA I INNE INFORMACJE
Co zawiera Octaplex w fiolce i po rozpuszczeniu w 20 ml (500 j.m.)/40 ml (1000 j.m.)
rozpuszczalnika
Substancjami czynnymi są:
| Nazwa substancji czynnej | Octaplex Zawartość w fiolce 500 j.m. | Octaplex Zawartość w fiolce 1000 j.m. | Octaplex Zawartość w 1 ml sporządzonego roztworu |
| Białko całkowite: | 260–820 mg | 520–1640 mg |
|
| Substancje czynne | |||
| Ludzki II czynnik krzepnięcia krwi | 280–760 j.m. | 560–1520 j.m. |
|
| Ludzki VII czynnik krzepnięcia krwi | 180–480 j.m. | 360–960 j.m. |
|
| Ludzki IX czynnik krzepnięcia krwi | 500 j.m. | 1000 j.m. | 25 j.m./ml |
| Ludzki X czynnik krzepnięcia krwi | 360–600 j.m. | 720–1200 j.m. |
|
| Dodatkowe substancje czynne | |||
| Białko C | 260–620 j.m. | 520–1240 j.m. |
|
| Białko S | 240–640 j.m. | 480–1280 j.m. |
|
Aktywność swoista produktu wynosi ≥ 0,6 j.m./mg, wyrażona jako aktywność czynnika IX.
Pozostałe składniki to:
heparyna, trisodu cytrynian dwuwodny , woda do wstrzykiwań.
Jak wygląda Octaplex i co zawiera opakowanie
Octaplex występuje w postaci proszku i rozpuszczalnika do sporządzania roztworu do infuzji. Jest to
higroskopijny, biały lub lekko zabarwiony proszek bądź krucha masa w szklanej fiolce.
Rozpuszczalnikiem jest woda do wstrzykiwań dostarczana w szklanej fiolce. Przygotowany roztwór
jest klarowny do lekko opalizującego i może być zabarwiony.
Octaplex jest sprzedawany w pojedynczym pudełku zawierającym:
- 1 fiolkę z proszkiem do sporządzania roztworu do infuzji
- 1 fiolkę z rozpuszczalnikiem, wodą do wstrzykiwań
- 1 zestaw do transferu Nextaro .
Podmiot odpowiedzialny i wytwórca
Octapharma (IP) SPRL
Allée de la Recherche 65
1070 Anderlecht
Belgia
W celu uzyskania bardziej szczegółowych informacji należy zwrócić się do miejscowego
przedstawiciela podmiotu odpowiedzialnego:
Octapharma Poland Sp. z o.o.
ul. Domaniewska 39a
02-135 Warszawa
tel. (22) 415-51-42
Wytwórcy:
Octapharma Pharmazeutika Produktionsges.m.b.H.
Oberlaaer Str. 235
1100 Vienna
Austria
Octapharma Lingolsheim S.A.S.
72 Rue du Maréchal Foch
67380 Lingolsheim
Francja
Ten produkt leczniczy jest dopuszczony do obrotu w krajach członkowskich Europejskiego
Obszaru Gospodarczego pod następującymi nazwami:
Austria, Belgia, Bułgaria, Chorwacja, Cypr, Dania, Estonia, Finlandia, Francja, Niemcy, Węgry,
Islandia, Irlandia, Łotwa, Litwa, Luksemburg, Malta, Holandia, Norwegia, Polska, Portugalia,
Słowenia, Słowacja, Hiszpania, Wielka Brytania: Octaplex
Czechy, Szwecja: Ocplex
Włochy, Rumunia: Pronativ
Data ostatniej aktualizacji ulotki: 06.07.2024 -------------------------------------------------------------------------------------------------------------------------
INFORMACJE DLA PERSONELU MEDYCZNEGO
Ogólne informacje dotyczące stosowania Octaplex przedstawiono w punkcie 3.
Poniższe informacje są przeznaczone wyłącznie dla personelu medycznego lub pracowników służby
zdrowia:
Instrukcje dotyczące leczenia
Należy przeczytać wszystkie instrukcje i postępować zgodnie z nimi!
Podczas opisanych poniżej czynności musi być zapewniona jałowość!
Produkt rozpuszcza się szybko w temperaturze pokojowej.
Rekonstytuowany roztwór powinien być przezroczysty lub lekko opalizujący.
Nie należy używać roztworów mętnych lub zawierających cząstki stale.
Przed podaniem należy ocenić wzrokowo czy roztwór nie zawiera cząstek stałych lub nie zmienił
zabarwienia.
Po rekonstytucji roztwór powinien być zużyty natychmiast.
Wszelkie pozostałości niezużytego produktu lub zużyty materiał należy usunąć zgodnie z lokalnymi
przepisami.
Dawkowanie
Krwawienia i profilaktyka krwawień w przypadku leczenia antagonistami witaminy K:
Dawka zależy od INR przed leczeniem i od masy ciała. W tabeli podano przybliżone dawki
(w jednostkach/kg masy ciała rekonstytuowanego produktu).
| INR przed leczeniem |
|
| > 6 |
| Dawka produktu leczniczego Octaplex (jednostki† czynnika IX) / kg masy ciała | 25 | 35 | 50 |
Dawka ustalana jest na podstawie masy ciała wynoszącej maksymalnie, ale nieprzekraczającej,
100 kg. Z tego względu w przypadku pacjentów o masie ciała powyżej 100 kg maksymalna dawka
jednorazowa (j.m. czynnika IX) nie powinna przekraczać 2 500 j.m. dla wartości INR wynoszących
- 2 – <4, 3 500 j.m. dla wartości INR wynoszących 4 – 6 oraz 5 000 j.m. dla wartości INR wynoszących > 6.
Podane dawkowanie jest obliczone na podstawie danych doświadczalnych, a odzysk i długość efektu
działania mogą się różnić, dlatego obowiązkowe jest monitorowanie INR w trakcie leczenia.
Krwawienia i profilaktyka krwawień w trakcie zabiegów operacyjnych we wrodzonych niedoborach
czynników krzepnięcia II i X zależnych od witaminy K, gdy nie jest dostępny produkt określonego
czynnika krzepnięcia:
Wymagana dawka jest obliczona na podstawie danych doświadczalnych takich, że około 1 j.m.
czynnika II lub X na kg masy ciała powoduje wzrost aktywności czynnika II lub X w osoczu
odpowiednio o 0,02 i 0,017 j.m./ml.
- Wymagana ilość jednostek = masa ciała (kg) x pożądany wzrost czynnika X (j.m./ml) x 60 gdzie 60 (ml/kg) jest wykładnikiem założonego odzysku.
- Wymagane dawki dla czynnika II: Wymagana ilość jednostek = masa ciała (kg) x pożądany wzrost czynnika II (j.m./ml) x 50 Jeżeli znane są indywidualne wartości odzysku, powinny być użyte do obliczeń.
Instrukcja rekonstytucji:
- 1. W razie potrzeby doprowadzić rozpuszczalnik (woda do wstrzykiwań) i proszek w zamkniętych fiolkach do temperatury pokojowej. Ta temperatura powinna być utrzymywana podczas rekonstytucji. Jeśli do ogrzewania jest używana kąpiel wodna, należy zwrócić uwagę, aby unikać kontaktu wody z gumowymi korkami lub wieczkami fiolek. Temperatura kąpieli wodnej nie powinna przekraczać 37°C.
- 2. Usunąć wieczka typu „flip-off” z fiolki z proszkiem i fiolki z rozpuszczalnikiem i odpowiednio zdezynfekować gumowe korki.
- 3. Oderwać wieczko opakowania zewnętrznego zestawu Nextaro . Umieścić fiolkę z rozpuszczalnikiem na płaskiej powierzchni i mocno przytrzymać. Bez zdejmowania opakowania zewnętrznego umieścić niebieską część Nextaro na górze fiolki z rozpuszczalnikiem i mocno wcisnąć aż do zatrzaśnięcia (ryc.1). Nie przekręcać podczas podłączania! Trzymając za fiolkę rozpuszczalnika, ostrożnie wyjąć opakowanie zewnętrzne z zestawu Nextaro zachowując ostrożność, aby pozostawić zestaw Nextaro mocno przymocowany do fiolki rozpuszczalnika (ryc. 2)
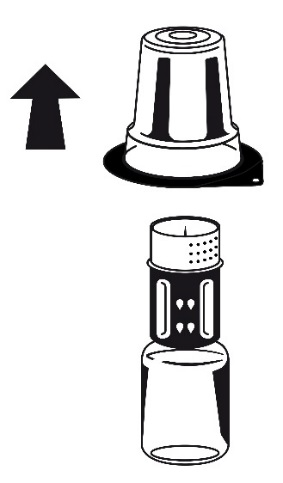
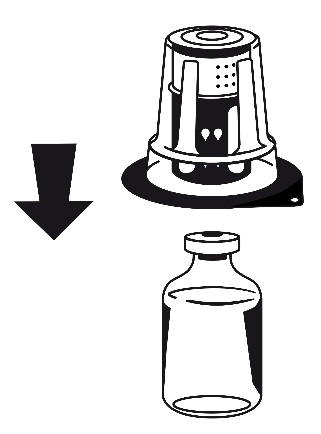
Ryc. 2
Ryc. 1
- 4. Umieścić fiolkę z proszkiem na płaskiej powierzchni i mocno przytrzymać. Wziąć fiolkę z rozpuszczalnikiem z podłączonym zestawem Nextaro®Mix2Vial™ i obrócić do góry dnem. Umieścić przezroczystą białą część łącznika Nextaro® na górze fiolki z proszkiem i mocno wcisnąć aż do zatrzaśnięcia (ryc. 3). Nie przekręcać podczas podłączania! Rozpuszczalnik przepływa automatycznie do fiolki z proszkiem.
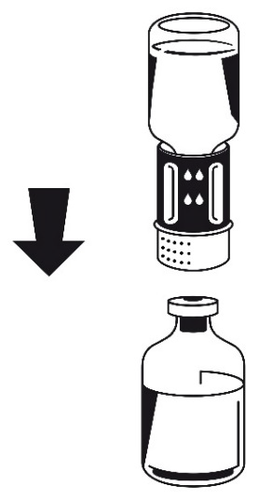
Ryc. 3
- 5. Z nadal podłączonymi obiema fiolkami delikatnie obracać fiolką z proszkiem aż produkt będzie rozpuszczony. Octaplex rozpuszcza się szybko w temperaturze pokojowej, dając roztwór przezroczysty do lekko niebieskiego. Rozkręcić Nextaro na dwie części (ryc. 4).
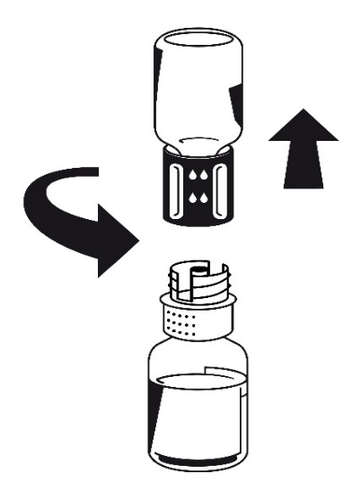
Wyrzucić pustą fiolkę z rozpuszczalnikiem z
niebieską częścią Nextaro .
Ryc. 4
Jeśli proszek nie jest całkowicie rozpuszczony lub tworzy się substancja stała, nie należy używać
produktu.
Instrukcja infuzji:
W celach zapobiegawczych należy zbadać tętno pacjenta przed i w czasie infuzji czynnika IX. Jeśli
pojawi się znaczący wzrost tętna należy zwolnić szybkość infuzji lub przerwać podawanie.
- 1. Podłączyć strzykawkę 20 ml (w przypadku fiolki 500 j.m.) lub 40 ml (w przypadku fiolki 1000 j.m.) do złącza luer lock na białej części Nextaro . Obrócić fiolkę do góry dnem i pobrać roztwór do strzykawki. Po przeniesieniu roztworu mocno przytrzymać tłok strzykawki (trzymając w dół) i wyjąć strzykawkę z Nextaro . Wyrzucić Nextaro i pustą fiolkę.
- 2. Zdezynfekować odpowiednio miejsce wstrzyknięcia.
- 3. Wstrzyknąć roztwór dożylnie z szybkością 0,12 ml/kg/min (~3 jednostki/kg/min), do maksymalnie 8 ml/min (~210 jednostek/min), w warunkach aseptycznych.
Do strzykawki nie powinna dostać się krew ze względu na ryzyko tworzenia skrzepów z fibryny.
Zestaw Nextaro jest przeznaczony wyłącznie do jednorazowego użycia.
- Kraj rejestracji
- Substancja czynna
- Wymaga receptyTak
- Producent
- ImporterOctapharma Pharmazeutika Produktionsgesellschaft mbH (OPG)
- Te informacje mają charakter wyłącznie poglądowy i nie stanowią porady medycznej. Przed zastosowaniem jakiegokolwiek leku zawsze skonsultuj się z lekarzem. Oladoctor nie ponosi odpowiedzialności za decyzje medyczne podjęte na podstawie tych treści.
- Zamienniki OctaplexPostać farmaceutyczna: Proszek, 1000 j.m.Substancja czynna: coagulation factor IX, II, VII and X in combinationWymaga receptyPostać farmaceutyczna: Proszek, 250 j.m.Substancja czynna: coagulation factor IX, II, VII and X in combinationWymaga receptyPostać farmaceutyczna: Proszek, 500 j.m.Substancja czynna: coagulation factor IX, II, VII and X in combinationWymaga recepty
Odpowiedniki Octaplex w innych krajach
Najlepsze odpowiedniki z tą samą substancją czynną i działaniem terapeutycznym.
Odpowiednik Octaplex – Hiszpania
Odpowiednik Octaplex – Ukraina
Lekarze online w sprawie Octaplex
Konsultacja w sprawie dawkowania, działań niepożądanych, interakcji, przeciwwskazań i odnowienia recepty na Octaplex – decyzja należy do lekarza, zgodnie z lokalnymi przepisami.














