
Beriplex P/N 500

Zapytaj lekarza o receptę na Beriplex P/N 500

Jak stosować Beriplex P/N 500
Ulotka dla Pacjenta
Beriplex P/N 500
Proszek i rozpuszczalnik do sporządzania roztworu do wstrzykiwań
Protrombiny ludzkiej zespół
Należy zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje ważne dla pacjenta.
- Należy zachować tę ulotkę, aby w razie potrzeby móc ją ponownie przeczytać
- Należy zwrócić się do lekarza lub farmaceuty w razie jakichkolwiek dalszych wątpliwości
- Lek ten został przepisany ściśle określonej osobie. Nie należy go przekazywać innym.
- Lek może zaszkodzić innej osobie, nawet jeśli objawy jej choroby są takie same.
- Jeśli wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie możliwe objawy niepożądane niewymienione w ulotce, należy powiedzieć o tym lekarzowi lub farmaceucie. Patrz punkt 4.
Spis treści ulotki:
- 1. Co to jest lek Beriplex P/N 500 i w jakim celu się go stosuje
- 2. Informacje ważne przed zastosowaniem leku Beriplex P/N 500
- 3. Jak stosować lek Beriplex P/N 500
- 4. Możliwe działania niepożądane
- 5. Jak przechowywać lek Beriplex P/N 500
- 6. Zawartość opakowania i inne informacje
1. Co to jest lek Beriplex P/N 500 i w jakim celu się go stosuje
Co to jest Beriplex P/N 500
Beriplex P/N 500 jest dostępny jako proszek wraz z dołączonym rozpuszczalnikiem. Jest to biały lub
lekko zabarwiony proszek lub krucha zestalona masa. Sporządzony roztwór przeznaczony jest do
wstrzykiwań dożylnych.
Beriplex P/N 500 jest wytwarzany z osocza ludzkiego (płynna część krwi) i zawiera ludzkie czynniki
krzepnięcia II, VII, IX i X. Koncentraty zawierające wyżej wymienione czynniki krzepnięcia są
nazywane produktami zespołu protrombiny. Zależne od witaminy K - II, VII, IX i X czynniki
krzepnięcia odgrywają ważną rolę w procesie krzepnięcia (koagulacji). Niedobór któregokolwiek
z wymienionych czynników krzepnięcia powoduje, że krew nie krzepnie tak szybko, jak powinna
i ryzyko krwawienia jest większe. Uzupełnienie II, VII, IX i X czynnika krzepnięcia poprzez
zastosowanie leku Beriplex P/N 500 doprowadzi do naprawienia mechanizmu krzepnięcia.
W jakim celu stosuje się Beriplex P/N 500
Beriplex P/N 500 jest używany w celu zapobiegania (podczas zabiegów chirurgicznych) i leczenia
krwawień spowodowanych nabytym lub wrodzonym niedoborem we krwi zależnych od witaminy K
czynników krzepnięcia II, VII, IX i X, kiedy lek zawierający oczyszczony, swoisty czynnik
krzepnięcia nie jest dostępny.
2. Informacje ważne przed zastosowaniem leku Beriplex P/N 500
W poniższym punkcie zawarte są informacje, z którymi pacjent i lekarz powinni zapoznać się przed
zastosowaniem leku Beriplex P/N 500.
Kiedy NIE stosować leku Beriplex P/N 500 :
jeśli pacjent ma uczulenie na substancje czynne lub którykolwiek z pozostałych składników
tego leku (wymienione w punkcie 6).
Należy poinformować lekarza o występowaniu alergii na jakiekolwiek leki lub pokarmy.
jeżeli występuje zwiększone ryzyko tworzenia się skrzeplin (pacjenci z grup ryzyka rozsianego
wykrzepiania wewnątrznaczyniowego)
w przypadku występowania reakcji alergicznej na heparynę, powodującej obniżenie liczby
płytek krwi (małopłytkowość zależna od heparyny typu II, HIT typ II).
Należy poinformować lekarza lub farmaceutę w przypadku występowania takiej choroby.
Ostrzeżenia i środki ostrożności
Przed rozpoczęciem stosowania leku Beriplex należy omówić to z lekarzem lub farmaceutą.
- W przypadku nabytego niedoboru zależnych od witaminy K czynników krzepnięcia. Może on być spowodowany przyjmowaniem leków blokujących działanie witaminy K. Beriplex P/N 500 może być stosowany tylko w razie konieczności szybkiego wyrównania poziomu czynników krzepnięcia kompleksu protrombiny, np. w przypadku dużych krwawień lub nagłych zabiegów chirurgicznych.
- W przypadku występowania wrodzonego niedoboru któregokolwiek z zależnych od witaminy K czynników krzepnięcia należy, o ile to możliwe, stosować lek zawierający swoisty czynnik krzepnięcia.
- W przypadku wystąpienia reakcji alergicznej lub anafilaktycznej (poważna reakcja alergiczna powodująca ciężkie zaburzenia oddychania lub zawroty głowy):
Podawanie leku Beriplex P/N 500 należy natychmiast zatrzymać (np. zaprzestać wstrzyknięcia).
- Jeżeli istnieje ryzyko zwiększonego tworzenia się skrzeplin w naczyniach krwionośnych (zakrzepica), w szczególności w następujących przypadkach:
- u pacjentów po ataku serca (z rozpoznaną chorobą wieńcową lub zawałem mięśnia sercowego)
- u pacjentów z chorobami wątroby
- u pacjentów bezpośrednio przed i po zabiegach operacyjnych
- u noworodków
- u pacjentów z podwyższonym ryzykiem powstawania skrzeplin (pacjenci z ryzykiem choroby zakrzepowo-zatorowej lub rozsianego wykrzepiania wewnątrznaczyniowego, lub samoistnym niedoborem inhibitorów krzepnięcia)
- Jeżeli występuje podwyższone ryzyko wystąpienia zaburzeń krzepnięcia spowodowanych zwiększonym zużyciem płytek krwi lub czynników krzepnięcia. Leczenie lekiem Beriplex P/N 500 może być rozpoczęte po zakończeniu leczenia choroby podstawowej.
- Zmniejszenie produkcji płytek krwi indukowane heparyną (małopłytkowość zależna od heparyny, HIT typ II). Heparyna, białko, którego efektem działania jest rozpuszczenie skrzepu krwi, jest składnikiem leku Beriplex. Znaczne obniżenie liczby płytek krwi może być związane z:
- tworzeniem się skrzeplin w naczyniach żylnych kończyn dolnych,
- zwiększeniem tendencji do powstawania skrzeplin,
- w niektórych przypadkach z wysypką skórną w miejscu wstrzyknięcia,
- wybroczynami oraz
- pojawieniem się smolistego stolca. W takich przypadkach działanie heparyny może być upośledzone (tolerancja heparyny). W przypadku wystąpienia tych objawów, należy natychmiast przerwać podawanie leku i skontaktować się z lekarzem. W przyszłości nie należy przyjmować leków zawierających heparynę.
- Szczególna postać zapalenia nerek została zgłoszona po leczeniu pacjentów cierpiących na hemofilię B z inhibitorami czynnika IX. U tych pacjentów występowały reakcje alergiczne w wywiadzie.
Lekarz powinien rozważyć korzyści płynące z terapii Beriplex P/N 500 wobec ryzyka wystąpienia
wymienionych powikłań.
Bezpieczeństwo przeciwwirusowe
W przypadku, kiedy leki otrzymywane są z ludzkiej krwi lub ludzkiego osocza, stosowane są różne
metody mające na celu zapobieżenie przenoszenia czynników zakaźnych do pacjenta. Należą do nich:
- właściwy dobór dawców krwi i osocza tak, aby wykluczyć możliwość przeniesienia czynników zakaźnych,
- badanie indywidualnych dawców oraz puli osocza na obecność wirusów oraz innych zakażeń,
- włączenie w procesie wytwarzania etapów mających na celu inaktywacje lub usunięcie wirusów.
Pomimo stosowania tych zabezpieczeń, przy zastosowaniu leków otrzymywanych z ludzkiej krwi lub
osocza nie można całkowicie wykluczyć ryzyka wystąpienia chorób zakaźnych z powodu możliwości
przeniesienia czynników zakaźnych. Odnosi się to również do nieznanych dotychczas patogenów
i innych rodzajów zakażeń.
Stosowane metody uważane są za skuteczne wobec takich wirusów otoczkowych jak wirus ludzkiego
niedoboru odporności (HIV, wirus powodujący AIDS), wirus zapalenia wątroby typu B, wirus
zapalenia wątroby typu C (wirusowe zapalenie wątroby) oraz bezotoczkowego wirusa zapalenia
wątroby typu A (wirusowe zapalenie wątroby) i parwowirus B19.
Lekarz może zalecić odpowiednie szczepienie przeciw wirusowemu zapaleniu wątroby typu A i B,
jeżeli regularnie/wielokrotnie przyjmowane są leki otrzymywane z ludzkiego osocza.
Zdecydowanie zalecane jest przy każdym podaniu leku Beriplex P/N 500 odnotowanie
w dokumentacji medycznej nazwy i serii leku w celu udokumentowania użytych serii leku.
Beriplex P/N 500 a inne leki
- Należy powiedzieć lekarzowi lub farmaceucie o wszystkich lekach przyjmowanych obecnie lub ostatnio a także o lekach, które pacjent planuje przyjmować.
- Beriplex P/N 500 może hamować działanie antagonistów witaminy K. Interakcje z innymi lekami nie są znane.
- Leku Beriplex P/N 500 nie należy mieszać z innymi lekami, z wyjątkiem tych wymienionych w punkcie 6.
Ciąża, karmienie piersią i wpływ na płodność
- W ciąży i w okresie karmienia piersią lub gdy istnieje podejrzenie, że kobieta jest w ciąży, lub gdy planuje ciążę, przed zastosowaniem tego leku należy poradzić się lekarza lub farmaceuty.
- U kobiet w okresie ciąży lub karmienia piersią lek Beriplex P/N 500 należy stosować tylko w uzasadnionych przypadkach.
- Brak dostępnych danych dotyczących wpływu na płodność.
Prowadzenie pojazdów i obsługiwanie maszyn
Nie ma odpowiednich badań dokumentujących wpływ stosowania leku na prowadzenie pojazdów
i obsługiwanie maszyn.
Beriplex P/N 500 zawiera sód
Beriplex P/N 500 zawiera do 343mg sodu (około 15 milimoli) w 100 ml. Ilość tę należy uwzględnić
w przypadku pacjentów będących na kontrolowanej diecie sodowej.
3. Jak stosować lek Beriplex P/N 500
Leczenie powinno być rozpoczęte pod nadzorem lekarza doświadczonego w terapii tego rodzaju
zaburzeń.
Dawkowanie
Zalecana dawka czynników II, VII, IX i X oraz czas trwania terapii zależy od kilku czynników, takich
jak masa ciała, stopień zaawansowania i przebieg choroby, umiejscowienie i intensywność krwawienia
oraz konieczność zapobiegnięcia krwawieniom podczas operacji lub prowadzenia diagnostyki chorego
(patrz punkt. „Informacje przeznaczone wyłącznie dla fachowego personelu medycznego”).
W przypadku jakichkolwiek wątpliwości dotyczących stosowania leku, należy skontaktować się
z lekarzem lub farmaceutą.
Przedawkowanie
W czasie leczenia lekarz powinien regularnie kontrolować poziom parametrów krzepnięcia.
Podawanie dużych dawek koncentratu czynników krzepnięcia zespołu protrombiny miało związek
z wystąpieniem zawału serca, rozwojem rozsianego krzepnięcia śródnaczyniowego oraz tworzeniem
się skrzeplin w naczyniach krwionośnych u pacjentów z grupy podwyższonego ryzyka występowania
tych zaburzeń.
4. Możliwe działania niepożądane
Jak każdy lek, lek ten może powodować działania niepożądane, chociaż nie u każdego one wystąpią.
Następujące działania niepożądane były obserwowane często(u mniej niż 1 na 10 pacjentów):
- Ryzyko nasilenia procesu tworzenia się skrzeplin (patrz punkt 2)
- Ból głowy
- Wzrost temperatury ciała
Następujące działania niepożądane były obserwowane niezbyt często(u mniej niż 1 na 100
pacjentów):
- Nadwrażliwość lub reakcje alergiczne (patrz punkt 2)
Częstość występowania następujących działań niepożądanych jest nieznana(nie może być określona
na podstawie dostępnych danych):
- Ciężkie krwawienia będące wynikiem nadmiernego wykrzepiania
- Reakcje anafilaktyczne ze wstrząsem włącznie (patrz punkt 2)
- Tworzenie krążących przeciwciał hamujących jeden lub więcej czynników krzepnięcia
Dzieci i młodzież
Brak danych dotyczących stosowania leku Beriplex u dzieci i młodzieży.
Zgłaszanie działań niepożądanych
Jeśli wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie objawy niepożądane niewymienione
w ulotce, należy powiedzieć o tym lekarzowi lub farmaceucie . Działania niepożądane można zgłaszać
bezpośrednio do Departamentu Monitorowania Niepożądanych Działań Produktów Leczniczych
Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych
Al. Jerozolimskie 181C
02-222 Warszawa
tel.: +48 22 49 21 301
fax.: +48 22 49 21 309
Strona internetowa: https://smz.ezdrowie.gov.pl
Działania niepożądane można zgłaszać również podmiotowi odpowiedzialnemu.
Dzięki zgłaszaniu działań niepożądanych można będzie zgromadzić więcej informacji na temat
bezpieczeństwa stosowania leku.
5. Jak przechowywać lek Beriplex P/N 500
- Lek należy przechowywać w miejscu niewidocznym i niedostępnym dla dzieci.
- Nie stosować leku Beriplex P/N 500 po upływie terminu ważności zamieszczonego na etykiecie i pudełku.
- Nie przechowywać w temperaturze powyżej 25 C.
- Nie zamrażać.
- Fiolkę przechowywać w opakowaniu zewnętrznym w celu ochrony przed światłem.
- Beriplex P/N 500 nie zawiera środków konserwujących, rozpuszczony produkt należy zużyć natychmiast.
6. Zawartość opakowania i inne informacje
Co zawiera Beriplex P/N 500
Beriplex P/N 500 zawiera 400-620 j.m. ludzkiego IX czynnika krzepnięcia krwi w fiolce.
Substancją czynną leku jest:
Koncentrat ludzkich czynników krzepnięcia II, VII, IX i X, białka C i S.
Pozostałe składniki to:
Ludzka antytrombina III, heparyna, albumina ludzka, sodu chlorek, sodu cytrynian, HCl lub NaOH
(w niewielkich ilościach, do ustalenia pH).
Rozpuszczalnik: Woda do wstrzykiwań.
Jak wygląda lek Beriplex P/N 500 i co zawiera opakowanie
Beriplex P/N 500 jest białym lub lekko zabarwionym proszkiem i jest dostarczany wraz z dołączoną
wodą do wstrzykiwań jako rozpuszczalnikiem. Proszek powinien być rozpuszczony w 20 ml wody do
wstrzykiwań.
Sporządzony roztwór powinien być przezroczysty lub lekko opalizujący, co oznacza, że może
połyskiwać oglądany pod światło, nie powinien zawierać żadnych stałych cząstek.
Dostępne opakowania
Opakowanie z lekiem w dawce 500 j.m. zawiera:
- 1 fiolkę z proszkiem
- 1 fiolkę z wodą do wstrzykiwań po 20 ml
- 1 system transferowy 20/20 z filtrem
Nazwa i adres podmiotu odpowiedzialnego oraz nazwa i adres wytwórcy:
CSL Behring GmbH
Emil-von-Behring-Str. 76
35041 Marburg
Niemcy
Ten produkt leczniczy jest dopuszczony do obrotu w krajach członkowskich Europejskiego
Obszaru Gospodarczego pod następującymi nazwami
Austria
Beriplex P/N 500 I.E. Pulver und Lösungsmittel zur Herstellung einer
Injektionslösung
Belgia
Confidex 500 I.E., poeder en oplosmiddel voor oplossing voor injectie
Bułgaria
Chorwacja
Czechy
Dania
Beriplex P/N 500, 500 IU, Powder and solvent for solution for injection
Beriplex P/N 500 IU prašak i otapalo za otopinu za injekciju
Beriplex 500 IU
Confidex
Finlandia
Confidex 500 IU injektiokuiva-aine ja liuotin, liuosta varten
Francja
Confidex 500 UI, poudre et solvant pour solution injectable
Niemcy
Beriplex P/N 500
Grecja
Beriplex P/N
Κόνις και διαλύτης για ενέσιμο διάλυμα 500 IU/vial
Węgry
Irlandia
Beriplex P/N 500 por és oldószer oldatos injekcióhoz
Beriplex P/N 500 IU, powder and solvent for solution for injection
Włochy
Confidex 500
Luxemburg
Confidex 500 UI poudre et solvant pour solution injectable
Malta
Holandia
Beriplex P/N 500, powder and solvent for solution for injection
Beriplex P/N 500 IE, poeder en oplosmiddel voor oplossing voor injectie
Norwegia
Polska
Confidex 500 IU pulver og væske til injeksjonsvæske, oppløsning
Beriplex P/N 500
Portugalia
Beriplex 500 UI pó e solvente para solução injectável
Rumunia
Słowacja
Słowenia
Hiszpania
Beriplex P/N 500 UI pulbere și solvent pentru soluție injectabilă
Beriplex 500 IU
Beriplex P/N 500 i.e. prašek in vehikel za raztopino za injiciranje
Beriplex 500 UI polvo y disolvente para solución inyectable
Szwecja
Confidex 500 IE, pulver och vätska till injektionsvätska, lösning
Wielka Brytania
Beriplex P/N 500 IU, powder and solvent for solution for injection
Data sporządzenia ulotki:
Informacje przeznaczone wyłącznie dla fachowego personelu medycznego
Skład ilościowy i jakościowy
Beriplex P/N 500 nominalnie zawiera następujące ilości j.m. ludzkich czynników krzepnięcia podane
w tabeli poniżej:
| Nazwa składnika | Zawartość po rekonstytucji (j.m./ml) | Zawartość w jednej fiolce Beriplex P/N 500 (j.m.) |
| Substancje czynne | ||
| Ludzki II czynnik krzepnięcia krwi |
|
|
| Ludzki VII czynnik krzepnięcia krwi |
| 200 -500 |
| Ludzki IX czynnik krzepnięcia krwi |
|
|
| Ludzki X czynnik krzepnięcia krwi |
|
|
| Pozostałe substancje czynne | ||
| Białko C |
|
|
| Białko S |
|
|
Zawartość białka całkowitego po rekonstytucji wynosi 6-14 mg/ml w roztworze.
Aktywność swoista czynnika IX wynosi 2,5 j.m. na mg białka całkowitego.
Aktywność wszystkich czynników krzepnięcia jak również białka C i S (antygeny) była badana
zgodnie z aktualnymi międzynarodowymi standardami WHO.
Dawkowanie i sposób podania Dawkowanie
Poniżej podano tylko ogólne zasady dawkowania.
Wielkość dawki oraz częstość jej podawania powinny być obliczone dla każdego pacjenta
indywidualnie. Odstępy między dawkami powinny być dostosowane do wartości okresu półtrwania
poszczególnych czynników krzepnięcia należących do zespołu protrombiny. Dawkę indywidualną
określa się w oparciu o regularne oznaczanie aktywności w osoczu poszczególnych czynników
krzepnięcia, lub na podstawie wyników badań laboratoryjnych ogólnie określających działanie zespołu
protrombiny (INR, wskaźnik Quicka) oraz poprzez ciągłe monitorowanie stanu klinicznego pacjenta.
W przypadku większych interwencji chirurgicznych konieczne jest dokładne monitorowanie leczenia
substytucyjnego (testy dla poszczególnych czynników krzepnięcia jak i ogólne dla czynników
krzepnięcia zespołu protrombiny).
- Krwawienia i profilaktyka okołooperacyjna krwawień podczas leczenia antagonistamiwitaminy K::
Dawka leku zależy od wartości wskaźnika INR oznaczonego przed rozpoczęciem leczenia oraz
od wartości wskaźnika INR, którą pacjent ma uzyskać. Wskaźnik INR przed leczeniem
powinien być mierzony w najkrótszym możliwym czasie przed podaniem leku, aby umożliwić
obliczenie odpowiedniej dawki produktu leczniczego Beriplex. Poniższa tabela określa
przybliżone dawki (ml/kg masy ciała rekonstytuowanego produktu oraz j.m. czynnika IX/kg
masy ciała), tak, aby uzyskać normalizację wskaźnika INR (tj.INR≤1.3) przy różnych
wyjściowych wartościach wskaźnika INR.
| Wartość INR przed leczeniem | 2,0 – 3,.9 | 4,0 – 6,.0 | >6,0 |
| Przybliżona dawka w ml/kg masy ciała | 1 |
| 2 |
| Przybliżona dawka w j.m. (czynnik IX) na kilogram masy ciała | 25 | 35 | 50 |
Dawkowanie jest ustalane w oparciu o masę ciała, gdy nie przekracza ona 100 kg. W przypadku
pacjentów o masie ciała powyżej 100 kg maksymalna pojedyncza dawka (j.m. czynnika IX) nie
powinna przekraczać 2500 j.m. dla wartości wskaźnika INR 2,0 -3,9; 3500 j.m. dla wartości
wskaźnika INR 4,0 – 6,0 oraz 5000 j.m. dla wartości wskaźnika INR >6,0.
Normalizacja zaburzeń hemostazy spowodowanych stosowaniem antagonistów witaminy K jest
zwykle osiągana po około 30 minutach po wstrzyknięciu .Równoczesne podawanie witaminy K
powinno być rozważone u pacjentów otrzymujących Beriplex w celu pilnego odwrócenia
działania antagonistów witaminy K, gdyż zazwyczaj efekt działania witaminy K jest osiągany
po 4-6 godzinach.
Powtarzane dawkowanie Beriplexu u pacjentów wymagających pilnego odwrócenia działania
antagonistów witaminy K nie jest wsparte badaniami klinicznymi i w związku z tym nie jest
zalecane.
Zalecenia te podano w oparciu o badania kliniczne na ograniczonej liczbie osobników.
Konieczne jest monitorowanie wartość wskaźnika INR podczas leczenia ponieważ skuteczność
i czas działania mogą się różnić u poszczególnych pacjentów.
- Krwawienia i profilaktyka okołooperacyjna u pacjentów we wrodzonych niedoborachktóregokolwiek czynnika krzepnięcia zależnego od witaminy K, kiedy zastosowaniepreparatu swoistego czynnika krzepnięcia nie jest możliwe
Wyliczenie wymaganej dawki koncentratu czynników krzepnięcia zespołu protrombiny
ustalone w oparciu o badania kliniczne:
- 1 j.m. czynnika IX na kg masy ciała powoduje spodziewany wzrostu aktywności czynnika IX w osoczu o 1,3% (0,013 j.m./ml) w stosunku do normy,
- 1 j.m. czynnika VII na kg masy ciała powoduje wzrost aktywności czynnika VII w osoczu o 1,7% w stosunku do normy (0,017 j.m./ml),
- 1 j.m. czynnika II na kg masy ciała zwiększa aktywność czynnika II w osoczu o 1,9% w stosunku do normy (0,019 j.m./ml),
- 1 j.m. czynnika X na kg masy ciała zwiększa aktywność czynnika X w osoczu o 1,9% w stosunku do normy (0,019 j.m./ml).
Dawka poszczególnego czynnika krzepnięcia wyrażana jest w jednostkach międzynarodowych
(j.m.), zgodnych z obowiązującym standardem dla każdego czynnika krzepnięcia
zatwierdzonym przez Światową Organizację Zdrowia (WHO). Aktywność czynnika krzepnięcia
w osoczu jest wyrażana procentowo (w stosunku do prawidłowego osocza ludzkiego) lub
w jednostkach międzynarodowych (zgodnie z międzynarodowym standardem dla konkretnego
czynnika krzepnięcia w osoczu).
Jedna jednostka międzynarodowa (j.m.) aktywności czynnika krzepnięcia jest równa
aktywności tego czynnika zawartego w 1 ml prawidłowego osocza ludzkiego.
Na przykład, obliczenie wymaganej dawki czynnika X opiera się na empirycznym stwierdzeniu,
że 1 j.m. czynnika X na kg masy ciała zwiększa aktywność osoczowego czynnika X o 0,019
j.m./ml.
Wymagane dawkowanie obliczane jest przy użyciu następującego wzoru:
Wymagana liczba jednostek = masa ciała [kg] x pożądany wzrost aktywności czynnika X
[j.m./ml] x 53,
gdzie 53 (ml/kg) jest odwrotnością szacowanej wartości odzysku.
Należy zauważyć, że obliczenia te są oparte na danych dotyczących pacjentów otrzymujących
antagonistów witaminy K. Obliczenia oparte na danych dotyczących zdrowych osób
dostarczyłyby niższej wartości wymaganej dawki.
Jeśli indywidualna wartość odzysku jest znana powinna być używana do obliczeń.
Dane dotyczące produktu są dostępne na podstawie badań klinicznych prowadzonych na
zdrowych ochotnikach (N=15), w odwróceniu działania antagonistów witaminy K w leczeniu
ostrych dużych krwawień lub profilaktyki krwawień okołooperacyjnych. (N=98, N=43)
Dzieci i młodzież
Bezpieczeństwo i skuteczność produktu leczniczego Beriplex P/N 500 u dzieci i młodzieży nie została
do tej pory ustalona w kontrolowanych badaniach klinicznych.
Osoby starsze
Dawkowanie i sposób podawania u ludzi starszych (> 65 roku życia) są zgodne z ogólnymi
zaleceniami.
Sposób podawania Instrukcje ogólne
- Roztwór powinien być przezroczysty lub lekko opalizujący. Po przefiltrowaniu oraz pobraniu roztworu po rekonstytucji (patrz niżej), przed jego podaniem należy sprawdzić, czy nie zawiera on widocznych gołym okiem cząstek lub odbarwień. Nie należy stosować roztworów mętnych lub zawierających osad lub cząstki.
- Rekonstytucję i pobieranie z fiolki należy przeprowadzić w warunkach aseptycznych.
Rekonstytucja
Doprowadzić rozpuszczalnik do temperatury pokojowej.
Upewnić się, czy wieczka fiolek z proszkiem i z rozpuszczalnikiem są usunięte, przetrzeć gumowe
korki płynem aseptycznym oraz pozwolić by korki wyschły przed otwarciem opakowania Mix2Vial.
1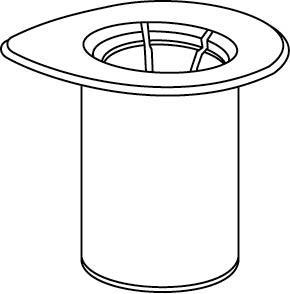 |
|
2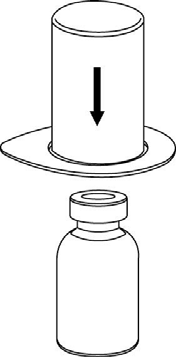 |
|
3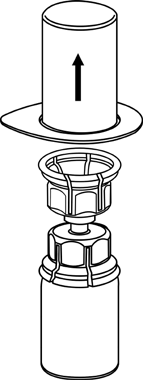 |
|
4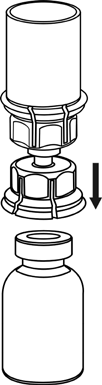 |
|
5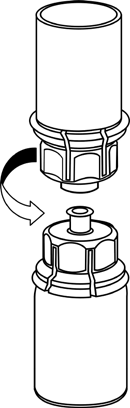 |
|
6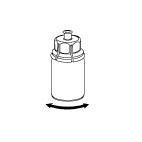 |
|
7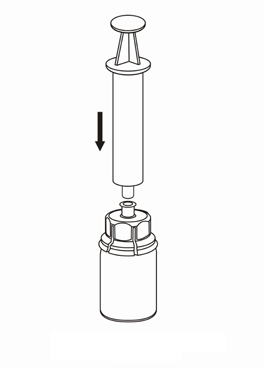 |
|
Pobieranie i podawanie
8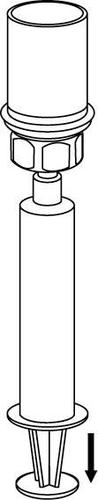 |
|
9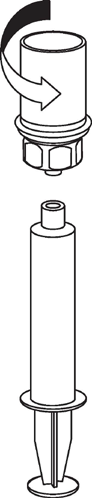 |
|
Należy uważać, aby krew nie dostała się do strzykawki wypełnionej produktem. Może to spowodować
reakcję czynników krzepnięcia znajdujących się w produkcie i powstania skrzepów fibryny, które
mogą być podane pacjentowi.
W przypadku jeżeli wymagane jest podanie więcej niż jednej fiolki produktu Beriplex, istnieje
możliwość połączenia kilku fiolek w celu podania jako pojedynczej infuzji przez dostępny na rynku
zestaw do podawania.
Roztworu produktu leczniczego Beriplex nie wolno rozcieńczać.
Roztwór po rekonstytucji powinien być podany dożylnie (nie szybciej niż 8 ml/min*).
Wszelkie niewykorzystanego resztki produktu leczniczego lub jego odpady należy usunąć w sposób
zgodny z lokalnymi przepisami.
Specjalne ostrzeżenia i środki ostrożności dotyczące stosowania.
Nie ma dostępnych danych klinicznych dotyczących stosowania leku Beriplex P/N 500 w przypadku
krwawień okołoporodowych z powodu niedoboru witaminy K u noworodków.
_________________________________________________
*W badaniach klinicznych Beriplexu pacjenci ważący poniżej 70 kg mieli zalecane dawkowanie z
maksymalną szybkością infuzji wynoszącą 0.12 ml/kg/min (poniżej 8 ml/min).
Uwagi dotyczące kontroli liczby płytek krwi:
Należy ściśle monitorować liczbę płytek krwi.
Interakcje z innymi lekami i inne rodzaje interakcji
W przypadku wykonywania testów krzepnięcia wrażliwych na obecność heparyny, u pacjentów
otrzymujących wysokie dawki czynników krzepnięcia zespołu protrombiny, w otrzymanych wynikach
testów należy uwzględnić dawkę heparyny zawartą w produkcie.
- Kraj rejestracji
- Substancja czynna
- Wymaga receptyTak
- ImporterCSL Behring GmbH
- Te informacje mają charakter wyłącznie poglądowy i nie stanowią porady medycznej. Przed zastosowaniem jakiegokolwiek leku zawsze skonsultuj się z lekarzem. Oladoctor nie ponosi odpowiedzialności za decyzje medyczne podjęte na podstawie tych treści.
- Zamienniki Beriplex P/N 500Postać farmaceutyczna: Proszek, 1000 j.m.Substancja czynna: coagulation factor IX, II, VII and X in combinationWymaga receptyPostać farmaceutyczna: Proszek, 250 j.m.Substancja czynna: coagulation factor IX, II, VII and X in combinationWymaga receptyPostać farmaceutyczna: Proszek, 500 j.m.Substancja czynna: coagulation factor IX, II, VII and X in combinationWymaga recepty
Odpowiedniki Beriplex P/N 500 w innych krajach
Najlepsze odpowiedniki z tą samą substancją czynną i działaniem terapeutycznym.
Odpowiednik Beriplex P/N 500 – Hiszpania
Odpowiednik Beriplex P/N 500 – Ukraina
Lekarze online w sprawie Beriplex P/N 500
Konsultacja w sprawie dawkowania, działań niepożądanych, interakcji, przeciwwskazań i odnowienia recepty na Beriplex P/N 500 – decyzja należy do lekarza, zgodnie z lokalnymi przepisami.














