
Octanate LV

Zapytaj lekarza o receptę na Octanate LV

Jak stosować Octanate LV
Ulotka dołączona do opakowania: informacja dla użytkownika
Octanate LV, 100 j.m./ml, proszek i rozpuszczalnik do sporządzania roztworu do wstrzykiwań
Ludzki VIII czynnik krzepnięcia krwi Octanate LV, 200j.m./ml, proszek i rozpuszczalnik do sporządzania roztworu do wstrzykiwań
Ludzki VIII czynnik krzepnięcia krwi
Należy zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje ważne dla pacjenta.
- Należy zachować tę ulotkę, aby w razie potrzeby móc ją ponownie przeczytać.
- Należy zwrócić się do lekarza, farmaceuty lub pielęgniarki w razie jakichkolwiek dalszych wątpliwości.
- Lek ten przepisano ściśle określonej osobie. Nie należy go przekazywać innym. Lek może zaszkodzić innej osobie, nawet jeśli objawy jej choroby są takie same.
- Jeśli nasili się którykolwiek z objawów niepożądanych lub wystąpią jakiekolwiek objawy niepożądane, w tym niewymienione w ulotce, należy powiedzieć o tym lekarzowi, farmaceucie lub pielęgniarce. Patrz punkt 4.
Spis treści ulotki:
- 1. Co to jest lek Octanate LV i w jakim celu się go stosuje
- 2. Informacje ważne przed zastosowaniem leku Octanate LV
- 3. Jak stosować lek Octanate LV
- 4. Możliwe działania niepożądane
- 5. Jak przechowywać lek Octanate LV
- 6. Zawartość opakowania i inne informacje
1. Co to jest lek Octanate LV i w jakim celu się go stosuje
Octanate LV należy do grupy leków nazywanych czynnikami krzepnięcia i zawiera ludzki VIII czynnik
krzepnięcia. Jest to specjalne białko, które zwiększa zdolność krwi do krzepnięcia.
Octanate LV stosuje się w leczeniu i profilaktyce krwawień u chorych na hemofilię A. Jest to stan, w którym
jest przedłużone krwawienie w stosunku do oczekiwanego. Wynika ono z wrodzonego niedoboru VIII
czynnika krzepnięcia we krwi.
2. Informacje ważne przed zastosowaniem leku Octanate LV
Stanowczo zaleca się, aby przy każdorazowym podaniu pacjentowi dawki Octanate LV zapisać nazwę i numer
serii produktu w celu zachowania informacji o użytej serii.
Lekarz może zalecić rozważenie szczepienia przeciw wirusowemu zapaleniu wątroby typu A i B w przypadku
regularnego lub powtarzanego otrzymywania produktów czynnika VIII pochodzenia ludzkiego.
Kiedy nie stosować leku Octanate LV
jeśli pacjent ma uczulenie na ludzki VIII czynnik krzepnięcia krwi lub którykolwiek z pozostałych składników
tego leku (wymienione w punkcie 6).
Ostrzeżenia i środki ostrożności
Przed rozpoczęciem przyjmowania Octanate LV należy zwrócić się do lekarza, farmaceuty lub pielęgniarki.
Octanate LV zawiera śladowe ilości innych ludzkich białek. Każdy lek, który zawiera białka i który jest
wstrzyknięty do żyły (podany dożylnie) może wywoływać reakcje alergiczne (patrz punkt 4. Możliwe
działania niepożądane).
Tworzenie inhibitorów (przeciwciał) jest znanym powikłaniem, które może występować w trakcie leczenia
wszystkimi lekami zawierającymi czynnik VIII. Inhibitory te, zwłaszcza przy wysokich stężeniach,
przerywają prawidłowe leczenie i pacjent będzie uważnie monitorowany pod kątem wytwarzania tych
inhibitorów. Jeżeli krwawienie u pacjenta nie jest prawidłowo kontrolowane przy użyciu leku Octanate LV,
należy natychmiast powiedzieć o tym lekarzowi.
Informacje odnośnie krwi i osocza użytych do wytwarzania Octanate LV
Podczas wytwarzania leków z ludzkiej krwi lub osocza, podejmowane są określone środki działania, mające
na celu zapobieganie przenoszeniu zakażeń na pacjentów. Obejmują one staranny dobór dawców krwi i
osocza, aby zapewnić wykluczenie dawców mogących być nosicielami zakażeń, jak również badania
wszystkich pobranych próbek i puli osocza, w celu wykrycia obecności wirusów/zakażeń. Wytwórcy tych
produktów wdrożyli do procesu przetwarzania krwi lub osocza etapy mające na celu inaktywację lub usunięcie
wirusów. Mimo tych działań, w przypadku podawania leków przygotowanych z ludzkiej krwi lub osocza, nie
można całkowicie wykluczyć możliwości przeniesienia zakażenia. Dotyczy to również nieznanych lub
pojawiających się od niedawna wirusów, lub innych rodzajów infekcji.
Podejmowane środki są uważane za skuteczne wobec wirusów otoczkowych, takich jak wirus ludzkiego
niedoboru odporności (HIV), wirus zapalenia wątroby typu B (HBV) i wirus zapalenia wątroby typu C (HCV)
oraz bezotoczkowego wirusa zapalenia wątroby typu A (HAV). Zastosowane metody mogą mieć ograniczoną
skuteczność w stosunku do wirusów bezotoczkowych takich, jak parwowirus B19.
Zakażenie parwowirusem B19 może być groźne dla kobiet w ciąży (zakażenie dziecka) oraz u osób, których
układ odpornościowy jest stłumiony lub, którzy chorują na niektóre rodzaje niedokrwistości (np.
niedokrwistość sierpowatokrwinkową lub nieprawidłowy rozpad krwinek czerwonych).
Inne leki i Octanate LV
Należy powiedzieć lekarzowi lub farmaceucie o wszystkich lekach przyjmowanych obecnie lub ostatnio, a
także o lekach, które pacjent planuje przyjmować, również tych, które wydawane są bez recepty.
Nie są znane interakcje ludzkiego VIII czynnika krzepnięcia z innymi produktami leczniczymi. Jednakże nie
należy mieszać Octanate LV z innymi lekami podczas infuzji.
Ciąża i karmienie piersią
Przed zastosowaniem każdego leku należy poradzić się lekarza lub farmaceuty.
Prowadzenie pojazdów i obsługiwanie maszyn
Nie obserwowano wpływu na zdolność prowadzenia pojazdów i obsługiwania maszyn.
Lek Octanate LV zawiera
do 40 mg sodu (głównego składnika soli kuchennej) na Opowiada to 2% zalecanego maksymalnego spożycia
2 g sodu dla osoby dorosłej.
3. Jak stosować lek Octanate LV
Octanate LV powinien być podawany dożylnie po rekonstytucji w załączonym rozpuszczalniku.
Leczenie należy rozpoczynać pod nadzorem medycznym.
Dawkowanie w zapobieganiu krwawieniom:W długoterminowej profilaktyce krwawień u pacjentów z
ciężką postacią hemofilii A powinno podawać się czynnik VIII w dawce 20 do 40 j.m. na kilogram masy ciała
w odstępach 2 do 3 dni. Dawkę należy dostosować do odpowiedzi klinicznej. W niektórych przypadkach
konieczne może być podawanie leku w krótszych odstępach czasu lub w większych dawkach.
Obliczanie dawki:
Octanate LV należy zawsze stosować zgodnie z zaleceniami lekarza. W przypadku wątpliwości należy
ponownie skontaktować się lekarzem lub farmaceutą.
Aktywność czynnika VIII w osoczu odpowiada zawartości czynnika VIII w osoczu. Jest wyrażona albo
procentowo (w stosunku do prawidłowego osocza ludzkiego) albo w jednostkach międzynarodowych (j.m.).
Dawka czynnika VIII jest wyrażona w j.m.
Jedna Jednostka Międzynarodowa (j.m.) aktywności czynnika VIII jest równoważna ilości czynnika VIII w 1
ml prawidłowego osocza ludzkiego. 1 j.m. czynnika VIII na kilogram masy ciała podwyższa aktywność
osoczowego czynnika VIII o 1,5% - 2% normalnej aktywności. Aby obliczyć należną dawkę, należy określić
aktywność czynnika VIII w osoczu pacjenta. To pozwoli na określenie o ile aktywność powinna być
zwiększona. Należy skonsultować się z lekarzem w przypadku niepewności o ile powinna być zwiększona
aktywność czynnika VIII w osoczu i jak obliczyć należną dawkę.
Wymagana dawka jest obliczana przy pomocy następującego wzoru:
wymagana ilość jednostek = masa ciała (kg) x wymagany wzrost aktywności czynnika VIII (%)
(j.m./dl) x 0,5
Ilość, jaka powinna być podana oraz częstość podawania produktu powinny być zawsze dostosowane do
skuteczności klinicznej u indywidualnego pacjenta.
W następujących przypadkach krwawień aktywność czynnika VIII nie powinna obniżać się poniżej podanego
poziomu aktywności osoczowej (w % wartości normalnych) w danym okresie.
Następująca tabela może być pomocna przy ustalaniu dawek w przypadkach krwawień lub zabiegów
chirurgicznych:
| Nasilenie krwawienia / Rodzaj procedury chirurgicznej | Wymagany poziom czynnika VIII (%) (j.m./dl) | Częstość podawania (godziny)/ Długość trwania terapii (dni) |
| Krwawienie | ||
| Wczesne krwawienie do stawów, mięśni lub z jamy ustnej | 20-40 | Powtarzać co 12 do 24 godzin. Co najmniej 1 dzień aż do ustąpienia bólu spowodowanego przez krwawienie lub zagojenia rany. |
| Bardziej nasilone krwawienie do stawów, mięśni lub krwiak | 30-60 | Powtarzać infuzję co 12 do 24 godzin przez 3- 4 dni lub więcej aż do momentu ustąpienia bólu i powrotu czynności. |
| Krwawienia zagrażające życiu | 60-100 | Powtarzać infuzję co 8 do 24 godzin aż do momentu ustąpienia zagrożenia. |
| Operacje | ||
| Mniejsze Włączając ekstrakcję zęba | 30-60 | Co 24 godziny, przez przynajmniej 1 dzień, aż do zagojenia. |
| Większe | 80-100 (przed- i pooperacyjne) | Powtarzać infuzję co 8 do 24 godzin aż do momentu odpowiedniego zagojenia rany, potem kontynuować terapię przez co najmniej 7 kolejnych dni w celu utrzymania aktywności czynnika VIII na poziomie 30% do 60%. |
Dawka i częstotliwość podawania Octanate LV będą ustalone przez lekarza.
Odpowiedź na czynnik VIII może różnić się u poszczególnych pacjentów. Dlatego w trakcie leczenia zalecane
jest oznaczanie poziomów czynnika VIII w celu ustalenia odpowiedniej dawki i częstości podawania infuzji.
Stosowanie u dzieci
W badaniach klinicznych nie stwierdzono żadnych specjalnych wymagań dotyczących dawkowania u dzieci.
Dawkowanie jest takie same u dorosłych i u dzieci, zarówno w ramach leczenia, jak i profilaktyki.
Instrukcja stosowania w domu
- Należy przeczytać wszystkie instrukcje i dokładnie ich przestrzegać!
- Nie stosować produktu Octanate LV po upływie terminu ważności zamieszczonego na etykiecie.
- Podczas opisanej poniżej procedury należy zachować warunki jałowe!
- Przed podaniem należy sprawdzić wzrokowo, czy przygotowany roztwór produktu nie zawiera cząsteczek stałych ani przebarwień.
- Roztwór powinien być przejrzysty lub lekko opalizujący. Nie stosować roztworów, które są mętne lub zawierają cząstki stałe.
- Przygotowany roztwór zużyć niezwłocznie w celu zapobiegnięcia skażeniu mikrobiologicznemu.
- Używać wyłącznie dostarczonego zestawu do infuzji. Stosowanie innego sprzętu do wstrzykiwań/infuzji może powodować dodatkowe zagrożenia i niepowodzenie leczenia.
Instrukcja przygotowania roztworu:
- 1. Nie używać produktu bezpośrednio po wyjęciu z lodówki. Pozostawić rozpuszczalnik i proszek w zamkniętych fiolkach aż do uzyskania temperatury pokojowej.
- 2. Usunąć wieczka z obu fiolek i wyczyścić gumowe korki jednym z dołączonych wacików nasączonych alkoholem.
- 3. Zestaw do transferu jest przedstawiony na ryc. 1. Umieścić fiolkę z rozpuszczalnikiem na płaskiej powierzchni i mocno przytrzymać. Wziąć zestaw do transferu i obrócić. Umieścić niebieską część zestawu do transferu na górze fiolki z rozpuszczalnikiem i mocno wcisnąć aż do zatrzaśnięcia (ryc. 2 + 3). Nie obracać podczas podłączania.
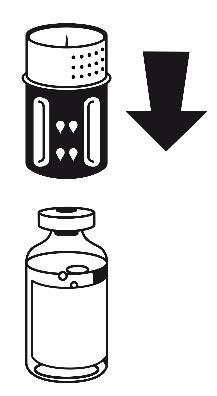
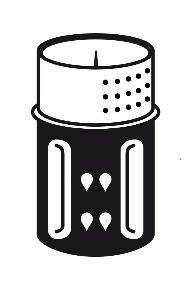
ryc. 1
ryc. 3
ryc. 2
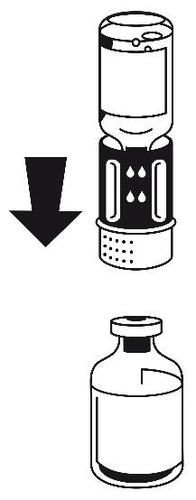
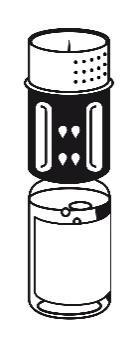
- 4. Umieścić fiolkę z proszkiem na płaskiej powierzchni i mocno przytrzymać. Wziąć fiolkę z rozpuszczalnikiem z podłączonym zestawem do transferu i obrócić ją do góry dnem. Umieścić białą część zestawu na górze fiolki z proszkiem i mocno wcisnąć aż do zatrzaśnięcia (ryc. 4). Nie obracać podczas podłączania. Rozpuszczalnik przepływa automatycznie do fiolki z proszkiem.
ryc. 4
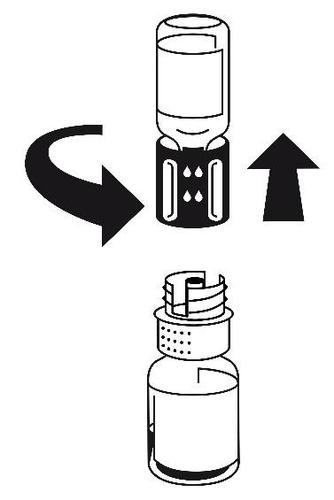
- 5. Z jednocześnie podłączonymi obiema fiolkami delikatnie obracać fiolką z proszkiem do czasu rozpuszczenia produktu. Rozpuszczanie jest zakończone w mniej niż 10 minut w temperaturze pokojowej. Podczas przygotowania może powstać nieznaczna piana. Rozkręcić zestaw do transferu na dwie części (ryc. 5). Piana zniknie.
Wyrzucić pustą fiolkę z rozpuszczalnikiem z niebieską częścią
zestawu do transferu.
ryc. 5
Instrukcja wykonywania wstrzyknięcia:
Jako środek ostrożności należy przed wstrzyknięciem i w czasie wstrzyknięcia zbadać tętno. W przypadku
znacznego zwiększenia częstotliwości tętna należy zmniejszyć szybkość wstrzykiwania lub przerwać
podawanie leku na krótki czas.
- 1. Podłączyć strzykawkę do białej części zestawu do transferu. Obrócić fiolkę do góry dnem i pobrać roztwór do strzykawki (ryc. 6). Roztwór powinien być przejrzysty lub lekko opalizujący. Po przeniesieniu roztworu mocno przytrzymać tłok strzykawki (trzymając go skierowanym do dołu) i wyjąć strzykawkę z zestawu do transferu (ryc. 7).
Wyrzucić pustą fiolkę razem z białą częścią zestawu do transferu.
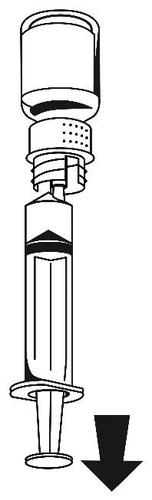
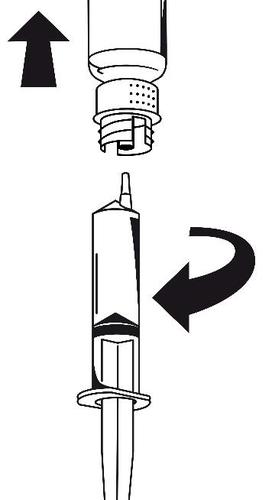
ryc. 6
ryc. 7
- 2. Oczyścić wybrane miejsce wstrzyknięcia jednym z dołączonych wacików nasączonych alkoholem.
- 3. Podłączyć dostarczony zestaw do infuzji do strzykawki.
- 4. Wprowadzić igłę do wybranej żyły. W przypadku użycia opaski uciskowej w celu uwidocznienia żyły należy rozluźnić opaskę przed rozpoczęciem wstrzykiwania produktu Octanate.
- 5. Krew nie może przedostać się do strzykawki z powodu ryzyka wytworzenia się skrzepów fibryny.
- 6. Roztwór wstrzykiwać powoli do żyły, nie szybciej niż 2-3 ml na minutę. W przypadku używania więcej niż jednej fiolki proszku Octanate w trakcie jednego podania możliwe jest ponowne zastosowanie tego samego zestawu do infuzji i strzykawki. Zestaw do transferu jest przeznaczony wyłącznie do jednorazowego użycia.
Wszelkie niewykorzystane resztki produktu lub jego odpady należy usunąć zgodnie z lokalnymi przepisami.
Zastosowanie większej niż zalecana dawki leku Octanate LV
Nie obserwowano objawów przedawkowania ludzkiego VIII czynnika krzepnięcia. Jednak zaleca się nie
przekraczać zalecanej dawki.
Pominięcie przyjęcia leku Octanate LV
Nie należy stosować dawki podwójnej w celu uzupełnienia pominiętej dawki. Należy niezwłocznie przejść do
kolejnej dawki i kontynuować dawkowanie zgodnie z zaleceniem lekarza lub farmaceuty.
Należy skontaktować się z lekarzem lub farmaceutą w przypadku innych pytań dotyczących stosowania tego
produktu.
4. Możliwe działania niepożądane
Jak każdy lek, lek ten może powodować działania niepożądane, chociaż nie u każdego one wystąpią.
Pomimo, że występują rzadko(występują u 1 do 10 na 10 000 pacjentów), obserowano występowanie reakcji
nadwrażliwości lub alergicznych u pacjentów leczonych produktami zawierającymi czynnik VIII.
Należy skontaktować się z lekarzem, jeśli wystąpią następujące objawy:
wymioty, uczucie pieczenia i parzącego bólu w miejscu infuzji, uczucie ucisku w klatce piersiowej, dreszcze,
tachykardia, nudności, uczucie mrowienia, zaczerwienienie, ból głowy, pokrzywka, spadek ciśnienia krwi,
wysypka, niepokój, obrzęk twarzy, ust, jamy ustnej, języka lub gardła, który może prowadzić do utrudnienia w
połykaniu lub oddychaniu (obrzęk naczynioruchowy), zmęczenie (letarg), świszczący oddech.
Bardzo rzadko(występują u mniej niż 1 na 10 000 pacjentów) nadwrażliwość może prowadzić do
wystąpienia zagrażającej życiu rekacji alergicznej nazywanej anafilkasją, która może obejmować wstrząs, jak
również część lub wszystkie objawy opisane powyżej. W takim przypadku należy natychmiast skontaktować
się z lekarzem lub wezwać pogotowie ratunkowe.
Inne rzadkie działania niepożądane (występują u 1 do 10 na 10 000 pacjentów)
Goraczka.
W przypadku dzieci nieleczonych wcześniej lekami zawierającymi czynnik VIII, przeciwciała blokujące
(patrz punkt 2) mogą powstawać bardzo często (więcej niż 1 na 10 pacjentów). Jednak u pacjentów, którzy
wcześniej byli leczeni czynnikiem VIII (ponad 150 dni leczenia), ryzyko jest niezbyt częste (mniej niż 1 na
100 pacjentów). Jeżeli tak się stanie, leki pacjenta mogą przestać działać prawidłowo i u pacjenta może
wystąpić utrzymujące się krwawienie. Jeżeli tak się stanie, należy natychmiast skontaktować się z lekarzem.
Informacje związane z bezpieczeństwem wirusowym, patrz punkt 2. (Należy zachować szczególną ostrożność
stosując Octanate LV).
Zgłaszanie działań niepożądanych
Jeśli wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie objawy niepożądane niewymienione w
ulotce, należy powiedzieć o tym lekarzowi, farmaceucie lub pielęgniarce. Działania niepożądane można
zgłaszać bezpośrednio do Departamentu Monitorowania Niepożądanych Działań Produktów Leczniczych
Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych
Al. Jerozolimskie 181C
PL-02 222 Warszawa
Tel.: + 48 22 49 21 301
Faks: + 48 22 49 21 309
e-mail: [email protected]
Dzięki zgłaszaniu działań niepożądanych można będzie zgromadzić więcej informacji na temat
bezpieczeństwa stosowania leku.
5. Jak przechowywać lek Octanate LV
Lek należy przechowywać w miejscu niewidocznym i niedostępnym dla dzieci.
Nie stosować tego leku po upływie terminu ważności podanym na etykiecie. Termin ważności odnosi się do
ostatniego dnia podanego miesiąca.
Przechowywać w lodówce (2˚C – 8˚C).
Nie zamrażać.
Przechowywać w opakowaniu zewnętrznym w celu ochrony przed światłem.
Roztwór po rekonstytucji należy zużyć natychmiast i tylko w trakcie jednego podania.
Nie stosować tego leku, jeśli zauważy się, że roztwór jest mętny lub niecałkowicie rozpuszczony.
Leków nie należy wyrzucać do kanalizacji ani domowych pojemników na odpadki. Należy zapytać
farmaceutę, jak usunąć leki, których się już nie używa. Takie postępowanie pomoże chronić środowisko.
6. Zawartość opakowania i inne informacje
Co zawiera lek Octanate LV
Substancją czynnąleku jest ludzki VIII czynnik krzepnięcia krwi.
Objętość i stężenia
| Wielkość fiolki z proszkiem Octanate LV (j.m. czynnika VIII) | Wielkość fiolki z rozpuszczalnikiem (do dodania do fiolki z proszkiem Octanate LV) (ml) | Nominalne stężenie roztworu po rekonstytucji (j.m. czynnika VIII/ml) |
| 500 j.m. | 5 | 100 |
| 1 000 j.m. | 5 | 200 |
Pozostałe składniki to:
Dla proszku: sodu cytrynian, sodu chlorek, wapnia chlorek, glicyna
Dla rozpuszczalnika: woda do wstrzykiwań
Jak wygląda lek Octanate LV i co zawiera opakowanie
Octanate LV występuje w postaci proszku i rozpuszczalnika do sporządzania roztworu do wstrzykiwań.
Proszek ma kolor biały lub bladożółty, może występować również w postaci zbrylonej.
Rozpuszczalnik jest przezroczystym, bezbarwnym płynem.
2 dostępne moce produktu leczniczego różnią się zawartością VIII czynnika krzepnięcia
i rozpuszczalnika:
100 j.m./ml proszek i rozpuszczalnik
- Proszek, 500 j.m., w fiolce z korkiem i wieczkiem typu flip-off
- 5 ml rozpuszczalnika w fiolce z korkiem i wieczkiem typu flip-off
- 1 opakowanie ze sprzętem do wstrzyknięcia dożylnego (1 zestaw do transferu, 1 zestaw do infuzji, 1 strzykawka jednorazowego użytku)
- 2 waciki nasączone alkoholem.
200 j.m./ml proszek i rozpuszczalnik
- Proszek, 1000 j.m., w fiolce z korkiem i wieczkiem typu flip-off
- 5 ml rozpuszczalnika w fiolce z korkiem i wieczkiem typu flip-off
- 1 opakowanie ze sprzętem do wstrzyknięcia dożylnego (1 zestaw do transferu, 1 zestaw do infuzji, 1 strzykawka jednorazowego użytku)
- 2 waciki nasączone alkoholem.
Nie wszystkie wielkości opakowań muszą być dostępne na rynku.
Podmiot odpowiedzialny
Octapharma (IP) SPRL
Allée de la Recherche 65
1070 Anderlecht
Belgia
Wytwórca
Octapharma Pharmazeutika Produktionsges.m.b.H
Oberlaaer Str. 235
1100 Wiedeń
Austria
Octapharma S.A.S
72 rue du Maréchal Foch
67380 Lingolsheim
Francja
Octapharma AB
Lars Forssells gata 23
112 75 Sztokholm
Szwecja
Ten produkt leczniczy jest zarejestrowany w państwach członkowskich Europejskiej Wspólnoty Gospodarczej
pod następującymi nazwami:
Octanate LV: Austria, Cypr, Dania, Francja, Holandia, Malta, Polska, Rumunia, Hiszpania, Szwecja, Wielka
Brytania
Octafil LV: Finlandia
Octanate: Belgia, Republika Czech, Niemcy, Irlandia, Włochy, Łotwa, Litwa, Luksemburg, Portugalia
Octanate Kons: Republika Słowenii
Data ostatniej aktualizacji ulotki:26.03.2021
- Kraj rejestracji
- Substancja czynna
- Wymaga receptyTak
- Producent
- ImporterOctapharma AB Octapharma Pharmazeutika Produktions.ges.m.b.H. Octapharma S.A.S.
- Te informacje mają charakter wyłącznie poglądowy i nie stanowią porady medycznej. Przed zastosowaniem jakiegokolwiek leku zawsze skonsultuj się z lekarzem. Oladoctor nie ponosi odpowiedzialności za decyzje medyczne podjęte na podstawie tych treści.
- Zamienniki Octanate LVPostać farmaceutyczna: Proszek, 1000 j.m.Substancja czynna: coagulation factor VIIIProducent: CSL Behring GmbHWymaga receptyPostać farmaceutyczna: Proszek, 2000 j.m.Substancja czynna: coagulation factor VIIIProducent: CSL Behring GmbHWymaga receptyPostać farmaceutyczna: Proszek, 250 j.m.Substancja czynna: coagulation factor VIIIProducent: CSL Behring GmbHWymaga recepty
Odpowiedniki Octanate LV w innych krajach
Najlepsze odpowiedniki z tą samą substancją czynną i działaniem terapeutycznym.
Odpowiednik Octanate LV – Hiszpania
Odpowiednik Octanate LV – Ukraina
Lekarze online w sprawie Octanate LV
Konsultacja w sprawie dawkowania, działań niepożądanych, interakcji, przeciwwskazań i odnowienia recepty na Octanate LV – decyzja należy do lekarza, zgodnie z lokalnymi przepisami.














