
NUWIQ 4000 IU POWDER AND SOLVENT FOR INJECTABLE SOLUTION

How to use NUWIQ 4000 IU POWDER AND SOLVENT FOR INJECTABLE SOLUTION
Translated with AI
This page provides general information and does not replace a doctor’s consultation. Always consult a doctor before taking any medication. Seek urgent medical care if symptoms are severe.
Show originalContents of the leaflet
Introduction
Package Leaflet: Information for the User
Nuwiq 250 UI powder and solvent for solution for injection
Nuwiq 500 UI powder and solvent for solution for injection
Nuwiq 1000 UI powder and solvent for solution for injection
Nuwiq 2000 UI powder and solvent for solution for injection
Nuwiq 2500 UI powder and solvent for solution for injection
Nuwiq 3000 UI powder and solvent for solution for injection
Nuwiq 4000 UI powder and solvent for solution for injection
simoctocog alfa (recombinant human coagulation factor VIII)
Read all of this leaflet carefully before you start using this medicine because it contains important information for you.
- Keep this leaflet, you may need to read it again.
- If you have any further questions, ask your doctor or pharmacist.
- This medicine has been prescribed for you only. Do not pass it on to others. It may harm them, even if their signs of illness are the same as yours.
- If you get any side effects, talk to your doctor or pharmacist. This includes any possible side effects not listed in this leaflet. See section 4.
Contents of the pack
- What is Nuwiq and what is it used for
- What you need to know before you use Nuwiq
- How to use Nuwiq
- Possible side effects
- Storage of Nuwiq
- Contents of the pack and other information
1. What is Nuwiq and what is it used for
Nuwiq contains the active substance recombinant human coagulation factor VIII (simoctocog alfa). Factor VIII is necessary for blood to clot and stop bleeding. In patients with hemophilia A (congenital factor VIII deficiency), factor VIII is missing or does not work properly.
Nuwiq replaces the missing factor VIII and is used to treat and prevent bleeding in patients with hemophilia A. It can be used in all age groups.
2. What you need to know before you use Nuwiq
Do not use Nuwiq:
- if you are allergic to simoctocog alfa or any of the other ingredients of this medicine (listed in section 6).
If you are not sure, ask your doctor.
Warnings and precautions
Talk to your doctor or nurse before you start using Nuwiq.
There is a rare possibility that you may experience an anaphylactic reaction (a sudden severe allergic reaction) to Nuwiq. You should be able to recognize the early signs of allergic reactions, which are listed in section 4 "Allergic reactions".
If any of these symptoms occur, stop the injection immediately and contact your doctor.
The formation of inhibitors (antibodies) is a known complication that can occur during treatment with all factor VIII medicines. These inhibitors, especially in large quantities, can prevent the treatment from working properly. You and your child will be closely monitored for the development of these inhibitors. If your bleeding or your child's bleeding is not controlled with Nuwiq, contact your doctor immediately.
Cardiovascular events
In patients with cardiovascular risk factors, replacement therapy with FVIII may increase the risk of cardiovascular events.
Complications associated with catheters
If you require a central venous access device (CVAD), you should be aware of the risk of CVAD-associated complications, including localized infections, bacteria in the blood, and thrombosis at the catheter implantation site.
It is strongly recommended that each time you are given Nuwiq, the name and batch number of the product should be recorded in order to maintain a record of the batches used.
Using Nuwiq with other medicines
Tell your doctor if you are using, have recently used, or might use any other medicines.
Pregnancy and breastfeeding
If you are pregnant or breastfeeding, think you may be pregnant, or are planning to have a baby, ask your doctor for advice before using this medicine.
Driving and using machines
Nuwiq does not affect the ability to drive and use machines.
Nuwiq contains sodium
This medicine contains less than 1 mmol of sodium (23 mg) per vial, which is essentially "sodium-free".
However, depending on your body weight and the dosage, you may be given more than one vial, which should be taken into account if you are on a low-sodium diet.
3. How to use Nuwiq
Treatment with Nuwiq will be started by a doctor who is experienced in the care of patients with hemophilia A. Follow exactly the instructions for administration of this medicine given by your doctor or nurse. If you are not sure, ask your doctor or nurse.
Nuwiq is usually injected into a vein (intravenously) by your doctor or a nurse who is experienced in the care of patients with hemophilia A. You or another person may also inject Nuwiq, but only after you have received proper training.
Your doctor will calculate your dose of Nuwiq (in International Units = IU) based on your condition, body weight, and whether it is being used for prevention or treatment of bleeding. How often you need an injection will depend on how well Nuwiq works for you. Normally, treatment for hemophilia A is lifelong.
Prevention of bleeding
The usual dose of Nuwiq is 20 to 40 IU per kilogram of body weight, given every 2 to 3 days. However, in some cases, especially in younger patients, more frequent injections or higher doses may be needed.
Treatment of bleeding
The dose of Nuwiq is calculated based on your body weight and the factor VIII levels that need to be achieved. The target factor VIII levels will depend on the severity and location of the bleeding.
If you think the effect of Nuwiq is too weak, talk to your doctor. Your doctor will do the relevant laboratory tests to make sure you have the right levels of factor VIII. This is especially important if you are going to have major surgery.
Patients who develop factor VIII inhibitors
If your plasma factor VIII levels do not reach the expected levels with Nuwiq, or if bleeding is not properly controlled, it may be due to the development of factor VIII inhibitors. Your doctor will check for this. You may need a higher dose of Nuwiq or a different product to control bleeding. Do not increase the total dose of Nuwiq to control your bleeding without talking to your doctor.
Use in children and adolescents
The way Nuwiq is used in children and adolescents is not different from the way it is used in adults. Since it may be necessary to administer factor VIII medicines more frequently in children and adolescents, a central venous access device (CVAD) may be needed. A CVAD is an external connector that allows access to the bloodstream through a catheter without injection through the skin.
If you use more Nuwiq than you should
No symptoms of overdose have been reported. If you have injected more Nuwiq than you should, talk to your doctor.
If you forget to use Nuwiq
Do not take a double dose to make up for a forgotten dose. Proceed with the next dose as planned and follow your doctor's recommendations.
If you stop using Nuwiq
Do not stop using Nuwiq without talking to your doctor.
If you have any further questions on the use of this medicine, ask your doctor.
4. Possible side effects
Like all medicines, this medicine can cause side effects, although not everybody gets them.
Allergic reactions
You should be able to recognize the early signs of allergic reactions. If severe allergic reactions (anaphylactic reactions) occur suddenly (very rare, may affect up to 1 in 10,000 people), the injection should be stopped immediately. Contact your doctor immediately if you notice any of the following symptoms:
- rash, hives, itching, swelling of the face, lips, tongue, or throat,
- difficulty breathing, wheezing, chest tightness,
- feeling unwell, dizziness, and fainting.
These symptoms can be early signs of an anaphylactic shock. If any of these symptoms occur, stop the injection immediately and contact your doctor. Severe symptoms require immediate emergency treatment.
Very common side effects that may affect more than 1 in 10 people
Factor VIII inhibitors in previously untreated patients.
In children and adolescents who have not received previous treatment with factor VIII medicines, inhibitory antibodies (see section 2) may occur very frequently (more than 1 in 10 patients).
However, in patients who have received previous treatment with factor VIII (more than 150 days of treatment), the risk is uncommon (less than 1 in 100 patients). If this happens, the medicines you or your child are taking may stop working properly, and you or your child may experience persistent bleeding. In this case, contact your doctor immediately.
Common side effects that may affect up to 1 in 10 people
Hypersensitivity, fever.
Uncommon side effects that may affect up to 1 in 100 people
Tingling or numbness (paresthesia), headache, inflammation and/or pain at the injection site, back pain, dizziness, dry mouth, hemorrhagic anemia, positive results for non-neutralizing antibody formation (in PTP).
Reporting of side effects
If you get any side effects, talk to your doctor or pharmacist. This includes any possible side effects not listed in this leaflet. You can also report side effects directly via the national reporting system listed in Appendix V. By reporting side effects, you can help provide more information on the safety of this medicine.
5. Storage of Nuwiq
Keep this medicine out of the sight and reach of children.
Do not use this medicine after the expiry date which is stated on the carton and vial after "EXP". The expiry date refers to the last day of the month shown.
Store in a refrigerator (2°C to 8°C). Do not freeze. Keep the vial in the original package to protect it from light.
Before Nuwiq powder is reconstituted, it can be stored at room temperature (up to 25°C) for a single period not exceeding 1 month. Record the date you start storing Nuwiq at room temperature on the packaging of the medicine. Do not store Nuwiq in the refrigerator again after it has been stored at room temperature.
Use the reconstituted solution immediately after reconstitution.
Warnings regarding visible signs of deterioration
Do not use this medicine if you notice visible signs of deterioration of the pack, especially the syringe and/or vial.
Medicines should not be disposed of via wastewater or household waste. Ask your pharmacist how to dispose of medicines no longer required. This will help protect the environment.
6. Container Contents and Additional Information
Nuwiq Composition
Powder:
- The active ingredient is human recombinant coagulation factor VIII (simoctocog alfa). Each vial of powder contains 250, 500, 1000, 2000, 2500, 3000, or 4000 IU of simoctocog alfa.
Each reconstituted solution contains approximately 100, 200, 400, 800, 1000, 1200, or 1600 IU/ml of simoctocog alfa.
- The other components are sucrose, sodium chloride, calcium chloride dihydrate, arginine hydrochloride, sodium citrate dihydrate, and poloxamer 188. See section 2, "Nuwiq contains sodium".
Solvent:
Water for injections
Appearance of Nuwiq and Container Contents
Nuwiq is supplied as a powder and solvent for solution for injection. The powder is white to off-white in a glass vial. The solvent is water for injections in a prefilled glass syringe.
After reconstitution, the solution is clear, colorless, and free from foreign particles.
Each Nuwiq container contains:
- 1 vial of powder with 250, 500, 1000, 2000, 2500, 3000, or 4000 IU of simoctocog alfa
- 1 prefilled syringe with 2.5 ml of water for injections
- 1 vial adapter
- 1 butterfly needle
- 2 alcohol swabs
Marketing Authorization Holder and Manufacturer
Octapharma AB, Lars Forssells gata 23, 112 75 Stockholm, Sweden
For any information about this medicinal product, please contact the local representative of the marketing authorization holder:
Belgium Octapharma Benelux (Belgium) Tel: +32 2 3730890 | Lithuania Octapharma Nordic AB (Sweden) Tel: +46 8 56643000 |
Bulgaria Octapharma Nordic AB (Sweden) Tel: +46 8 56643000 | Luxembourg Octapharma Benelux (Belgium) Tel: +32 2 3730890 |
Czech Republic Octapharma CZ s.r.o. Tel: +420 266 793 510 | Hungary Octapharma Nordic AB (Sweden) Tel: +46 8 56643000 |
Denmark Octapharma Nordic AB (Sweden) Tel: +46 8 56643000 | Malta Octapharma Nordic AB (Sweden) Tel: +46 8 56643000 |
Germany Octapharma GmbH Tel: +49 2173 9170 | Netherlands Octapharma Benelux (Belgium) Tel: +32 2 3730890 |
Estonia Octapharma Nordic AB (Sweden) Tel: +46 8 56643000 | Norway Octapharma AS Tel: +47 63988860 |
Greece Octapharma Hellas SA Tel: +30 210 8986500 | Austria Octapharma Handelsgesellschaft m.b.H. Tel: +43 1 610321222 |
Spain Octapharma S.A. Tel: +34 91 6487298 | Poland Octapharma Poland Sp. z o.o. Tel: +48 22 2082734 |
France Octapharma France Tel: +33 1 41318000 | Portugal Octapharma Produtos Farmacêuticos Lda. Tel: +351 21 8160820 |
Croatia Octapharma Nordic AB (Sweden) Tel: +46 8 56643000 | Romania Octapharma Nordic AB (Sweden) Tel: +46 8 56643000 |
Ireland Octapharma AB (Sweden) Tel: +46 8 56643000 | Slovenia Octapharma Nordic AB (Sweden) Tel: +46 8 56643000 |
Iceland Octapharma AS (Norway) Tel: +47 63988860 | Slovakia Octapharma AG, o.z.z.o. Tel: +421 2 54646701 |
Italy Kedrion S.p.A. Tel: +39 0583 767507 | Finland Octapharma Nordic AB Tel: +358 9 85202710 |
Cyprus Octapharma Nordic AB (Sweden) Tel: +46 8 56643000 | Sweden Octapharma Nordic AB Tel: +46 8 56643000 |
Latvia Octapharma Nordic AB (Sweden) Tel: +46 8 56643000 | United Kingdom Octapharma Limited Tel: +44 161 8373770 |
Date of Last Revision of this Leaflet
Detailed information on this medicinal product is available on the European Medicines Agency website: http://www.ema.europa.eu.
This information is intended only for healthcare professionals:
On-demand treatment
The dose to be administered and the frequency of administration should always be oriented towards clinical efficacy in each individual case.
In the case of the following hemorrhagic episodes, the factor VIII activity should not be lower than the given plasma activity level (in % of normal or IU/dl) during the corresponding period. The following table can be used as a dosing guide in surgery and in hemorrhagic episodes.
Severity of Hemorrhage / Type of Surgical Procedure | Required Factor VIII Level (%) (IU/dl) | Dosing Frequency (hours) / Duration of Treatment (days) |
Hemorrhage | ||
Early hemarthrosis, muscle or oral hemorrhage | 20–40 | Repeat every 12 to 24 hours. At least 1 day until the hemorrhagic episode, as indicated by pain, is resolved or healing is achieved. |
More extensive hemarthrosis, muscle hemorrhage, or hematoma | 30-60 | Repeat infusion every 12 to 24 hours, for 3 to 4 days or more, until pain and acute disability cease. |
Potentially life-threatening hemorrhage | 60-100 | Repeat infusion every 8 to 24 hours until the danger has passed |
Surgery | ||
Minor surgery, including dental extraction | 30-60 | Every 24 hours, for at least 1 day, until healing is achieved. |
Major surgery | 80-100 (pre- and post-operative) | Repeat infusion every 8-24 hours until adequate wound healing is achieved, and then for at least another 7 days of treatment to maintain a factor VIII activity of 30% to 60% (IU/dl). |
INSTRUCTIONS FOR PREPARATION AND ADMINISTRATION
- Allow the syringe of solvent (water for injections) and the powder to reach room temperature in the closed vial. You can do this by holding them in your hands until they reach the same temperature as your hands. Do not heat the vial and prefilled syringe in any other way. This temperature should be maintained during reconstitution.
- Remove the flip-off plastic cap from the powder vial to expose the central part of the rubber stopper. Do not remove the gray stopper or the metal ring that surrounds the top of the vial.
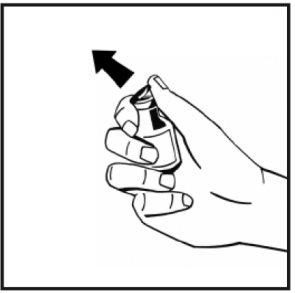
- Clean the top of the vial with an alcohol swab. Let the alcohol dry.
- Remove the paper cover from the vial adapter package. Do not remove the adapter from its package.
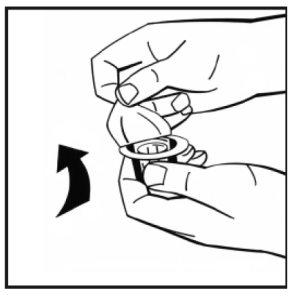
- Place the powder vial on a flat surface and hold it. Take the adapter package and place the vial adapter over the center of the rubber stopper of the powder vial. Press the adapter package firmly downwards until the tip of the adapter pierces the rubber stopper. The adapter will be secured to the vial when done.
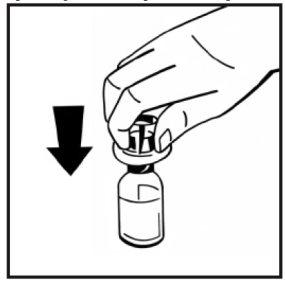
- Remove the paper cover from the prefilled syringe package. Hold the plunger rod by the end and do not touch the shaft. Attach the threaded end of the plunger rod to the syringe plunger. Turn the plunger rod clockwise until you feel a slight resistance.
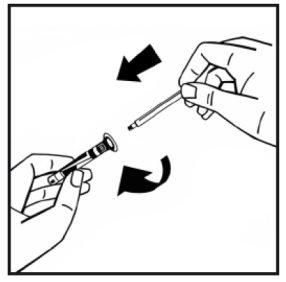
- Break the plastic protective tip of the solvent syringe by breaking the perforation of the cap. Do not touch the inside of the cap or the tip of the syringe. If you do not use the solution immediately, close the filled syringe with the plastic protective tip to store it.
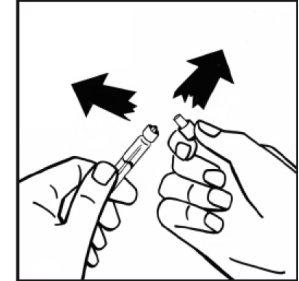
- Remove the adapter packaging and discard it.
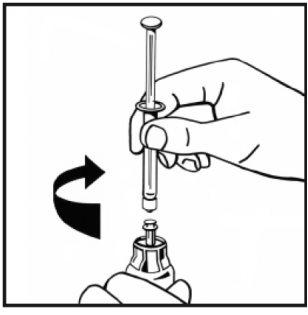
- Securely attach the solvent syringe to the vial adapter by turning it clockwise until you feel a slight resistance.
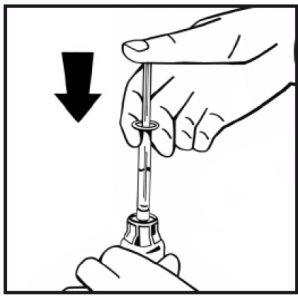
- Slowly inject all of the solvent into the powder vial by pressing the plunger rod downwards.
- Without removing the syringe, gently move or rotate the vial a few times to dissolve the powder. Do not shake. Wait until all of the powder is completely dissolved.
- Check if the final solution has particles before administering it. The solution should be clear and colorless, practically free from visible particles. Do not use cloudy or sedimented solutions.
- Turn the vial attached to the syringe upside down and slowly withdraw the solution into the syringe. Make sure to transfer all of the vial contents into the syringe.
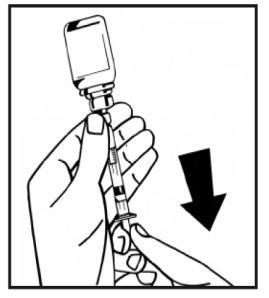
- Separate the filled syringe from the vial adapter by turning it counterclockwise and discard the empty vial.
- The solution is now ready for immediate use. Do not refrigerate.
- Clean the chosen injection site with one of the provided alcohol swabs.
- Attach the provided injection kit to the syringe.
Insert the injection kit needle into the chosen vein. If you have used a tourniquet to make the vein more visible, it should be released before starting to inject the solution.
Do not allow blood to enter the syringe due to the risk of fibrin clot formation.
- Inject the solution into the vein slowly, no faster than 4 ml per minute.
If you use more than one vial of powder for a treatment, you may use the same needle again. The vial adapter and syringe are for single use only.
- Country of registration
- Active substance
- Prescription requiredYes
- Manufacturer
- This information is for reference only and does not constitute medical advice. Always consult a doctor before taking any medication. Oladoctor is not responsible for medical decisions based on this content.
- Alternatives to NUWIQ 4000 IU POWDER AND SOLVENT FOR INJECTABLE SOLUTIONDosage form: INJECTABLE, 1,000 IUActive substance: coagulation factor VIIIManufacturer: Takeda Manufacturing Austria AgPrescription requiredDosage form: INJECTABLE, 1500 IUActive substance: coagulation factor VIIIManufacturer: Takeda Manufacturing Austria AgPrescription requiredDosage form: INJECTABLE, 1000 IU - after reconstitution in 2 ml of water for injections, the dose is 500 IU/mlActive substance: coagulation factor VIIIManufacturer: Takeda Manufacturing Austria AgPrescription required
Online doctors for NUWIQ 4000 IU POWDER AND SOLVENT FOR INJECTABLE SOLUTION
Discuss questions about NUWIQ 4000 IU POWDER AND SOLVENT FOR INJECTABLE SOLUTION, including use, safety considerations and prescription review, subject to medical assessment and local regulations.
Frequently Asked Questions















