TAVLIANT 40 MICROGRAMOS/ML COLIRIO EN SOLUCION

Cómo usar TAVLIANT 40 MICROGRAMOS/ML COLIRIO EN SOLUCION
Traducción generada por IA
Este contenido ha sido traducido automáticamente y se ofrece solo con fines informativos. No sustituye la consulta con un profesional sanitario.
Ver originalContenido del prospecto
Introducción
Prospecto: información para el usuario
Tavliant 40 microgramos/ml colirio en solución
travoprost
Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene información importante para usted.
- Conserve este prospecto, ya que puede tener que volver a leerlo.
- Si tiene alguna duda, consulte a su médico o farmacéutico.
- Este medicamento se le ha recetado a usted, y no debe dárselo a otras personas aunque tengan los mismos síntomas que usted, ya que puede perjudicarles.
- Si experimenta efectos adversos, consulte a su médico o farmacéutico, incluso si se trata de efectos adversos que no aparecen en este prospecto. Ver sección 4.
Contenido del prospecto
- Qué es Tavliant y para qué se utiliza
- Qué necesita saber antes de empezar a usar Tavliant
- Cómo usar Tavliant
- Posibles efectos adversos
- Conservación de Tavliant
- Contenido del envase e información adicional
1. Qué es Tavliant y para qué se utiliza
Tavliant contiene travoprostque forma parte de un grupo de medicamentos llamados análogos de las prostaglandinas. Actúa disminuyendo la presión en el ojo. Se puede utilizar solo o con otras gotas oftálmicas, por ejemplo con betabloqueantes, que también reducen la presión en el ojo.
Tavliant seutilizaparareducirlapresiónelevadaenelojoenadultos,adolescentes y niños a partir de 2 meses de edad. Esta presión puede dar lugar a una enfermedad llamada glaucoma.
2. Qué necesita saber antes de empezar a usar Tavliant
NO use Tavliant
- Si es alérgico a travoprost o a cualquiera de los demás componentes de este medicamento (incluidos en la sección 6).
Consulte a su médico si se encuentra en esta situación.
Advertencias y precauciones
- Travoprost puede aumentarla longitud, el grosor, color y/o número de sus pestañas. También se han observado cambios como crecimiento inusual del vello en los párpados o en los tejidos de alrededor del ojo.
- Travoprost puede alterar el color del iris(la parte coloreada del ojo). Este cambio puede ser permanente. También puede producir un cambio de color de la piel alrededor del ojo.
- Si se ha sometido a una operación de cataratas, consulte a su médico antes de empezar a usar este medicamento.
- Si sufre o ha sufrido anteriormente una inflamacióndel ojo(iritis y uveítis), consulte a su médico antes de empezar a usar este medicamento.
- Travoprost puede causar, en raras ocasiones, falta de alientoo respiración ruidosao aumentar los síntomas del asma. Si está preocupado por los cambios en su respiración mientras utilizatravoprost, consulte a su médico lo antes posible.
- Travoprost puede absorberse a través de la piel.En caso de contactodel medicamento con la piel,debe eliminarse lavandoinmediatamente.Esto es especialmente importante en mujeres embarazadas o que estén intentando quedarse embarazadas.
- Si lleva lentes de contacto blandas, no se aplique las gotas mientras las lleve puestas. Después de aplicar las gotas, espere 15 minutos antes de volver a colocarse las lentes.
Niños y adolescentes
Se puede usar travoprost en niños desde los 2 meses de edad a < de 18 años con la misma dosis que en adultos. No se recomienda el uso de travoprost en niños menores de 2 meses de edad.
Otros medicamentos y Tavliant
Informe a su médico o farmacéutico si está utilizando, ha utilizado recientemente o podría tener que utilizar cualquier otro medicamento.
Embarazo, lactanciay fertilidad
No utilice Tavliant si está embarazada.Si cree que podría estar embarazada dígaselo en seguida a su médico. Si usted puede quedarse embarazada, debe utilizar un método anticonceptivo adecuado mientras esté utilizando travoprost.
No utilice Tavliant si está amamantando.Travoprost puede pasar a la leche materna.
Consulte a su médico antes de utilizar cualquier medicamento.
Conducción y uso de máquinas
Inmediatamente después de la aplicación de travoprost puede notar que su visión se vuelve
borrosa. No conduzca ni utilice máquinas hasta que hayan desaparecido estos efectos.
Tavliant contiene cloruro de benzalconio
Este medicamento contiene 0,15 mg de cloruro de benzalconio en cada ml.
El cloruro de benzalconio se puede absorber por las lentes de contacto blandas y puede alterar el color de las lentes de contacto. Retirar las lentes de contacto antes de usar este medicamento y esperar 15 minutos antes de volver a colocarlas.
El cloruro de benzalconio puede causar irritación ocular, especialmente si padece de ojo seco u otras enfermedades de la córnea (capa transparente de la zona frontal del ojo). Consulte a su médico si siente una sensación extraña, escozor o dolor en el ojo después de usar este medicamento.
Tavliant contiene hidroxiestearato de macrogolglicerol
Este medicamento puede causar reacciones en la piel porque contiene hidroxiestearato de macrogolglicerol.
3. Cómo usar Tavliant
Siga exactamente las instrucciones de administración de este medicamento indicadas por su médico o el médico que trata al niño. En caso de duda, consulte de nuevo a su médico, al médico que trata al niño o al farmacéutico.
La dosis recomendada es
Una gota en el ojo u ojos afectados, una vez al día-por la noche.
Solo debe aplicarse travoprost en los dos ojos si su médico así se lo indica. Siga el tratamiento durante el periodo de tiempo indicado por su médico o el médico que trata al niño.
Travoprost solo debe utilizarse como gotas para sus ojos o los de los niños.
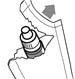
1 |
|
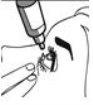
2 |
|
3 |
|
4 |
|
Si una gota cae fuera del ojo,inténtelo de nuevo.
Si usted o el niño están utilizando otros medicamentos oftálmicos, como colirios o pomadas para los ojos, espere por lo menos 5 minutos entre la aplicación de travoprost y de los otros medicamentos oftálmicos.
Si usted oel niñoreciben más Tavliant del que deben
Puede eliminarlo lavando su ojo con agua templada. No se aplique más gotas hasta que le toque la siguiente dosis.
Si olvidó usar Tavliant
Continúe con la siguiente dosis que estaba prevista. Noaplique una dosis doblepara compensar la dosis olvidada. Nunca aplique más de una gota al día en el ojo(s) afectado(s).
Si interrumpe el tratamiento con Tavliant
No deje de utilizar travoprost sin consultar antes con su médico o el médico que trata al niño, la presión en su ojo o en el ojo del niño no estará controlada lo que le podría provocar pérdida de visión.
Si tiene cualquier otra duda sobre el uso de este medicamento, pregunte a su médico, al médico que está tratando al niño o al farmacéutico.
4. Posibles efectos adversos
Al igual que todos los medicamentos, este medicamento puede producir efectos adversos, aunque no todas las personas los sufran.
Puede seguir normalmente el tratamiento a no ser que los efectos adversos sean graves. Si estos efectos le preocupan, consulte a su médico o farmacéutico. No deje de aplicarse travoprost sin consultar a su médico.
Con travoprost se han observado los siguientes efectos adversos:
Efectos adversos muy frecuentes (pueden afectar a más de 1 de cada 10 personas):
Efectos en el ojo:
- Enrojecimiento del ojo
Efectos adversos frecuentes(pueden afectar hasta 1 de cada 10 personas):
Efectos en el ojo:
- cambios en el color del iris (parte coloreada del ojo)
- dolor en el ojo
- molestia en el ojo
- ojo seco
- picor en el ojo
- irritación en el ojo
Efectos adversos poco frecuentes(pueden afectar hasta 1 de cada 100 personas):
Efectos en el ojo:
- alteración corneal
- inflamación del ojo
- inflamación del iris
- inflamación dentro del ojo
- inflamación con o sin daño de la superficie del ojo
- sensibilidad a la luz
- secreción del ojo
- inflamación del párpado
- enrojecimiento del párpado
- hinchazón alrededor del ojo
- picor en el párpado
- visión borrosa
- aumento de la producción de lágrimas
- infección o inflamación de la conjuntiva (conjuntivitis)
- vuelta anormal hacia fuera del párpado inferior
- visión ensombrecida
- costras en el párpado
- crecimiento de las pestañas
Otros efectos:
- aumento de los síntomas alérgicos
- dolor de cabeza
- frecuencia cardiaca irregular
- tos
- nariz taponada
- irritación de garganta
- oscurecimiento de la piel alrededor de los ojos
- oscurecimiento de la piel
- textura anormal del pelo
- aumento excesivo del crecimiento del vello
Efectos adversos raros(pueden afectar hasta 1 de cada 1.000 personas):
Efectos en el ojo:
- percepción de destellos de luz
- eczema de los párpados
- pestañas anormalmente posicionadas que crecen hacia dentro del ojo
- hinchazón del ojo
- visión reducida
- halo visual
- sensación disminuida en el ojo
- inflamación de las glándulas de los párpados
- pigmentación dentro del ojo
- aumento en el tamaño de la pupila
- engrosamiento de las pestañas
- cambio del color de las pestañas
- ojos cansados
Otros efectos:
- infección vírica en el ojo
- mareo
- mal sabor de boca
- frecuencia cardiaca irregular o disminuida
- presión sanguínea aumentada o disminuida
- falta de aliento
- asma
- alergia nasal o inflamación
- sequedad nasal
- cambios de voz
- úlcera o malestar gastrointestinal
- estreñimiento
- boca seca
- enrojecimiento o picor de la piel
- erupción
- cambio del color del vello
- pérdida de pestañas
- dolor articular
- dolor musculo esquelético
- debilidad generalizada
Frecuencia no conocida (no puede estimarse a partir de los datos disponibles):
Efectos en el ojo:
- inflamación de la parte posterior del ojo
- ojos hundidos
Otros efectos:
- depresión
- ansiedad
- insomnio
- sensación falsa de movimiento
- pitidos en oídos
- dolor en el pecho
- ritmo cardíaco anormal
- aumento de la frecuencia cardíaca
- empeoramiento del asma
- diarrea
- sangrado de nariz
- dolor abdominal
- náusea
- vómitos
- picor
- crecimiento anormal del pelo
- micción dolorosa o involuntaria (orinar de forma involuntaria o dolor al orinar)
- aumento del marcador del cáncer de próstata.
En niños y adolescentes, los efectos adversos más frecuentes observados con travoprost son enrojecimiento del ojo y crecimiento de las pestañas. Ambos efectos adversos se observaron con una incidencia mayor en niños y adolescentes comparado con adultos.
Comunicación de efectos adversos
Si experimenta cualquier tipo de efecto adverso, consulte a su médico o farmacéutico, incluso si se trata de posibles efectos adversos que no aparecen en este prospecto. También puede comunicarlos directamente a través del Sistema Español de Farmacovigilancia de Medicamentos de Uso Humano: https://www.notificaram.es. Mediante la comunicación de efectos adversos usted puede contribuir a proporcionar más información sobre la seguridad de este medicamento.
5. Conservación de Tavliant
Mantener este medicamento fuera de la vista y del alcance de los niños.
No utilice este medicamento después de la fecha de caducidad que aparece en el frasco y en la caja después de CAD. La fecha de caducidad es el último día del mes que se indica.
No utilice este medicamento si observa que el precinto está roto o dañado antes de la primera apertura.
Este medicamento no requiere ninguna temperatura especial de conservación. Mantener el frasco dentro de la bolsa antes de su apertura.
Este medicamento no requiere condiciones especiales de conservación tras la primera apertura.
Para evitar infecciones, debe desechar el frasco 4 semanas después de haberlo abierto por primera vez, y utilizar un frasco nuevo.Anote la fecha de apertura en el espacio reservado en la caja.
Los medicamentos no se deben tirar por los desagües ni a la basura. Deposite los envases y los medicamentos que no necesita en el Punto SIGRE de la farmacia. En caso de duda pregunte a su farmacéutico cómo deshacerse de los envases y de los medicamentos que no necesita. De esta forma, ayudará a proteger el medio ambiente.
6. Contenido del envase e información adicional
Composición de Tavliant
- El principio activo es travoprost. Este medicamento contiene 40 microgramos/ml de travoprost.
- Los demás componentes son cloruro de benzalconio, hidroxiestearato de macrogolglicerol, trometamol, edetato disódico, ácido bórico, manitol, hidróxido de sodio para ajustar el pH y agua purificada.
Aspecto del producto y contenido del envase
Tavliant es una solución incolora y transparente que se presenta en envases que contienen bolsas con frasco(s) de 5 ml de polipropileno translucido con cuentagotas de polietileno de baja densidad (LDPE) transparente y tapón precinto de polietileno de alta densidad (HDPE) blanco. Cada envase contiene un frasco con 2.5 ml de colirio en solución.
.
Titular de la autorización de comercialización y responsable de la fabricación
Titular de la autorización de comercialización
Laboratorio Stada, S.L
Frederic Mompou, 5
08960 Sant Just Desvern (Barcelona)
España
Responsable de la fabricación
Pharmathen S.A.
6, Dervenakion str., 15351 Pallini, Atenas
Grecia
o
BALKANPHARMA-RAZGRAD AD
68 Aprilsko vastanie Blvd., Razgrad 7200
Bulgaria
o
STADA Arzneimittel AG
Stadastrasse 2-18, 61118 Bad Vilbel
Alemania
o
JADRAN – GALENSKI LABORATORIJ d.d.
Svilno 20,
Rijeka, 51000
Croacia
Fecha de la última revisión del prospecto: Agosto 2024
La información detallada y actualizada de este medicamento está disponible en la página web de la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) http://www.aemps.gob.es/
- País de registro
- Principio activo
- Requiere recetaSí
- Fabricante
- Esta información es de carácter general y no sustituye la consulta con un profesional sanitario.
- Alternativas a TAVLIANT 40 MICROGRAMOS/ML COLIRIO EN SOLUCIONForma farmacéutica: COLIRIO, 40 microgramos/mlPrincipio activo: travoprostFabricante: Alfred E. Tiefenbacher Gmbh & Co. KgRequiere recetaForma farmacéutica: COLIRIO, 40 microgramos/mlPrincipio activo: travoprostFabricante: Horus PharmaRequiere recetaForma farmacéutica: COLIRIO, 0,04 mg/mlPrincipio activo: travoprostFabricante: Omnivision GmbhRequiere receta
Médicos online para TAVLIANT 40 MICROGRAMOS/ML COLIRIO EN SOLUCION
Comenta la dosis, los posibles efectos secundarios, interacciones, contraindicaciones o la revisión de receta de TAVLIANT 40 MICROGRAMOS/ML COLIRIO EN SOLUCION, sujeto a valoración médica y a la normativa local.
Preguntas frecuentes