
Iavrix Adult

Consulta con un médico sobre la receta médica de Iavrix Adult

Cómo usar Iavrix Adult
Hoja de instrucciones para el paciente: información para el usuario
Havrix Adult, suspensión para inyección
Vacuna contra la hepatitis viral tipo A, inactivada, adsorbida
Es importante leer atentamente el contenido de esta hoja de instrucciones antes de administrar la vacuna, ya que contiene
información importante para el paciente.
- Debe conservar esta hoja de instrucciones para poder volver a leerla si es necesario.
- En caso de dudas, debe consultar a su médico, farmacéutico o enfermera.
- Esta vacuna ha sido prescrita específicamente para usted. No debe dársela a otros.
- Si el paciente experimenta algún efecto adverso, incluidos todos los efectos adversos no mencionados en esta hoja de instrucciones, debe informar a su médico, farmacéutico o enfermera. Véase el punto 4.
El contenido de esta hoja de instrucciones se ha redactado con la suposición de que será leído por la persona que recibe la vacuna. Sin embargo, como esta vacuna puede administrarse a adolescentes a partir de 16 años, es posible que los padres o tutores del niño lean el contenido de esta hoja de instrucciones.
Índice de la hoja de instrucciones:
- 1. Qué es la vacuna Havrix Adult y para qué se utiliza
- 2. Información importante antes de administrar la vacuna Havrix Adult
- 3. Cómo administrar la vacuna Havrix Adult
- 4. Posibles efectos adversos
- 5. Cómo conservar la vacuna Havrix Adult
- 6. Contenido del envase y otra información
1. Qué es la vacuna Havrix Adult y para qué se utiliza
Para qué se utiliza la vacuna Havrix Adult
La vacuna Havrix Adult se utiliza para prevenir la hepatitis viral tipo A (HVA) en personas de 16 años o más que estén expuestas al virus de la hepatitis A (HAV).
Qué es la hepatitis viral tipo A:
‐
La HVA es una enfermedad del hígado causada por el virus de la hepatitis A (HAV).
‐
El virus HAV se transmite de persona a persona o a través del contacto con agua, alimentos y bebidas contaminados.
‐
Los síntomas de la hepatitis A varían desde leves hasta graves y pueden incluir fiebre, malestar general, pérdida de apetito, diarrea, náuseas, dolor abdominal, orina oscura y ictericia (amarillamiento de los ojos y la piel). La mayoría de los pacientes se recuperan completamente, pero a veces la enfermedad puede ser grave y requerir hospitalización, y en casos raros puede llevar a una insuficiencia hepática aguda.
Cómo funciona Havrix Adult:
‐
Havrix Adult ayuda al cuerpo a producir su propia protección (anticuerpos) contra el virus.
‐
Al igual que con todas las vacunas, Havrix Adult puede no proteger completamente a todas las personas vacunadas.
2. Información importante antes de administrar la vacuna Havrix Adult
Cuándo no administrar la vacuna Havrix Adult
‐
si el paciente es alérgico a la sustancia activa o a alguno de los demás componentes de esta vacuna (enumerados en el punto 6) o a la neomicina o al formaldehído,
‐
si ha habido una reacción alérgica previa a cualquier vacuna contra la hepatitis viral tipo A.
Los síntomas de una reacción alérgica pueden incluir erupción cutánea con picazón, dificultad para respirar, hinchazón de la cara o la lengua.
No debe administrarse la vacuna Havrix Adult si alguna de estas situaciones se aplica al paciente. En caso de duda antes de administrar la vacuna Havrix Adult, debe consultar a su médico, farmacéutico o enfermera.
Advertencias y precauciones
Antes de administrar la vacuna Havrix Adult, debe discutir con su médico si:
‐
el paciente tiene una infección grave con fiebre alta. En este caso, la vacunación se retrasará. Una infección leve, como un resfriado, no debe ser una contraindicación para la vacunación, pero primero debe informar a su médico,
‐
el paciente tiene un sistema inmunológico debilitado debido a una enfermedad y/o medicamentos. El médico decidirá si es necesario administrar dosis adicionales,
‐
hay problemas de sangrado o se producen moretones con facilidad.
Después de o incluso antes de la administración de cada vacuna en forma de inyección, puede ocurrir un desmayo. En relación con esto, debe informar a su médico, farmacéutico o enfermera si ha tenido un desmayo durante la administración de una inyección.
La vacuna Havrix Adult y otros medicamentos
Debe informar a su médico, farmacéutico o enfermera sobre todos los medicamentos que esté tomando actualmente o recientemente, así como sobre los medicamentos que planea tomar y sobre las vacunas que ha recibido recientemente.
La vacuna Havrix Adult se puede administrar al mismo tiempo que algunas otras vacunas y gammaglobulinas, pero los sitios de inyección deben ser diferentes.
Embarazo y lactancia
Si la paciente está embarazada o en período de lactancia, sospecha que puede estar embarazada o planea tener un hijo, debe consultar a su médico, farmacéutico o enfermera antes de utilizar esta vacuna.
Conducción de vehículos y uso de máquinas
La vacuna Havrix Adult no tiene o tiene un efecto insignificante en la capacidad para conducir vehículos y utilizar máquinas.
Havrix Adult contiene fenilalanina, sodio y potasio
Esta vacuna contiene 0,166 mg de fenilalanina por dosis.
La fenilalanina puede ser perjudicial para los pacientes con fenilcetonuria, una enfermedad genética rara, en la que la fenilalanina se acumula en el cuerpo porque el cuerpo no la elimina adecuadamente.
Esta vacuna contiene menos de 1 mmol (23 mg) de sodio por dosis y menos de 1 mmol (39 mg) de potasio por dosis, es decir, la vacuna se considera "libre de sodio y potasio".
3. Cómo administrar la vacuna Havrix Adult
Cómo se administra la vacuna Havrix Adult
‐
La vacuna Havrix Adult se administra mediante inyección intramuscular, generalmente en el músculo del brazo.
‐
En pacientes con recuento bajo de plaquetas o con trastornos graves de coagulación, la vacuna Havrix Adult puede administrarse subcutáneamente en casos excepcionales.
Dosis
‐
El paciente recibirá 1 dosis de la vacuna Havrix Adult (1 ml de suspensión) en la fecha acordada con su médico o enfermera.
‐
Se recomienda administrar una segunda dosis (dosis de refuerzo) entre 6 y 12 meses después de la primera dosis, pero puede administrarse hasta 5 años después de la primera dosis para garantizar una protección a largo plazo.
Administración de una dosis mayor que la recomendada de la vacuna Havrix Adult
La sobredosis es muy poco probable, ya que la vacuna se suministra en un frasco o jeringa con una dosis única y se administra por un médico o enfermera. Se han notificado algunos casos de administración accidental de una dosis mayor, y los efectos adversos notificados fueron similares a los notificados con la administración normal de la vacuna (enumerados en la sección 4).
Si se pierde una dosis de la vacuna Havrix Adult
Debe ponerse en contacto con su médico, quien decidirá si es necesario administrar otra dosis.
4. Posibles efectos adversos
Como cualquier medicamento, esta vacuna puede causar efectos adversos, aunque no todos los pacientes los experimentarán.
Efectos adversos graves
Debe informar inmediatamente a su médico si experimenta alguno de los siguientes efectos adversos graves - puede ser necesario un tratamiento de emergencia:
‐
reacciones alérgicas - los síntomas pueden incluir erupción cutánea localizada o generalizada que puede picar o formar ampollas, hinchazón de los ojos y la cara, dificultad para respirar o tragar, caída repentina de la presión arterial y pérdida de conciencia.
Estas reacciones pueden ocurrir antes de salir de la consulta del médico.
En caso de que ocurra alguno de los efectos adversos graves mencionados anteriormente, debe informar inmediatamente a su médico.
Durante los estudios clínicos de Havrix Adult, se produjeron los siguientes efectos adversos:
Muy frecuentes(pueden ocurrir en más de 1 de cada 10 dosis de la vacuna):
- dolor de cabeza
- dolor y enrojecimiento en el lugar de la inyección
- fatiga
Frecuentes(pueden ocurrir en hasta 1 de cada 10 dosis de la vacuna):
- pérdida de apetito
- náuseas (vómitos)
- vómitos
- diarrea
- malestar general
- fiebre ≥ 37,5°C
- hinchazón o endurecimiento en el lugar de la inyección
Poco frecuentes(pueden ocurrir en hasta 1 de cada 100 dosis de la vacuna):
- infección de las vías respiratorias superiores
- congestión nasal o resfriado
- mareos
- dolor muscular, rigidez muscular, no causado por el ejercicio
- síntomas similares a los de la gripe, como fiebre alta, dolor de garganta, resfriado, tos y escalofríos
Raros(pueden ocurrir en hasta 1 de cada 1000 dosis de la vacuna):
- disminución o pérdida de sensibilidad cutánea al dolor o al tacto
- entumecimiento
- picazón
- escalofríos
Los siguientes efectos adversos se han producido después de la comercialización de la vacuna Havrix Adult:
‐
convulsiones
‐
estrechamiento o bloqueo de los vasos sanguíneos
‐
reacción alérgica grave que causa hinchazón de la cara, la lengua o la garganta, lo que puede causar dificultad para tragar o respirar
‐
urticaria, manchas rojas, a menudo con picazón, que comienzan en las extremidades y a veces en la cara y el resto del cuerpo
‐
dolor articular
Notificación de efectos adversos
Si se producen efectos adversos, incluidos todos los efectos adversos no mencionados en esta hoja de instrucciones, debe informar a su médico, farmacéutico o enfermera. Los efectos adversos pueden notificarse directamente al Departamento de Vigilancia de Medicamentos del Ministerio de Sanidad: Calle de Alcalá, 56, 28071 Madrid, teléfono: 91 596 24 00, fax: 91 596 24 01, sitio web: www.aemps.gob.es
Los efectos adversos también pueden notificarse al titular de la autorización de comercialización.
La notificación de efectos adversos permite recopilar más información sobre la seguridad de este medicamento.
5. Cómo conservar la vacuna Havrix Adult
El medicamento debe conservarse en un lugar donde no pueda ser visto o alcanzado por los niños.
Conservar en refrigerador (2 °C – 8 °C).
No congelar.
Conservar en el embalaje original para protegerlo de la luz.
No utilizar esta vacuna después de la fecha de caducidad que se indica en el embalaje después de "EXP". La fecha de caducidad es el último día del mes indicado.
El código "Lote" es el número de lote del producto.
6. Contenido del envase y otra información
Qué contiene la vacuna Havrix Adult
- La sustancia activa de la vacuna Havrix Adult es:
Virus de la hepatitis A, cepa HM175 (inactivado)
no menos de 1440 unidades ELISA
producido en cultivo de células diploides humanas MRC-5
adsorbido en hidróxido de aluminio hidratado
0,5 mg de Al
- Los demás componentes son: polisorbato 20, aminoácidos para inyección (incluyendo fenilalanina), fosfato sódico, fosfato potásico, cloruro sódico, cloruro potásico, agua para inyección.
Cómo se presenta la vacuna Havrix Adult y qué contiene el envase
Havrix Adult es una suspensión blanca ligeramente opaca en un frasco o jeringa precargada.
Envases disponibles:
1 frasco de 1 ml en una caja de cartón
1 jeringa precargada con aguja de 1 ml en una caja de cartón
1 jeringa precargada de 1 ml con aguja unida al embalaje en una caja de cartón
Título del responsable y fabricante
GlaxoSmithKline Biologicals S.A.
calle del Instituto, 89
1330 Rixensart, Bélgica
Para obtener más información, debe ponerse en contacto con el representante local del titular de la autorización de comercialización:
GSK Services, S.L.
calle de Rzymowskiego, 53
02-697 Varsovia
teléfono: +48 (22) 576-90-00
Este medicamento está autorizado en los estados miembros del Espacio Económico Europeo bajo los siguientes nombres:
| República Checa, Dinamarca, Estonia, Finlandia, Grecia, Islandia, Italia | HAVRIX |
| Noruega, Suecia | Havrix |
| Austria, Bélgica, Hungría, Luxemburgo, Países Bajos | HAVRIX 1440 |
| Alemania | Havrix 1440 |
| Bulgaria | ХАВРИКС 1440 инжекционна суспензия (доза за възрастни) |
| Chipre | HAVRIX 1440 IU |
| Francia | HAVRIX 1440 U/1ml ADULTES |
| Irlanda, Malta | HAVRIX MONODOSE |
| Letonia | HAVRIX 1440 ELISA vienības/ml suspensija injekcijām |
| Lituania | Havrix 1440 ELISA vienetų/ml injekcinė suspensija |
| Polonia | HAVRIX ADULT |
| Portugal | HAVRIX 1440 ADULTO |
| Rumania | HAVRIX ADULT 1440 suspensie injectabilă |
| República Eslovaca | HAVRIX 1440 Dosis adulta |
| Eslovenia | HAVRIX 1440 ELISA enot suspensija za injiciranje |
Fecha de la última revisión de la hoja de instrucciones:
08/2024
Información destinada exclusivamente al personal médico o sanitario:
Durante el almacenamiento, puede aparecer un precipitado blanco en el fondo del frasco o jeringa y un líquido transparente e incoloro por encima. Antes de la administración, la vacuna debe ser examinada en busca de cuerpos extraños y/o cambios físicos.
Antes de su uso, debe agitarse el frasco o la jeringa para obtener una suspensión blanca ligeramente opaca.
En caso de observar algún cambio en el aspecto de la vacuna, no debe administrarse.
| para adultos | |
| España | HAVRIX 1440 suspensión inyectable en jeringa precargada |
Instrucciones para la jeringa precargada
Debe sostener la jeringa precargada por el cuerpo, no por el émbolo.
Debe girar la tapa de la jeringa precargada en el sentido contrario a las agujas del reloj.
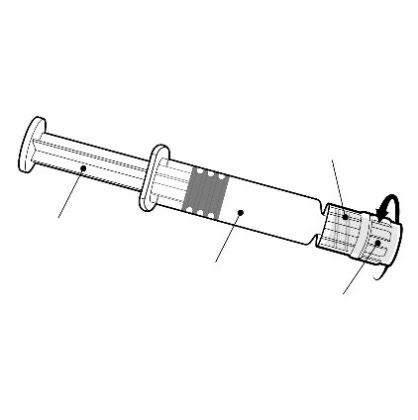
Adaptador Luer Lock
Émbolo
Cuerpo
Tapa
Debe fijar la aguja a la jeringa precargada conectando la tapa de la aguja al adaptador Luer Lock (LLA) y girándola un cuarto de vuelta en el sentido de las agujas del reloj, hasta que se sienta el bloqueo de la aguja.
No debe retirar el émbolo del cuerpo de la jeringa precargada. Si esto sucede, no debe administrarse la vacuna.
Eliminación
Todos los residuos de producto no utilizados o desechos deben eliminarse de acuerdo con las regulaciones locales.
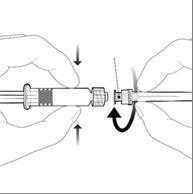
Tapa de la aguja
- País de registro
- Principio activo
- Requiere recetaSí
- Fabricante
- ImportadorGlaxoSmithKline Biologicals S.A.
- Esta información ha sido traducida con IA y es solo orientativa. No constituye asesoramiento médico. Consulta siempre con un médico antes de tomar cualquier medicamento.
- Alternativas a Iavrix AdultForma farmacéutica: Suspensión, 160 unidades antigénicas ELISA del virus de la hepatitis A, cepa GBM/0,5 ml; 1 dosis (0,5 ml)Principio activo: hepatitis A, inactivated, whole virusRequiere recetaForma farmacéutica: Suspensión, al menos 720 unidades ELISA de virus de la hepatitis A, cepa HM175/0.5 ml; 1 dosis (0.5 ml)Principio activo: hepatitis A, inactivated, whole virusFabricante: GlaxoSmithKline Biologicals S.A.Requiere recetaForma farmacéutica: Suspensión, 25 U de virus de la hepatitis A, cepa CR326F/0.5 ml; 1 dosis (0.5 ml), para niños y adolescentesPrincipio activo: hepatitis A, inactivated, whole virusFabricante: Merck Sharp & Dohme B.V.Requiere receta
Alternativas a Iavrix Adult en otros países
Las mejores alternativas con el mismo principio activo y efecto terapéutico.
Alternativa a Iavrix Adult en España
Alternativa a Iavrix Adult en Ucrania
Médicos online para Iavrix Adult
Consulta sobre dosis, efectos secundarios, interacciones, contraindicaciones y renovación de la receta de Iavrix Adult – sujeta a valoración médica y normativa local.














