HAVRIX 1440 ADULTO, SUSPENSION INYECTABLE EN JERINGA PRECARGADA

Cómo usar HAVRIX 1440 ADULTO, SUSPENSION INYECTABLE EN JERINGA PRECARGADA
Traducción generada por IA
Este contenido ha sido traducido automáticamente y se ofrece solo con fines informativos. No sustituye la consulta con un profesional sanitario.
Ver originalContenido del prospecto
Introducción
Prospecto: información para el usuario
Havrix 1440 Adulto, suspensión inyectable en jeringa precargada
Vacuna frente a la hepatitis A (inactivada, adsorbida)
Lea todo el prospecto detenidamente antes deque usted o su hijo empiece arecibir esta vacuna, porque contiene información importante para usted.
- Conserve este prospecto, ya que puede tener que volver a leerlo.
- Si tiene alguna duda, consulte a su médico, farmacéutico o enfermero.
- Esta vacuna se le ha recetado solamente a usted o a su hijo, y no debe dárselo a otras personas.
- Si usted o su hijo experimenta efectos adversos, consulte a su médico, farmacéutico o enfermero, incluso si se trata de efectos adversos que no aparecen en este prospecto. Ver sección 4.
Este prospecto se ha escrito asumiendo que la persona que recibe la vacuna es quien lo lee, aunque se puede administrar a adolescentes a partir de los 16 años de edad, por lo que es posible que usted tenga que leerlo para su hijo.
Contenido del prospecto
- Qué es Havrix 1440 Adulto y para qué se utiliza
- Qué necesita saber antes de empezar a recibir Havrix 1440 Adulto
- Cómo se administra Havrix 1440 Adulto
- Posibles efectos adversos
- Conservación de Havrix 1440 Adulto
- Contenido del envase e información adicional
1. Qué es Havrix 1440 Adulto y para qué se utiliza
Para qué se utilizaHavrix1440 Adulto
Havrix 1440 Adulto es una vacuna que se utiliza para proteger a adolescentes a partir de los 16 años de edad y adultos frente a la infección causada por el virus de la hepatitis A.
Qué es la hepatitis A
- La hepatitis A es una enfermedad del hígado causada por el virus de la hepatitis A.
- El virus de la hepatitis A puede transmitirse de persona a persona o por el contacto con agua, alimentos y bebidas contaminadas.
- Los síntomas de la hepatitis A varían de leves a graves, y pueden incluir: fiebre, malestar general, pérdida de apetito, diarrea, náuseas, malestar abdominal, orina de color oscuro e ictericia (coloración amarillenta de los ojos y la piel). La mayoría de las personas se recuperan por completo aunque, a veces, la enfermedad puede ser grave y requerir hospitalización y, en raras ocasiones, puede provocar insuficiencia hepática aguda.
Cómo funciona Havrix1440 Adulto
Havrix 1440 Adulto ayuda a su cuerpo a producir su propia protección (anticuerpos) contra el virus. Estos anticuerpos ayudan a protegerle contra la enfermedad.
Como ocurre con todas las vacunas, puede que Havrix 1440 Adulto no proteja completamente a todas las personas vacunadas.
2. Qué necesita saber antes de empezar a recibir Havrix 1440 Adulto
No se debe administrarHavrix1440 Adultosi:
- usted es alérgico al principio activo o a alguno de los demás componentes de esta vacuna (incluidos en la sección 6) o a la neomicina o al formaldehido,
- usted ya ha tenido una reacción alérgica a cualquier vacuna frente a la hepatitis A.
Los signos de una reacción alérgica pueden incluir: erupción cutánea con picazón, dificultad para respirar e hinchazón de la cara o la lengua.
No se debe administrar Havrix 1440 Adulto si cualquiera de las situaciones anteriores le aplica a usted. Si no está seguro, consulte a su médico, farmacéutico o enfermero antes de que le administren Havrix 1440 Adulto.
Advertencias y precauciones
Consulte a su médico, farmacéutico o enfermero antes de recibir Havrix 1440 Adulto si:
- usted tiene una infección grave con temperatura alta (fiebre). La vacuna se puede administrar una vez que se haya recuperado. Una infección menor, como un resfriado, no debería ser un problema, pero consulte primero a su médico,
- usted tiene un sistema inmunológico debilitado debido a enfermedades y/o tratamientos. Su médico determinará si se necesitan más inyecciones,
- usted tiene problemas de sangrado o le salen cardenales con facilidad.
El desmayo puede ocurrir antes o después de cualquier inyección con aguja. Por tanto, informe al médico, farmacéutico o enfermero si se ha desmayado con una inyección anterior.
Otros medicamentos yHavrix1440 Adulto
Informe a su médico, farmacéutico o enfermero si está usando, ha usado recientemente o pudiera tener que usar cualquier otra vacuna o medicamento.
Havrix 1440 Adulto se puede administrar al mismo tiempo que otras vacunas e inmunoglobulinas. Se debe usar un lugar de inyección diferente para cada inyección.
Embarazo ylactancia
Si está embarazada o en periodo de lactancia, cree que podría estar embarazada o tiene intención de quedarse embarazada, consulte a su médico, farmacéutico o enfermero antes de recibir Havrix 1440 Adulto.
Conducción y uso de máquinas
La influencia de Havrix 1440 Adulto sobre la capacidad para conducir y utilizar máquinas es nula o insignificante.
Havrix1440 Adulto contienefenilalanina, polisorbato 20, sodio y potasio
Esta vacuna contiene 0,166 mg de fenilalanina en cada dosis.
La fenilalanina puede ser perjudicial en caso de padecer fenilcetonuria (FCN), una enfermedad genética rara en la que la fenilalanina se acumula debido a que el organismo no es capaz de eliminarla correctamente.
Esta vacuna contiene 0,050 mg de polisorbato 20 en cada dosis. Los polisorbatos pueden provocar reacciones alérgicas. Informe a su médico si tiene cualquier alergia conocida.
Este medicamento contiene menos de 1 mmol de sodio (23 mg) por dosis; esto es, esencialmente “exento de sodio”.
Este medicamento contiene potasio, menos de 1 mmol (39 mg) por dosis; esto es, esencialmente “exento de potasio”.
3. Cómo se administra Havrix 1440 Adulto
Cómo se administra la vacuna
- El médico o enfermero le administrará Havrix 1440 Adulto mediante una inyección en un músculo, normalmente en la parte superior del brazo.
- Havrix 1440 Adulto puede inyectarse excepcionalmente bajo la piel si padece trombocitopenia o si tiene trastornos hemorrágicos graves.
Cuánto se administra
- Recibirá 1 dosis de Havrix 1440 Adulto (suspensión de 1 ml) en la fecha acordada con su médico o enfermero.
- Se recomienda administrar una segunda dosis (refuerzo) entre 6 y 12 meses después de la primera dosis, aunque se puede administrar hasta cinco años después de la primera dosis, para garantizar una protección a largo plazo.
Si recibe másHavrix 1440 Adultodel que debe
Es muy poco probable que se produzca una sobredosis porque la vacuna se suministra en un vial o jeringa de dosis única y es administrada por un médico o un enfermero. Se notificaron pocos casos de administración accidental y los efectos adversos notificados fueron similares a los notificados con la administración normal de la vacuna (enumerados en la sección 4).
Si olvidó recibirHavrix 1440 Adulto
Contacte con su médico, quien decidirá si se requiere una dosis y cuándo administrarla..
4. Posibles efectos adversos
Al igual que todos los medicamentos, esta vacuna puede producir efectos adversos, aunque no todas las personas los sufran.
Efectos adversos graves
Informe a su médico inmediatamente si nota cualquiera de los siguientes efectos adversos graves; puede que necesite tratamiento médico urgente:
- reacciones alérgicas: los signos pueden incluir erupciones locales o generalizadas que pueden causar picazón o ampollas, hinchazón de los ojos y la cara, dificultad para respirar o tragar, una caída repentina de la presión arterial y pérdida del conocimiento.
Estas reacciones pueden ocurrir antes de salir de la consulta del médico.
Informe a su médico inmediatamente si nota cualquiera de los efectos adversos graves que anteriormente se enumeran.
Los efectos adversos que ocurrieron durante los ensayos clínicos con Havrix1440 Adultofueron los siguientes:
Muy frecuentes(estos pueden ocurrir con más de 1 de cada 10 dosis de la vacuna):
- dolor de cabeza
- dolor y enrojecimiento en el lugar de la inyección
- cansancio
Frecuentes(estos pueden ocurrir hasta con 1 de cada 10 dosis de la vacuna):
- pérdida de apetito
- náuseas
- vómitos
- diarrea
- sensación de malestar general
- fiebre de 37,5°C o más
- hinchazón o endurecimiento en el lugar de la inyección
Poco frecuentes(estos pueden ocurrir hasta con 1 de cada 100 dosis de vacuna):
- infección de las vías respiratorias superiores
- goteo o taponamiento nasal
- mareo
- dolor muscular, rigidez muscular no causada por el ejercicio
- síntomas similares a los de la gripe, como temperatura alta, dolor de garganta, secreción nasal, tos y escalofríos
Raros(estos pueden ocurrir hasta con 1 de cada 1.000 dosis de la vacuna):
- disminución o pérdida de la sensibilidad de la piel al dolor o al tacto
- agujetas
- picor
- escalofríos
Los efectos adversos que ocurrieron tras la comercialización de Havrix1440 Adultofueron los siguientes:
- ataques o convulsiones
- inflamación de los vasos sanguíneos que produce estrechamiento u obstrucción (vasculitis)
- reacción alérgica grave que causa hinchazón de la cara, lengua o garganta que puede causar dificultad para tragar o respirar
- habones, manchas rojas que frecuentemente pican y que comienzan en las extremidades y, a veces, en la cara y el resto del cuerpo.
- dolor en las articulaciones.
Comunicación de efectos adversos
Si experimenta cualquier tipo de efecto adverso, consulte a su médico, farmacéutico o enfermero, incluso si se trata de posibles efectos adversos que no aparecen en este prospecto. También puede comunicarlos directamente a través del Sistema Español de Farmacovigilancia de Medicamentos de Uso Humano: www.notificaRAM.es. Mediante la comunicación de efectos adversos usted puede contribuir a proporcionar más información sobre la seguridad de este medicamento.
5. Conservación de Havrix 1440
Mantener esta vacuna fuera de la vista y del alcance de los niños.
No utilice esta vacuna después de la fecha de caducidad que aparece en el envase. La fecha de caducidad es el último día del mes que se indica.
Conservar en nevera (entre 2 ºC y 8 ºC).
No congelar.
Conservar en el embalaje original para protegerla de la luz.
Los medicamentos no se deben tirar por los desagües ni a la basura. Deposite los envases y los medicamentos que no necesita en el Punto SIGRE de la farmacia. En caso de duda pregunte a su farmacéutico cómo deshacerse de los envases y de los medicamentos que no necesita. De esta forma, ayudará a proteger el medio ambiente.
6. Contenido del envase e información adicional
Composición de Havrix 1440 Adulto
El principio activo es el virus de la hepatitis A (inactivado) adsorbido en hidróxido de aluminio. Cada dosis de 1 ml de la vacuna contiene 1440 unidades ELISA del virus de la hepatitis A.
Los demás componentes son aminoácidos para inyección (contienen fenilalanina), fosfato disódico, fosfato monopotásico, polisorbato 20 (E-432), cloruro de potasio, cloruro de sodio, agua para preparaciones inyectables (ver sección 2).
Aspecto del producto y contenido del envase
Suspensión inyectable.
Havrix 1440 Adulto es un líquido inyectable turbio.
Havrix 1440 Adulto está disponible en jeringa precargada de 1 dosis con o sin agujas; tamaños de envase de 1, 5, 10 y 25.
Puede que solamente estén comercializados algunos tamaños de envases..
Titular de la autorización de comercialización y responsable de la fabricación
Titular de la autorización de comercialización:
GlaxoSmithKline, S.A.
P.T.M. C/ Severo Ochoa, 2
28760 Tres Cantos (Madrid)
España
Tel.: +34 900 202 700
Responsable de la fabricación:
SmithKline Beecham, S.A.
Carretera de Ajalvir, km.2,5
28806 Alcalá de Henares (Madrid)
España
o
GlaxoSmithKline Biologicals s.a.
Rue de l´Institut 89
B-1330 Rixensart
Bélgica
Este medicamento está autorizado en los estados miembros del Espacio Económico Europeocon los siguientes nombres:
Austria | Havrix (Hepatitis A-Impfstoff) 1440 EI.U/1 ml |
Bélgica, Alemania, Hungría, Luxemburgo, Países Bajos | Havrix 1440 |
Bulgaria | HAVRIX 1440 suspension for injection (Adult dose) ??????? 1440 ??????????? ????????? (???? ?? ?????????) |
Chipre | Havrix Adults 1440 |
República Checa, Dinamarca, Finlandia, Islandia, Noruega | Havrix |
Estonia | Havrix, 1440 ELISA ühikut/ml süstesuspensioon |
Francia | HAVRIX 1440 U/1ml ADULTES |
Grecia, Italia | HAVRIX |
Irlanda | Havrix Monodose |
Letonia | Havrix 1440 ELISA vienibas/ml suspensija injekcijam |
Lituania | Havrix 1440 ELISA vienetu/ml injekcine suspensija |
Malta | Havrix Monodose Vaccine |
Polonia | HAVRIX ADULT |
Portugal | Havrix 1440 Adulto |
Rumanía | HAVRIX ADULT 1440 VACCIN HEPATITIC A |
República Eslovaca | HAVRIX 1440 Dosis adulta |
Eslovenia | HAVRIX 1440 |
España | Havrix 1440 Adulto suspensión inyectable en jeringa precargada |
Suecia | Havrix 1440 ELISA U/1 ml |
Fecha de la última revisión de este prospecto:03/2025
Otras fuentes de información
La información detallada de este medicamento está disponible en la página web de la Agencia Española de Medicamentos y Productos sanitarios (AEMPS) http://www.aemps.gob.es/.
--------------------------------------------------------------------------------------------------------------------
Esta información está destinada únicamente a profesionales del sector sanitario:
Havrix 1440 Adulto es una suspensión líquida turbia. Durante el almacenamiento, el contenido puede presentar un depósito blanco fino y un sobrenadante transparente e incoloro.
Antes de la administración, se debe inspeccionar la vacuna visualmente para detectar cualquier partícula extraña y/o variación del aspecto físico. Antes de usar Havrix 1440 Adulto, se debe agitar bien la jeringa precargada para obtener una suspensión blanca ligeramente opaca. Desechar la vacuna si el contenido muestra otro aspecto.
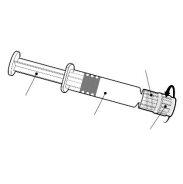
Instrucciones para la jeringa precargada
| Sostenga la jeringa por el cuerpo, no por el émbolo. Desenrosque el tapón de la jeringa girándola en sentido contrario a las agujas del reloj. |
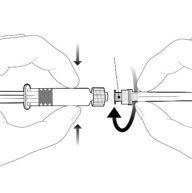
| Para insertar la aguja, conecte la base al adaptador luer-locky gírelo un cuarto de vuelta en el sentido de las agujas del reloj hasta que sienta que se bloquea. No saque el émbolo de la jeringa del cuerpo. Si esto ocurre, no administre la vacuna. |
Eliminación de residuos
La eliminación del medicamento no utilizado y de todos los materiales que hayan estado en contacto con él se realizará de acuerdo con la normativa local.
- País de registro
- Precio medio en farmacia45.27 EUR
- Principio activo
- Requiere recetaSí
- Fabricante
- Esta información es de carácter general y no sustituye la consulta con un profesional sanitario.
- Alternativas a HAVRIX 1440 ADULTO, SUSPENSION INYECTABLE EN JERINGA PRECARGADAForma farmacéutica: INYECTABLE, 80 U ELISAPrincipio activo: hepatitis A, inactivated, whole virusFabricante: Sanofi Winthrop IndustrieRequiere recetaForma farmacéutica: INYECTABLE, 0,5 mlPrincipio activo: hepatitis A, inactivated, whole virusFabricante: Sanofi Winthrop IndustrieRequiere recetaForma farmacéutica: INYECTABLE, 720 U ELISA antigeno hepatitis A/ 0,5 mlPrincipio activo: hepatitis A, inactivated, whole virusFabricante: Glaxosmithkline S.A.Requiere receta
Médicos online para HAVRIX 1440 ADULTO, SUSPENSION INYECTABLE EN JERINGA PRECARGADA
Comenta la dosis, los posibles efectos secundarios, interacciones, contraindicaciones o la revisión de receta de HAVRIX 1440 ADULTO, SUSPENSION INYECTABLE EN JERINGA PRECARGADA, sujeto a valoración médica y a la normativa local.
Preguntas frecuentes