
Віллфацт 1000 й.м.
Запитайте лікаря про рецепт на Віллфацт 1000 й.м.

Інструкція із застосування Віллфацт 1000 й.м.
УПАКОВКА ДО ДОДАТКУ: ІНФОРМАЦІЯ ДЛЯ КОРИСТУВАЧА
Willfact 500 од.х.
Порошок і розчинник для приготування розчину для ін'єкцій
Willfact 1000 од.х. порошок і розчинник для приготування розчину для ін'єкцій
Willfact 2000 од.х. порошок і розчинник для приготування розчину для ін'єкцій
Людський фон Віллебранда
Перш ніж використовувати препарат, уважно ознайомтеся з вмістом цієї інструкції, оскільки вона містить важливу інформацію для пацієнта.
- Збережіть цю інструкцію, щоб у разі необхідності знову її прочитати.
- Якщо у вас виникли будь-які сумніви, зверніться до лікаря, фармацевта або медсестри.
- Цей препарат призначений для конкретної особи. Не передавайте його іншим. Препарат може нашкодити іншій особі, навіть якщо симптоми її хвороби такі самі.
- Якщо в пацієнта виникли будь-які побічні ефекти, включаючи будь-які побічні ефекти, не перелічені в цій інструкції, повідомте про це лікаря, фармацевта або медсестру. Див. пункт 4.
Зміст інструкції
- 1. Що таке препарат Willfact і для чого він використовується
- 2. Інформація, яку потрібно знати до використання препарату Willfact
- 3. Як використовувати препарат Willfact
- 4. Можливі побічні ефекти
- 5. Як зберігати препарат Willfact
- 6. Зміст упаковки і інші відомості
1. Що таке препарат Willfact і для чого він використовується
Препарат Willfact виготовляється з людської плазми (рідкої частини крові) і містить активну речовину під назвою людський фон Віллебранда (vWF).
Фон Віллебранда бере участь у згортанні крові. Недостатність цього фактору, як це відбувається, наприклад, при хворобі Віллебранда, призводить до того, що кров не згортається так швидко, як повинно, а тому виникає підвищена схильність до кровотеч.
Заміна vWF препаратом Willfact тимчасово відновлює механізми згортання крові.
Препарат Willfact показаний для профілактики кровотеч, пов'язаних з хірургічними операціями, та інших кровотеч у пацієнтів з діагнозом хвороби Віллебранда, якщо лікування тільки десмопресином (DDAVP) неефективне або протипоказане.
Препарат Willfact можна використовувати у всіх вікових групах.
Препарат Willfact не слід використовувати для лікування гемофілії типу А.
2. Інформація, яку потрібно знати до використання препарату Willfact
Коли не використовувати препарат Willfact
- Якщо пацієнт має алергію на людський фон Віллебранда або будь-який інший компонент цього препарату (перелічені в пункті 6).
- Якщо в пацієнта діагностовано гемофілію типу А.
Попередження та обережність
Лікування препаратом Willfact повинно завжди контролюватися лікаремз досвідом лікування порушень згортання крові.
Якщо в пацієнта виникають сильні кровотечі, а аналіз крові підтверджує зменшення кількості фактору VIII, пацієнт отримує препарат фактору згортання VIII та додатково препарат vWF протягом перших 12 годин.
Алергічні реакції
Можуть виникнути реакції гіперчутливості з алергічним характером,подібні до тих, які виникають після введення інших білкових внутрішньовенних препаратів, отриманих з людської крові або плазми.
Пацієнта буде моніторити під час ін'єкції для виявлення ранніх ознак гіперчутливості.
До них належать висип, свербіж, відчуття стискання в грудній клітці, свистячий дихання, зниження артеріального тиску (гіпотонія) та важкі алергічні реакції (анafilаксія).
Лікар проінформує пацієнта про попереджувальні ознаки алергічної реакції.
У разі виникнення об'єктивних або суб'єктивних ознак гіперчутливості лікування слід припинити та негайно звернутися за медичною допомогою.
Вірусна безпека
Під час виробництва препаратів з людської крові або плазми застосовуються певні заходи для запобігання передачі інфекцій пацієнтам. До них належать:
- докладний відбір донорів крові та плазми, який дозволяє виключити осіб, що належать до групи ризику інфекцій,
- аналіз кожної партії та пула плазми на наявність вірусу/інфекції,
- введення в процес обробки крові або плазми кроків, які дозволяють інактивувати або видалити віруси.
Незважаючи на застосування цих заходів під час введення препаратів, виготовлених з людської крові або плазми, не можна повністю виключити можливість передачі інфекції. Це стосується також невідомих або нових вірусів чи інфекцій іншого типу.
Захід, який приймається, вважається ефективним у випадку вірусів з оболонкою, таких як людський вірус імунодефіциту (ВІЛ, який спричиняє СНІД), вірус гепатиту типу Б і вірус гепатиту типу С.
Захід, який приймається, має обмежену цінність у випадку вірусів без оболонки, таких як вірус гепатиту типу А і парвовірус В19. Інфекція парвовірусом В19 може бути серйозною у вагітних жінок (оскільки існує ризик інфекції ненародженої дитини) та пацієнтів з ослабленою імунною системою або певним типом анемії (наприклад, серпоподібноклітинною анемією або гемолітичною анемією).
Вакцинація
Лікар може порекомендувати пацієнту прийняти вакцини проти вірусного гепатиту типу А та типу Б, якщо пацієнт регулярно/повторно приймає виготовлений з плазми людський фон Віллебранда.
Реєстрація номера серії
Надійно рекомендується, щоб під час введення кожної дози препарату Willfact реєструвати ім'я та прізвище пацієнта, а також номер серії препарату, щоб задокументувати, які серії препарату були введені.
Ризик тромбозу
Може виникнути блокування судин крові тромбами (тромбоз). Ризик особливо високий, якщо в анамнезі або лабораторних дослідженнях виявлені певні фактори ризику. У такому випадку стан пацієнта буде дуже докладно спостерігатися щодо ранніх ознак тромбозу. Також слід призначити препарати, які запобігають блокуванню судин крові тромбами (профілактика).
Лікар, який призначає фактор згортання VIII, який містить фактор Віллебранда, повинен пам'ятати, що продовження лікування може призвести до надмірного збільшення активності фактору VIII. Якщо пацієнт отримує препарат vWF, який містить фактор згортання VIII, лікар повинен регулярно моніторити активність фактору VIII в плазмі. Це захистить пацієнта від надмірної активності фактору VIII в плазмі, яка може збільшити ризик виникнення тромботичних подій.
Обмеження ефективності
У пацієнтів з хворобою Віллебранда (особливо типу 3) можуть утворюватися білки, які нейтралізують дію фактору Віллебранда. Такі білки називаються нейтралізуючими антитілами або інгібіторами. Лікар перевірить, чи утворюються інгібітори vWF в організмі пацієнта, якщо результати лабораторних досліджень показують відсутність належного відновлення концентрацій vWF або якщо кровотечі не зменшуються尽管 використання відповідної дози препарату Willfact. Якщо існує високий рівень інгібіторів, то лікування vWF може бути неефективним. У таких випадках слід розглянути інші методи лікування. Нову терапію проведе лікар з досвідом лікування порушень згортання крові.
Препарат Willfact та інші препарати
Повідомте лікаря або фармацевта про всі препарати, які пацієнт зараз приймає або приймав раніше, а також про препарати, які пацієнт планує приймати.
Вагітність і годування грудьми
Препарат Willfact можна використовувати у вагітних жінок або жінок, які годують грудьми, тільки якщо це явно показано.
Не проводилися контрольовані клінічні дослідження щодо оцінки безпеки використання препарату Willfact у вагітних жінок та жінок, які годують грудьми, а дослідження на тваринах недостатні для підтвердження безпеки використання в контексті фертильності, вагітності та розвитку дитини під час вагітності та після пологів.
Якщо пацієнтка вагітна або годує грудьми, підозрює, що може бути вагітною або планує мати дитину, вона повинна проконсультуватися з лікарем або фармацевтом перед прийняттям цього препарату.
Керування транспортними засобами та обслуговування машин
Не спостерігалося впливу на здатність керувати транспортними засобами або обслуговувати машини.
Препарат Willfact містить натрій
Одна флакон з 5 мл (500 од.х.) препарату Willfact містить 0,15 ммоль (3,4 мг) натрію.
Це відповідає 0,17% рекомендованої максимальної добової норми споживання натрію для дорослої людини.
Одна флакон з 10 мл (1000 од.х.) препарату Willfact містить 0,3 ммоль (6,9 мг) натрію.
Це відповідає 0,35% рекомендованої максимальної добової норми споживання натрію для дорослої людини.
Одна флакон з 20 мл (2000 од.х.) препарату Willfact містить 0,6 ммоль (13,8 мг) натрію.
Це відповідає 0,69% рекомендованої максимальної добової норми споживання натрію для дорослої людини.
3. Як використовувати препарат Willfact
Лікування повинно розпочинати та контролювати лікар з досвідом лікування порушень кровотечі.
Якщо лікар вважає, що пацієнт може вводити препарат вдома, він належним чином проінформує пацієнта.
Дозування
Цей препарат завжди повинен прийматися згідно з рекомендаціями лікаря. У разі сумнівів зверніться до лікаря.
Найкраще, якщо препарат Willfact вводить лікар або медсестра. Якщо jedoch пацієнт отримав препарат Willfact для використання вдома, лікар упевниться, що пацієнт проінформований про спосіб виконання ін'єкції та правильну дозу препарату. Слід дотримуватися рекомендацій лікаря та попросити про допомогу у разі проблем з використанням шприца. Шприц може використовувати лише підготовлена до цього особа.
Лікар розрахує правильну дозу препарату Willfact (виражену в міжнародних одиницях — од.х.).
Доза залежить від:
- маси тіла,
- місця кровотечі,
- інтенсивності кровотечі,
- клінічного стану пацієнта,
- необхідності проведення операції,
- активності vWF у крові після проведення операції,
- інтенсивності хвороби.
Доза знаходиться в межах 40–80 од.х./кг маси тіла.
Лікар порекомендує проведення під час лікування аналізів крові щодо:
- концентрації фактору VIII (FVIII:C),
- концентрації фактору Віллебранда (vWF:RCo),
- належності інгібіторів,
- початкових ознак утворення тромбів - у пацієнтів групи ризику виникнення таких ускладнень.
На підставі результатів цих аналізів лікар може коригувати частоту виконання ін'єкцій та введену дозу.
У певних випадках може бути необхідним використання препарату фактору VIII (іншого білка з коагуляційною дією) в додаток до препарату Willfact, щоб забезпечити швидше лікування або профілактику кровотечі (у нагальних ситуаціях або у випадку гострого кровотечі).
Препарат Willfact також можна використовувати для тривалої профілактики, в цьому випадку дозу також встановлює лікар індивідуально. Введення препарату Willfact у дозі 40–60 од.х./кг маси тіла двічі чи тричі на тиждень зменшує кількість епізодів кровотечі.
Якщо пацієнт вважає, що препарат Willfact діє занадто сильно або занадто слабко, слід звернутися до лікаря.
Використання у дітей та підлітків
Дозування у дітей та підлітків базується на масі тіла. У деяких випадках, особливо у молодших пацієнтів (до 6 років), може бути необхідним використання вищих доз (до 100 од.х./кг маси тіла).
Спосіб введення
Детальні інструкції щодо реконструкції та введення препарату наведені в кінці інструкції.
Використання більшої ніж рекомендована дози препарату Willfact
Не повідомлялося про симптоми передозування препарату Willfact, однак у разі введення великої кількості не можна виключити ризик тромбозу.
Пропуск введення препарату Willfact
У разі пропуску введення препарату Willfact слід звернутися до лікаря.
Не слід вводити подвійну дозу для компенсації пропущеної дози.
У разі будь-яких подальших сумнівів щодо використання цього препарату слід звернутися до лікаря, фармацевта або медсестри.
4. Можливі побічні ефекти
Як і будь-який препарат, цей препарат може викликати побічні ефекти, хоча не у всіх вони виникнуть.
Негайно зверніться до лікаря у наступних випадках:
- Виникнення ознак гіперчутливості або алергічних реакцій (спостерігаються не дуже часто, можуть стосуватися до 1 з 100 пацієнтів). У деяких випадках такі реакції можуть перетворитися на важку алергічну реакцію (анafilаксію), у тому числі анафілактичний шок (спостерігається з невідомою частотою).
Попереджувальні ознаки алергічної реакції:
- затруднення дихання та ковтання,
- свистячий дихання,
- стиск у грудній клітці,
- пришвидшення серцебиття,
- зниження артеріального тиску,
- омдленіння,
- крайнє втомлення,
- нервозність,
- головний біль,
- дрожи, відчуття холоду,
- спалахи жару,
- опухання різних частин тіла,
- висипка на шкірі, уртикарний висип,
- відчуття печіння та колючості в місці введення,
- поколювання,
- вомітування,
- нудота.
Якщо виникла одна з цих ознак, слід негайно припинити лікування та повідомити лікаря,щоб розпочати відповідне лікування, залежно від типу та ступеня алергічної реакції.
- Виявлення зникнення належної дії препарату (відсутність контролю кровотечі). Це може бути пов'язано з гальмуванням фактору Віллебранда (спостерігається з невідомою частотою).
У пацієнтів з хворобою Віллебранда, особливо типу 3, можливе утворення білків, які нейтралізують дію vWF. Такі білки називаються нейтралізуючими антитілами або інгібіторами.
Пацієнтів, які лікуються vWF, слід докладно моніторити лікарем щодо виникнення інгібіторів шляхом відповідної клінічної спостереження та проведення лабораторних досліджень. У разі виникнення інгібіторів такий стан може проявлятися у вигляді недостатньої клінічної відповіді. Він також може супроводжуватися важкими алергічними реакціями.
- Виявлення ознак порушень кровообігу в кінцівках (наприклад, холодні та бліді кінцівки) або важливих органах (наприклад, сильний біль у грудній клітці). Це може бути пов'язано з утворенням тромбів у судинах крові (спостерігається з невідомою частотою).
Існує ризик утворення тромбів (тромбозу), особливо у пацієнтів групи ризику. Після корекції дефіциту фактору Віллебранда пацієнтів слід моніторити щодо ранніх ознак тромбозу або дисемінованого внутрішньосудинного згортання та застосувати лікування, яке запобігає тромбозу, у ситуаціях, коли ризик його виникнення підвищений (після операцій, у пацієнтів, які лежать, у разі дефіциту інгібітора коагуляції або ферменту фібринолітичного).
Якщо пацієнт приймає препарати vWF, які містять FVIII, ризик тромбозу може бути вищим через тривало підвищені концентрації FVIII в плазмі.
Наступні побічні ефекти спостерігаються часто(могут стосуватися до 1 з 10 пацієнтів):
- реакції в місці введення ін'єкції.
Наступні побічні ефекти спостерігаються не дуже часто(могут стосуватися до 1 з 100 пацієнтів):
- головокружіння,
- парестезія, оніміння,
- спалахи жару,
- свербіння,
- відчуття стискання в грудній клітці,
- дрожи, відчуття холоду.
Наступні побічні ефекти спостерігаються з невідомою частотою:
- гарячка.
Зголошення побічних ефектів
Якщо виникли будь-які побічні ефекти, включаючи будь-які побічні ефекти, не перелічені в цій інструкції, повідомте про це лікаря або фармацевта, або медсестру. Побічні ефекти можна zgолошувати безпосередньо до Департаменту моніторингу небажаних дій лікарських засобів Управління реєстрації лікарських засобів, медичних виробів та біоцидів:
Аль. Єрусалимські 181С
02-222 Варшава
Тел.: + 48 22 49 21 301
Факс: + 48 22 49 21 309
Сайт: https://smz.ezdrowie.gov.pl
Побічні ефекти також можна zgолошувати подові відповідального суб'єкта.
Зголошуючи побічні ефекти, можна буде зібрати більше інформації про безпеку використання препарату.
5. Як зберігати препарат Willfact
Препарат слід зберігати в місці, недоступному для дітей.
Не використовувати цей препарат після закінчення терміну придатності, вказаного на етикетці флакона та пачки.
Не зберігати при температурі вище 25°C. Зберігати в оригінальній упаковці для захисту від світла.
Не заморожувати.
Для збереження стерильності продукт слід використовувати безпосередньо після реконструкції. Однак було доведено хімічну та фізичну стабільність продукту після зберігання протягом 24 годин при 25°C.
Не використовувати цей препарат, якщо ви помітили замутнення або твердих частинок у розчині.
Лікарських засобів не слід викидати в каналізацію чи домашні контейнери для відходів. Слід запитати фармацевта, як видалити лікарські засоби, які вже не використовуються. Таке поводження допоможе захистити навколишнє середовище.
6. Зміст упаковки та інші відомості
Що містить препарат Willfact
Активна речовина— людський фон Віллебранда (500 од.х., 1000 од.х., 2000 од.х.) виражена в міжнародних одиницях активності кофактора ристоцетину (vWF:RCo).
Після реконструкції з 5 мл (500 од.х.), 10 мл (1000 од.х.) або 20 мл (2000 од.х.) води для ін'єкцій одна флакон містить приблизно 100 од.х./мл людського фон Віллебранда.
До додавання альбуміну специфічна активність розчину становить не менше 60 од.х. vWF:RCo на 1 мг загального білка.
Інші компоненти:
Порошок: людська альбуміна, аргінін хлорид, гліцин, натрій цитрат і кальцій хлорид дигідрат.
Розчинник: вода для ін'єкцій.
Як виглядає препарат Willfact та що містить упаковка
Препарат Willfact поставляється у вигляді білого або блідо-жовтого порошку або крихкого твердого тіла та прозорого, безбарвного розчинника для приготування розчину для ін'єкцій після реконструкції за допомогою системи для перекачування.
Доступні розміри упаковки препарату Willfact: 500 од.х./5 мл, 1000 од.х./10 мл, 2000 од.х./20 мл.
Розчин після реконструкції повинен бути прозорим або легенько опалесцентним, безбарвним або легенько жовтим.
Відповідальний суб'єкт та виробник
LFB-BIOMEDICAMENTS
3, авеню де Тропіки,
ZA де Куртабеф,
91940 ЛЕ Уліс,
Франція
[email protected]
Виробники
LFB-BIOMEDICAMENTS
3, авеню де Тропіки,
ZA де Куртабеф,
91940 ЛЕ Уліс,
Франція
LFB-BIOMEDICAMENTS
59 Рю де Тревіз
59000 Лілль
Франція
Цей препарат дозволений до обігу в країнах-членах Європейського економічного простору та у Сполученому Королівстві (Північній Ірландії) під наступними назвами:
Австрія
Willfact
Чехія
WILLFACT
Данія
Willfact
Іспанія
Willfact
Німеччина
WILLFACT
Норвегія
Willfact
Польща
Willfact
Словаччина
Willfact
Швеція
Willfact
Угорщина
Willfact
Сполучене Королівство (Північна Ірландія)
Willfact
Дата останньої актуалізації інструкції:
- 01.2024 ________________________________________________________________________________________
ІНСТРУКЦІЯ ВИКОРИСТАННЯ:
Дозування
Загалом введення 1 од.х./кг маси тіла фактору Віллебранда призводить до збільшення активності циркулюючого vWF:RCo на приблизно 0,02 од.х./мл (2%).
Слід стремитися до досягнення концентрації vWF:RCo на рівні >0,6 од.х./мл (60%) та FVIII:C на рівні >0,4 од.х./мл (40%).
Досягнення гемостазу є невизначеним до моменту досягнення коагуляційної активності фактору VIII (FVIII:C) на рівні 0,4 од.х./мл (40%). Введення самого фактору Віллебранда не призводить до максимального збільшення активності FVIII:C протягом принаймні 6–12 годин. Це не достатньо для негайної нормалізації активності FVIII:C. Тому якщо початкова активність FVIII:C у пацієнта нижче критичної значення, а необхідне швидке виправлення гемостазу — наприклад, у рамках лікування кровотечі, важкого травматизму або під час проведення нагальної операції — з першим введенням фактору Віллебранда слід введені фактор VIII, щоб можна було досягти активності FVIII:C в плазмі, яка забезпечує гемостаз.
Якщо jedoch негайне збільшення активності FVIII:C не є необхідним — наприклад, у разі планової операції — або якщо початкова активність FVIII:C дозволяє підтримувати гемостаз, лікар може вирішити питання про пропуск введення FVIII разом з першим введенням фактору Віллебранда.
- Початок лікування: Перша доза препарату Willfact становить 40-80 од.х./кг маси тіла у разі лікування кровотечі або травматизму. Вона вводиться в поєднанні з необхідною кількістю продукту, який містить фактор VIII, розрахованого на підставі початкової активності FVIII:C в плазмі пацієнта, щоб досягти належної активності FVIII:C в плазмі, безпосередньо перед операцією або якомога швидше після початку епізоду кровотечі або виникнення важкого травматизму. У разі планової операції перше введення слід здійснити за годину до операції. Введення початкової дози 80 од.х./кг маси тіла препарату Willfact може бути необхідним особливо у пацієнтів з хворобою Віллебранда типу 3, у разі якої підтримання належної активності може вимагати доз вищих, ніж у разі інших типів vWD.
У разі планової операції перше введення препарату Willfact повинно бути здійснено за 12–24 години до операції, а друге введення — безпосередньо перед операцією. У таких випадках одночасне введення препарату фактору VIII не є необхідним, оскільки перед операцією концентрація ендогенної FVIII:C зазвичай досягає критичної значення 0,4 од.х./мл (40%). Однак це слід підтвердити у кожного пацієнта.
- Наступні введення: У разі необхідності лікування слід продовжувати препаратом Willfact в монотерапії в дозі 40-80 од.х./кг маси тіла на добу в 1 або 2 введеннях на добу протягом одного чи кількох днів. Доза та частота введень повинні бути завжди кориговані залежно від типу операції, клінічного стану та біологічного (vWF:RCo та FVIII:C) пацієнта, а також типу та інтенсивності епізоду кровотечі.
- Профілактика: Препарат Willfact може бути введений для тривалої профілактики в дозі, коригованій індивідуально для кожного пацієнта. Препарат Willfact у дозі 40-60 од.х./кг маси тіла, введений 2-3 рази на тиждень, зменшує кількість епізодів кровотечі.
- Лікування амбулаторно: За згоди лікаря, особливо у разі незначного або помірного кровотечі або тривалої профілактики кровотеч, можна розпочати лікування вдома.
Діти та підлітки
Розмір дози у разі кожного показання базується на масі тіла. Дозу та тривалість лікування слід коригувати залежно від клінічного стану пацієнта та концентрації vWF:RCo та FVIII:C в плазмі.
- Початок лікування
- У дітей віком до 6 років початкова доза може бути встановлена на підставі збільшення відновлення (IR) у пацієнта або, у разі відсутності даних IR, може бути необхідна початкова доза, рівна 60-100 од.х./кг маси тіла, щоб збільшити концентрацію vWF:RCo у пацієнта до 100 од.х./дл.
- У дітей віком понад 6 років та підлітків дозування є таким самим, як у дорослих пацієнтів.
- Наступні введення У дітей та підлітків наступні дози слід встановлювати індивідуально залежно від клінічного стану та концентрації vWF:RCo та коригувати залежно від клінічної відповіді.
Операція в плановому порядку
- У дітей віком до 6 років після першої дози, введеної за 12-24 години до операції, повторну дозу можна ввести за 30 хвилин до операції.
- У дітей віком понад 6 років та підлітків дозування є таким самим, як у дорослих пацієнтів.
- Профілактика У дітей та підлітків дозу та частоту повторного введення слід встановлювати індивідуально залежно від збільшення відновлення та концентрації vWF:RCo у пацієнта та коригувати залежно від клінічної відповіді.
Спосіб та шлях введення
Внутрішньовенне введення
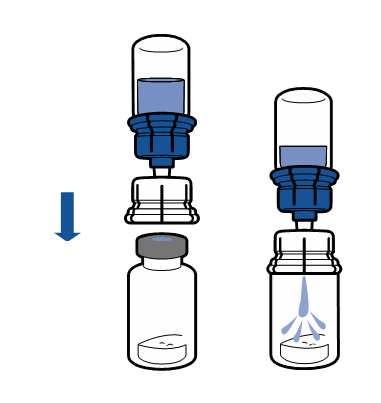
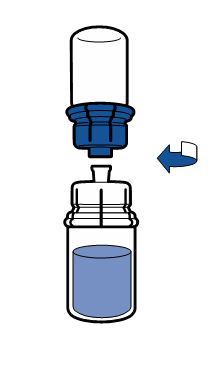
Реконструкція
Слід дотримуватися актуальних рекомендацій щодо асептичної техніки роботи. Систему для перекачування слід використовувати лише для реконструкції препарату, згідно з описом нижче. Система не призначена для введення препарату пацієнту.
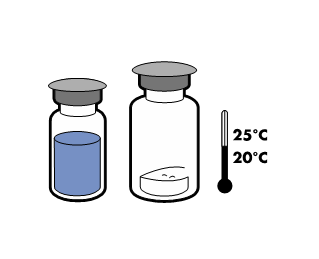 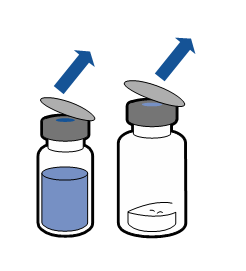 |
|
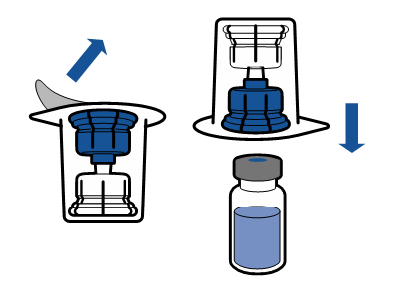 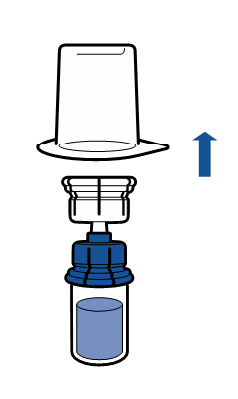   |
|
Порошок повинен розчинитися за час коротший за 5 хвилин, зазвичай розчиняється негайно.
Отриманий розчин повинен бути прозорим або легенько опалесцентним, безбарвним або легенько жовтим. Перед введенням зреконструйований продукт слід контролювати візуально щодо наявності твердих частинок та забарвлення.
Не використовувати розчин, який є мутним або містить осад.
Не змішувати з іншими препаратами.
Не розбавляти продукт після реконструкції.
Введення
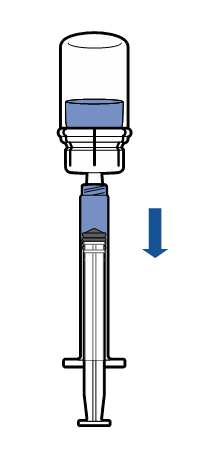 |
|
Зберігання після реконструкції
Для збереження стерильності продукт слід використовувати безпосередньо після реконструкції. Однак було доведено хімічну та фізичну стабільність продукту після зберігання протягом 24 годин при 25°C.
Всі невикористані залишки продукту або його відходи слід видалити згідно з місцевими правилами.
- Країна реєстрації
- Діючі речовини
- Потрібен рецептНі
- Виробник
- ІмпортерLFB-Biomedicamensts LFB-Biomedicaments
- Інформація є довідковою і не є медичною порадою. Перед прийомом будь-яких препаратів обов'язково проконсультуйтеся з лікарем. Oladoctor не несе відповідальності за медичні рішення, прийняті на основі цього контенту.
- Альтернативи до Віллфацт 1000 й.м.Форма випуску: Порошок, 2000 МО/20 млДіючі речовини: von Willebrand factorВиробник: LFB-Biomedicamensts LFB-BiomedicamentsНе потрібен рецептФорма випуску: Порошок, 500 МО/5 млДіючі речовини: von Willebrand factorВиробник: LFB-Biomedicamensts LFB-BiomedicamentsНе потрібен рецептФорма випуску: Порошок, 1000 МОДіючі речовини: coagulation factor VIIIВиробник: CSL Behring GmbHПотрібен рецепт
Аналоги Віллфацт 1000 й.м. в інших країнах
Найкращі аналоги з тією самою діючою речовиною та терапевтичним ефектом.
Аналог Віллфацт 1000 й.м. у Hiszpania
Лікарі онлайн щодо Віллфацт 1000 й.м.
Консультація щодо дозування, побічних ефектів, взаємодій, протипоказань та поновлення рецепта на Віллфацт 1000 й.м. – за рішенням лікаря та згідно з місцевими правилами.














