
Гадовіст 1,0

Запитайте лікаря про рецепт на Гадовіст 1,0

Інструкція із застосування Гадовіст 1,0
УЛЯНКА ДЛЯ ПАЦІЄНТА: ІНФОРМАЦІЯ ДЛЯ КОРИСТУВАЧА
Gadovist 1,0, 1,0 ммоль/мл, розчин для ін'єкцій
Гадобутрол
Перш ніж використовувати препарат, уважно ознайомтеся з вмістом цієї уллянки, оскільки вона містить важливу інформацію для пацієнта.
- Збережіть цю уллянку, щоб у разі потреби ви могли її знову прочитати.
- Якщо у вас виникнуть будь-які сумніви, зверніться до лікаря (радіолога) або персоналу відділення магнітно-резонансної томографії.
- Якщо в пацієнта виникнуть будь-які побічні ефекти, включаючи будь-які побічні ефекти, не перераховані в цій уллянці, повідомте про це лікарю або персоналу відділення магнітно-резонансної томографії. Див. пункт 4.
Зміст уллянки:
- 1. Що таке препарат Gadovist 1,0 і для чого він використовується
- 2. Інформація, яка повинна бути відомою перед застосуванням препарату Gadovist 1,0
- 3. Як застосовувати препарат Gadovist 1,0
- 4. Можливі побічні ефекти
- 5. Як зберігати препарат Gadovist 1,0
- 6. Зміст упаковки і інші відомості
1. Що таке препарат Gadovist 1,0 і для чого він використовується
Препарат призначений виключно для діагностики.
Препарат Gadovist 1,0 є продуктом (контрастним засобом) для використання під час магнітно-резонансної томографії, призначеним для дослідження різних частин тіла, таких як: мозок,
хребет, голова, шия, грудна клітка, груди, живіт (у тому числі підшлункова залоза, печінка і селезінка),
таз (у тому числі простата, сечовий міхур, матка), простір, що називається позаочеревинним
у задній частині черевної порожнини (у тому числі нирки), кінцівки (верхні і нижні) і м'язово-
скелетна система (м'язи, кістки і суглоби), кровоносні судини і серце. Можна оцінювати кровопостачання міокарда під час навантаження (спровокованого, наприклад, ліками). Можна діагностувати
живучість міокарда (наприклад, можна виявити наявність рубцевої тканини).
Дослідження МРТ є видом діагностичної візуалізації в медицині, який використовує
інше поведінку молекул води в здорових і хворобливих тканинах. Дослідження
проводиться за допомогою складних магнітних систем і радіохвиль. Активність реєструється комп'ютерами, які перетворюють її на зображення.
Препарат Gadovist 1,0 застосовується у дорослих осіб, а також у дітей і підлітків будь-якого віку (у тому числі у новонароджених немовлят).
Препарат Gadovist 1,0 вводиться у вигляді внутрішньовенної ін'єкції. Препарат повинен бути введений кваліфікованим медичним персоналом з досвідом виконання досліджень методом магнітно-резонансної томографії (МРТ).
2. Інформація, яка повинна бути відомою перед застосуванням препарату Gadovist 1,0
Коли не застосовувати препарат Gadovist 1,0
якщо пацієнт має алергію на активну речовину або будь-який з інших компонентів цього препарату
(перелічених у пункті 6). Не існує інших абсолютних протипоказань до застосування препарату Gadovist 1,0.
Попередження і обережність
Перш ніж почати застосування препарату Gadovist 1,0, пацієнт повинен звернутися до лікаря, якщо у нього:
- виявлена алергія (гіперчутливість) до гадобутролю або будь-якого з інших компонентів препарату Gadovist 1,0 (див. «Що містить препарат Gadovist 1,0»),
- існує алергія (наприклад, сінна лихоманка, кропив'янка) або бронхіальна астма,
- були реакції на контрастний засіб,
- існують захворювання мозку з судомами або інші захворювання нервової системи. Лікар вирішить, чи можливо виконання призначеного дослідження. Після застосування препарату Gadovist 1,0 можуть виникнути реакції типу алергії або інші види реакцій, які призводять до порушення роботи серця, труднощів з диханням або шкірних реакцій. Можливі реакції важкого ступеня. Більшість реакцій виникає протягом півгодини після введення. Тому рекомендується спостереження за пацієнтом. Реєструвалися випадки запізнілих реакцій (після багатьох годин або днів) (див. пункт 4 «Можливі побічні ефекти»).
- Пацієнт повинен повідомити лікаря, якщо у нього є імплантований кардіостимулятор або будь-які імплантати, що містять залізо. Порушення функції нирок і (або) печінки Пацієнт повинен повідомити лікаря, якщо:
- нирки пацієнта не функціонують正常но,
- пацієнт недавно переніс або найближчим часом має перенести трансплантацію печінки.
Новонароджені та немовлята
Через недорозвинену функцію нирок у новонароджених (дітей до 4 тижнів життя) та у немовлят
(дітей до 1 року життя), препарат Gadovist 1,0 повинен застосовуватися у цих пацієнтів лише після ретельного розгляду лікарем.
Лікар може вирішити питання про виконання аналізу крові для перевірки функції нирок
до прийняття рішення про застосування препарату Gadovist 1,0, особливо у осіб віком понад 65 років.
Якщо нирки не функціонують正常но, лікар забезпечить, щоб препарат Gadovist 1,0 був виведений з організму, перш ніж пацієнт отримає наступну ін'єкцію препарату Gadovist 1,0.
Препарат Gadovist 1,0 може бути виведений з організму за допомогою діалізу. Якщо нирки не функціонують正常но, лікар може вирішити питання про застосування діалізу після отримання препарату Gadovist 1,0.
Існують повідомлення про важку реакцію, головним чином пов'язану з загусанням шкіри і сполучної тканини
(неркопохідне фіброзне захворювання, англ. nephrogenic systemic fibrosis– NSF). NSF може
призвляти значне порушення рухливості суглобів, слабкість м'язів або може впливати на
правильну функцію внутрішніх органів, що може становити загрозу для життя. NSF пов'язане з застосуванням деяких продуктів, що містять гадолін (у тому числі Gadovist 1,0) у пацієнтів з важкими порушеннями функції нирок. Також воно пов'язане з застосуванням деяких продуктів, що містять гадолін (у тому числі Gadovist 1,0) у пацієнтів з гострою нирковою недостатністю, через печінково-ниркову недостатність (ниркова недостатність у пацієнтів з прогресуючою хронічною хворобою печінки) або у пацієнтів з гострою нирковою недостатністю, які недавно перенесли або найближчим часом мають перенести трансплантацію печінки (див. пункт «Можливі побічні ефекти»).
Препарат Gadovist 1,0 та інші препарати
Пацієнт повинен повідомити лікаря про всі препарати, які він зараз приймає, а також про препарати, які він планує приймати.
Вагітність і годування грудьми
Перш ніж застосовувати будь-який препарат, пацієнт повинен проконсультуватися з лікарем.
Вагітність
Гадобутрол може проникати через плаценту. Не відомо, чи це впливає на дитину. Жінки, які вважають, що вони вагітні або можуть бути вагітними, повинні повідомити про це лікарю, оскільки препарат Gadovist 1,0 не повинен застосовуватися під час вагітності, якщо це не абсолютно необхідно.
Годування грудьми
Жінки, які годують грудьми або планують почати годування грудьми, повинні повідомити про це лікарю. Лікар обговорить з пацієнткою, чи повинна вона продовжувати годування грудьми, чи повинна перервати годування грудьми на період 24 годин після застосування препарату Gadovist 1,0.
Препарат Gadovist 1,0 містить натрій
Цей препарат містить менше 1 ммоль натрію (23 мг) у одній дозі (обчисленій на основі середньої
кількості, введеної особі з масою тіла 70 кг), тобто вважається «безнатрієвим».
3. Як застосовувати препарат Gadovist 1,0
Препарат Gadovist 1,0 вводиться через тонку голку у вену медичним персоналом. Препарат Gadovist
1,0 буде введений безпосередньо перед дослідженням методом магнітно-резонансної томографії.
Після ін'єкції пацієнт буде спостерігатися протягом щонайменше 30 хвилин.
Фактична доза препарату Gadovist 1,0, яка підходить для пацієнта, буде залежати від маси тіла
і досліджуваної області тіла.
У дорослих осіб рекомендується одноразова ін'єкція дози 0,1 мілілітра препарату Gadovist 1,0 на кілограм маси тіла (що означає, що особа з масою тіла 70 кг отримає дозу 7 мілілітрів). У
дослідженнях зображення центральної нервової системи (ЦНС) та CE-MRA (англ. contrast
enhancement in magnetic resonance angiography- посилення контрасту в ангіографії з використанням магнітно-резонансної томографії) разом можна вводити максимально 0,3 мілілітра препарату Gadovist 1,0 на кілограм маси тіла (що означає, що особа з масою тіла 70 кг отримає дозу 21 мілілітр). У
дослідженнях зображення ЦНС мінімальна доза, яку можна вводити, становить 0,075 мілілітра препарату Gadovist 1,0 на кілограм маси тіла (що означає, що особа з масою тіла 70 кг отримає дозу 5,25 мілілітра).
Для зображення методом магнітно-резонансної томографії мозку, хребта, печінки та нирок
зазвичай достатньо одноразової ін'єкції 0,1 мілілітра препарату Gadovist 1,0 на кілограм маси тіла.
Для зображення методом магнітно-резонансної томографії судин, залежно від типу дослідження,
рекомендується одноразова ін'єкція від 7,5 до 15 мілілітрів (у пацієнтів з масою тіла менше 75 кілограмів) або 10 до 20 мілілітрів (у пацієнтів з масою тіла 75 кілограмів або більше).
Дозування у спеціальних групах пацієнтів
Не рекомендується застосовувати препарат Gadovist 1,0 у пацієнтів з важкими захворюваннями нирок, а також
у пацієнтів, які недавно перенесли або найближчим часом мають перенести трансплантацію печінки.
Якщо застосування препарату є необхідним, пацієнт повинен отримати лише одну дозу препарату Gadovist 1,0 під час дослідження і не повинен отримувати другу ін'єкцію протягом щонайменше 7 днів.
Застосування у дітей та підлітків
У дітей будь-якого віку (у тому числі у новонароджених немовлят) рекомендується одноразова
ін'єкція дози 0,1 мілілітра препарату Gadovist 1,0 на кілограм маси тіла (див. пункт 1: «Що таке препарат Gadovist 1,0 і для чого він використовується»). Через недорозвинену функцію нирок у новонароджених
(дітей до 4 тижнів життя) та у немовлят (дітей до 1 року життя), препарат Gadovist 1,0 повинен застосовуватися у цих пацієнтів лише після ретельного розгляду лікарем. Новонароджені та немовлята
повинні отримати одноразову дозу під час дослідження і не повинні отримувати другу ін'єкцію протягом щонайменше 7 днів.
Особи похилого віку
Не існує необхідності коригування доз у пацієнтів віком понад 65 років, але необхідно виконати
аналіз крові для перевірки функції нирок.
Більше інформації про застосування та підготовку до застосування препарату Gadovist 1,0 знаходиться
в кінцевій частині уллянки.
Застосування більшої ніж рекомендована дози препарату Gadovist 1,0:
До цього часу не повідомлялося про випадки передозування. Якщо це трапиться, лікар буде
лікувати всі виниклі симптоми і контролювати, чи серце і нирки пацієнта функціонують正常но.
У разі будь-яких подальших сумнівів, пов'язаних з застосуванням препарату, слід звернутися до лікаря або персоналу відділення магнітно-резонансної томографії.
4. Можливі побічні ефекти
Як і будь-який препарат, Gadovist 1,0 може спричиняти побічні ефекти, хоча не у всіх вони виникнуть. Більшість цих реакцій виникає протягом півгодини після застосування препарату Gadovist 1,0.
У рідких випадках реєструвалися запізнілі алергічні реакції або інші види побічних ефектів, які виникають протягом кількох годин до кількох днів після застосування препарату Gadovist 1,0. Якщо це трапиться, негайно повідомте про це лікарю або радіологу.
Більшість побічних ефектів має ступінь від легкого до помірного. Найчастішими побічними ефектами у пацієнтів, які отримують препарат Gadovist 1,0 (можуть виникнути у 5 або більше випадках на 1000 пацієнтів), є: головний біль, нудота (чуття нудоти) та головокружіння.
Найважчими побічними ефектами(у деяких випадках загрозливими для життя або смертельними) є: зупинка серця (серце перестає бити), важка хвороба легенів (синдром гострої респіраторної недостатності)/ рідина в легенях (едем легенів)і важкі реакції типу алергії
(псевдоанafilактичні) (у тому числі зупинка дихання і анафілактичний шок.
Крім того, реєструвалися побічні ефекти (у деяких випадках загрозливими для життя або смертельними): задишка (плоске дихання) і втрата свідомості (омдлення).
Рідко можуть виникнути випадки реакцій типу алергії, у тому числі важкі реакції, які можуть вимагати медичної інтервенції.
Пацієнт повинен негайно повідомити персонал відділення магнітно-резонансної томографії,якщо
виникнуть:
- опухання обличчя, губ, язика або горла,
- кашель і чхання,
- труднощі з диханням,
- свербіння,
- кATAR,
- кропив'янка (специфічний тип висипки).
Ці симптоми можуть бути першими ознаками виникнення важкої реакції, що означає, що може
бути необхідним перервати дослідження і застосувати відповідне лікування.
Найчастішими побічними ефектами(можуть виникнути у 5 або більше випадках на 1000 осіб) є: головний біль, нудота, головокружіння.
Більшість побічних ефектів має ступінь від легкого до помірного.
Нижче перераховані можливі побічні ефекти, які були спостережені під час проведення клінічних досліджень, до дозволу препарату до обігу, згідно з частотою їх виникнення.
Часто(можуть виникнути не частіше ніж у 1 з 10 осіб):
- головний біль
- нудота (чуття нудоти) Не дуже часто(можуть виникнути не частіше ніж у 1 з 100 осіб):
- реакції типу алергії (гіперчутливість, псевдоанafilактична реакція), наприклад:
- гіпотонія (низький тиск крові)
- кропив'янка
- опухання обличчя (опухання обличчя)
- опухання повік (опухання повік)
- червоність Частота виникнення наступних реакцій типу алергії невідома:
- анафілактичний шок (важка реакція типу алергії)
- колапс (шок)
- зупинка дихання (зупинка дихання)
- спазм бронхів (труднощі з диханням)
- синюшність (синій колір губ)
- опухання порожнини рота і горла (опухання порожнини рота і горла)
- опухання горла (опухання горла)
- гіпертонія (високий тиск крові)
- біль у грудній клітці
- опухання судин (наприклад, опухання обличчя, горла, губ і [або] язика)
- кон'юнктивіт
- надмірне потіння (збільшене потіння)
- кашель
- чхання
- чуття паління
- блідість (блідість шкіри)
- головокружіння, порушення смаку (порушення відчуття смаку), парестезії ( оніміння і поколювання)
- задишка (плоске дихання)
- вомітування
- червоність шкіри
- свербіння (у тому числі загальне свербіння) (свербіння)
- висипка (у тому числі загальна висипка, плямиста висипка [малі, плоскі червоні плями], гранульована висипка [малі, випуклі, обмежені зміни], червоність зі свербінням [свербляча висипка])
- різні види реакцій в місці ін'єкції (наприклад, витік через оточуючі тканини, чуття паління, чуття холоду, чуття тепла, червоність, свербіння, біль або синяк)
- чуття жару Рідко(можуть виникнути не частіше ніж у 1 з 1000 осіб):
- втрата свідомості (омдлення)
- судоми
- галюцинації (порушення відчуття запаху)
- тахікардія (швидке серцебиття)
- пальпітації (серцебиття)
- сухість у порожнині рота
- зле самопочуття
- чуття холоду
Побічні ефекти, повідомлені після дозволу препарату Gadovist 1,0 до обігу
Частота виникнення невідома(не може бути визначена на основі наявних даних):
- зупинка серця (серце перестає бити)
- важка хвороба легенів (синдром гострої респіраторної недостатності)
- рідина в легенях (едем легенів)
- повідомлялося про випадки неркопохідного фіброзного захворювання (хвороби, пов'язаної з загусанням шкіри, яка також може охоплювати м'які тканини і внутрішні органи), з яких більшість виникла у пацієнтів, які отримували Gadovist 1,0 у поєднанні з іншими препаратами, що містять гадолін. Після застосування препарату Gadovist 1,0 реєструвалися зміни в аналізах крові щодо функції нирок (наприклад, збільшення рівня креатинін у сироватці).
Повідомлення про побічні ефекти
Якщо виникнуть будь-які симптоми, включаючи будь-які симптоми, не перераховані в цій уллянці, повідомте про це лікарю або медсестрі. Побічні ефекти можна повідомляти безпосередньо до Департаменту моніторингу побічних ефектів лікарських засобів Міністерства охорони здоров'я України, вул. Перемоги, 14, м. Київ, 01135, телефон: +38 (044) 206-25-44, факс: +38 (044) 206-25-44, електронна пошта: [[email protected]](mailto:[email protected]).
Побічні ефекти також можна повідомляти відповідальному суб'єкту.
Завдяки повідомленню про побічні ефекти можна буде зібрати більше інформації про безпеку застосування препарату.
5. Як зберігати препарат Gadovist 1,0
Зберігайте в місці, недоступному для дітей.
Зберігайте при температурі до 30°C.
Хімічна, фізична і мікробіологічна стабільність була доведена протягом 24 годин при температурі від 20
до 25°C. З мікробіологічної точки зору препарат повинен бути використаний негайно після відкриття.
Не застосовуйте препарат Gadovist 1,0 після закінчення терміну придатності, вказаного на упаковці після терміну придатності (EXP). Термін придатності означає останній день вказаного місяця.
Номер серії на упаковці вказано після напису Lot.
Ліки не повинні бути викинуті у каналізацію або домашні контейнери для відходів. Зверніться до фармацевта, щоб дізнатися, як видалити ліки, які вже не використовуються. Таке поводження допоможе захистити довкілля.
6. Зміст упаковки і інші відомості
Що містить препарат Gadovist 1,0
- Активною речовиною препарату є гадобутрол. 1 мілілітр розчину для ін'єкцій містить 604,72 мг гадобутролю (еквівалент 1,0 ммоль гадобутролю, який містить 157,25 мг гадоліну ).
- Інші компоненти: калькобутрол натрію, трометамол, соляна кислота 3,6% і вода для ін'єкцій. 1 флакон містить 2 мл розчину, що відповідає 1209,44 мг гадобутролю. 1 флакон містить 7,5 мл розчину, що відповідає 4535 мг гадобутролю. 1 флакон містить 10 мл розчину, що відповідає 6047,20 мг гадобутролю. 1 флакон містить 15 мл розчину, що відповідає 9070 мг гадобутролю. 1 флакон містить 30 мл розчину, що відповідає 18141 мг гадобутролю. 1 шприц містить 5,0 мл розчину, що відповідає 3023 мг гадобутролю. 1 шприц містить 7,5 мл розчину, що відповідає 4535 мг гадобутролю. 1 шприц містить 10 мл розчину, що відповідає 6047 мг гадобутролю. 1 шприц містить 15 мл розчину, що відповідає 9070 мг гадобутролю. 1 шприц містить 20 мл розчину, що відповідає 12094 мг гадобутролю. 1 картридж для шприцу-інжектора містить 15 мл розчину, що відповідає 9070 мг гадобутролю. 1 картридж для шприцу-інжектора містить 20 мл розчину, що відповідає 12094 мг гадобутролю. 1 картридж для шприцу-інжектора містить 30 мл розчину, що відповідає 18140 мг гадобутролю. 1 пляшка з продуктом для інфузії містить 65 мл розчину, що відповідає 39307 мг гадобутролю.
Як виглядає препарат Gadovist 1,0 і що містить упаковка
Перш ніж використовувати препарат, його потрібно оглянути. Препарат Gadovist 1,0 є прозорим, безбарвним або
слабожовтим розчином. Не слід використовувати препарат Gadovist 1,0 у разі значного забарвлення,
належності твердих частинок або пошкодження контейнера.
Упаковки містять:
1 або 3 флакони, кожний з яких містить 2 мл розчину для ін'єкцій для внутрішньовенних ін'єкцій.
1 або 10 флаконів, кожний з яких містить 7,5; 15 або 30 мл розчину для ін'єкцій для внутрішньовенних ін'єкцій.
10 флаконів, кожний з яких містить 10 мл розчину для ін'єкцій для внутрішньовенних ін'єкцій.
1 або 5 шприців, кожний з яких містить 5, 7,5 або 10 мл розчину для ін'єкцій для внутрішньовенних ін'єкцій (у шприці-інжекторі об'ємом 10 мл).
1 або 5 шприців, кожний з яких містить 15 мл розчину для ін'єкцій для внутрішньовенних ін'єкцій
(у шприці-інжекторі об'ємом 17 мл або у шприці-інжекторі об'ємом 20 мл).
1 або 5 шприців, кожний з яких містить 20 мл розчину для ін'єкцій для внутрішньовенних ін'єкцій
(у шприці-інжекторі об'ємом 20 мл).
1 або 5 картриджів для шприцу-інжектора, кожний з яких містить 15, 20 або 30 мл розчину для ін'єкцій для внутрішньовенних ін'єкцій (картридж об'ємом 65 мл).
1 або 10 пляшок, кожна з яких містить 65 мл розчину для ін'єкцій (у пляшці для інфузії об'ємом 100 мл).
Не всі розміри упаковок повинні бути в обігу.
Відповідальний суб'єкт і виробник
Відповідальний суб'єкт:
Bayer AG
Кайзер-Вільгельм-Алле, 1
51373 Леверкузен,
Німеччина
Виробник:
Bayer AG
Мюллерштрассе, 178
13353 Берлін
Німеччина
Для отримання більш детальної інформації зверніться до представника відповідального суб'єкта:
Bayer ТОВ
вул. Львівська, 7
03115 Київ
Україна
телефон: (0-44) 207-45-00
Дата останньої актуалізації уллянки: Липень 2025
---------------------------------------------------------------------------------------------------------------------------
Інформація, призначена лише для фахового медичного персоналу (див. також пункти від 1
до 6):
Спосіб застосування
Препарат призначений лише для внутрішньовенних ін'єкцій. Після застосування препарату необхідно спостерігати за пацієнтом протягом щонайменше півгодини, оскільки досвід показує, що протягом цього періоду виникає
більшість побічних ефектів.
Вимагану дозу необхідно вводити в одноразовій швидкій внутрішньовенній ін'єкції. Дослідження МРТ з
застосуванням контрастного засобу можна розпочати негайно після ін'єкції (або через короткий час після ін'єкції, залежно від застосованих імпульсних послідовностей і протоколу дослідження) через швидке виникнення ефекту посилення контрасту. Оптимальне контрастування виникає під час першого проходження артерій у разі ангіографічного дослідження
(ангіографія з використанням магнітно-резонансної томографії з посиленням контрасту, англ. contrast
enhancement in magnetic resonance angiography– CE-MRA) і протягом близько 15 хвилин після ін'єкції препарату Gadovist 1,0 у разі оцінки центральної нервової системи (ЦНС) (час залежить від типу хворобливої зміни і тканини).
Інструкція використання
- Перед ін'єкцією Перед застосуванням препарату необхідно оглянути. Не слід використовувати препарат Gadovist 1,0 у разі значного забарвлення, наявності твердих частинок або пошкодження контейнера.
- Спосіб підготовки Флакони Препарат Gadovist 1,0 необхідно витягувати в шприц безпосередньо перед застосуванням. Не слід проколювати корк більше 1 разу. Препарат, який не був використаний під час одного дослідження, повинен бути викинутий. Шприци-інжектори Продукт Gadovist готовий до застосування. Шприц-інжектор необхідно підготувати до ін'єкції безпосередньо перед застосуванням. Необхідно видалити затичку кінця шприцу-інжектора безпосередньо перед застосуванням. Препарат, який не був використаний під час одного дослідження, повинен бути викинутий. Шприци-інжектори скляні (тільки): ВСТАНОВЛЕННЯ В РУЦІ
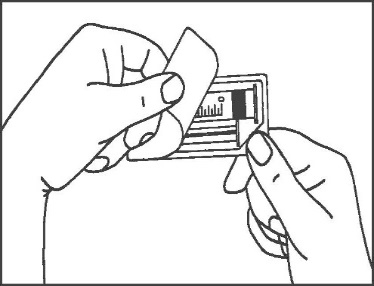
- 1. Відкрити упаковку
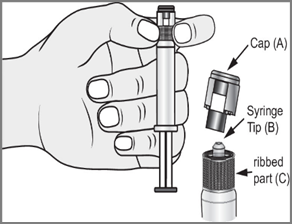
- 2.
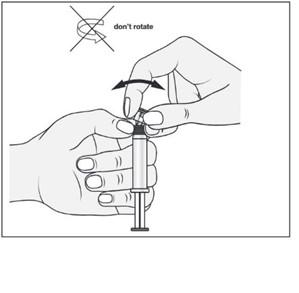
- 3. Другою рукою взяти за насадку (А) системи закриття і обережно нахилити її вперед і назад, поки насадка не від'єднається і не можна буде її зняти (всі пломби будуть зламані)
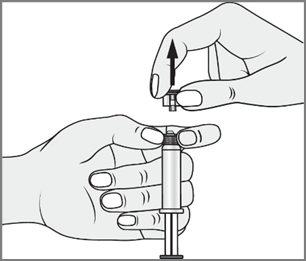
- 4. Зняти насадку (А) в напрямку прямо вгору. Не торкайтеся кінця шприцу
- (Б), щоб зберегти його стерильність.
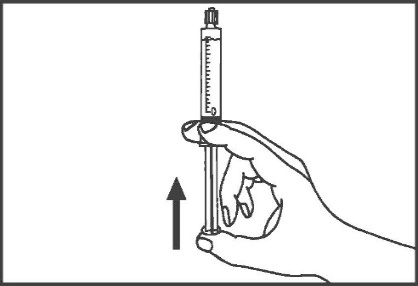
Шприци-інжектори пластикові:
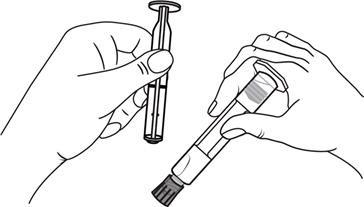
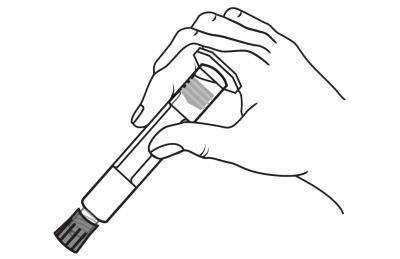
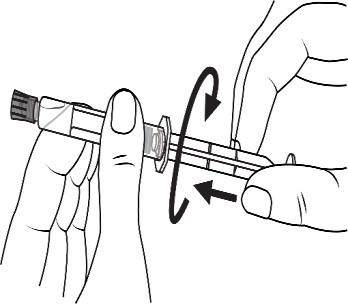
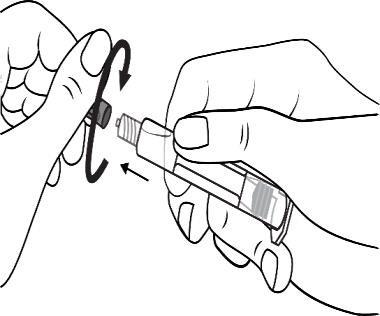
Відкрити затичку кінця шляхом
відкручування
Вкрутити поршень у шприц за годинниковою стрілкою
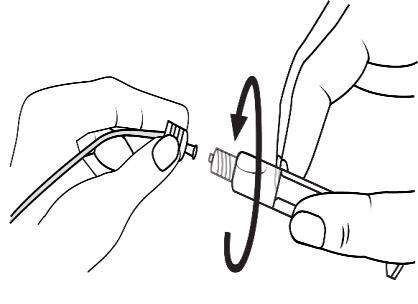
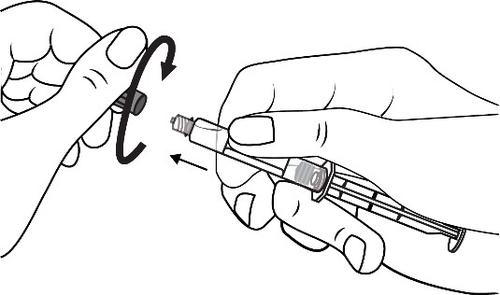
З'єднати кінець шприцу з дреном
обертанням за годинниковою стрілкою. Далі слідувати інструкції з експлуатації.
Відкрити затичку кінця шляхом
відкручування
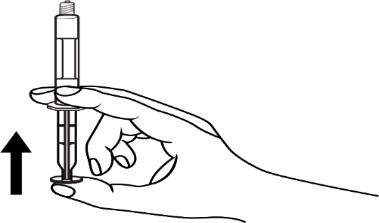
- 4. Видалити повітря з шприцу
Картриджі для шприців-інжекторів
Препарат повинен бути введений кваліфікованим медичним персоналом з використанням
відповідних процедур і обладнання.
Необхідно зберігати стерильність під час усіх ін'єкцій препарату.
Інструкція з експлуатації обладнання повинна бути надана виробником.
Препарат, який не був використаний під час одного дослідження, повинен бути викинутий.
Пляшки
Пляшка містить 65 мл розчину.
Препарат може бути введений за допомогою автоматичного дозатора.
Інструкція з експлуатації обладнання повинна бути надана виробником.
Інші відомості див. пункт: «Як зберігати препарат Gadovist 1,0».
Всі залишки незастосованого препарату або його відходи повинні бути видалені у відповідності з місцевими правилами.
Зірвану з флакону або шприцу-інжектора або картриджа або пляшки етикетку необхідно приклеїти до картки пацієнта для забезпечення правильної реєстрації застосованого препарату, що містить гадолін. Також необхідно зазначити дозу. Якщо застосовуються електронні картки пацієнта, необхідно ввести назву препарату, номер серії та дозу.
Несумісність
Оскільки не проводилися дослідження щодо сумісності, препарат не слід змішувати з іншими
лікарськими засобами.
Дозування
Необхідно застосовувати мінімальну дозу, яка забезпечує контрастне посилення, достатнє для діагностичних цілей. Дозу необхідно розрахувати на основі маси тіла пацієнта. Вона не повинна перевищувати рекомендовану дозу на кілограм маси тіла, вказану в цьому пункті.
Дорослі
Доза залежить від показання. Одноразова ін'єкція 0,1 ммоль препарату Gadovist 1,0 на кілограм маси тіла
(що відповідає 0,1 мл/кг маси тіла) зазвичай є достатньою. Загальна, максимальна доза становить 0,3 ммоль препарату Gadovist 1,0 на кілограм маси тіла (що відповідає 0,3 мл/кг маси тіла).
Дослідження ЦНС:
Зазвичай рекомендована доза для встановлення діагнозу становить 0,1 ммоль на кілограм маси тіла.
Якщо незважаючи на негативний результат дослідження МРТ все ще існує клінічно значуще підозření наявності
хворобливої зміни або якщо отримання більш точної інформації може вплинути на лікування
пацієнта, можна виконати другу ін'єкцію препарату урівноважуючи дозу до максимальної
дози 0,2 ммоль/кг маси тіла протягом 30 хвилин після першого введення. У дослідженнях зображення ЦНС мінімальна доза, яку можна вводити, становить 0,075 ммоль гадобутролю на кілограм маси тіла (що відповідає 0,075 мл препарату Gadovist 1,0 на кілограм маси тіла).
Дослідження МРТ всього тіла (крім CE-MRA):
Для встановлення діагнозу зазвичай достатньою є доза 0,1 мл/кг маси тіла препарату Gadovist 1,0.
Ангіографічне дослідження:
Зображення 1 поля зору (англ. field of view– FOV):
- 7,5 мл при масі тіла менше 75 кг; 10 мл при масі тіла 75 кг і більше (що відповідає 0,1- 0,15 ммоль/кг маси тіла)
- Зображення більше 1 поля зору (FOV):
- 15 мл при масі тіла менше 75 кг; 20 мл при масі тіла 75 кг і більше (що відповідає 0,2- 0,3 ммоль/кг маси тіла).
Спеціальні групи пацієнтів
Діти і підлітки
У дітей будь-якого віку (у тому числі у новонароджених немовлят) рекомендована доза становить 0,1 ммоль гадобутролю на кілограм маси тіла (див. пункт 1: «Що таке препарат Gadovist 1,0 і для чого він використовується»). Через недорозвинену функцію нирок у новонароджених
(дітей до 4 тижнів життя) та у немовлят (дітей до 1 року життя), препарат Gadovist 1,0 повинен застосовуватися у цих пацієнтів лише після ретельного розгляду лікарем. Новонароджені та немовлята
повинні отримати одноразову дозу під час дослідження і не повинні отримувати другу ін'єкцію протягом щонайменше 7 днів.
Спеціальні попередження і обережність при застосуванні
Гіперчутливість
Як і у випадку з іншими контрастними засобами, застосування препарату Gadovist 1,0 може бути
пов'язане з ризиком виникнення реакцій типу алергії, гіперчутливості або ідiosynкразії,
характеризованих симптомами з боку серцево-судинної системи, дихальної системи або шкірними симптомами, аж до важких реакцій, включаючи шок. Загалом, пацієнти з захворюваннями серцево-судинної системи більш схильні
до виникнення важких симптомів, навіть смерті внаслідок важких реакцій гіперчутливості.
Ризик виникнення реакції гіперчутливості може збільшуватися у разі:
- відбулися реакції на контрастні засоби,
- астма бронхів у анамнезі,
- алергічні захворювання у анамнезі. У пацієнтів зі схильністю до алергії рішення про застосування препарату Gadovist 1,0 повинно бути прийняте після ретельного розгляду співвідношення користі та ризику. Більшість реакцій виникає протягом півгодини після введення препарату. Тому рекомендується спостереження за пацієнтом. Необхідно забезпечити доступ до лікарських засобів, які застосовуються при реакціях гіперчутливості, та відповідного обладнання. Рідко реєструвалися запізнілі реакції (після кількох годин до кількох днів). Порушення функції нирок
Перед застосуванням препарату Gadovist 1,0 рекомендується провести дослідження щодо порушення функції нирок, яке включає лабораторні тести.
Згідно з повідомленнями, неркопохідне фіброзне захворювання (англ. nephrogenic systemic fibrosis– NSF) було пов'язано з застосуванням деяких лікарських засобів, що містять гадолін
(у тому числі Gadovist 1,0) у пацієнтів, у яких спостерігалося гостре або хронічне важке порушення функції нирок (креатинінова кліренс <30 мл хв 1,73 м). Пацієнти, які перенесли трансплантацію печінки, особливо схильні, оскільки ризик виникнення гострої ниркової недостатності у цій групі пацієнтів високий. Через можливість nsf під час застосування препарату gadovist 1,0 цей препарат можна застосовувати з важкими порушеннями функції нирок та період трансплантації печінки лише після ретельного розгляду співвідношення користі ризику якщо діагностична інформація є необхідною і недоступна для дослідження МРТ без контрастного посилення. Якщо необхідним, доза не повинна перевищувати 0,1 ммоль кг маси тіла. Не слід більше однієї дози дослідження. відсутність даних щодо багаторазового ін'єкції повинні повторюватися, інтервали між ін'єкціями становлять менше 7 днів.
Гемодіаліз одразу після застосування препарату Gadovist 1,0 може полегшити його виведення з організму. Відсутні дані, які б виправдовували початок гемодіалізу для профілактики або лікування NSF
у пацієнтів, які ще не піддавалися гемодіалізу.
Тому препарат Gadovist 1,0 повинен застосовуватися у цих пацієнтів після ретельного розгляду співвідношення користі та ризику (див. пункт 4.8).
Вагітність і годування грудьми
Препарату Gadovist 1,0 не слід застосовувати під час вагітності, якщо стан клінічного пацієнта не вказує на
необхідність застосування гадобутролю.
Лікар разом з годуючою матір'ю повинні вирішити питання про продовження годування грудьми або про його переривання на період 24 годин після застосування препарату Gadovist 1,0.
Побічні ефекти
Підсумування профілю безпеки базується на даних клінічних досліджень, проведених з участю понад 6300 пацієнтів і даних після дозволу препарату до обігу.
Передозування
Одноразові дози гадобутролю до 1,5 ммоль/кг маси тіла були добре перенесені.
У разі передозування як заходи обережності рекомендується контролювати функцію серцево-судинної системи (у тому числі ЕКГ) та функцію нирок.
У разі передозування препарат Gadovist 1,0 можна вивести з організму за допомогою діалізу.
- Країна реєстрації
- Діючі речовини
- Потрібен рецептТак
- Виробник
- ІмпортерBayer AG Bayer Schering Pharma AG
- Інформація є довідковою і не є медичною порадою. Перед прийомом будь-яких препаратів обов'язково проконсультуйтеся з лікарем. Oladoctor не несе відповідальності за медичні рішення, прийняті на основі цього контенту.
- Альтернативи до Гадовіст 1,0Форма випуску: Розчин, 279,3 мг/млДіючі речовини: gadobutrolВиробник: BIPSO GmbH Bracco Imaging S.p.A.Не потрібен рецептФорма випуску: Розчин, 0,5 ммоль/млДіючі речовини: gadoteric acidВиробник: GE Healthcare AS GE Healthcare IrelandПотрібен рецептФорма випуску: Розчин, 0,5 ммоль/млДіючі речовини: gadoteric acidВиробник: GE Healthcare ASПотрібен рецепт
Аналоги Гадовіст 1,0 в інших країнах
Найкращі аналоги з тією самою діючою речовиною та терапевтичним ефектом.
Аналог Гадовіст 1,0 у Україна
Аналог Гадовіст 1,0 у Іспанія
Лікарі онлайн щодо Гадовіст 1,0
Консультація щодо дозування, побічних ефектів, взаємодій, протипоказань та поновлення рецепта на Гадовіст 1,0 – за рішенням лікаря та згідно з місцевими правилами.














