
Цуросурф

Запитайте лікаря про рецепт на Цуросурф

Інструкція із застосування Цуросурф
Листок-вкладення до упаковки: інформація для батьків та опікунів
Увага! Необхідно зберегти листок. Інформація на безпосередній упаковці іноземною мовою.
Curosurf, 80 мг/мл (120 мг/1,5 мл), суспензія для інгаляційного та інтратрахейного застосування
(Порактант альфа)
Фракція фосфоліпідів з легень свині
Необхідно уважно ознайомитися з вмістом листка перед застосуванням препарату, оскільки він містить важливу інформацію для пацієнта.
- Необхідно зберегти цей листок, щоб у разі потреби можна було його знову прочитати.
- У разі будь-яких сумнівів необхідно звернутися до лікаря.
- Якщо в пацієнта з'являться будь-які побічні ефекти, включаючи будь-які побічні ефекти, не перелічені в цьому листку, необхідно повідомити про це лікаря або медсестру. Див. пункт 3.
Зміст листка:
- 1. Що таке препарат Curosurf і для чого він застосовується
- 2. Як застосовувати препарат Curosurf
- 3. Можливі побічні ефекти
- 4. Як зберігати препарат Curosurf
- 5. Зміст упаковки та інші відомості
1. ШО ЦЕ Є ПРЕПАРАТ CUROSURF І ДЛЯ ЧОГО ВІН ЗАСТОСОВУЄТЬСЯ
Препарат Curosurf застосовується для лікування та профілактики синдрому дихальної недостатності (англ.
Respiratory Distress Syndrome: RDS) у новонароджених. У більшості новонароджених у легенях присутня
речовина, звана поверхнево-активною субстанцією (фактор поверхневої активності). Ця речовина покриває
легеневі пухирці, запобігає їх злипанню та забезпечує нормальне дихання. Однак, деякі
новонароджені, особливо недоношені, народжуються з дефіцитом поверхнево-активної субстанції, що призводить до розвитку
RDS. Препарат Curosurf є природнім поверхнево-активним засобом, який діє так само, як поверхнево-активна субстанція,
вироблена новонародженим, і тому допомагає новонародженим нормально дихати до моменту, поки
вони не почнуть виробляти свою природню поверхнево-активну субстанцію.
У новонародженого можуть виникнути інші захворювання, які можуть потребувати іншого лікування.
2. ЯК ЗАСТОСОВУВАТИ ПРЕПАРАТ CUROSURF
Дозування:
Лікар вибирає відповідну дозу препарату, залежно від маси тіла дитини. Якщо дитині вводять
препарат Curosurf, щоб запобігти виникненню RDS, препарат необхідно ввести протягом 15 хвилин після народження.
Якщо дитині вводять препарат Curosurf для лікування RDS, препарат необхідно ввести якнайшвидше після
діагностики захворювання. Якщо дитина потребує додаткової дози препарату Curosurf, її вводять
через 12 годин після введення першої дози. За необхідності, після наступних 12 годин можна
ввести третю дозу.
Застосування препарату Curosurf у недоношених дітей з нирковою або печінковою недостатністю не було вивчено.
Спосіб введення препарату:
Препарат Curosurf вводиться дитині в інкубаторі лікарем або медсестрою. Препарат буде
підігріт до кімнатної температури, а потім введений за допомогою шприца через інтубаційну трубку в трахею дитини. Для цього може знадобитися відключення дитини від апарату штучного дихання на кілька хвилин.
Може бути застосовано також метод менш інвазивного введення поверхнево-активної субстанції через тонкий катетер (LISA – англ. Less Invasive Surfactant Administration).
Препарат Curosurf містить натрій
Препарат містить менше 1 ммоль (23 мг) натрію в одній ампулі, тобто препарат вважається «безнатрієвим».
3. МОЖЛИВІ ПОБІЧНІ ЕФЕКТИ
Як і будь-який препарат, цей препарат може викликати побічні ефекти, хоча вони не виникнуть у кожного.
Можливі побічні ефекти перелічені нижче залежно від частоти їх виникнення:
У разі сумнівів щодо побічних ефектів необхідно звернутися до лікаря.
Не дуже часто(виникають у менше 1 з 100 пацієнтів):
- інфекція
- кровотеча в мозок
- повітря в грудній клітці, викликане пошкодженням легень
Рідко(виникають у менше 1 з 1000 пацієнтів):
- сповільнення серцевої діяльності
- низький тиск крові
- хронічне захворювання легень
- зниження рівня кисню в організмі
Крім того, були зареєстровані наступні побічні ефекти:
- збільшення рівня кисню в організмі
- синюшність шкіри або слизових оболонок, викликана недостатністю кисню
- зупинка дихання
- ускладнення після введення трубок в легені
- зниження мозкової активності
Під час введення препарату Curosurf через тонкий катетер були зареєстровані деякі легкі та короткочасні побічні ефекти: брадикардія, апное, зниження насичення крові киснем, піна на устах, кашель, задуха та чхання.
Звітність про побічні ефекти
Якщо виникнуть будь-які побічні ефекти, включаючи будь-які побічні ефекти, не перелічені в цьому листку, необхідно повідомити про це лікаря або медсестру.
Побічні ефекти можна зареєструвати безпосередньо в Департаменті моніторингу небажаних дій лікарських засобів Міністерства охорони здоров'я,
вул. Джерозолімі 181С, 02-222 Варшава, тел.: +48 22 49 21 301, факс: +48 22 49 21 309, веб-сайт: https://smz.ezdrowie.gov.pl
Звітність про побічні ефекти дозволить зібрати більше інформації про безпеку застосування препарату.
4. ЯК ЗБЕРІГАТИ ПРЕПАРАТ CUROSURF
- Препарат необхідно зберігати в місці, недоступному для дітей.
- Зберігати в холодильнику (2°C - 8°C). Зберігати в оригінальній упаковці для захисту від світла. Перед введенням дитині необхідно підігріти до кімнатної температури.
- Неоткриті та невикористані ампули препарату Curosurf, які були підігріті до кімнатної температури, протягом 24 годин можна повернути в холодильник для подальшого використання. Препарат не можна підігрівати до кімнатної температури та повертати в холодильник більше одного разу.
- Не застосовувати цей препарат після закінчення терміну придатності, вказаного на пачці та ампулі. Термін придатності позначає останній день вказаного місяця.
- Одну упаковку необхідно використовувати один раз, а залишки викинути. Лікарня повинна забезпечити безпечне видалення невикористаних залишків препарату Curosurf.
- Лікарських засобів не слід викидати в каналізацію. Необхідно запитати у фармацевта, як видалити лікарські засоби, які вже не використовуються. Таке поводження допоможе захистити навколишнє середовище
5. ЗМІСТ УПАКОВКИ ТА ІНШІ ВІДОМОСТІ
Що містить препарат Curosurf
- Активною речовиною є суміш ліпідів та білків, отриманих з легеневих пухирців свині.
- Інші складові частини: хлорид натрію, вода для ін'єкцій.
Як виглядає препарат Curosurf та що містить упаковка
Препарат Curosurf є стерильною суспензією. Він доступний у одноразових скляних ампулах,
які містять 1,5 мл (120 мг) фракції фосфоліпідів, отриманих з легеневих пухирців свині.
Кожен мл стерильної суспензії містить 80 мг фракції фосфоліпідів з легеневих пухирців свині. В
одній упаковці містяться 2 ампули по 1,5 мл суспензії препарату Curosurf.
Для отримання більш детальної інформації необхідно звернутися до особи, відповідальній за випуск препарату, або паралельного імпортера.
Особа, відповідальна за випуск препарату в Румунії, країні експорту:
CHIESI FARMACEUTICI SpA
Віа Пальєрмо 26/А, 43122 Парма, Італія
Виробник:
CHIESI FARMACEUTICI SpA
Віа Пальєрмо 26/А, 43122 Парма, Італія
CHIESI FARMACEUTICI S.p.A
Віа Сан-Леонардо 96, 43122 Парма, Італія
CHIESI PHARMACEUTICALS GmbH
Гонзагагассе 16/16, 1010 Відень, Австрія
Паралельний імпортер:
Delfarma Sp. z o.o.
вул. Св. Терези від Дітей Ісуса 111
91-222 Лодзь
Перепаковано в:
Delfarma Sp. z o.o.
вул. Св. Терези від Дітей Ісуса 111
91-222 Лодзь
Номер дозволу в Румунії, країні експорту: 272/2007/01
Номер дозволу на паралельний імпорт: 85/19
Дата затвердження листка:12.02.2024
[Інформація про зареєстрований товарний знак]
Будь ласка, прочитайте інформацію на зворотному боці листка
------------------------------------------------------------------------------------------------------------------------
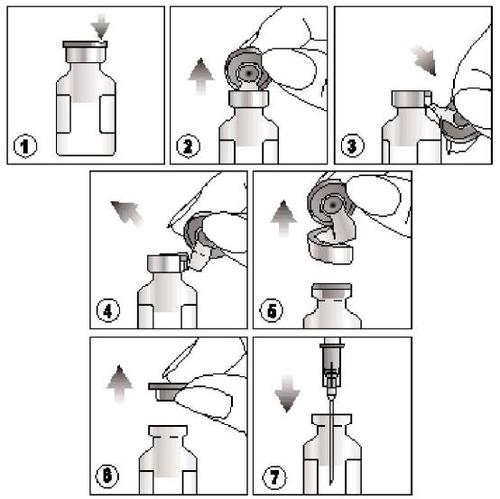
Як витягти продукт?
- 1) Знайти різку, розташовану на кольоровому пластиковому ковпачку,
- 2) Підняти ковпачок у місці різки та потягнути його вгору,
- 3) Потягнути вниз пластикову частину ковпачка разом з його алюмінієвою частиною,
- 4) та 5) Видалити весь ковпачок, знімаючи алюмінієвий кільце
- 6) та 7) Зняти гумовий корк перед витягуванням вмісту ампули.
Для одноразового використання. Невикористану суспензію, яка залишилася в ампулі, необхідно викинути.
Не зберігати невикористану суспензію для повторного використання.
Всі залишки невикористаного продукту або його відходи необхідно видалити у відповідності з правилами.
- Країна реєстрації
- Діючі речовини
- Потрібен рецептНі
- Власник реєстраційного посвідчення (MAH)Chiesi Farmaceutici S.p.A.
- Інформація є довідковою і не є медичною порадою. Перед прийомом будь-яких препаратів обов'язково проконсультуйтеся з лікарем. Oladoctor не несе відповідальності за медичні рішення, прийняті на основі цього контенту.
- Альтернативи до ЦуросурфФорма випуску: Суспензія, 80 мг, що відповідає приблизно 74 мг загального вмісту фосфоліпідів та 0,9 мг низькомолекулярних гідрофобних білків.Діючі речовини: natural phospholipidsНе потрібен рецептФорма випуску: Суспензія, 80 мг/млДіючі речовини: natural phospholipidsНе потрібен рецептФорма випуску: Пастилки, 1500 мг + 125 мгДіючі речовини: nikethamideНе потрібен рецепт
Аналоги Цуросурф в інших країнах
Найкращі аналоги з тією самою діючою речовиною та терапевтичним ефектом.
Аналог Цуросурф у Україна
Аналог Цуросурф у Іспанія
Лікарі онлайн щодо Цуросурф
Консультація щодо дозування, побічних ефектів, взаємодій, протипоказань та поновлення рецепта на Цуросурф – за рішенням лікаря та згідно з місцевими правилами.














