
SMOFKABIVEN EXTRA NITROGEN SIN ELECTROLITOS EMULSION PARA PERFUSION
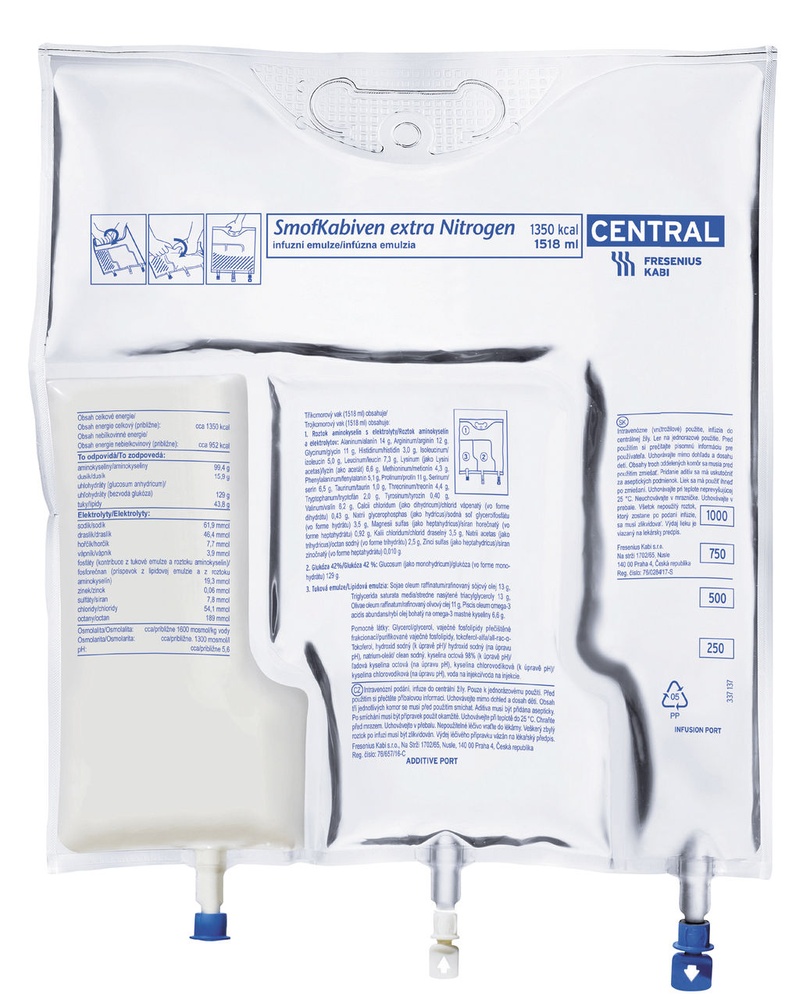

Cómo usar SMOFKABIVEN EXTRA NITROGEN SIN ELECTROLITOS EMULSION PARA PERFUSION
Traducción generada por IA
Este contenido ha sido traducido automáticamente y se ofrece solo con fines informativos. No sustituye la consulta con un profesional sanitario.
Ver originalContenido del prospecto
- Introducción
- Qué es SmofKabiven extra Nitrogen sin electrolitos y para qué se utiliza
- Qué necesita saber antes de empezar a usar SmofKabiven extra Nitrogen sin electrolitos
- Cómo usar SmofKabiven extra Nitrogen sin electrolitos
- Posibles efectos adversos
- Conservación de SmofKabiven extra Nitrogen sin electrolitos
- Contenido del envase e información adicional
Introducción
Prospecto: información para el usuario
SmofKabiven extra Nitrogen sin electrolitos emulsión para perfusión
Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene información importante para usted.
- Conserve este prospecto, ya que puede tener que volver a leerlo.
- Si tiene alguna duda, consulte a su médico, farmacéutico o enfermero.
- Si experimenta efectos adversos, consulte a su médico, farmacéutico o enfermero, incluso si se trata de efectos adversos que no aparecen en este prospecto. Ver sección 4.
Contenido del prospecto
- Qué es SmofKabiven extra Nitrogen sin electrolitos y para qué se utiliza
- Qué necesita saber antes de empezar a usar SmofKabiven extra Nitrogen sin electrolitos
- Cómo usar SmofKabiven extra Nitrogen sin electrolitos
- Posibles efectos adversos
- Conservación de SmofKabiven extra Nitrogen sin electrolitos
- Contenido del envase e información adicional
1. Qué es SmofKabiven extra Nitrogen sin electrolitos y para qué se utiliza
SmofKabiven extra Nitrogen sin electrolitos es una emulsión para perfusión que se administra en su sangre mediante un gotero (perfusión intravenosa). El producto contiene aminoácidos (componentes utilizados en la formación de proteínas), glucosa (carbohidratos) y lípidos (grasa), en una bolsa de plástico y puede ser administrado a adultos y niños a partir de 2 años de edad.
Un profesional sanitario le administrará SmofKabiven extra Nitrogen sin electrolitos cuando otras formas de alimentación no sean suficientemente buenas o no sean posibles.
2. Qué necesita saber antes de empezar a usar SmofKabiven extra Nitrogen sin electrolitos
No use SmofKabiven extra Nitrogen sin electrolitos:
- si es alérgico (hipersensible) a los principios activos o a cualquiera de los demás componentes de este medicamento (incluidos en la sección 6)
- si usted es alérgico al pescado o al huevo
- si usted es alérgico a los cacahuetes o a la soja, no debería utilizar este producto. SmofKabiven extra Nitrogen sin electrolitos contiene aceite de soja
- si usted tiene demasiados lípidos en su sangre (hiperlipidemia)
- si usted padece una alteración hepática grave
- si usted sufre problemas de coagulación de la sangre (alteraciones de la coagulación)
- si su organismo presenta problemas para la utilización de los aminoácidos
- si usted sufre enfermedad renal grave sin posibilidad de diálisis
- si usted se encuentra en shock agudo
- si usted tiene demasiado azúcar en su sangre (hiperglucemia), que no está controlada
- si usted tiene líquido en los pulmones (edema pulmonar agudo)
- si usted tiene demasiado líquido en su organismo (hiperhidratado)
- si usted presenta insuficiencia cardíaca que no está en tratamiento
- si usted tiene un defecto en su sistema de coagulación de la sangre (síndrome hemofagocitótico)
- si usted se encuentra en una situación inestable, como después de un trauma grave, diabetes mellitus no controlada, ataque cardíaco agudo, derrame cerebral, coágulo de sangre, acidosis metabólica (una alteración que da lugar a demasiado ácido en su sangre), infección grave (sepsis grave), coma, y si usted no tiene suficiente líquido en su organismo (deshidratación hipotónica).
- en niños recién nacidos o menores de 2 años
Advertencias y precauciones
Consulte a su médico antes de empezar a usar SmofKabiven extra Nitrogen sin electrolitos si tiene:
- problemas renales
- diabetes mellitus
- pancreatitis (inflamación del páncreas)
- problemas hepáticos
- hipotiroidismo (problemas tiroideos)
- sepsis (infección grave)
Si durante la perfusión aparece fiebre, erupción cutánea, hinchazón, dificultad para respirar, escalofríos, sudoración, náuseas o vómitos, informe a su profesional sanitario inmediatamente, porque estos síntomas podrían ser causados por una reacción alérgica, o porque usted está recibiendo demasiada cantidad del medicamento.
Su doctor necesitará controlar regularmente su sangre, por medio de análisis de la función hepática y otros valores.
Niños y adolescentes
SmofKabiven extra Nitrogen sin electrolitos no está pensado para niños recién nacidos ni niños de menos de 2 años de edad.
SmofKabiven extra Nitrogen sin electrolitos puede ser administrado a niños de 2 a 16/18 años de edad.
Uso de SmofKabiven extra Nitrogen sin electrolitos con otros medicamentos
Informe a su médico si está tomando, ha tomado recientemente o podría tener que tomar cualquier otro medicamento incluso los adquiridos sin receta.
Embarazo y lactancia
No existe información sobre el uso de SmofKabiven extra Nitrogen sin electrolitos durante el embarazo o en el período de lactancia. Por lo tanto, SmofKabiven extra Nitrogen sin electrolitos debería ser administrado a mujeres embarazadas o en período de lactancia, sólo si el médico lo considera necesario. No obstante, el uso de SmofKabiven extra Nitrogen sin electrolitos puede ser considerado en el embarazo y la lactancia, si su médico lo aconseja.
Conducción y uso de máquinas
No es relevante, ya que este medicamento se administra en el hospital.
3. Cómo usar SmofKabiven extra Nitrogen sin electrolitos
Siga exactamente las instrucciones de administración de este medicamento indicadas por su médico. En caso de duda, consulte de nuevo a su médico.
Su médico decidirá la dosis para usted de forma individual dependiendo de su peso corporal y su situación. SmofKabiven extra Nitrogen sin electrolitos le será administrado por un profesional sanitario.
Si usa más SmofKabiven extra Nitrogen sin electrolitos del que debe
Es muy poco probable que usted reciba demasiada cantidad de medicamento, ya que SmofKabiven extra Nitrogen sin electrolitos le será administrado por un profesional sanitario.
4. Posibles efectos adversos
Al igual que todos los medicamentos, SmofKabiven extra Nitrogen sin electrolitos puede producir efectos adversos, aunque no todas las personas los sufran.
Frecuentes(pueden afectar hasta 1 de cada 10 pacientes): un ligero aumento de la temperatura corporal.
Poco frecuentes(pueden afectar hasta 1 de cada 100 pacientes): niveles elevados en sangre (plasma) de componentes hepáticos, ausencia de apetito, náuseas, vómitos, escalofríos, mareos y dolor de cabeza.
Raros(pueden afectar hasta 1 de cada 1000 pacientes): presión sanguínea baja o elevada, dificultad para respirar, frecuencia cardíaca rápida (taquicardia). Reacciones de hipersensibilidad (que pueden dar síntomas como hinchazón, fiebre, descenso de la presión sanguínea, erupciones cutáneas, ronchas (zonas rojas hinchadas), enrojecimiento, dolor de cabeza). Sensaciones de frío y calor. Palidez. Labios y piel con coloración azulada (debido a la falta de oxígeno en su sangre). Dolor en cuello, espalda, huesos, pecho y zona lumbar.
Comunicación de efectos adversos
Si experimenta cualquier tipo de efecto adverso, consulte a su médico, farmacéutico o enfermero, incluso si se trata de posibles efectos adversos que no aparecen en este prospecto. También puede comunicarlos directamente a través del Sistema Español de Farmacovigilancia de medicamentos de Uso Humano: https://www.notificaram.es. Mediante la comunicación de efectos adversos usted puede contribuir a proporcionar más información sobre la seguridad de este medicamento.
5. Conservación de SmofKabiven extra Nitrogen sin electrolitos
Mantener este medicamento fuera de la vista y del alcance de los niños.
Mantener en la sobrebolsa. No conservar a temperatura superior a 25º C. No congelar.
No utilice este medicamento después de la fecha de caducidad que aparece en la bolsa y en la caja. La fecha de caducidad es el último día del mes que se indica.
6. Contenido del envase e información adicional
SmofKabiven extra Nitrogen sin electrolitos contiene
Las sustancias activas son | g por 1000 ml |
Alanina | 9,2 |
Arginina | 7,9 |
Glicina | 7,2 |
Histidina | 2,0 |
Isoleucina | 3,3 |
Leucina | 4,8 |
Lisina (como acetato) | 4,3 |
Metionina | 2,8 |
Fenilalanina | 3,3 |
Prolina | 7,3 |
Serina | 4,3 |
Taurina | 0,65 |
Treonina | 2,9 |
Triptófano | 1,3 |
Tirosina | 0,26 |
Valina | 4,1 |
Glucosa (como monohidrato) | 85 |
Aceite de soja, refinado | 8,7 |
Triglicéridos de cadena media | 8,7 |
Aceite de oliva, refinado | 7,2 |
Aceite de pescado, rico en ácidos grasos omega-3 | 4,3 |
Los demás componentes son: glicerol, fosfolípidos de huevo purificados, todo-rac-α-tocoferol, hidróxido sódico (ajuste pH), oleato sódico, ácido acético glacial (ajuste pH), ácido clorhídrico (ajuste pH) y agua para preparaciones inyectables.
Aspecto del producto y contenido del envase
Las soluciones de glucosa y aminoácidos son transparentes, incoloras o ligeramente amarillas y libres de partículas. La emulsión lipídica es blanca y homogénea.
Tamaños de envase:
1 x 506 ml, 6 x 506 ml
1 x 1012 ml, 4 x 1012 ml
1 x 1518 ml, 4 x 1518 ml
1 x 2025 ml, 4 x 2025 ml
1 x 2531 ml, 3 x 2531 ml
Titular de la autorización de comercialización y responsable de la fabricación
Titular de la autorización de comercialización
Fresenius Kabi España S.A.U.
C/ Marina 16-18.
08005 Barcelona (España )
Responsable de la fabricación
Fresenius Kabi AB, SE-751 74 Uppsala, Suecia
Fecha de la última revisión de este prospecto: Marzo 2023
La información detallada y actualizada de este medicamento está disponible en la página Web de la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) http://www.aemps.gob.es/
------------------------------------------------------------------------------------------------------------------------
Esta información está destinada únicamente a profesionales del sector sanitario:
Advertencias y precauciones especiales de uso
Para evitar los riesgos asociados con velocidades de perfusión demasiado rápidas, se recomienda el uso de una perfusión continua y bien controlada, si es posible mediante el uso de una bomba de perfusión.
Dado que el uso de una vena central está asociado a un elevado riesgo de infección, deben tomarse precauciones asépticas estrictas para evitar cualquier contaminación durante la inserción del catéter y la manipulación.
Deben monitorizarse la glucosa sérica, los electrolitos y la osmolaridad, así como el balance hídrico, el equilibrio ácido-base y los niveles de enzimas hepáticos.
Ante cualquier signo o síntoma de reacción anafiláctica (como fiebre, temblores, erupción cutánea o disnea) debe interrumpirse inmediatamente la perfusión.
SmofKabiven extra Nitrogen sin electrolitos no debería ser administrado simultáneamente con sangre en el mismo equipo de perfusión, debido al riesgo de pseudoaglutinación.
Forma de administración
Vía intravenosa, perfusión en una vena central.
Para proporcionar una nutrición parenteral completa, deben añadirse a SmofKabiven extra Nitrogen sin electrolitos oligoelementos y vitaminas, de acuerdo con las necesidades del paciente.
Posología
Adultos
Dosificación:
El rango de dosis de 13-31 ml SmofKabiven extra Nitrogen sin electrolitos/kg pc/día aportará 0,14 – 0,32 g de nitrógeno/kg pc/día (correspondientes a 0,85 – 2,0 g aminoácidos/kg pc/día) y 12 – 28 kcal/kg pc/día de energía total (8 – 19 kcal/kg pc/día de energía no-proteica).
Velocidad de perfusión
La velocidad de perfusión máxima usual para glucosa es 0,25 g/kg pc/h, para los aminoácidos 0,1 g/kg pc/h, y para lípidos 0,15 g/kg pc/h.
La velocidad de perfusión no debe exceder de 1,5 ml/kg pc/hora (correspondiente a 0,13 g de glucosa, 0,10 g de aminoácidos y 0,04 g de lípidos/kg pc/h). El período de perfusión recomendado es de 14 – 24 horas.
Nutrición parenteral intradiálisis (NPID)
La velocidad máxima de infusión para la nutrición parenteral intradialítica (NPID) en pacientes adultos estables en tratamieno renal sustitutivo crónico es de 3,0 ml/kg/h (correspondiente a 0,20 g de aminoácidos/kg/h, 0,25 g de glucosa/kg/h y 0,09 g de lítpidos/kg/h). El volumen de infusión en la NPID debe guiarse por la diferencia entre la ingesta de alimentos por vía oral y las ingestas de nutrientes recomendadas, las pérdidas de nutrientes inevitables causadas por la terapia de sustitución renal, así como por la tolerancia metabólica invidual del paciente. El tiempo de infusión habitual para su uso en la NPID es de 3 a 5 horas, dependiendo de las necesidades del paciente y de la duración prevista de la sesión de terapia de sustitución renal. La dosis diaria máxima recomendada no se modifica.
Dosis máxima diaria:
La dosis máxima diaria varía con la situación clínica del paciente e incluso puede cambiar de un día a otro. La dosis diaria máxima recomendada es de 31 ml/kg pc/día.
Población pediátrica
Niños (2-11 años)
Dosificación:
La dosis de hasta 31 ml/kg pc/día debe ser ajustada regularmente de acuerdo con los requerimientos del paciente pediátrico que varían más que en los pacientes adultos.
Velocidad de perfusión:
La velocidad máxima de perfusión es de 1,8 ml/kg pc/h (correspondiente a 0,12 g de aminoácidos/kg/h, 0,15 g/glucosa/kg/h y 0,05 g lípidos/kg/h). A la velocidad de perfusión máxima recomendada, no usar periodos de perfusión mayores de 17 horas, excepto en casos excepcionales y bajo estrecha monitorización.
El periodo de perfusión recomendado es de 12 – 24 horas.
Dosis máxima diaria:
La dosis máxima diaria varía con la condición clínica del paciente y puede incluso cambiar de día a día. La dosis máxima diaria es de 31 ml/kg pc/día.
Adolescentes (12-16/18 años)
SmofKabiven extra Nitrogen sin electrolitos puede usarse en adolescentes de la misma forma que en los adultos.
Precauciones de eliminación
No utilizar si el envase está deteriorado.
Utilizar sólo si las soluciones de aminoácidos y glucosa son transparentes e incoloras o ligeramente amarillas, y si la emulsión lipídica es blanca y homogénea. Debe mezclarse el contenido de las tres cámaras separadas antes de utilizar, y antes de realizar cualquier adición a través del puerto de aditivos. Después de la apertura de las soldaduras tipo peel, la bolsa debe ser invertida varias veces con el fin de garantizar una mezcla homogénea, que no muestre evidencia de una separación de fases.
Para un solo uso. Debe desecharse cualquier mezcla sobrante después de la perfusión.
Compatibilidad
Están disponibles datos de compatibilidad con los productos de marca Dipeptiven 200 mg/ml, Supliven, Glycophos 216 mg/ml, Vitalipid Adultos/Infantil y Soluvit liofilizado en cantidades definidas y con soluciones con electrolitos en concentraciones definidas. Al adicionar los electrolitos, deben tenerse en cuenta las cantidades ya presentes en la bolsa de acuerdo con las necesidades clínicas del paciente. Los datos generados respaldan adiciones a la bolsa activada de acuerdo con la tabla siguiente:
Rango de compatibilidad estable durante 7 días, es decir, 6 días de almacenamiento a 2-8ºC seguido de 24 horas a 20-25ºC.
Unidades | Contenido total máximo | |||||
Tamaño de la bolsa de SmofKabiven Extra Nitrogen Sin Electrolitos | ml | 506 | 1012 | 1518 | 2025 | 2531 |
Aditivo | Volumen | |||||
Dipeptiven | ml | 0-150 | 0 - 300 | 0 - 300 | 0 - 300 | 0 - 300 |
Supliven | ml | 0 - 10 | 0 - 20 | 0 - 20 | 0 - 20 | 0 - 20 |
Soluvit | vial | 0 - 1 | 0 - 2 | 0 - 2 | 0 - 2 | 0 - 2 |
Vitalipid Adultos/Infantil | ml | 0 - 10 | 0 - 20 | 0 - 20 | 0 - 20 | 0 - 20 |
Límites de los electrolitos1 | Concentración | |||||
Sodio | mmol | ≤ 150 | ≤ 150 | ≤ 150 | ≤ 150 | ≤ 150 |
Potasio | mmol | ≤ 150 | ≤ 150 | ≤ 150 | ≤ 150 | ≤ 150 |
Calcio | mmol | ≤ 5 | ≤ 5 | ≤ 5 | ≤ 5 | ≤ 5 |
Magnesio | mmol | ≤ 5 | ≤ 5 | ≤ 5 | ≤ 5 | ≤ 5 |
Fostato orgánico (Glycophos) | mmol | ≤ 30 | ≤ 30 | ≤ 30 | ≤ 30 | ≤ 30 |
Zinc | mmol | ≤ 0,2 | ≤ 0,2 | ≤ 0,2 | ≤ 0,2 | ≤ 0,2 |
Selenio | µmol | ≤ 2 | ≤ 2 | ≤ 2 | ≤ 2 | ≤ 2 |
1incluye las cantidades de todos los productos.
Nota: Esta tabla indica la compatibilidad. No es una pauta de dosificación.
En el caso de los productos con nombre comercial, antes de prescribirlos, consulte la ficha técnica aprobada.
Existen datos sobre la compatibilidad con otros aditivos y el tiempo de conservación de las diferentes mezclas, disponibles bajo petición.
Las adiciones deben realizarse asépticamente.
Período de validez después de la mezcla de las cámaras de la bolsa
Se ha demostrado la estabilidad física y química de la bolsa de tres cámaras mezclada durante 48 horas a 20-25°C. Desde un punto de vista microbiológico, el producto debería utilizarse inmediatamente. Si no es utilizado inmediatamente, el tiempo de conservación hasta su utilización y las condiciones previas a su uso son responsabilidad del usuario y normalmente no deberían ser superiores a 24 horas a 2-8º C, a menos que la mezcla se haya realizado en condiciones asépticas controladas y validadas.
Período de validez después de la mezcla con aditivos
Se ha demostrado estabilidad fisicoquímica en uso de la bolsa mixta de tres cámaras con aditivos (ver apartado 6.6) hasta 7 días, es decir, 6 días a 2-8ºC seguidos de 24 horas a 20-25ºC, incluyendo la duración de la administración. Desde un punto de vista microbiológico, el producto debería utilizarse inmediatamente después de realizar las adiciones. Si no es utilizado inmediatamente, el tiempo de conservación hasta su utilización y las condiciones previas a su uso son responsabilidad del usuario. El tiempo de conservación normalmente no debería ser superior a 24 horas a 2-8º C, a menos que la adición de los suplementos se haya realizado en condiciones asépticas controladas y validadas.
Instrucciones para el uso de SmofKabiven extra Nitrogen sin electrolitos
La bolsa
506 ml,1012 ml, 1518 ml, 2025 ml, 2531 ml
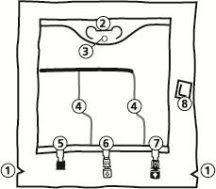
- Muescas en la sobrebolsa
- Asa
- Orificio para colgar la bolsa
- Sellos rompibles
- Puerto ciego (utilizado sólo durante la fabricación)
- Puerto de adición
- Puerto de perfusión
- Absorbente de oxígeno
- Apertura de la sobrebolsa
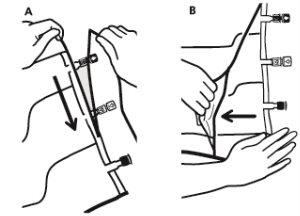
- Para extraer la sobrebolsa, sujetarla en posición horizontal y rasgar por la muesca hacia los puertos a lo largo del borde superior (A)
- Entonces, simplemente rasgar a lo largo del envase; separar la sobrebolsa y desecharla junto con el absorbente de oxígeno (B).
- Mezclado
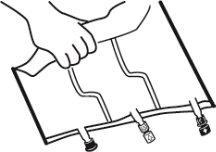
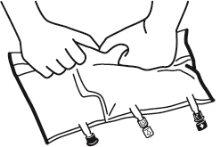
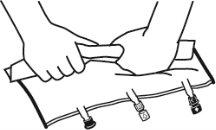
- Colocar la bolsa en una superficie plana.
- Enrollar la bolsa desde la parte del colgador hacia la parte de los puertos, primero con la mano derecha y a continuación aplicando una presión constante con la mano izquierda hasta que las soldaduras verticales se hayan abierto. Las soldaduras peel verticales se abren debido a la presión del líquido.
Las soldaduras peel también pueden abrirse antes de retirar la sobrebolsa.
Nota:los líquidos se mezclan fácilmente aunque la soldadura horizontal permanezca cerrada.
506 ml, 1012 ml, 1518 ml, 2025 ml, 2531 ml
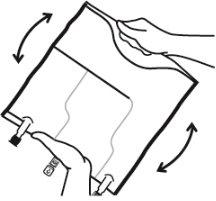
- Mezclar los contenidos de las tres cámaras invirtiendo la bolsa tres veces hasta que los componentes estén completamente mezclados.
- Finalización de la preparación:
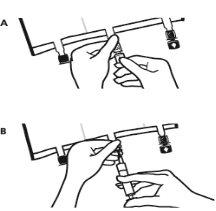
- Colocar la bolsa de nuevo sobre una superficie plana. Poco antes de inyectar los aditivos, romper el puerto de adición blanco por la marca en forma de flecha (A).
Nota:La membrana del puerto de aditivos es estéril.
- Sujetar la base del puerto de aditivos. Insertar la aguja, inyectar los aditivos (de compatibilidad conocida) por el centro del punto de inyección (B).
- Mezclar completamente entre cada adición, invirtiendo la bolsa tres veces. Utilizar jeringas con agujas de calibre 18-23 y una longitud máxima de 40 mm.
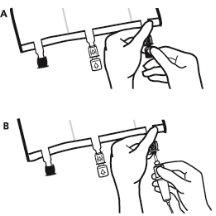
- Poco antes de insertar el set de perfusión, romper el puerto de perfusión azul por la marca en forma de flecha (A).
Nota:La membrana del puerto de perfusión es estéril.
- Usar un equipo de perfusión no venteado o cerrar la entrada del aire del equipo venteado.
- Sujetar la base del puerto de perfusión.
- Introducir el punzón a través del puerto de perfusión. El punzón deberá estar totalmente insertado para asegurar su retención.
Nota:La parte interna del puerto de perfusión es estéril.
- Colgado de la bolsa
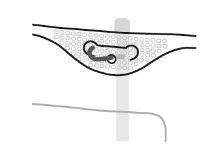
- Colgar la bolsa por la anilla que hay bajo el colgador
- País de registro
- Principio activo
- Requiere recetaSí
- Fabricante
- Esta información es de carácter general y no sustituye la consulta con un profesional sanitario.
- Alternativas a SMOFKABIVEN EXTRA NITROGEN SIN ELECTROLITOS EMULSION PARA PERFUSIONForma farmacéutica: INYECTABLE PERFUSION, 3,92 g / 1,26 g / 7,21 g / 3,36 g / 4,2 g / 5,11 g / 2,94 g / 2,8 g / 4,76 g / 5,07 g / 4,06 g / 14,49 g / 0,28 g / 8,05 g / 3,5 g / 200 gPrincipio activo: combinationsFabricante: Baxter S.L.Requiere recetaForma farmacéutica: INYECTABLE PERFUSION, 3,5 g / 200 g / 5,22 g / 1,88 g / 3,92 g / 1,26 g / 7,21 g / 3,36 g / 4,2 g / 5,11 g / 2,94 g / 2,8 g / 662 mg / 1,02 g / 4,76 g / 5,15 g / 5,07 g / 4,06 g / 14,49 g / 0,28 g / 8,05 gPrincipio activo: combinationsFabricante: Baxter S.L.Requiere recetaForma farmacéutica: INYECTABLE PERFUSION, 4,25 g / 300 g / 5,22 g / 1,54 g / 4,76 g / 1,53 g / 8,76 g / 4,08 g / 5,1 g / 6,2 g / 3,57 g / 3,4 g / 662 mg / 1,02 g / 5,78 g / 5,94 g / 6,16 g / 4,93 g / 17,6 g / 0,34 g / 9,78 gPrincipio activo: combinationsFabricante: Baxter S.L.Requiere receta
Médicos online para SMOFKABIVEN EXTRA NITROGEN SIN ELECTROLITOS EMULSION PARA PERFUSION
Comenta la dosis, los posibles efectos secundarios, interacciones, contraindicaciones o la revisión de receta de SMOFKABIVEN EXTRA NITROGEN SIN ELECTROLITOS EMULSION PARA PERFUSION, sujeto a valoración médica y a la normativa local.
Preguntas frecuentes















