
Смофкабивен Перипгерал

Спросите врача о рецепте на Смофкабивен Перипгерал

Инструкция по применению Смофкабивен Перипгерал
Инструкция, прилагаемая к упаковке: информация для пользователя
СмофКабивен Периферальный, эмульсия для инфузии
Прежде чем использовать препарат, необходимо внимательно ознакомиться с содержанием инструкции, поскольку она содержит
важную информацию для пациента.
- Необходимо сохранить эту инструкцию, чтобы в случае необходимости можно было ее повторно прочитать.
- В случае любых сомнений необходимо обратиться к врачу, фармацевту или медсестре
- Если у пациента出现ы какие-либо нежелательные реакции, включая любые нежелательные реакции, не указанные в этой инструкции, необходимо сообщить об этом врачу, фармацевту или медсестре. См. пункт 4.
Содержание инструкции
- 1. Что такое СмофКабивен Периферальный и для чего он используется
- 2. Важная информация перед использованием препарата СмофКабивен Периферальный
- 3. Как использовать СмофКабивен Периферальный
- 4. Возможные нежелательные реакции
- 5. Как хранить СмофКабивен Периферальный
- 6. Содержание упаковки и другие сведения
1. Что такое СмофКабивен Периферальный и для чего он используется
СмофКабивен Периферальный является эмульсией для инфузии, вводимой пациенту через капельницу (внутривенная инфузия).
Упаковка препарата представляет собой пластиковый мешок, содержащий аминокислоты (необходимые для
синтеза белков), глюкозу (углеводы), жиры (липиды) и соли (электролиты). Препарат может быть
использован у взрослых и детей старше 2 лет.
Препарат СмофКабивен Периферальный вводится квалифицированным медицинским персоналом, если другие методы питания недостаточны или невозможны.
2. Важная информация перед использованием препарата СмофКабивен Периферальный
Не использовать препарат СмофКабивен Периферальный, если у пациента:
- аллергия на активные вещества или на любой из других компонентов этого препарата (перечисленных в пункте 6);
- аллергия на рыбный белок или яйца;
- аллергия на арахис или сою (СмофКабивен Периферальный содержит соевое масло);
- слишком высокая концентрация жиров в крови (гиперлипидемия);
- тяжелые нарушения функции печени;
- проблемы с свертываемостью крови (нарушения свертываемости);
- нарушения обмена аминокислот;
- тяжелая болезнь почек, без возможности проведения диализа;
- острая шоковая реакция;
- неуправляемая, повышенная концентрация глюкозы в крови (гипергликемия);
- повышенная концентрация в крови (сыворотке) любого из электролитов, содержащихся в препарате СмофКабивен Периферальный;
- жидкость в легких (острый отек легких);
- слишком много жидкости в организме (перегидратация);
- необработанная сердечная недостаточность;
- нарушения свертываемости крови (гемофагоцитарный синдром);
- неустойчивое общее состояние, например, тяжелая травма, неуправляемый диабет, острый инфаркт миокарда, инсульт, тромбоз, метаболический ацидоз (нарушение, характеризующееся слишком большим количеством веществ с кислым характером в крови), тяжелая инфекция (тяжелая сепсис), кома, недостаток жидкости (гипотоническая дегидратация). Не следует использовать препарат СмофКабивен Периферальный у детей младше 2 лет.
Предостережения и меры предосторожности
Прежде чем начать использовать препарат СмофКабивен Периферальный, необходимо обсудить это с врачом, если у пациента:
- болезнь почек;
- диабет;
- панкреатит;
- болезнь печени;
- гипотиреоз (нарушения функции щитовидной железы);
- сепсис (тяжелая инфекция).
Если во время инфузии появляется лихорадка, сыпь, отек, затруднение дыхания, озноб, потливость, тошнота или рвота, необходимо немедленно сообщить об этом квалифицированному медицинскому персоналу, поскольку эти симптомы могут быть вызваны аллергической реакцией или введением слишком большой дозы препарата.
Врач может рекомендовать регулярное проведение анализов крови для определения функции печени и других показателей.
Дети и подростки
СмофКабивен Периферальный не предназначен для введения новорожденным или детям младше 2 лет. СмофКабивен Периферальный можно вводить детям в возрасте от 2 до 16/18 лет.
СмофКабивен Периферальный и другие препараты
Необходимо сообщить врачу о всех препаратах, которые пациент принимает в настоящее время или принимал недавно, а также о препаратах, которые пациент планирует принимать, включая те, которые отпускаются без рецепта.
Беременность и грудное вскармливание
Нет данных о использовании препарата СмофКабивен Периферальный во время беременности или в период грудного вскармливания. СмофКабивен Периферальный вводится беременным женщинам или во время грудного вскармливания только в том случае, если врач считает это необходимым. СмофКабивен Периферальный во время беременности и в период грудного вскармливания может быть введен по назначению врача.
Вождение транспортных средств и эксплуатация механизмов
Не применимо, поскольку СмофКабивен Периферальный используется в больнице.
3. Как использовать СмофКабивен Периферальный
Этот препарат должен использоваться всегда в соответствии с рекомендациями врача. В случае сомнений необходимо обратиться к врачу.
Врач выбирает индивидуальную дозу в зависимости от веса и клинического состояния пациента.
СмофКабивен Периферальный вводится только квалифицированным медицинским персоналом.
Использование большей, чем рекомендуемая, дозы препарата СмофКабивен Периферальный
Мало вероятно, что пациент получит слишком большую дозу препарата СмофКабивен Периферальный, поскольку этот препарат вводится квалифицированным медицинским персоналом.
4. Возможные нежелательные реакции
Как и любой препарат, этот препарат может вызывать нежелательные реакции, хотя они не появляются у каждого пациента.
Часто встречающиеся нежелательные реакции(могут появляться не чаще чем у 1 из 10 пациентов): незначительное повышение температуры тела, воспаление поверхностных вен периферии в месте введения.
Нечасто встречающиеся нежелательные реакции(могут появляться не чаще чем у 1 из 100 пациентов): высокая концентрация ферментов печени в крови, отсутствие аппетита, тошнота, рвота, озноб, головокружение и головные боли.
Редко встречающиеся нежелательные реакции(могут появляться не чаще чем у 1 из 1000 пациентов): низкое или высокое кровяное давление, затруднение дыхания, ускоренный сердечный ритм (тахикардия). Реакции повышенной чувствительности (которые могут проявляться такими симптомами, как отек, лихорадка, падение кровяного давления, сыпь на коже, пузырьки (выступающие, красные места), покраснение, головная боль).
Чувство жара и холода. Бледность. Легкая синюшность губ и кожи (связанная с недостатком кислорода в крови).
Боли в шее, спине, костях, груди и пояснице.
Сообщение о нежелательных реакциях
Если появляются какие-либо нежелательные реакции, включая любые нежелательные реакции, не указанные в этой инструкции, необходимо сообщить об этом врачу, фармацевту или медсестре. Нежелательные реакции можно сообщать напрямую в Департамент мониторинга нежелательных реакций лекарственных препаратов Управления регистрации лекарственных препаратов, медицинских изделий и биоцидных продуктов
ул. Аллея Ерозолимских, 181С, 02-222 Варшава
тел.: +48 22 49 21 301, факс: +48 22 49 21 309
веб-сайт: https://smz.ezdrowie.gov.pl
Нежелательные реакции также можно сообщать в организацию, ответственной за выпуск препарата.
Благодаря сообщению о нежелательных реакциях можно будет собрать больше информации о безопасности использования препарата.
5. Как хранить СмофКабивен Периферальный
Препарат должен храниться в месте, недоступном для детей.
Не хранить при температуре выше 25°C. Не замораживать. Хранить в наружном мешке.
Не использовать этот препарат после истечения срока годности, указанного на мешке и картонной коробке. Срок годности указывает последний день указанного месяца.
6. Содержание упаковки и другие сведения
Что содержит СмофКабивен Периферальный
Активными веществами препарата являются:
г на 1000 мл
глюкоза (моногидрат)
аланин
71
4,4
аргинин
3,8
глицин
3,5
гистидин
0,93
изолейцин
1,6
лейцин
2,3
лизин (в виде ацетата)
2,1
метионин
1,3
фенилаланин
1,6
пролин
3,5
серин
2,1
таурин
0,32
треонин
1,4
триптофан
0,63
тирозин
0,12
валин
2,0
хлорид кальция (в виде двуводного соединения)
0,18
глицерофосфат натрия (в виде гидратированного соединения)
1,3
сульфат магния (в виде седмиводного соединения)
0,38
хлорид калия
1,4
ацетат натрия (в виде тригидратированного соединения)
1,1
сульфат цинка (в виде седмиводного соединения)
0,004
очищенное соевое масло
8,5
триглицериды насыщенных жирных кислот со средней длиной цепи
8,5
очищенное оливковое масло
7,0
рыбий жир, богатый омега-3 кислотами
4,2
Другие компоненты (вспомогательные вещества) являются: глицерол, очищенные фосфолипиды из куриного яйца, все-
рак-α-тokoферол, гидроксид натрия (для установления pH), олеинат натрия, уксусная кислота (для установления pH) и вода для инъекций.
Как выглядит СмофКабивен Периферальный и что содержит упаковка
Растворы глюкозы и аминокислот являются прозрачными, бесцветными до слабо желтых, без твердых частиц. Жировая эмульсия является белой и однородной.
Варианты упаковки:
1 × 1206 мл, 4 × 1206 мл
1 × 1448 мл, 4 × 1448 мл
1 × 1904 мл, 4 × 1904 мл
Не все варианты упаковки могут находиться в обращении.
Ответственное лицо и производитель
Ответственное лицо
Fresenius Kabi AB
SE-751 74 Уппсала
Швеция
Производитель
Fresenius Kabi Austria GmbH
Хафнерштрассе 36
8055 Грац
Австрия
Fresenius Kabi AB
SE-751 74 Уппсала
Швеция
Для получения более подробной информации необходимо обратиться к представителю ответственного лица:
Fresenius Kabi Polska Sp. z o.o.
ул. Аллея Ерозолимских, 134
02-305 Варшава
тел.: +48 22 345 67 89
Дата последнего обновления инструкции:01.06.2023 г.
---------------------------------------------------------------------------------------------------------------------------
Информация, предназначенная только для квалифицированного медицинского персонала:
Предостережения и меры предосторожности при использовании
Чтобы избежать опасностей, связанных с инфузией со скоростью, превышающей рекомендуемую, рекомендуется проводить ее непрерывно и под контролем, по возможности с использованием объёмной помпы.
Поскольку использование периферической вены для инфузии связано с повышенным риском инфекции, при установке и обслуживании катетера необходимо тщательно соблюдать правила асептического поведения, чтобы избежать любой инфекции.
Рекомендуется также контролировать концентрацию глюкозы и электролитов в сыворотке, осмолярность, а также баланс жидкости и кислотно-щелочное равновесие, а также проводить ферментативные пробы печени.
В случае появления любых признаков или симптомов анафилактической реакции (таких как лихорадка, озноб, сыпь или затруднение дыхания) необходимо немедленно прекратить инфузию.
Не следует вводить препарат СмофКабивен Периферальный одновременно с кровью в том же инфузионном наборе, из-за риска появления псевдоагглютинации.
При введении инфузии в периферические вены существует возможность появления тромбофлебита. Необходимо ежедневно проверять, не появились ли местные признаки тромбофлебита в месте введения катетера.
Способ введения
Внутривенное введение, инфузия в периферическую или центральную вену.
Чтобы обеспечить полное парентеральное питание, необходимо добавлять к препарату СмофКабивен Периферальный микроэлементы, витамины и, при необходимости, электролиты (учитывая электролиты, уже присутствующие в препарате СмофКабивен Периферальный), в соответствии с потребностями пациента.
Дозирование
Взрослые пациенты
Рекомендуемая доза
Диапазон доз составляет от 20 до 40 мл препарата СмофКабивен Периферальный/кг массы тела/день, что обеспечивает введение от 0,6 до 1,3 г аминокислот/кг массы тела/день (что соответствует от 0,10 до 0,20 г азота/кг массы тела/день) и от 14 до 28 ккал/кг массы тела/день общей энергии (от 11 до 22 ккал/кг массы тела/день энергии, не связанной с белком).
Скорость инфузии
Максимальная скорость инфузии глюкозы составляет 0,25 г/кг массы тела/час, аминокислот 0,1 г/кг массы тела/час, а жиров 0,15 г/кг массы тела/час.
Скорость инфузии не должна превышать 3,0 мл/кг массы тела/час (что соответствует 0,10 г аминокислот, 0,21 г глюкозы и 0,08 г жиров/кг массы тела/час). Рекомендуемое время инфузии составляет от 14 до 24 часов.
Максимальная суточная доза
Максимальная суточная доза зависит от клинического состояния пациента и может меняться даже из дня в день. Рекомендуемая максимальная суточная доза составляет 40 мл/кг массы тела/день.
Дети и подростки
Дети в возрасте 2-11 лет
Рекомендуемая доза
Доза до 40 мл/кг массы тела/день должна быть регулярно корректирована в соответствии с потребностями пациента в детском возрасте, которые различаются намного больше, чем у взрослых пациентов .
Скорость инфузии
Рекомендуемая максимальная скорость инфузии составляет 3,0 мл/ кг массы тела/час (что соответствует 0,10 г аминокислот/кг массы тела/час, 0,21 г глюкозы/кг массы тела/час и 0,08 г жиров/кг массы тела/час).
Рекомендуемое время инфузии составляет от 12 до 24 часов.
За исключением особых случаев, при использовании максимальной рекомендуемой суточной дозы время инфузии должно быть не менее 13 часов, чтобы избежать превышения максимальной скорости инфузии.
Максимальная суточная доза
Максимальная суточная доза является переменной в зависимости от клинического состояния пациента и может меняться даже из дня в день. Максимальная рекомендуемая суточная доза составляет 40 мл/кг массы тела/день.
Подростки в возрасте 12-16/18 лет
У подростков СмофКабивен Периферальный можно вводить как у взрослых пациентов.
Особые меры предосторожности при удалении и подготовке препарата к использованию
Не использовать, если упаковка повреждена.
Использовать только в том случае, если растворы аминокислот и глюкозы являются прозрачными, бесцветными до слабо желтых, а жировая эмульсия является белой и однородной .Содержимое трех отдельных камер необходимо смешать перед использованием, а также перед возможным добавлением других веществ через специальный порт.
После удаления защитных средств необходимо несколько раз перевернуть мешок, чтобы тщательно смешать все компоненты препарата и получить однородную смесь, в которой не должны быть видны признаки разделения фаз.
Использовать только для одноразового использования. Любые неиспользованные остатки препарата, оставшиеся после инфузии, необходимо уничтожить.
Совместимость
Данные о совместимости доступны для препаратов Дипептивен, Аддамель Н/Супливен, Гликофос, Аддифос, Виталипид Н Взрослый/Младенец и Солувит Н в определенных количествах и в электролитах с определенной концентрацией. При добавлении электролитов необходимо учитывать их количества, уже присутствующие в мешке, для удовлетворения клинических потребностей пациента. Доступные данные подтверждают возможность добавления вышеуказанных препаратов в активированный мешок в соответствии с нижеприведенной таблицей:
Диапазон совместимости: стабильный в течение 7 дней, т.е. 6 дней при температуре 2-8 °C, а затем 24 часа при температуре 20-25 °C.
| Единица | Максимальная общая содержание | |||
| Объем мешка СмофКабивен Периферальный | мл | 1206 | 1448 | 1904 |
| Добавка | Объем | |||
| Дипептивен | мл |
|
|
|
| Супливен/Аддамель Н | мл |
|
|
|
| Солувит Н | флакон |
|
|
|
| Виталипид Н Взрослый/Младенец | мл |
|
|
|
| Лимиты электролитов | Количество на мешок | |||
| Натрий | ммоль | ≤ 180 | ≤ 225 | ≤ 300 |
| Калий | ммоль | ≤ 180 | ≤ 225 | ≤ 300 |
| Кальций | ммоль | ≤ 6 | ≤ 7,5 | ≤ 10 |
| Магний | ммоль | ≤ 6 | ≤ 7,5 | ≤ 10 |
| Фосфат неорганический (Аддифос) или фосфат органический (Гликофос) | ммоль | ≤ 18 | ≤ 22,5 | ≤ 30 |
| Цинк | ммоль | ≤ 0,2 | ≤ 0,25 | ≤ 0,3 |
| Селен | мкмоль | ≤ 1 | ≤ 1 | ≤ 1 |
Примечание: эта таблица предназначена для демонстрации совместимости. Она не является руководством по дозированию. Перед назначением вышеуказанных препаратов необходимо ознакомиться с утвержденными инструкциями.
Информация о совместимости с другими добавками, а также сроки хранения различных смесей будут доступны по запросу.
Все добавки необходимо смешивать с препаратом в асептических условиях.
Срок годности после смешивания содержимого камер мешка
Показана физическая и химическая стабильность смешанного содержимого трёхкамерного мешка в течение 48 часов при температуре 20-25 °C. С микробиологической точки зрения препарат необходимо использовать немедленно. В противном случае, за срок хранения во время использования и за условия хранения перед использованием отвечает пользователь. Этот срок не должен превышать 24 часа при температуре 2-8 °C, если смешивание не проводилось в контролируемых и валидированных асептических условиях.
Срок годности после смешивания с дополнительными веществами
Показана физико-химическая стабильность смешанного содержимого трёхкамерного мешка с дополнительными веществами в течение до 7 дней, т.е. 6 дней при температуре 2-8 °C, а затем 24 часа при температуре 20-25 °C, включая время инфузии. С микробиологической точки зрения препарат необходимо использовать немедленно после добавления других компонентов. В противном случае, за срок хранения во время использования и за условия хранения перед использованием отвечает пользователь. Этот срок не должен превышать 24 часа при температуре 2-8 °C, если смешивание не проводилось в контролируемых и валидированных асептических условиях.
СмофКабивен Периферальный. Инструкция по подготовке мешка к использованию
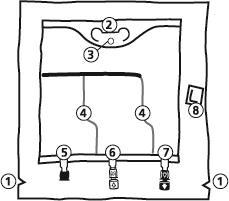
- 1. Надрез в наружном мешке
- 2. Ручка мешка
- 3. Отверстие для подвешивания мешка
- 4. Сварные швы, разделяющие отдельные камеры мешка
- 5. Слепой порт (используется только в производстве)
- 6. Порт для введения дополнительных веществ
- 7. Порт для инфузии
- 8. Поглотитель кислорода
1. Удаление наружного мешка
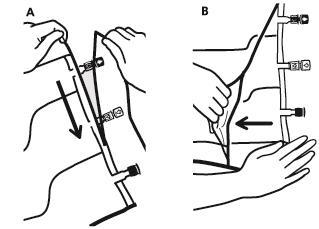 | |
| расположенного возле портов, разрывать вдоль верхнего края (А). | |
| |
| с поглотителем кислорода (Б). | |
2. Смешивание
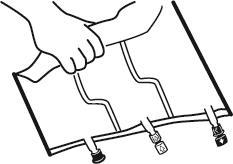
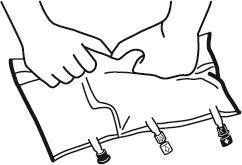
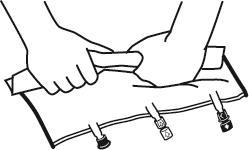
- Положить мешок на плоскую поверхность.
- Начиная с стороны ручки, сильно скрутить мешок в направлении портов, сначала правой рукой, а затем, применяя постоянное давление левой рукой, пока не разорвутся сварные швы. Они открываются под действием давления жидкости. Сварные швы можно также открыть до удаления наружного мешка. Примечание: жидкость смешивается легко, хотя сварной шов остается целым.
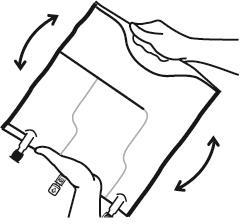
- Перемешать содержимое трех камер, переворачивая мешок три раза, что должно обеспечить тщательное перемешивание компонентов.
3. Окончательные подготовительные действия
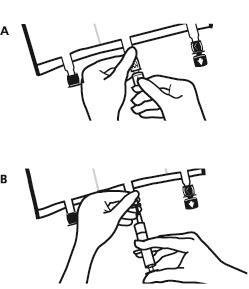
- Снова положить мешок на плоскую, ровную поверхность. Прямо перед введением дополнительных веществ снять метку, указывающую стрелкой, пробку одноразового использования, защищающую белый порт для введения дополнительных веществ (А). Примечание: мембрана порта для введения дополнительных веществ является стерильной.
- Удерживать основу порта для введения дополнительных веществ. Ввести иглу, ввести дополнительные вещества (с известной совместимостью) через центр места для инъекции (Б).
- Перемешать тщательно содержимое мешка после добавления каждого компонента, переворачивая мешок три раза после каждого добавления. Использовать шприцы с иглами диаметром 18-23 Г и длиной не более 40 мм.
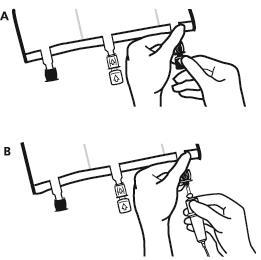
- Прямо перед подключением инфузионного набора снять пробку одноразового использования, защищающую синий порт для инфузии (А). Примечание:мембрана порта для инфузии является стерильной.
- Использовать инфузионные наборы без воздушного клапана или закрыть воздушный клапан.
- Удерживать основу порта для инфузии.
- Ввести иглу инфузионного набора в порт для инфузии. Чтобы обеспечить хорошее крепление иглы, необходимо ввести всю ее длину. Примечание: внутренняя поверхность порта для инфузии является стерильной.
4. Подвешивание мешка
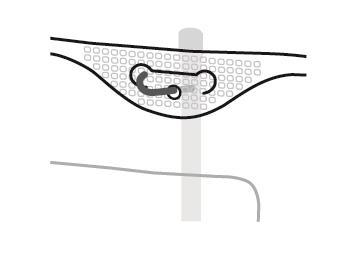 | |
- Подвесить мешок, используя отверстие, расположенное под ручкой.
- Страна регистрации
- Активное вещество
- Требуется рецептНет
- Производитель
- ИмпортерFresenius Kabi AB Fresenius Kabi Austria GmbH
- Информация носит справочный характер и не является медицинской рекомендацией. Перед приемом любых препаратов проконсультируйтесь с врачом. Oladoctor не несет ответственности за медицинские решения, принятые на основе этого контента.
- Аналоги Смофкабивен ПерипгералФорма выпуска: Раствор, -Активное вещество: combinationsНе требуется рецептФорма выпуска: Раствор, -Активное вещество: combinationsНе требуется рецептФорма выпуска: Раствор, -Активное вещество: combinationsНе требуется рецепт
Аналоги Смофкабивен Перипгерал в других странах
Лучшие аналоги с тем же действующим веществом и терапевтическим эффектом.
Аналог Смофкабивен Перипгерал в Испания
Аналог Смофкабивен Перипгерал в Украина
Врачи онлайн по Смофкабивен Перипгерал
Консультация по дозировке, побочным эффектам, взаимодействиям, противопоказаниям и продлению рецепта на Смофкабивен Перипгерал – по решению врача и с учетом местных правил.














