
Цуросурф

Спросите врача о рецепте на Цуросурф

Инструкция по применению Цуросурф
Инструкция, прилагаемая к упаковке: информация для родителей и опекунов
Куросурф, 80 мг/мл, суспензия для интратрахеального и внутрипульмонного введения
(Порактант альфа)
Фракция фосфолипидов из свинных легких
Необходимо внимательно ознакомиться с содержанием инструкции перед применением препарата, поскольку она содержит важную информацию для пациента.
- Необходимо сохранить эту инструкцию, чтобы иметь возможность повторно прочитать ее при необходимости.
- В случае любых сомнений необходимо обратиться к врачу.
- Если у пациента出现ят любые нежелательные реакции, включая любые нежелательные реакции, не указанные в этой инструкции, необходимо сообщить об этом врачу или медсестре. См. пункт 3.
Содержание инструкции:
- 1. Что такое препарат Куросурф и для чего он используется
- 2. Как применять препарат Куросурф
- 3. Возможные нежелательные реакции
- 4. Как хранить препарат Куросурф
- 5. Содержание упаковки и другие сведения
1. ЧТО ТАКОЕ ПРЕПАРАТ КУРОСУРФ И ДЛЯ ЧЕГО ОН ПРИМЕНЯЕТСЯ
Куросурф используется для лечения и профилактики синдрома дыхательной недостаточности (англ. Respiratory
Distress Syndrome: RDS) у новорожденных. У большинства новорожденных в легких присутствует
вещество, называемое сурфактантом (поверхностно-активное вещество). Это вещество покрывает легочные пузырьки, предотвращает их слипание и обеспечивает нормальное дыхание. Однако, некоторые новорожденные,
особенно недоношенные, рождаются с дефицитом сурфактанта, что приводит к развитию RDS. Куросурф
является натуральным сурфактантом, который действует таким же образом, как сурфактант, вырабатываемый новорожденными, и поэтому помогает новорожденным дышать нормально до тех пор, пока они не начнут производить свой
собственный сурфактант.
У новорожденного могут возникнуть другие заболевания, которые могут потребовать другого лечения.
2. КАК ПРИМЕНЯЕТСЯ ПРЕПАРАТ КУРОСУРФ
Дозировка:
Врач выбирает подходящую дозу препарата в зависимости от веса ребенка. Если ребенку вводят Куросурф
для профилактики RDS, препарат необходимо ввести в течение 15 минут после рождения. Если
ребенку вводят Куросурф для лечения RDS, препарат необходимо ввести как можно скорее после диагностики
заболевания. Если ребенку необходимо дополнительное введение препарата Куросурф, его вводят через 12 часов после первого введения. При необходимости через 12 часов можно ввести третью дозу.
Применение препарата Куросурф у недоношенных детей с нарушением функции печени или почек не было изучено.
1
Способ введения препарата:
Куросурф вводится ребенку в инкубаторе врачом или медсестрой. Препарат нагревается до комнатной температуры, а затем вводится с помощью шприца через интубационную трубку в трахею ребенка. Для этого может потребоваться кратковременное отключение ребенка от респиратора.
Может быть также использован метод менее инвазивного введения сурфактанта через тонкий катетер (LISA – анг. Less Invasive Surfactant Administration ).
Куросурф содержит натрий
Препарат содержит менее 1 ммоль (23 мг) натрия в одной ампуле, то есть препарат считается «не содержащим натрия».
3. ВОЗМОЖНЫЕ НЕЖЕЛАТЕЛЬНЫЕ РЕАКЦИИ
Как и любой препарат, Куросурф может вызывать нежелательные реакции, хотя они не возникают у каждого пациента. Возможные нежелательные реакции перечислены ниже в зависимости от частоты их возникновения:
В случае сомнений относительно нежелательных реакций необходимо обратиться к врачу.
Не очень часто(встречаются у менее 1 из 100
пациентов):
Редко(встречаются у менее 1 из 1000
пациентов):
- инфекция
- кровоизлияние в мозг
- воздух в грудной полости
- замедление сердечной деятельности
- низкое кровяное давление
- хроническое заболевание легких
- снижение уровня кислорода в организме
Кроме того, были зарегистрированы следующие нежелательные реакции:
- повышение уровня кислорода в организме
- синюшная окраска кожи или слизистых оболочек из-за недостатка кислорода
- затруднение дыхания
- осложнения, связанные с введением трубок в легкие
- понижение мозговой активности
Во время введения препарата Куросурф через тонкий катетер были зарегистрированы некоторые легкие и кратковременные нежелательные реакции: брадикардия, апноэ, снижение насыщения крови кислородом, пена на губах, кашель, удушение и чихание.
Сообщение о нежелательных реакциях
Если возникают любые нежелательные реакции, включая любые нежелательные реакции, не указанные в инструкции, необходимо сообщить об этом врачу, фармацевту или медсестре.
Нежелательные реакции можно сообщать trực tiếp в Департамент мониторинга нежелательных реакций лекарственных препаратов Управления по регистрации лекарственных препаратов, медицинских изделий и биоцидных продуктов, ул. Ерозолимские 181С, 02-222 Варшава,
тел.: + 48 22 49 21 301, факс: + 48 22 49 21 309, эл. почта: [email protected] .
Нежелательные реакции можно также сообщать в организацию, ответственной за выпуск препарата.
Благодаря сообщению о нежелательных реакциях можно будет собрать больше информации о безопасности применения препарата.
повреждением легких
2
4. КАК ХРАНИТЬ ПРЕПАРАТ КУРОСУРФ
- Препарат необходимо хранить в месте, недоступном для детей.
- Хранить в холодильнике при температуре от 2°C до 8°C, хранить в оригинальной упаковке для защиты от света. Перед введением ребенку необходимо нагреть до комнатной температуры.
- Неоткрытые и неиспользованные ампулы препарата Куросурф, которые были нагреты до комнатной температуры, можно хранить в холодильнике в течение 24 часов для последующего использования. Препарат не следует нагревать до комнатной температуры и хранить в холодильнике более одного раза.
- Не использовать препарат после истечения срока годности, указанного на упаковке и ампуле. Срок годности указывает последний день месяца.
- Одну упаковку необходимо использовать один раз, а остатки выбросить. Больница должна обеспечить безопасное утилизацию неиспользованных остатков Куросурф.
- Препараты не следует выбрасывать в канализацию. Необходимо спросить у фармацевта, как утилизировать препараты, которые больше не используются. Такое поведение поможет защитить окружающую среду
5. СОДЕРЖАНИЕ УПАКОВКИ И ДРУГИЕ СВЕДЕНИЯ
Что содержит препарат Куросурф
- -Активным веществом является смесь липидов и белков, полученных из легких свиней.
- Другими компонентами являются: хлорид натрия, вода для инъекций, гидрокарбонат натрия (для регулирования pH).
Как выглядит препарат Куросурф и что содержит упаковка
Препарат Куросурф представляет собой стерильную суспензию. Он выпускается в одноразовых стеклянных ампулах объемом 5 мл, содержащих 1,5 мл (120 мг) или
3 мл (240 мг) фракции фосфолипидов, полученных из легких свиней. В 1 мл стерильной суспензии содержится 80 мг фракции фосфолипидов из легких свиней. В одной упаковке содержится 2 ампулы по 1,5 мл суспензии или 1 ампула по 3 мл суспензии препарата Куросурф.
Не все размеры упаковок могут находиться в обращении.
Ответственное лицо:
Chiesi Farmaceutici S.p.A, Via Palermo 26/A, 43 122 Парма, Италия.
Производитель:
Chiesi Farmaceutici S.p.A, Via San Leonardo 96 - Via Palermo 26/A, 43 122 Парма, Италия.
Chiesi Pharmaceuticals GmbH, Gonzagagasse 16/16, A-1010 Вена, Австрия.
Для получения более подробной информации необходимо обратиться к представителю ответственного лица в Польше:
Chiesi Poland Sp. z o.o., Ал. Ерозолимские 134, 02-305 Варшава
тел.: (22) 620 14 21, факс: (22) 652 37 79, эл. почта: [email protected]
Дата последнего обновления инструкции:
Просим прочитать информацию на обратной стороне инструкции
-------------------------------------------------------------------------------------------------------------------------
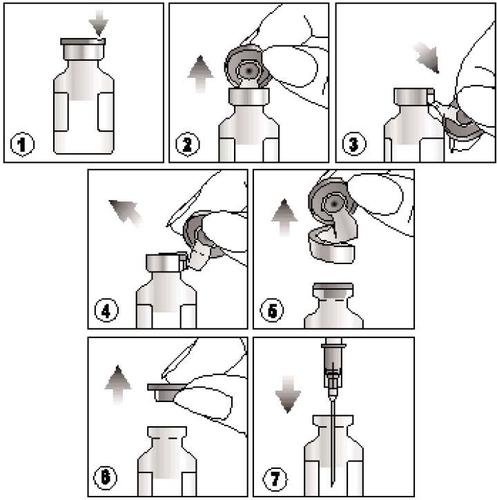
Как получить продукт?

3
- 1) Найти разрез на цветном пластиковом колпаче,
- 2) Поднять колпачок в месте разреза и потянуть его вверх,
- 3) Потянуть вниз пластиковую часть колпачка вместе с его алюминиевой частью,
- 4) и 5) Удалить весь колпачок, сняв алюмининое кольцо
- 6) и 7) Снять резиновую пробку перед извлечением содержимого ампулы.
Для одноразового использования. Неиспользованную суспензию, оставшуюся в ампуле, необходимо выбросить.
Не хранить неиспользованную суспензию для повторного использования.
Все остатки неиспользованного продукта или его отходы необходимо утилизировать в соответствии с правилами.
4
- Страна регистрации
- Активное вещество
- Требуется рецептНет
- Производитель
- ИмпортерChiesi Farmaceutici S.p.A. Chiesi Pharmaceuticals GmbH
- Информация носит справочный характер и не является медицинской рекомендацией. Перед приемом любых препаратов проконсультируйтесь с врачом. Oladoctor не несет ответственности за медицинские решения, принятые на основе этого контента.
- Аналоги ЦуросурфФорма выпуска: Суспензия, 80 мг/млАктивное вещество: natural phospholipidsНе требуется рецептФорма выпуска: Суспензия, 80 мг/млАктивное вещество: natural phospholipidsНе требуется рецептФорма выпуска: Пастилки, 1500 мг + 125 мгАктивное вещество: НикетамидПроизводитель: Przedsiębiorstwo Produkcyjno-Handlowe EWA S.A.Не требуется рецепт
Аналоги Цуросурф в других странах
Лучшие аналоги с тем же действующим веществом и терапевтическим эффектом.
Аналог Цуросурф в Украина
Аналог Цуросурф в Испания
Врачи онлайн по Цуросурф
Консультация по дозировке, побочным эффектам, взаимодействиям, противопоказаниям и продлению рецепта на Цуросурф – по решению врача и с учетом местных правил.














