

ELYMBUS 0,1 mg/g GEL OFTÁLMICO EM EMBALAGEM UNIDOSE

Pergunte a um médico sobre a prescrição de ELYMBUS 0,1 mg/g GEL OFTÁLMICO EM EMBALAGEM UNIDOSE

Como usar ELYMBUS 0,1 mg/g GEL OFTÁLMICO EM EMBALAGEM UNIDOSE
Introdução
PROSPECTO
Prospecto:informação para o paciente
Elymbus 0,1 mg/g gel oftálmico em envase unidose
bimatoprost
Leia todo o prospecto detenidamente antes de começar a usar este medicamento,porque contém informações importantes para si.
- Conserva este prospecto, pois pode ter que voltar a lê-lo.
- Se tiver alguma dúvida, consulte o seu médico ou farmacêutico.
- Este medicamento foi prescrito apenas para si, e não deve dá-lo a outras pessoas, mesmo que tenham os mesmos sintomas que si, pois pode prejudicá-las.
- Se experimentar efeitos adversos, consulte o seu médico ou farmacêutico, mesmo que se trate de efeitos adversos que não aparecem neste prospecto. Ver seção 4.
Conteúdo do prospecto
- O que é Elymbus e para que se utiliza
- O que precisa saber antes de começar a usar Elymbus
- Como usar Elymbus
- Possíveis efeitos adversos
5 Conservação de Elymbus
- Conteúdo do envase e informação adicional
1. O que é Elymbus e para que se utiliza
Elymbus é um medicamento para o glaucoma. Elymbus pertence a um grupo de medicamentos chamados prostamidas.
Elymbus gel oftálmico se utiliza para reduzir a pressão elevada do olho em adultos. Este medicamento pode ser usado sozinho ou com outros colírios chamados betabloqueantes que também reduzem a pressão.
O olho contém um líquido transparente, aquoso, que mantém a parte interior do olho. Este líquido se drena continuamente para fora do olho e se gera novo líquido para substituí-lo. Se o líquido não se drena com a suficiente velocidade, aumenta a pressão dentro do olho. Este medicamento actua aumentando o drenagem do líquido. Isso reduz a pressão dentro do olho. Se esta pressão não se reduz, poderia provocar uma doença denominada glaucoma e danificar a sua visão.
2. O que precisa saber antes de começar a usar Elymbus
Não use Elymbus:
- Se é alérgico ao bimatoprost ou a algum dos outros componentes deste medicamento (incluídos na seção 6).
Advertências e precauções
Consulte o seu médico ou farmacêutico antes de começar a usar Elymbus.
Consulte o seu médico se:
- tem algum problema respiratório.
- tem problemas de fígado ou rins.
- teve uma cirurgia de catarata no passado.
- apresenta ou apresentou uma tensão arterial baixa ou uma frequência cardíaca baixa.
- teve uma infecção viral ou inflamação do olho.
Durante o tratamento, Elymbus pode provocar uma perda de gordura ao redor do olho que pode causar aprofundamento do sulco palpebral, afundamento dos olhos (enoftalmos), queda das pálpebras superiores (ptose), estiramento da pele ao redor do olho (involução da dermatocalase) e que a parte branca inferior do olho se torne mais visível (exposição escleral inferior). As alterações são geralmente leves, mas se se acentuarem, podem afetar o seu campo de visão. As alterações podem desaparecer se deixar de usar Elymbus. Elymbus também pode causar escurecimento e crescimento das pestanas, bem como escurecimento da pele ao redor da pálpebra. Pode escurecer o tom do íris. Estas alterações podem ser permanentes e mais visíveis se apenas estiver a tratar um olho.
Crianças e adolescentes
Elymbus não foi estudado em menores de 18 anos e, por conseguinte, não deve ser utilizado em pacientes com menos de 18 anos de idade.
Outros medicamentos e Elymbus
Informa o seu médico ou farmacêutico se está a utilizar, utilizou recentemente ou pode ter que utilizar qualquer outro medicamento.
Gravidez, lactação e fertilidade
Se está grávida ou em período de lactação, acredita que possa estar grávida ou tem intenção de engravidar, consulte o seu médico ou farmacêutico antes de utilizar este medicamento.
Elymbus pode passar para o leite materno, por conseguinte, não deve utilizá-lo se estiver em período de lactação.
Condução e uso de máquinas
Após a aplicação de Elymbus, pode aparecer visão borrosa durante um curto período de tempo. Não conduza nem use máquinas até ver com clareza.
3. Como usar Elymbus
Siga exatamente as instruções de administração deste medicamento indicadas pelo seu médico ou farmacêutico. Em caso de dúvida, pergunte ao seu médico ou farmacêutico.
Elymbus deve ser utilizado apenas no olho. A dose recomendada é uma gota em cada olho que precise tratamento, uma vez ao dia, à noite.
Se utilizar Elymbus com outra medicação ocular, deve administrá-la pelo menos 15 minutos antes que Elymbus. Elymbus deve ser usado por último.
Não utilize o medicamento mais de uma vez ao dia, pois pode reduzir-se a eficácia do tratamento.
Utilizadores de lentes de contacto
Se utiliza lentes de contacto, deve retirá-las antes de utilizar Elymbus. Após a aplicação de Elymbus, deve esperar 15 minutos antes de voltar a colocar as lentes de contacto.
Instruções de uso
Este medicamento deve ser administrado no olho.
Siga estas instruções para utilizar o colírio:
- Lave as mãos e sente-se ou permaneça confortavelmente de pé.
- Abra o sobro que contém 10 envases unidose.
- Separe um envase unidose da tira.
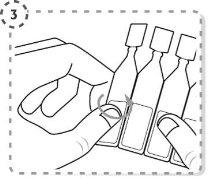
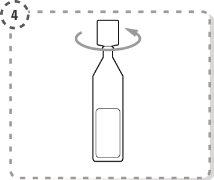
- Gire a ponta do envase unidose tal como se mostra. Não toque a ponta após abrir o envase.
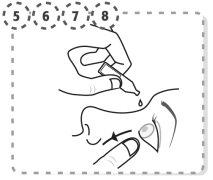
- Utilize o seu dedo para separar suavemente a pálpebra inferior do olho afetado.
- Incline a cabeça para trás e olhe para o teto.
- Coloque a ponta do envase unidose perto do olho, mas sem chegar a tocá-lo.
- Pressione suavemente o envase unidose de forma que caia uma gota no olho e, em seguida, retire o dedo da pálpebra inferior.
- Repita a operação no outro olho, se o seu médico o indicou. Cada envase unidose contém quantidade suficiente para os dois olhos.
- Solte a pálpebra inferior e feche os olhos durante um momento.
- Limpe qualquer excesso que corra pela bochecha. Se uma gota não atingir o olho, tente novamente.
- Elimine o envase unidose após utilizá-lo. Não o guarde para utilizá-lo novamente. Como não se pode garantir a esterilidade do envase unidose após a abertura (gel oftálmico sem conservantes), deve abrir um novo envase antes de cada uso.
- Limpe qualquer excesso de líquido com um pano limpo.
- Coloque os envases unidose não abertos dentro do sobro. Os envases não abertos devem ser utilizados em 1 mês após a abertura do sobro.
Se usar mais Elymbus do que deve
Se aplicou mais gotas no olho do que deve, é improvável que isso lhe cause algum dano sério. Aplique a próxima dose à hora habitual. Se estiver preocupado, fale com o seu médico ou farmacêutico.
Em caso de sobredosagem ou ingestão acidental, consulte imediatamente o seu médico ou farmacêutico ou ligue para o Serviço de Informação Toxicológica, telefone: 91 562 04 20, indicando o medicamento e a quantidade ingerida.
Se esqueceu de usar Elymbus
Se esqueceu de aplicar Elymbus, use uma única gota assim que se lembrar e, em seguida, volte à sua rotina habitual. Não aplique uma dose dupla para compensar a dose esquecida.
Se interromper o tratamento com Elymbus
Elymbus deve ser usado todos os dias para que funcione bem. Se deixar de usar Elymbus, a pressão no interior do olho pode aumentar, por isso, consulte com o seu médico antes de interromper o tratamento.
Se tiver alguma outra dúvida sobre o uso deste medicamento, pergunte ao seu médico ou farmacêutico.
4. Possíveis efeitos adversos
Como todos os medicamentos, este medicamento pode produzir efeitos adversos, embora nem todas as pessoas os sofram.
Os seguintes efeitos adversos podem ocorrer com Elymbus:
Efeitos adversos frequentes
Podem afetar até 1 de cada 10 pessoas
Que afetam o olho
- Leve rubor
- Dor ocular
- Irritação ocular
- Rubor e incômodo ocular
- Sensação de ter algo no olho
- Secura ocular
- Coceira ocular
- Dificuldade temporária para ver com clareza
Efeitos adversos pouco frequentes
Podem afetar até 1 de cada 100 pessoas
Que afetam o olho
- Pequenas erosões epiteliais no olho, com ou sem inflamação
- Sensações como adormecimento, formigamento e sensação de picadas no olho
- Pálpebras inflamadas
- Perda de pestanas
- Pestanas mais longas
- Sensibilidade à luz
- Aumento de lágrimas
- Pestanas mais escuras
- Cor da pálpebra mais escuro
- Inchaço da pálpebra
- Pele das pálpebras seca, vermelha e com coceira
Que afetam o corpo
- Tontura
Foram observados os seguintes efeitos adversos com bimatoprost colírio em solução (0,1 mg/ml, formulação com conservantes):
Efeitos adversos muito frequentes
Podem afetar mais de 1 de cada 10 pessoas
Que afetam o olho
- Leve rubor (até 29% das pessoas)
- Perda de gordura na região do olho que pode causar aprofundamento do sulco palpebral, afundamento dos olhos (enoftalmos), queda das pálpebras (ptose), estiramento da pele ao redor do olho (involução da dermatocalase) e que a parte branca inferior do olho se torne mais visível (exposição escleral inferior).
Efeitos adversos frequentes
Podem afetar até 1 de cada 10 pessoas
Que afetam o olho
- Pequenas erosões epiteliais no olho, com ou sem inflamação
- Irritação
- Coceira nos olhos
- Pestanas mais longas
- Irritação ao instilar a gota no olho
- Dor ocular
Que afetam a pele
- Pálpebras vermelhas e com coceira
- Pele de cor mais escura ao redor do olho.
- Crescimento do pelo ao redor do olho.
Efeitos adversos pouco frequentes
Podem afetar até 1 de cada 100 pessoas
Que afetam o olho
- Cor mais escuro do íris
- Cansaço ocular
- Inflamação da superfície do olho
- Visão borrosa
- Perda das pestanas
Que afetam a pele
- Secura cutânea
- Descamação do bordo palpebral
- Inchaço da pálpebra
- Coceira
Que afetam o corpo
- Dor de cabeça
- Sensação de mal-estar
Efeitos adversos de frequência não conhecida
Que afetam o olho
- Edema macular (inflamação da retina na parte posterior do olho que pode dar lugar a um agravamento da visão)
- Pálpebra mais escura
- Secura
- Olhos pegajosos
- Sensação de corpo estranho no olho
- Inflamação do olho
- Aumento das lágrimas
- Incômodos oculares
- Sensibilidade à luz
Que afetam o corpo
- Asma
- Piora da asma
- Piora da doença pulmonar denominada doença pulmonar obstructiva crônica (DPOC)
- Dificuldade para respirar
- Sintomas de reação alérgica (inflamação, rubor do olho e erupção na pele)
- Tontura
- Pressão arterial elevada
- Descoloração da pele (periocular)
Além dos efeitos adversos descritos anteriormente, foram observados os seguintes efeitos adversos com outro medicamento que contém uma maior concentração de bimatoprost (0,3 mg/ml):
- Queimadura ocular
- Uma reação alérgica no olho
- Pálpebras inflamadas
- Dificuldade para ver com clareza
- Piora da visão
- Inflamação da camada transparente que cobre o olho
- Lágrimas
- Pestanas mais escuras
- Hemorragia retiniana
- Inflamação no interior do olho
- Edema macular cístico (inflamação da retina no interior do olho que dá lugar a um agravamento da visão)
- Fasciculações da pálpebra
- A pálpebra se contraiu afastando-se da superfície do olho
- Rubor cutâneo ao redor do olho
- Fraqueza
- Um aumento nos resultados dos exames de sangue que mostram atividade hepática
Comunicação de efeitos adversos
Se experimentar qualquer tipo de efeito adverso, consulte o seu médico ou farmacêutico, mesmo que se trate de possíveis efeitos adversos que não aparecem neste prospecto. Também pode comunicá-los diretamente através do Sistema Espanhol de Farmacovigilância de Medicamentos de Uso Humano: https://www.notificaram.es. Mediante a comunicação de efeitos adversos, você pode contribuir para fornecer mais informações sobre a segurança deste medicamento.
5. Conservação de Elymbus
Mantenha este medicamento fora da vista e do alcance das crianças.
Não utilize este medicamento após a data de validade que aparece na caixa, sobre e envases unidose após CAD. A data de validade é o último dia do mês que se indica.
Este medicamento não requer condições especiais de temperatura para a sua conservação.
Após a primeira abertura do sobro:utilize os envases unidose em 1 mês.
Para ajudá-lo a lembrar, escreva a data de primeira abertura do sobro.
Guarde os envases unidose não utilizados dentro do sobro aberto para protegê-los da luz.
Após a primeira abertura do envase unidose:utilize imediatamente e elimine o envase unidose após utilizá-lo.
Os medicamentos não devem ser jogados nos esgotos nem na lixeira. Deposite os envases e os medicamentos que não precisa no Ponto SIGRE da farmácia. Em caso de dúvida, pergunte ao seu farmacêutico como se livrar dos envases e dos medicamentos que não precisa. Dessa forma, você ajudará a proteger o meio ambiente.
6. Conteúdo do envase e informação adicional
Composição de Elymbus
O princípio ativo é bimatoprost. Cada g de gel contém 0,1 mg de bimatoprost.
Os outros componentes são: sorbitol, carbômero, trihidrato de acetato de sódio, macrogol, hidróxido de sódio (ajuste do pH), água para preparações injetáveis.
Aspecto do produto e conteúdo do envase
Elymbus é um gel oftálmico incolor opalescente em envase unidose. Apresenta-se em envases unidose dentro de um sobro com 10 unidades.
Cada envase unidose contém 0,3 g de produto.
As caixas contêm 10, 30 (3 sobros com 10) ou 90 (9 sobros com 10) envases unidose.
Pode ser que apenas alguns tamanhos de envases estejam comercializados.
Titular da autorização de comercialização e responsável pela fabricação
Titular da autorização de comercialização
Laboratoires THEA
12, rue Louis Blériot
63100 CLERMONT-FERRAND
França
Fabricante
LABORATOIRE UNITHER
1 rue de l’Arquerie
50200 Coutances
França
Pode solicitar mais informações sobre este medicamento dirigindo-se ao representante local do titular da autorização de comercialização:
LABORATORIOS THEA, S.A.
C/ Enric Granados nº 86-88, 2ª planta
08008 Barcelona
Espanha
Este medicamento está autorizado nos estados membros do Espaço Econômico Europeu com os seguintes nomes:
Alemanha, Áustria, Bélgica, Bulgária, Chipre, Croácia, Dinamarca, Eslováquia, Eslovênia, Espanha, Estônia, Finlândia, Grécia, Holanda, Hungria, Irlanda, Islândia, Itália, Letônia, Lituânia, Luxemburgo, Noruega, Polônia, Portugal, República Checa, Romênia, Suécia……………………………………………………………………………… Elymbus
França……………………………………………………………………………...Elumibus
Data da última revisão desteprospecto: maio 2023
A informação detalhada deste medicamento está disponível na página web da Agência Espanhola de Medicamentos e Produtos Sanitários (AEMPS) http://www.aemps.gob.es/.
- País de registo
- Substância ativa
- Requer receita médicaSim
- Fabricante
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a ELYMBUS 0,1 mg/g GEL OFTÁLMICO EM EMBALAGEM UNIDOSEForma farmacêutica: COLÍRIO, 0.3 mg/mlSubstância ativa: bimatoprostFabricante: Tiedra Farmaceutica S.L.Requer receita médicaForma farmacêutica: COLÍRIO, 0.3 mg/mlSubstância ativa: bimatoprostFabricante: Sifi S.P.A.Requer receita médicaForma farmacêutica: COLÍRIO, 0,3 mg/mlSubstância ativa: bimatoprostFabricante: Laboratorio Stada S.L.Requer receita médica
Alternativas a ELYMBUS 0,1 mg/g GEL OFTÁLMICO EM EMBALAGEM UNIDOSE noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a ELYMBUS 0,1 mg/g GEL OFTÁLMICO EM EMBALAGEM UNIDOSE em Polónia
Alternativa a ELYMBUS 0,1 mg/g GEL OFTÁLMICO EM EMBALAGEM UNIDOSE em Ukraine
Médicos online para ELYMBUS 0,1 mg/g GEL OFTÁLMICO EM EMBALAGEM UNIDOSE
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de ELYMBUS 0,1 mg/g GEL OFTÁLMICO EM EMBALAGEM UNIDOSE – sujeita a avaliação médica e regras locais.














