
BERINERT 500 UI PÓ E SOLVENTE PARA SOLUÇÃO INJETÁVEL E PARA PERFUSÃO

Pergunte a um médico sobre a prescrição de BERINERT 500 UI PÓ E SOLVENTE PARA SOLUÇÃO INJETÁVEL E PARA PERFUSÃO

Como usar BERINERT 500 UI PÓ E SOLVENTE PARA SOLUÇÃO INJETÁVEL E PARA PERFUSÃO
Introdução
Prospecto: informação para o utilizador
Berinert 500 UI
Pó e dissolvente para solução injectável e para perfusão.
Inibidor da C1 esterase humano
Leia todo o prospecto atentamente antes de começar a usar este medicamento.
- Conserva este prospecto, pois pode ter que voltar a lê-lo.
- Se tiver alguma dúvida, consulte o seu médico ou farmacêutico.
- Este medicamento foi prescrito apenas para si e não deve dá-lo a outras pessoas, mesmo que tenham os mesmos sintomas que o senhor, pois pode prejudicá-las.
- Se experimentar efeitos adversos, consulte o seu médico ou farmacêutico, mesmo que se trate de efeitos adversos que não aparecem neste prospecto. Ver secção 4.
Conteúdo do prospecto
- O que é Berinert e para que é utilizado
- O que precisa saber antes de começar a usar Berinert
- Como usar Berinert
- Possíveis efeitos adversos
- Conservação de Berinert
- Conteúdo do envase e informação adicional
1. O que é Berinert e para que é utilizado
O que é Berinert?
Berinert apresenta-se como pó e dissolvente. A solução preparada deve ser administrada por injeção ou perfusão numa veia.
Berinert é preparado a partir de plasma humano (a parte líquida do sangue), o princípio ativo é a proteína inibidora da C1 esterase humana, obtida a partir do plasma.
Para que é utilizado Berinert?
Berinert é utilizado para o tratamento e prevenção pré-operatória do angioedema hereditário de tipo I e II (AEH, edema = inchação). O angioedema hereditário é uma doença congénita do sistema vascular. AEH não é uma doença alérgica. AEH é causado por uma síntese insuficiente, ausente ou defeituosa do inibidor da C1 esterase, que é uma proteína importante. A doença caracteriza-se pelos seguintes sintomas:
- inchação súbita das mãos e pés,
- inchação súbita da face com sensação de tensão,
- inchação das pálpebras, lábios, possível inchação da laringe (órgão da voz) com dificuldades respiratórias,
- inchação da língua,
- dor de tipo cólico na região abdominal.
Geralmente, todas as partes do corpo podem ser afetadas.
2. O que precisa saber antes de começar a usar Berinert
As secções seguintes contêm informação que o seu médico deve ter em consideração antes de administrar-lhe Berinert.
Não use Berinert:
- Se é alérgico ao inibidor da C1 esterase ou a qualquer um dos outros componentes deste medicamento (incluídos na secção 6).
Informa ao seu médico ou farmacêutico se é alérgico a algum medicamento ou a algum alimento.
Advertências e precauções
- Se sofreu reações alérgicas a Berinert no passado. Deve tomar antihistamínicos e corticosteroides como profilaxia, se for aconselhado pelo seu médico.
- Quando ocorrerem reações alérgicas ou anafilácticas (reação alérgica grave que produz graves dificuldades respiratórias ou tonturas). A administração de Berinert deve ser interrompida imediatamente (por exemplo, interrompendo a perfusão).
- Se sofre inchação na laringe (edema de laringe). Deve ser supervisionado cuidadosamente e ter tratamento de urgência pronto para ser usado.
- Durante o uso para o tratamento de indicações e posologias para as quais o medicamento não foi aprovado (por exemplo, o Síndrome de extravasação capilar, SEC). Ver a secção 4. "Possíveis efeitos adversos".
O seu médico sopesará minuciosamente o benefício do tratamento com Berinert comparando com o risco de padecer estas complicações.
Segurança vírica
Quando se administram medicamentos derivados do sangue ou plasma humanos, há que levar a cabo certas medidas para evitar que as infecções passem aos pacientes. Tais medidas incluem:
- selecção cuidadosa dos doadores de sangue e plasma para excluir aqueles que estão em risco de ser portadores de doenças infecciosas, e
- análise de marcadores específicos de vírus e infecções nas doações individuais e nas misturas de plasma,
Os fabricantes destes produtos também incluem etapas no processamento do sangue ou plasma para eliminar ou inativar vírus. Apesar disto, quando se administram medicamentos derivados do sangue ou plasma humanos, a possibilidade de transmissão de agentes infecciosos não pode ser excluída totalmente. Isto também se refere a vírus emergentes ou de natureza desconhecida ou outro tipo de infecções.
As medidas aplicadas consideram-se eficazes para os vírus envoltos, tais como o vírus de imunodeficiência humano (VIH, o vírus da SIDA), o vírus da hepatite B, o vírus da hepatite C (inflamação do fígado) e para vírus não envoltos, como o vírus da hepatite A (inflamação do fígado) e o parvovirus B19.
É possível que o seu médico lhe recomende a vacinação contra a hepatite A e B se o senhor se tratar periodicamente/repetidamente com medicamentos derivados do plasma humano.
Recomenda-se encarecidamente que cada vez que se administre Berinert, o seu médico registe a data de administração, o número do lote e o volume injetado.
Uso de Berinert com outros medicamentos
- Informa ao seu médico ou farmacêutico se está utilizando, utilizou recentemente ou possa ter que utilizar qualquer outro medicamento, mesmo os medicamentos sem receita.
- Berinert não deve ser misturado com outros medicamentos e diluentes na mesma seringa ou equipamento de perfusão.
Gravidez e lactação
- Se está grávida ou em período de lactação, acredita que possa estar grávida ou tem intenção de engravidar, consulte o seu médico ou farmacêutico antes de utilizar este medicamento.
- Durante a gravidez e a lactação, Berinert apenas deve ser utilizado se estiver claramente indicado.
Condução e uso de máquinas
A influência de Berinert sobre a capacidade para conduzir e usar máquinas é nula ou insignificante.
Berinert contém sódio
Berinert contém até 49 mg de sódio (componente principal do sal de mesa/para cozinhar) em cada frasco. Isto equivale a 2,5% da ingestão diária máxima de sódio recomendada para um adulto.
3. Como usar Berinert
O tratamento deve ser iniciado e supervisionado por um médico com experiência no tratamento da deficiência do inibidor da C1 esterase.
Posologia
Adultos
Tratamento de ataques de angioedema agudo:
20 UI por quilograma de peso corporal (20 UI/kg de p.c.).
Prevenção pré-operatória de ataques de angioedema agudo:
1000 UI antes de 6 horas de uma intervenção médica, dental ou cirúrgica.
População pediátrica
Tratamento de ataques de angioedema agudo:
20 UI por quilograma de peso corporal (20 UI/kg de p.c.).
Prevenção pré-operatória de ataques de angioedema agudo:
De 15 a 30 UI por quilograma de peso corporal (15-30 UI/kg de p.c.) antes de 6 horas de uma intervenção médica, dental ou cirúrgica. A dose deve ser escolhida tendo em conta as circunstâncias clínicas (por exemplo, o tipo de intervenção e a severidade da doença).
Se usa mais Berinert do que deve
Não foram descritos casos de sobredosagem.
Reconstituição e forma de administração
Berinert é injetado numa veia (administração intravenosa), habitualmente pelo seu médico ou enfermeira. O senhor ou o seu cuidador também podem injetar Berinert, mas apenas após receberem uma formação adequada. Se o seu médico decidir que o senhor pode tratar-se em casa, ele dar-lhe-á instruções detalhadas. Ser-lhe-á entregue um diário onde anotará cada injeção administrada em casa, que o senhor levará consigo cada vez que visitar o médico. Será revisto regularmente a si ou ao seu cuidador como administram as injeções para assegurar que o fazem corretamente ao longo do tempo.
Instruções gerais
- O pó deve ser dissolvido e extraído do frasco sob condições assépticas. Utilize a seringa fornecida com o produto.
- A solução preparada deve ser transparente e clara. Depois de filtrar ou trasvasar a solução (consulte mais adiante), deve ser verificada visualmente que a solução não contenha partículas nem apresente decoloração antes de administrá-la.
- Não use a solução se estiver visivelmente turva ou se contiver partículas ou resíduos.
- Qualquer quantidade do medicamento que não tenha sido usada ou qualquer material residual deve ser eliminada de acordo com a regulamentação local e seguindo as instruções do seu médico.
Reconstituição
Antes de abrir qualquer frasco, tempere o pó Berinert e o dissolvente até que estejam à temperatura ambiente. Para consegui-lo, pode deixar os frascos à temperatura ambiente durante aproximadamente uma hora ou bem pode tê-los nas mãos fechadas durante alguns minutos. NÃO exponha os frascos ao calor direto. Os frascos não devem ser aquecidos a uma temperatura superior à do corpo (37 °C).
Retire com cuidado as cápsulas protectoras do frasco do dissolvente e do frasco com o pó. Limpe os tampões de borracha expostos de ambos os frascos com uma toalhita impregnada em álcool e deixe-os secar. Agora pode transferir o dissolvente para o frasco do pó com o sistema de administração incluído (Mix2Vial). Por favor, siga as instruções seguintes:
|
|
|
|
|
|
|
|
|
Elimine o frasco do dissolvente com o adaptador azul do Mix2Vial acoplado. |
|
|
|
|
Transvasamento da solução reconstituída para a seringa e administração
8 |
|
9 |
|
Administração
A solução deve ser administrada por via intravenosa (v. i.) lenta, bem por injeção, bem por perfusão (4 ml/minuto).
4. Possíveis efeitos adversos
Como todos os medicamentos, este medicamento pode produzir efeitos adversos, embora nem todas as pessoas os sofram.
Entre em contacto imediatamente com o seu médico
- se produzir qualquer efeito adverso ou
- se notar qualquer efeito adverso não mencionado neste prospecto.
Os efeitos adversos com Berinert são raros.
Os efeitos adversos seguintes foram observados raramente (entre 1 e 10 de cada 10.000 pessoas/pacientes):
? Há um maior risco de trombose (formação de coágulos de sangue) em tentativas de tratamento profilático ou terapêutico do Síndrome de extravasação capilar (saída de fluido dos vasos sanguíneos pequenos para os tecidos), por exemplo, durante e após cirurgia cardíaca com circulação extracorpórea. Ver a secção 2.“Advertências e precauções”.
- Aumento da temperatura corporal, assim como queimadura e picadura no local onde foi administrada a injeção.
- Reações de hipersensibilidade ou alérgicas (como por exemplo frequência cardíaca irregular, o coração bate mais rápido, queda da pressão sanguínea, rubor da pele, exantema, dificuldades respiratórias, dor de cabeça, tonturas, sentir-se doente).
Em casos muito raros (menos de 1 de cada 10.000 pacientes/pessoas ou casos isolados) as reações alérgicas podem chegar ao choque.
Comunicação de efeitos adversos
Se experimentar qualquer tipo de efeito adverso, consulte o seu médico ou farmacêutico, mesmo que se trate de possíveis efeitos adversos que não aparecem neste prospecto. Também pode comunicá-los directamente através do Sistema Espanhol de Farmacovigilância de Medicamentos de Uso Humano: www.notificaRAM.es. Mediante a comunicação de efeitos adversos, o senhor pode contribuir para proporcionar mais informação sobre a segurança deste medicamento.
5. Conservação de Berinert
- Mantenha este medicamento fora da vista e do alcance das crianças.
- Não utilize Berinert após a data de validade, que aparece na etiqueta e no envase de cartão.
- Não conserve a uma temperatura superior a 30 °C.
- Não congele.
- Conserva o envase no embalagem para protegê-lo da luz.
- Berinert não contém conservantes, de modo que é preferível que a solução preparada seja utilizada imediatamente.
- Se a solução preparada não for administrada imediatamente, deve ser utilizada no prazo de 8 horas. O produto reconstituído apenas deve ser conservado no frasco.
6. Conteúdo do envase e informação adicional
Composição de Berinert
O princípio ativo é:
Inibidor da C1 esterase humano (500 UI/frasco; após a reconstituição: 50 UI/ml)
Para mais informações, consulte a secção “Estainformação está destinada exclusivamente a profissionais do sector sanitário”.
Os outros componentes são:
Glicina, cloreto de sódio, citrato de sódio.
Consulte o último parágrafo da secção 2. "Berinert contém sódio”.
Veículo:água para preparações injetáveis.
Aspecto do produto e conteúdo do envase
Berinert apresenta-se como um pó branco e é fornecido com água para preparações injetáveis como veículo.
A solução preparada deve ser transparente e clara.
Apresentação
Caixa com 500 UI contém:
1 frasco com pó (500 UI)
1 frasco com 10 ml de água para preparações injetáveis
1 transferidor com filtro 20/20
Equipamento de administração (caixa interior):
1 seringa de 10 ml de uso único
1 equipamento para venopunção
2 compressas com álcool
1 penso
Título da autorização de comercialização e responsável pela fabricação
CSL Behring GmbH
Emil von Behring Strasse, 76
35041 Marburg, Alemanha
Pode solicitar mais informações sobre este medicamento dirigindo-se ao representante local do título da autorização de comercialização:
CSL Behring S.A.
c/ Tarragona 157, planta 18
08014 Barcelona
Espanha
Este medicamento está autorizado nos estados membros do Espaço Económico Europeue no Reino Unido (Irlanda do Norte)com os seguintes nomes:
Berinert 500 IE Pó e
veículo para solução injetável ou infusão Áustria
Berinert 500 Bélgica, Chipre, Alemanha, Grécia, Luxemburgo, Polónia, Portugal
Berinert 500, 500 IU Pó e veículo
para solução injetável/infusão Bulgária
Berinert 500 IU República Checa, Eslováquia
Berinert Dinamarca, Itália
Berinert 500 IU, injetável/infusão pó
e veículo, solução para Finlândia
Berinert 500 UI, pó e veículo para
solução injetável/perfusão França
Berinert 500 NE e veículo para
injeção ou infusão Hungria
Berinert 500 IU pó e líquido para
injeção/infusão, solução Noruega
Berinert 500 UI, pó e veículo para
solução injetável/perfusão Roménia
Berinert 500 i.e. pó e veículo para
injeção ou infusão Eslovénia
Berinert 500 UI Pó e veículo para solução
injetável e para perfusão Espanha
Berinert 500 IE, pó e líquido para
injeção/infusão, solução_____ Suécia
Berinert 500 UI pó e veículo para solução
injetável/infusão Reino Unido
Data da última revisão deste prospecto:Outubro 2021
A informação detalhada e actualizada sobre este medicamento está disponível na página Web da Agência Espanhola de Medicamentos e Produtos Sanitários (AEMPS) http://www.aemps.gob.es
Estainformação está destinada exclusivamente a profissionais do sector sanitário
COMPOSIÇÃO QUALITATIVA E QUANTITATIVA
A potência do inibidor da C1 esterase humano é expressa em Unidades Internacionais (UI), que está relacionada com o actual padrão da OMS para os produtos inibidores da C1 esterase.
- País de registo
- Substância ativa
- Requer receita médicaSim
- Fabricante
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a BERINERT 500 UI PÓ E SOLVENTE PARA SOLUÇÃO INJETÁVEL E PARA PERFUSÃOForma farmacêutica: INJETÁVEL, 1500 UISubstância ativa: c1-inhibitor, plasma derivedFabricante: Csl Behring GmbhRequer receita médicaForma farmacêutica: INJETÁVEL, 2000 UISubstância ativa: c1-inhibitor, plasma derivedFabricante: Csl Behring GmbhRequer receita médicaForma farmacêutica: INJETÁVEL, 3000 UISubstância ativa: c1-inhibitor, plasma derivedFabricante: Csl Behring GmbhRequer receita médica
Alternativas a BERINERT 500 UI PÓ E SOLVENTE PARA SOLUÇÃO INJETÁVEL E PARA PERFUSÃO noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a BERINERT 500 UI PÓ E SOLVENTE PARA SOLUÇÃO INJETÁVEL E PARA PERFUSÃO em Poland
Alternativa a BERINERT 500 UI PÓ E SOLVENTE PARA SOLUÇÃO INJETÁVEL E PARA PERFUSÃO em Ukraine
Médicos online para BERINERT 500 UI PÓ E SOLVENTE PARA SOLUÇÃO INJETÁVEL E PARA PERFUSÃO
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de BERINERT 500 UI PÓ E SOLVENTE PARA SOLUÇÃO INJETÁVEL E PARA PERFUSÃO – sujeita a avaliação médica e regras locais.




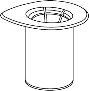 1
1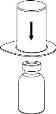 2
2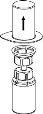 3
3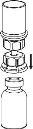 4
4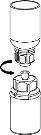 5
5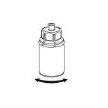 6
6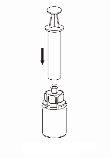 7
7









