

Olimel N7e

Pergunte a um médico sobre a prescrição de Olimel N7e

Como usar Olimel N7e
Folheto para o paciente: Informação para o utilizador
OLIMEL N7E, emulsão para infusão
Deve ler atentamente o conteúdo do folheto antes de administrar o medicamento, pois contém informações importantes para o paciente.
- Deve guardar este folheto para poder relê-lo se necessário.
- Em caso de dúvidas, deve consultar um médico ou enfermeiro.
- Se o paciente apresentar algum efeito indesejado, incluindo qualquer efeito indesejado não mencionado neste folheto, deve informar o médico ou enfermeiro. Ver ponto 4.
Índice do folheto
- 1. O que é o medicamento OLIMEL N7E, emulsão para infusão e para que é utilizado
- 2. Informações importantes antes de administrar o medicamento OLIMEL N7E, emulsão para infusão
- 3. Como usar o medicamento OLIMEL N7E, emulsão para infusão
- 4. Efeitos indesejados
- 5. Como armazenar o medicamento OLIMEL N7E, emulsão para infusão
- 6. Conteúdo do pacote e outras informações
1. O que é o medicamento OLIMEL N7E, emulsão para infusão e para que é utilizado
OLIMEL é uma emulsão para infusão. O medicamento é fornecido em um saco de três câmaras.
Na primeira câmara, há uma solução de glicose com cálcio, na segunda — uma emulsão lipídica, e na
terceira — uma solução de aminoácidos com outros eletrólitos.
OLIMEL é utilizado para nutrição parenteral de adultos e crianças com mais de 2 anos de idade, quando a nutrição oral não é adequada.
OLIMEL só deve ser utilizado sob controle médico.
2. Informações importantes antes de administrar o medicamento OLIMEL N7E, emulsão para infusão
Quando não usar o medicamento OLIMEL N7E, emulsão para infusão:
- em prematuros, recém-nascidos e crianças com menos de 2 anos de idade;
- se o paciente tiver alergia a ovos, soja, proteínas de amendoim, milho/ produtos que contenham milho (ver também o ponto "Advertências e precauções" abaixo) ou a qualquer um dos outros componentes do medicamento (listados no ponto 6);
- se a administração de alguns aminoácidos causar uma reação anormal do organismo do paciente;
- se o paciente tiver um nível muito alto de lipídios no sangue;
- se o paciente tiver hiperglicemia (nível muito alto de açúcar no sangue);
- se o paciente tiver um nível anormalmente alto de qualquer um dos eletrólitos (sódio, potássio, magnésio, cálcio e/ou fósforo) no sangue.
Em cada caso, o médico decidirá sobre a administração do medicamento com base em fatores como idade,
peso corporal do paciente e seu estado de saúde, incluindo os resultados dos exames realizados.
Advertências e precauções
Antes de iniciar a administração de OLIMEL N7E, deve discutir com o médico ou enfermeiro.
A administração excessivamente rápida de soluções para nutrição parenteral total pode resultar em lesão ou
morte do paciente.
Se ocorrerem sinais ou sintomas atípicos de reação alérgica (como suor, febre, calafrios, dor de cabeça,
erupção cutânea ou problemas respiratórios), a infusão deve ser interrompida imediatamente. O medicamento
contém óleo de soja e fosfolipídios de ovo de galinha. As proteínas de soja e ovo podem causar reações de
hipersensibilidade. Foram observadas reações alérgicas cruzadas entre as proteínas de soja e amendoim.
O medicamento OLIMEL contém glicose derivada do milho, o que pode causar reações de hipersensibilidade,
se o paciente tiver alergia ao milho ou produtos que contenham milho (ver ponto "Quando não usar o medicamento OLIMEL N7E, emulsão para infusão:" acima).
Dificuldades respiratórias também podem ser um sinal de que partículas pequenas estão bloqueando os vasos
sanguíneos nos pulmões (depósitos nos vasos pulmonares). Se ocorrerem dificuldades respiratórias, o paciente
deve informar o médico ou enfermeiro. Eles decidirão sobre a ação apropriada.
O antibiótico ceftriaxona não deve ser misturado ou administrado simultaneamente com qualquer solução
que contenha cálcio (incluindo o medicamento OLIMEL) por infusão intravenosa.
Esses medicamentos não devem ser administrados simultaneamente, mesmo por linhas de infusão ou locais de
infusão diferentes.
No entanto, o medicamento OLIMEL e a ceftriaxona podem ser administrados sequencialmente, se as linhas de
infusão forem inseridas em locais diferentes ou forem trocadas ou limpas completamente com solução salina
fisiológica entre as infusões, para evitar a formação de depósitos (precipitação de sais de cálcio da ceftriaxona).
Alguns medicamentos e doenças podem aumentar o risco de infecção ou sepse (presença de bactérias no sangue).
Um risco especial de infecção ou sepse existe após a inserção de um cateter (cateter venoso) na veia do paciente.
O médico monitorará o paciente para detectar qualquer sinal de infecção. Pacientes que necessitam de nutrição parenteral
(administração de substâncias nutricionais por meio de um cateter inserido na veia) estão, devido ao seu estado
clínico, mais propensos a desenvolver infecções. A adoção de procedimentos assépticos durante a inserção,
manuseio do cateter e preparo do medicamento para nutrição (nutrição parenteral total) pode reduzir o risco de
infecção.
Se o paciente estiver gravemente desnutrido, de modo que precise receber alimento intravenosamente, o médico
deve iniciar o tratamento lentamente. Ao mesmo tempo, o médico deve monitorar o paciente para evitar mudanças
repentinas nos níveis de líquidos, vitaminas, eletrólitos e minerais.
Antes de iniciar a infusão, deve-se corrigir as alterações no equilíbrio hídrico-eletrolítico e metabólico do paciente.
O médico monitorará o paciente durante a terapia e pode ajustar a dosagem ou, se achar necessário, prescrever
suplementos nutricionais adicionais, como vitaminas, eletrólitos e minerais.
Em pacientes que recebem terapia de nutrição parenteral, foram relatados distúrbios da função hepática, incluindo
dificuldades na eliminação da bile (colestase), acúmulo de gordura (esteatose hepática), fibrose, que pode levar à
insuficiência hepática, e também inflamação da vesícula biliar e cálculos biliares. Acredita-se que as causas desses
distúrbios possam variar entre os pacientes. Se o paciente apresentar sintomas como náuseas, vômitos, dor abdominal,
icterícia ou olhos amarelados, deve consultar o médico para identificar as possíveis causas e medidas terapêuticas e
preventivas.
O médico deve ser informado sobre:
- doenças renais graves. O médico também deve ser informado se o paciente está submetido a diálise (rim artificial) ou outros métodos de limpeza do sangue;
- doenças hepáticas graves;
- distúrbios da coagulação do sangue;
- disfunção adrenal (insuficiência adrenal). As glândulas adrenais são glândulas com forma triangular, localizadas no topo dos rins;
- insuficiência cardíaca;
- doenças pulmonares;
- acúmulo de líquidos no organismo (hiperhidratação);
- falta de líquidos no organismo (desidratação);
- diabetes mellitus não tratada;
- infarto do miocárdio ou choque devido à insuficiência cardíaca aguda;
- acidose metabólica grave (pH do sangue muito ácido);
- sepse generalizada;
- coma.
Para verificar a eficácia e segurança do medicamento, durante a administração do medicamento, o paciente será
submetido a exames clínicos e laboratoriais prescritos pelo médico. Se o medicamento for administrado por várias
semanas, o sangue do paciente será examinado regularmente.
A capacidade reduzida do organismo de eliminar os lipídios contidos no medicamento administrado pode resultar
em um quadro conhecido como síndrome de sobrecarga lipídica (ver ponto 4 - "Efeitos indesejados").
Se ocorrer dor, ardor ou inchaço no local da infusão ou vazamento do líquido infundido, o paciente deve informar
o médico ou enfermeiro.
A administração do medicamento será interrompida imediatamente e, em seguida, reiniciada em outra veia.
Se o nível de glicose no sangue aumentar excessivamente, o médico deve ajustar a velocidade de administração do
medicamento OLIMEL ou administrar um medicamento para controlar o nível de açúcar no sangue (insulina).
OLIMEL pode ser administrado por um cateter (cateter venoso) inserido em uma veia grande no tórax do paciente
(veia central).
Crianças e adolescentes
Quando utilizado em crianças abaixo de 18 anos de idade, deve-se ter cuidado para administrar a dose correta do
medicamento. Devido à maior sensibilidade das crianças ao risco de infecção, também devem ser tomadas medidas
de precaução aumentadas. Sempre é necessário enriquecer com vitaminas e minerais.
Para crianças, devem ser utilizadas formulações e quantidades pediátricas.
OLIMEL e outros medicamentos
Deve informar o médico sobre todos os medicamentos que o paciente está tomando ou utilizando atualmente ou
recentemente, bem como sobre medicamentos que o paciente planeja tomar ou utilizar.
A administração concomitante de outros medicamentos geralmente não é contraindicada. No entanto, é necessário
informar o médico sobre todos os medicamentos tomados recentemente, incluindo os vendidos sem prescrição, para
verificar a compatibilidade.
Deve informar o médico sobre a administração de:
- insulina,
- heparina.
Não se deve administrar o medicamento OLIMEL simultaneamente com sangue pelo mesmo conjunto de infusão.
OLIMEL contém cálcio. Não se deve administrar com o antibiótico ceftriaxona ou pela mesma linha de infusão,
pois podem se formar partículas. Se esses medicamentos forem administrados sequencialmente por meio do mesmo
dispositivo, este deve ser completamente lavado.
Devido ao risco de precipitação, o medicamento OLIMEL não deve ser administrado pela mesma linha de infusão
ou adicionado à amplicilina (antibiótico) ou fosfenitoína (medicamento anticonvulsivante).
Óleo e óleo de soja presentes no medicamento OLIMEL contêm vitamina K. Geralmente, isso não afeta a ação de
medicamentos anticoagulantes, como a cumarina. No entanto, se o paciente estiver tomando medicamentos
anticoagulantes, deve informar o médico.
Os lipídios presentes na emulsão podem interferir nos resultados de alguns exames laboratoriais, se a amostra de sangue
for coletada antes que os lipídios sejam eliminados do sangue do paciente (eles são eliminados do sangue após 5 a 6
horas após a administração dos lipídios).
OLIMEL contém potássio. Deve-se ter cuidado especial em pacientes que estejam tomando medicamentos
diuréticos, inibidores da enzima conversora de angiotensina (ECA), antagonistas do receptor de angiotensina II
(medicamentos utilizados na hipertensão) ou medicamentos imunossupressores. Medicamentos dessa classe podem
causar um aumento no nível de potássio no sangue.
Gravidez e amamentação
Se a paciente estiver grávida ou amamentando, acredita que possa estar grávida ou planeja ter um filho, deve consultar
o médico antes de administrar este medicamento.
Falta de experiência adequada sobre o uso do medicamento OLIMEL N7E em mulheres grávidas ou lactantes.
Se necessário, pode-se considerar a administração do medicamento OLIMEL N7E durante a gravidez e amamentação.
O medicamento OLIMEL N7E deve ser administrado a mulheres grávidas ou lactantes apenas após uma avaliação cuidadosa.
Condução de veículos e operação de máquinas
Não se aplica.
3. Como usar o medicamento OLIMEL N7E, emulsão para infusão
Dosagem
OLIMEL deve ser utilizado apenas em adultos e em crianças com mais de 2 anos de idade.
O medicamento tem a forma de emulsão para infusão administrada por um cateter (cateter venoso) em uma veia
grande no tórax do paciente.
Antes de usar, OLIMEL deve estar à temperatura ambiente.
OLIMEL é destinado apenas para uso único.
A infusão de 1 saco geralmente dura de 12 a 24 horas.
Dosagem — adultos
A velocidade de administração, de acordo com as necessidades e o estado clínico do paciente, será determinada
pelo médico.
O medicamento pode ser utilizado por tanto tempo quanto necessário, dependendo do estado clínico do paciente.
Dosagem — crianças com mais de 2 anos de idade e adolescentes
A dose do medicamento e o período de administração são determinados pelo médico. Dependem da idade, peso,
altura, estado de saúde e capacidade do organismo de decompor e utilizar os componentes do medicamento
OLIMEL N7E.
Uso de dose maior do que a recomendada do medicamento OLIMEL N7E, emulsão para infusão
Se o paciente receber uma dose excessiva do medicamento ou uma infusão muito rápida, os aminoácidos presentes
podem contribuir para o aumento da acidez do sangue e a ocorrência de sintomas de hipervolemia (aumento do volume
de sangue circulante). O nível de glicose no sangue e na urina pode aumentar, e pode ocorrer um quadro de
hiperosmolaridade (viscosidade excessiva do sangue), e os lipídios presentes na emulsão podem aumentar o nível de
triglicérides no sangue. A administração de uma infusão com velocidade excessiva ou volume excessivo do medicamento
OLIMEL pode causar náuseas, vômitos, calafrios, dor de cabeça, ondas de calor, suor excessivo (hiperidrose) e distúrbios
eletrolíticos. Nesse caso, a infusão deve ser interrompida imediatamente.
Em alguns casos graves, para ajudar os rins do paciente a eliminar o excesso de medicamento, o médico pode ser
obrigado a submeter o paciente a diálise renal temporária.
Para evitar essas situações, o médico monitora regularmente o estado do paciente e verifica os parâmetros do sangue.
Em caso de dúvidas sobre o uso do medicamento, deve-se consultar o médico.
4. Efeitos indesejados
Como qualquer medicamento, este medicamento pode causar efeitos indesejados, embora não ocorram em todos.
Se ocorrerem alterações no bem-estar durante o tratamento ou após a sua interrupção, deve-se informar imediatamente
o médico ou enfermeiro.
Os exames realizados pelo médico durante o tratamento do paciente devem minimizar o risco de efeitos indesejados.
Se ocorrerem sinais ou sintomas atípicos de reação alérgica, como suor excessivo, febre, calafrios, dor de cabeça,
erupção cutânea ou problemas respiratórios, a infusão deve ser interrompida imediatamente.
Durante o uso do medicamento OLIMEL, foram relatados os seguintes efeitos indesejados:
Frequência — Frequente: pode afetar até 1 em 10 pessoas
- batimento cardíaco acelerado (taquicardia);
- perda de apetite;
- nível aumentado de lipídios no sangue (hipertrigliceridemia);
- dor abdominal;
- diarreia;
- náuseas;
- pressão arterial aumentada (hipertensão).
Frequência — Desconhecida: frequência não pode ser estimada com base nos dados disponíveis
- reações de hipersensibilidade, incluindo suor, febre, calafrios, dor de cabeça, erupção cutânea (eritematosa, papulosa, pustulosa, maculopapulosa, erupção generalizada), prurido, ondas de calor, dificuldades respiratórias;
- vazamento da infusão para o tecido circundante (extravasamento) pode levar a dor, irritação, inchaço/edema, vermelhidão (eritema)/aquecimento, necrose da pele ou bolhas/bolhas, inflamação, espessamento ou contração da pele no local da infusão:
- vômitos.
Durante o uso de medicamentos semelhantes para nutrição parenteral, foram relatados os seguintes efeitos indesejados:
Frequência — Muito rara: pode afetar até 1 em 10.000 pessoas
- capacidade reduzida de eliminar lipídios (síndrome de sobrecarga lipídica) relacionada ao agravamento súbito do estado de saúde do paciente. Os sintomas da síndrome de sobrecarga lipídica geralmente desaparecem após a interrupção da infusão da emulsão lipídica. o Febre o Redução do número de glóbulos vermelhos, que pode causar palidez da pele e ser a causa de fraqueza ou falta de ar (anemia) o Baixo número de glóbulos brancos, que pode aumentar o risco de infecções (leucopenia) o Baixo número de plaquetas, que pode aumentar o risco de hematomas e/ou sangramentos (trombocitopenia) o Distúrbios da coagulação, que afetam a capacidade de coagulação do sangue o Nível alto de lipídios no sangue (hiperlipidemia) o Infiltração lipídica no fígado (hepatomegalia) o Deterioração da função hepática o Sintomas do sistema nervoso central (por exemplo, coma).
Frequência — Desconhecida: frequência não pode ser estimada com base nos dados disponíveis
- reações alérgicas;
- resultado anormal do exame de sangue para função hepática;
- problemas na eliminação da bile (colestase);
- aumento do tamanho do fígado (hepatomegalia);
- doenças hepáticas relacionadas à nutrição parenteral (ver "Advertências e precauções" no ponto 2);
- icterícia;
- baixo número de plaquetas (trombocitopenia);
- nível aumentado de azoto no sangue (azotemia);
- atividade aumentada de enzimas hepáticas;
- formação de partículas pequenas que podem bloquear os vasos sanguíneos nos pulmões (depósitos nos vasos pulmonares) levando a embolia pulmonar e dificuldades respiratórias (insuficiência respiratória).
Notificação de efeitos indesejados
Se ocorrerem efeitos indesejados, incluindo qualquer efeito indesejado não mencionado no folheto, deve-se informar
o médico ou enfermeiro. Efeitos indesejados podem ser notificados diretamente ao Departamento de Monitoramento
de Efeitos Indesejados de Produtos Farmacêuticos da Agência Reguladora de Produtos Farmacêuticos, Dispositivos
Médicos e Produtos Biocidas
Al. Jerozolimskie 181C
02-222 Varsóvia
Telefone: + 48 22 49 21 301
Fax: + 48 22 49 21 309
Site: https://smz.ezdrowie.gov.pl
Efeitos indesejados também podem ser notificados ao titular da autorização de comercialização.
A notificação de efeitos indesejados permitirá reunir mais informações sobre a segurança do medicamento.
5. Como armazenar o medicamento OLIMEL N7E, emulsão para infusão
O medicamento deve ser armazenado em um local não visível e inacessível a crianças.
Não use este medicamento após a data de validade impressa no recipiente e embalagem externa (MM/AAAA).
A data de validade é o último dia do mês indicado.
Não congelar.
Armazenar na embalagem protetora.
Medicamentos não devem ser jogados na canalização ou lixeiras domésticas. Deve-se perguntar ao farmacêutico como
descartar medicamentos que não são mais utilizados. Essa ação ajudará a proteger o meio ambiente.
6. Conteúdo do pacote e outras informações
O que contém o medicamento OLIMEL N7E, emulsão para infusão
Os componentes ativos em cada um dos sacos da emulsão pronta são: 11,1% (coincide com 11,1 g/100 ml)
solução de L-aminoácidos (alanina, arginina, glicina, histidina, isoleucina, leucina, lisina (na forma de lisina
acetato), metionina, fenilalanina, prolina, serina, treonina, triptofano, tirosina, valina, ácido aspártico, ácido
glutâmico) com eletrólitos (sódio, potássio, magnésio, fosfatos, acetatos, cloretos),
20% (coincide com 20 g/100 ml) emulsão lipídica (óleo de oliva purificado e óleo de soja purificado) e 35%
(coincide com 35 g/100 ml) solução de glicose (na forma de glicose monohidratada) com cálcio.
Outros componentes do medicamento são:
| Câmara que contém emulsão lipídica | Câmara que contém solução de aminoácidos | Câmara que contém solução de glicose |
| Fosfolipídios de ovo de galinha purificados, glicerol, oleato de sódio, hidróxido de sódio (para ajustar o pH), água para injeção | Ácido acético glacial (para ajustar o pH), água para injeção | Ácido clorídrico (para ajustar o pH), água para injeção |
Como é o medicamento OLIMEL N7E, emulsão para infusão e o que o pacote contém
OLIMEL é uma emulsão para infusão fornecida em um saco de três câmaras. A primeira câmara contém a emulsão
lipídica, a segunda câmara contém a solução de aminoácidos com eletrólitos, e a terceira câmara contém a solução
de glicose com cálcio. As câmaras são separadas por selos não permeáveis.
Antes da administração, o conteúdo das câmaras deve ser misturado girando o saco em direção a si mesmo, começando
da parte superior do saco, até que os selos se abram.
Aspecto antes da mistura:
- As soluções de aminoácidos e glicose são transparentes, incolores ou ligeiramente amareladas.
- A emulsão lipídica é homogênea com aparência leitosa.
Aspecto após a mistura: emulsão homogênea com aparência leitosa.
O saco de três câmaras é uma bolsa plástica multicamada. A camada interna (em contato) do saco é compatível com os
componentes e aditivos permitidos.
Para evitar o contato com o oxigênio contido no ar, o saco é embalado em uma embalagem protetora, que protege
contra a entrada de oxigênio com um sachê que absorve oxigênio.
Tamanhos do pacote
saco de 1000 ml: 1 caixa de papelão com 6 sacos
saco de 1500 ml: 1 caixa de papelão com 4 sacos; 1 caixa de papelão com 5 sacos
saco de 2000 ml: 1 caixa de papelão com 4 sacos; 1 caixa de papelão com 5 sacos
1 saco com capacidade de 1000 ml, 1500 ml e 2000 ml.
Nem todos os tamanhos de pacotes precisam estar disponíveis.
Titular da autorização de comercialização e fabricante
Titular da autorização de comercialização
Baxter Polska Sp. z o. o.
Ul. Kruczkowskiego 8
00-380 Varsóvia
Fabricante
BAXTER S.A.
Boulevard Rene Branquart 80
7860 Lessines, Bélgica
Este medicamento é autorizado para comercialização nos países membros da Área Econômica Europeia sob os seguintes nomes:
Nome do medicamento
França, Portugal, Estônia, Polônia, Lituânia, Bulgária, Romênia, Letônia, República Tcheca, Bélgica, Espanha,
Eslováquia, Holanda, Luxemburgo, Eslovênia, Itália, Grécia, Chipre: OLIMEL N7E
Em alguns países, é registrado sob um nome comercial diferente, como descrito abaixo:
Áustria: ZentroOLIMEL 4,4 % com eletrólitos
Alemanha: Olimel 4,4% E
Dinamarca, Islândia, Suécia, Noruega, Finlândia: Olimel N7E
Reino Unido, Irlanda, Malta: Triomel 7g/l nitrogênio 1140 kcal/l com eletrólitos
Data da última atualização do folheto: abril de 2025
--------------------------------------------------------------------------------------------------------------------------------
Informações destinadas apenas ao pessoal médico especializado:
Grupo farmacoterapêutico: soluções para nutrição parenteral/misturas
Código ATC: B05 BA10.
A. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA
OLIMEL tem a forma de um saco de três câmaras.
Cada saco contém uma solução de glicose com cálcio, uma emulsão lipídica e uma solução de aminoácidos com outros
eletrólitos:
| Conteúdo por saco | |||
| 1000 ml | 1500 ml | 2000 ml | |
| 35% solução de glicose (coincide com 35 g/100 ml) | 400 ml | 600 ml | 800 ml |
| 11,1% solução de aminoácidos (coincide com 11,1 g/100 ml) | 400 ml | 600 ml | 800 ml |
| 20% emulsão lipídica (coincide com 20 g/100 ml) | 200 ml | 300 ml | 400 ml |
Composição da emulsão pronta após a mistura do conteúdo das três câmaras:
| Componentes ativos | 1000 ml | 1500 ml | 2000 ml |
| Óleo de oliva purificado + óleo de soja purificado | 40,00 g | 60,00 g | 80,00 g |
| Alanina | 6,41 g | 9,61 g | 12,82 g |
| Arginina | 4,34 g | 6,51 g | 8,68 g |
| Ácido aspártico | 1,28 g | 1,92 g | 2,56 g |
| Ácido glutâmico | 2,21 g | 3,32 g | 4,42 g |
| Glicina | 3,07 g | 4,60 g | 6,14 g |
| Histidina | 2,64 g | 3,97 g | 5,29 g |
| Isoleucina | 2,21 g | 3,32 g | 4,42 g |
| Leucina | 3,07 g | 4,60 g | 6,14 g |
| Lisina (coincide com acetato de lisina) | 3,48 g (4,88 g) | 5,23 g (7,31 g) | 6,97 g (9,75 g) |
| Metionina | 2,21 g | 3,32 g | 4,42 g |
| Fenilalanina | 3,07 g | 4,60 g | 6,14 g |
| Prolina | 2,64 g | 3,97 g | 5,29 g |
| Serina | 1,75 g | 2,62 g | 3,50 g |
| Treonina | 2,21 g | 3,32 g | 4,42 g |
| Triptofano | 0,74 g | 1,10 g | 1,47 g |
| Tirosina | 0,11 g | 0,17 g | 0,22 g |
| Valina | 2,83 g | 4,25 g | 5,66 g |
| Octanato de sódio tri-hidratado | 1,50 g | 2,24 g | 2,99 g |
| Glicerofosfato de sódio hidratado | 3,67 g | 5,51 g | 7,34 g |
| Cloruro de potássio | 2,24 g | 3,35 g | 4,47 g |
| Cloruro de magnésio hexa-hidratado | 0,81 g | 1,22 g | 1,62 g |
| Cloruro de cálcio di-hidratado | 0,52 g | 0,77 g | 1,03 g |
| Glicose (coincide com glicose monohidratada) | 140,00 g (154,00 g) | 210,00 g (231,00 g) | 280,00 g (308,00 g) |
Os componentes auxiliares são:
| Câmara que contém emulsão lipídica | Câmara que contém solução de aminoácidos com eletrólitos | Câmara que contém solução de glicose com cálcio |
| Fosfolipídios de ovo de galinha purificados, glicerol, oleato de sódio, hidróxido de sódio (para ajustar o pH), água para injeção | Ácido acético glacial (para ajustar o pH), água para injeção | Ácido clorídrico (para ajustar o pH), água para injeção |
Valores nutricionais da emulsão pronta, de acordo com o tamanho dos sacos:
| 1000 ml | 1500 ml | 2000 ml | |
| Gorduras | 40 g | 60 g | 80 g |
| Aminoácidos | 44,3 g | 66,4 g | 88,6 g |
| Azoto | 7,0 g | 10,5 g | 14,0 g |
| Glicose | 140,0 g | 210,0 g | 280,0 g |
| Valor energético: Valor energético total aproximado Valor energético não proteico Valor energético da glicose Valor energético lipídico Relação: valor energético não proteico/azoto Relação: valor energético da glicose/lipídios Gorduras/valor energético total | 1140 kcal 960 kcal 560 kcal 400 kcal 137 kcal/g 58/42 35% | 1710 kcal 1440 kcal 840 kcal 600 kcal 137 kcal/g 58/42 35% | 2270 kcal 1920 kcal 1120 kcal 800 kcal 137 kcal/g 58/42 35% |
| Eletrólitos: Sódio Potássio Magnésio Cálcio Fosfatos Acetatos Cloruros | 35,0 mmol 30,0 mmol 4,0 mmol 3,5 mmol 15,0 mmol 45 mmol 45 mmol | 52,5 mmol 45,0 mmol 6,0 mmol 5,3 mmol 22,5 mmol 67 mmol 68 mmol | 70,0 mmol 60,0 mmol 8,0 mmol 7,0 mmol 30,0 mmol 89 mmol 90 mmol |
| pH | 6,4 | 6,4 | 6,4 |
| Osmolalidade | 1360 mOsm/l | 1360 mOsm/l | 1360 mOsm/l |
B. POSOLOGIA E MODO DE ADMINISTRAÇÃO
Dosagem
OLIMEL não é recomendado para uso em crianças com menos de 2 anos de idade, devido à composição e volume
inadequados (ver pontos 4.4; 5.1 e 5.2 do RCP).
Não se deve exceder a dosagem diária máxima indicada abaixo. Devido à composição constante do saco de três
câmaras, pode não ser possível atender a todas as necessidades nutricionais do paciente ao mesmo tempo. Pode
haver situações clínicas em que os pacientes precisem de quantidades diferentes de nutrientes do que as contidas no
saco de composição constante. Nesse caso, qualquer alteração no volume (dose) deve levar em consideração o
impacto sobre a dosagem de todos os outros nutrientes do medicamento OLIMEL.
Adultos
A dosagem depende do gasto energético do paciente, estado clínico, peso corporal e capacidade de metabolizar os
componentes do medicamento OLIMEL, bem como dos nutrientes energéticos ou proteicos adicionais administrados
por via oral/enteral; portanto, é necessário escolher o tamanho do saco apropriado.
A necessidade diária média é:
- 0,16 a 0,35 g de azoto/kg de peso corporal (1 a 2 g de aminoácidos/kg), dependendo do estado nutricional do paciente e do grau de catabolismo,
- 20 a 40 kcal/kg,
- 20 a 40 ml de líquido/kg ou 1 a 1,5 ml por kcal consumida.
Para o medicamento OLIMEL, a dosagem diária máxima é determinada com base na ingestão total de calorias, 40 kcal/kg
em um volume de 35 ml/kg, o que corresponde a 1,5 g de aminoácidos/kg, 4,9 g de glicose/kg, 1,4 g de gorduras/kg,
1,2 mmol de sódio/kg e 1,1 mmol de potássio/kg. Para um paciente com 70 kg, isso corresponderia a 2450 ml do medicamento
OLIMEL por dia, o que significa a ingestão de 108 g de aminoácidos, 343 g de glicose e 98 g de gorduras (ou seja, 2352 kcal
não proteicas e um total de 2793 kcal).
Geralmente, a velocidade de administração deve aumentar gradualmente durante a primeira hora e, em seguida, a velocidade
de infusão deve ser ajustada com base na dose, volume diário do medicamento administrado e duração da infusão.
Para o medicamento OLIMEL, a velocidade máxima de infusão é de 1,7 ml/kg/h, o que corresponde a 0,08 g de aminoácidos/kg/h,
0,24 g de glicose/kg/h e 0,07 g de gorduras/kg/h.
Crianças com mais de 2 anos de idade e adolescentes
Não foram realizados estudos nessa população pediátrica.
A dosagem depende do gasto energético do paciente, estado clínico, peso corporal e capacidade de metabolizar os
componentes do medicamento OLIMEL, bem como dos nutrientes energéticos ou proteicos adicionais administrados
por via oral/enteral; portanto, é necessário escolher o tamanho do saco apropriado.
Além disso, a necessidade diária de líquidos, azoto e energia diminui constantemente com a idade. Foram considerados
dois grupos, de 2 a 11 anos e de 12 a 18 anos.
Para o medicamento OLIMEL N7E, em ambos os grupos etários, o fator limitante para a dosagem diária é a concentração
de magnésio. Em ambos os grupos etários, o fator limitante para a velocidade de administração por hora é a concentração
de glicose. Os valores resultantes são apresentados abaixo:
| Componente | 2 a 11 anos | 12 a 18 anos | ||
| Recomendado | Volume máximo de OLIMEL N7E | Recomendado | Volume máximo de OLIMEL N7E | |
| Dosagem diária máxima | ||||
| Líquidos (ml/kg/dia) |
| 25 |
| 25 |
| Aminoácidos (g/kg/dia) |
| 1,1 |
| 1,1 |
| Glicose (g/kg/dia) | 1,4 – 8,6 | 3,5 | 0,7 – 5,8 | 3,5 |
| Gorduras (g/kg/dia) | 0,5 - 3 | 1,0 | 0,5 - 2 (até 3) | 1,0 |
| Valor energético total: Valor energético total aproximado Valor energético não proteico Valor energético da glicose Valor energético lipídico Relação: valor energético não proteico/azoto Relação: valor energético da glicose/gorduras Gorduras/valor energético total |
| 28,5 |
| 28,5 |
| Velocidade máxima de administração por hora | ||||
| OLIMEL N7E (ml/kg/h) | 2,6 | 1,7 | ||
| Aminoácidos (g/kg/h) | 0,20 | 0,11 | 0,12 | 0,08 |
| Glicose (g/kg/h) | 0,36 | 0,36 | 0,24 | 0,24 |
| Gorduras (g/kg/h) | 0,13 | 0,10 | 0,13 | 0,07 |
Geralmente, a velocidade de administração deve aumentar gradualmente durante a primeira hora e, em seguida, a velocidade
de infusão deve ser ajustada com base na dose, volume diário do medicamento administrado e duração da infusão.
Em geral, em crianças pequenas, é recomendável iniciar a infusão com uma dose diária baixa e aumentá-la gradualmente
até a dosagem máxima (ver acima).
Modo de administração
Apenas para uso único.
Recomenda-se que, após a abertura, o conteúdo do saco seja usado imediatamente e não armazenado para uma
próxima infusão.
Após a mistura, a emulsão pronta tem uma aparência leitosa homogênea.
As instruções para a preparação e administração da emulsão para infusão estão no ponto 6.6 do RCP.
Devido à alta osmolalidade, OLIMEL só pode ser administrado em uma veia central.
O tempo de infusão recomendado para o saco de nutrição parenteral é de 12 a 24 horas.
O tratamento com nutrição parenteral pode ser continuado por tanto tempo quanto necessário, dependendo do estado clínico
do paciente.
C. INCOMPATIBILIDADES FARMACÊUTICAS
Não se deve adicionar nenhum medicamento ou substância a nenhum dos componentes do saco ou à emulsão pronta sem
antes verificar a compatibilidade e estabilidade do produto resultante (especialmente a estabilidade da emulsão lipídica).
Incompatibilidades podem resultar, por exemplo, de uma acidez excessiva (pH baixo) ou de uma quantidade inadequada de
cationes divalentes (Ca e Mg), que podem desestabilizar a emulsão lipídica.
Assim como no caso da preparação de outras misturas para nutrição parenteral, deve-se considerar a relação entre o teor de
cálcio e fosfatos. O acréscimo excessivo de cálcio e fosfato, especialmente na forma de sais inorgânicos, pode causar a
formação de depósitos de fosfato de cálcio.
OLIMEL contém íons de cálcio, o que representa um risco adicional de formação de coágulos em preparações de sangue ou
componentes sanguíneos com adição de citrato como anticoagulante/conservante.
Não se deve misturar ou administrar ceftriaxona simultaneamente com soluções para infusão que contenham cálcio, incluindo
o medicamento OLIMEL, pela mesma linha de infusão (por exemplo, por um conector em forma de Y), devido ao risco de
precipitação de sais de cálcio da ceftriaxona (ver pontos 4.4 e 4.5 do RCP). A ceftriaxona e as soluções que contenham
cálcio podem ser administradas sequencialmente, se as linhas de infusão forem inseridas em locais diferentes ou forem
trocadas ou limpas completamente com solução salina fisiológica entre as infusões, para evitar a formação de depósitos.
Devido ao risco de precipitação, o medicamento OLIMEL não deve ser administrado pela mesma linha de infusão ou adicionado
à amplicilina ou fosfenitoína.
Deve-se verificar a compatibilidade com as soluções administradas simultaneamente pela mesma linha de infusão, cateter
ou cânula.
Devido ao risco de pseudoaglutinação, não se deve administrar este medicamento antes, durante ou após a administração de
sangue pela mesma linha de infusão.
D. PRECAUÇÕES ESPECIAIS PARA ELIMINAÇÃO E PREPARO DO MEDICAMENTO PARA USO
PREPARO DO MEDICAMENTO
Revisão dos estágios de preparação para a administração de OLIMEL é apresentada na Figura 1.
Abertura
Remover o saco protetor.
Descartar o sachê que absorve oxigênio.
Verificar se o saco ou os selos estão danificados. Use apenas se o saco estiver intacto e os selos não estiverem rompidos
(ou seja, o conteúdo das 3 câmaras não foi misturado), as soluções de aminoácidos e glicose são transparentes,
incolores ou ligeiramente amareladas, praticamente livres de partículas visíveis e a emulsão lipídica é homogênea com
aparência leitosa.
Mistura das soluções e emulsões
Antes de romper os selos, certifique-se de que o medicamento está à temperatura ambiente.
Inicie a partir da parte superior do saco (perto da alça), role o saco com as duas mãos. Os selos desaparecerão a partir
da extremidade dos portos. Continue rolando o saco até que os selos se abram até metade de sua extensão.
Misture, girando o saco pelo menos 3 vezes.
Após a mistura, o medicamento tem a forma de uma emulsão homogênea com aparência leitosa.
Adição de componentes adicionais
O volume do saco é suficiente para permitir a adição de vitaminas, eletrólitos e minerais traços.
Qualquer aditivo (incluindo vitaminas) deve ser introduzido na emulsão pronta (após a abertura dos selos e mistura do
conteúdo das 3 câmaras).
As vitaminas também podem ser adicionadas à câmara que contém a glicose antes da preparação da emulsão pronta
(antes de abrir os selos e misturar o conteúdo das 3 câmaras).
Ao introduzir componentes adicionais em produtos que contenham eletrólitos, é necessário considerar a quantidade de eletrólitos
presentes no saco.
Os componentes adicionais devem ser introduzidos por pessoal qualificado em condições assépticas.
Para o medicamento OLIMEL, os eletrólitos podem ser adicionados de acordo com a tabela abaixo:
| Por 1000 ml | |||
| Conteúdo | Adição máxima | Conteúdo máximo | |
| Sódio | 35 mmol | 115 mmol | 150 mmol |
| Potássio | 30 mmol | 120 mmol | 150 mmol |
| Magnésio | 4,0 mmol | 1,6 mmol | 5,6 mmol |
| Cálcio | 3,5 mmol | 1,5 (0,0a) mmol | 5,0 (3,5a) mmol |
| Fosfatos inorgânicos | 0 mmol | 3,0 mmol | 3,0 mmol |
| Fosfatos orgânicos | 15 mmolb | 10 mmol | 25 mmolb |
Minerais traços e vitaminas:
Foi demonstrada a estabilidade após a adição de produtos de vitaminas e minerais traços disponíveis no mercado (contendo
até 1 mg de ferro).
A compatibilidade com outros componentes adicionais está disponível a pedido.
Ao adicionar componentes, é necessário:
- controlar as condições de assepsia,
- preparar o local de injeção no saco,
- perfurar o local de injeção e injetar os componentes adicionais com uma agulha para injeção ou dispositivo para preparo do medicamento,
- misturar o conteúdo do saco com os componentes adicionais.
Preparo da infusão
Controlar as condições de assepsia.
Suspender o saco.
Remover a proteção plástica do porto de administração do medicamento.
Inserir firmemente a agulha do conjunto de infusão no porto de administração do medicamento.
Figura 1. Etapas de preparação para a administração de OLIMEL.



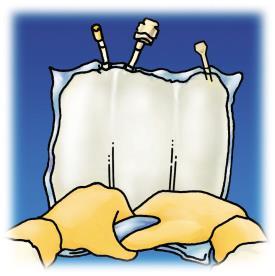
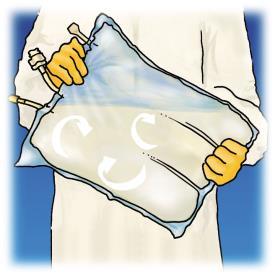
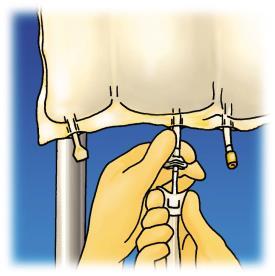
Administração
Exclusivamente para uso único.
Administrar o produto apenas após quebrar as soldas que separam as 3 câmaras e misturar o seu conteúdo.
Deve-se certificar de que a emulsão pronta para infusão não apresenta separação de fases.
Após a abertura do saco, o conteúdo deve ser utilizado imediatamente. Não é permitido armazenar
o saco aberto para a próxima infusão. Não reconectar sacos parcialmente utilizados.
Para evitar a possibilidade de formação de embolias aéreas, causadas pela presença de gás
contido no primeiro saco, não conectar sacos em série.
Qualquer resíduo de produto não utilizado ou resíduos e todo o conjunto de infusão deve ser
destruído.
Extravasação
O local de inserção do cateter deve ser monitorizado regularmente para detectar sinais de extravasação.
Em caso de extravasação, deve-se interromper imediatamente a administração do preparado, deixando o cateter ou a cânula no local para implementar imediatamente o procedimento terapêutico. Se possível,
antes de remover o cateter/cânula inserido, deve-se realizar uma aspiração do líquido através do cateter/cânula para reduzir a quantidade de líquido nos tecidos.
Dependendo do tipo de produto extravasado (incluindo o produto(s) misturado(s) com o produto
OLIMEL, se aplicável) e do grau/extentão do possível dano, devem ser tomadas medidas corretivas adequadas. As opções de tratamento podem incluir tratamento não farmacológico,
farmacológico e (ou) intervenção cirúrgica. Em caso de grande extravasação, deve-se consultar um cirurgião plástico dentro de 72 horas.
O local de extravasação deve ser monitorizado pelo menos a cada quatro horas durante as primeiras
24 horas, e subsequentemente uma vez por dia.
Não deve ser reiniciada a infusão na mesma veia central.
Baxter e Olimel são marcas registadas da Baxter International Inc.
- País de registo
- Substância ativa
- Requer receita médicaSim
- Fabricante
- ImportadorBaxter S.A.
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a Olimel N7eForma farmacêutica: Solução, -Substância ativa: combinationsNão requer receita médicaForma farmacêutica: Solução, -Substância ativa: combinationsNão requer receita médicaForma farmacêutica: Solução, -Substância ativa: combinationsNão requer receita médica
Alternativas a Olimel N7e noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a Olimel N7e em Hiszpania
Alternativa a Olimel N7e em Ukraina
Médicos online para Olimel N7e
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de Olimel N7e – sujeita a avaliação médica e regras locais.














