

Octaplex

Pergunte a um médico sobre a prescrição de Octaplex

Como usar Octaplex
folheto INCLUÍDO NA EMBALAGEM: INFORMAÇÃO PARA O UTILIZADOR
Octaplex, 500 UI, pó e solvente para solução para infusão
Complexo de protrombina humana
Octaplex, 1000 UI, pó e solvente para solução para infusão
Complexo de protrombina humana
Deve ler atentamente o conteúdo do folheto antes de tomar o medicamento, pois contém informações importantes para o doente.
- Deve guardar este folheto para poder relê-lo se necessário.
- Em caso de alguma dúvida, deve consultar o médico, farmacêutico ou enfermeiro.
- Se o doente apresentar algum efeito não desejado, incluindo quaisquer efeitos não desejados não mencionados neste folheto, deve informar o médico, farmacêutico ou enfermeiro. Ver ponto 4.
Índice do folheto:
- 1. O que é Octaplex e para que é utilizado
- 2. Informações importantes antes de tomar Octaplex
- 3. Como tomar Octaplex
- 4. Efeitos não desejados
- 5. Como conservar Octaplex
- 6. Conteúdo da embalagem e outras informações
1. O QUE É OCTAPLEX E PARA QUE É UTILIZADO
Octaplex pertence a um grupo de medicamentos denominados factores de coagulação. Contém factores de coagulação humana dependentes de vitamina K II, VII, IX e X.
Octaplex é utilizado para tratar e prevenir hemorragias:
- causadas por tratamento com antagonistas da vitamina K (como a warfarina). Estes medicamentos bloqueiam a ação da vitamina K e causam deficiência de factores de coagulação dependentes de vitamina K. Octaplex é utilizado quando é necessário um ajuste rápido da deficiência;
- em doentes nascidos com deficiência de factores de coagulação II e X dependentes de vitamina K. É administrado quando o produto de um factor de coagulação específico não está disponível.
2. INFORMAÇÕES IMPORTANTES ANTES DE TOMAR OCTAPLEX
Quando não tomar Octaplex:
- se o doente for alérgico a qualquer um dos componentes deste medicamento (listados no ponto 6),
- se o doente tiver alergia à heparina ou se já teve uma redução do número de plaquetas após a heparina.
- se o doente tiver deficiência de IgA com presença de anticorpos contra IgA.
Precauções e advertências
- Deve procurar aconselhamento de um especialista com experiência no tratamento de distúrbios de coagulação durante o tratamento com Octaplex.
- Nos doentes com deficiência adquirida de factores de coagulação dependentes de vitamina K (por exemplo, causada por tratamento com antagonistas da vitamina K), Octaplex deve ser utilizado apenas quando for necessária uma correção rápida do nível de complexo de protrombina, como no caso de hemorragias graves ou procedimentos cirúrgicos de emergência. Noutros casos, a redução da dose de antagonistas da vitamina K e/ou a administração de vitamina K é geralmente suficiente.
- Os doentes tratados com antagonistas da vitamina K (como a warfarina) podem ter um risco aumentado de formação de coágulos. Nesse caso, o tratamento com Octaplex pode aumentar o risco.
- Na deficiência congénita de um factor de coagulação dependente de vitamina K, deve ser utilizado o produto específico desse factor de coagulação se estiver disponível.
- Em caso de reação alérgica ou anafilactoide, a infusão deve ser interrompida imediatamente e deve ser administrado um tratamento adequado.
- Existe um risco de trombose ou síndrome de coagulação disseminada (uma condição grave que envolve a formação de coágulos em todo o corpo) nos doentes que recebem Octaplex (especialmente quando é administrado regularmente). Os doentes que recebem complexo de protrombina humana devem ser monitorizados de perto para sinais e sintomas de síndrome de coagulação disseminada e trombose. Isso é especialmente importante em doentes com doença cardíaca isquémica prévia, doença hepática, doentes que estão para ser submetidos a uma operação e quando Octaplex é administrado a crianças pequenas.
- Não há dados disponíveis sobre o uso de Octaplex em caso de hemorragia pós-parto relacionada com deficiência de vitamina K em recém-nascidos.
Segurança viral
- No caso de produtos medicinais obtidos a partir de sangue ou plasma humano, são utilizadas métodos adequados para prevenir a transmissão de infecções para os doentes. Estes incluem uma seleção rigorosa dos doadores de sangue e plasma para eliminar os doadores infectados, e testes para detectar marcadores virais específicos. Os fabricantes destes produtos também incluem métodos no processo de fabrico para inativar ou remover vírus. No entanto, no caso da administração de produtos obtidos a partir de sangue ou plasma humano, a possibilidade de transmissão de um agente infeccioso não pode ser completamente excluída. Isso inclui infecções causadas por vírus desconhecidos ou novos, ou outros tipos de infecções. Os métodos utilizados são considerados eficazes contra vírus envelopados, como o vírus da imunodeficiência humana (HIV), o vírus da hepatite B (HBV) e o vírus da hepatite C (HCV). Os métodos podem ter uma eficácia limitada contra vírus não envelopados, como o vírus da hepatite A (HAV) ou o parvovirus B19. O parvovirus B19 pode ser perigoso para as mulheres grávidas (infecção do feto) e para doentes com deficiências imunológicas ou com certos tipos de anemia (por exemplo, anemia falciforme ou anemia hemolítica). Recomenda-se registar o nome e o número de lote do produto em cada administração de Octaplex para poder associar ao lote utilizado.
- São recomendadas vacinações adequadas (contra a hepatite viral A e B) em caso de administração regular/repetida de produtos de complexo de protrombina obtidos a partir de plasma humano.
Crianças e adolescentes
Não há dados disponíveis sobre o uso de Octaplex em crianças e adolescentes.
Octaplex e outros medicamentos
O medicamento Octaplex não deve ser misturado com outros medicamentos.
Octaplex neutraliza o efeito do tratamento com antagonistas da vitamina K, mas não são conhecidas interações com outros
medicamentos .
Octaplex pode afetar os resultados dos testes de coagulação que dependem da heparina.
Deve informar o médico ou farmacêutico sobre todos os medicamentos que o doente está a tomar atualmente ou recentemente, e sobre os medicamentos que o doente planeia tomar.
Gravidez e amamentação
Octaplex deve ser utilizado durante a gravidez e amamentação apenas se for estritamente necessário. Antes de utilizar o produto, deve consultar o médico ou farmacêutico.
Condução de veículos e utilização de máquinas
Não é conhecido o efeito de Octaplex na capacidade de conduzir veículos ou utilizar máquinas
movidas por motor.
Informações importantes sobre alguns componentes de Octaplex
- A heparina pode causar reações alérgicas e uma redução do número de plaquetas no sangue. Os doentes com alergia conhecida à heparina devem evitar o uso de medicamentos que contenham heparina.
- O medicamento contém 75-125 mg (frasco de 500 UI) ou 150-250 mg (frasco de 1000 UI) de sódio (principal componente do sal de cozinha) em cada frasco. Isso corresponde a 3,8-6,3% ou 7,5-12,5% da dose diária máxima recomendada de sódio na dieta para adultos.
3. COMO TOMAR OCTAPLEX
O tratamento com Octaplex deve ser iniciado sob a supervisão de um médico especialista em distúrbios de coagulação.
- Em primeiro lugar, o pó deve ser dissolvido em água para injeção.
- Em seguida, a solução deve ser administrada por via intravenosa.
A dose de Octaplex a administrar e a duração do tratamento dependem de:
- gravidade da doença;
- local da hemorragia, sua gravidade e
- estado geral do doente.
Uso de uma dose maior do que a recomendada de Octaplex
Em caso de sobredose, aumenta o risco de
- desenvolvimento de complicações trombóticas (como ataque cardíaco e trombose venosa ou pulmonar),
- coagulação disseminada (uma condição grave que envolve a formação de coágulos em todo o corpo).
4. EFEITOS NÃO DESEJADOS
Como qualquer medicamento, Octaplex pode causar efeitos não desejados, embora não todos os doentes os experimentem.
Frequente (pode ocorrer em até 1 em cada 10 doentes)
Coágulos nos vasos sanguíneos.
Não muito frequente (pode ocorrer em até 1 em cada 100 doentes)
Ansiedade, aumento da pressão arterial, sintomas semelhantes à asma, hemoptise, sangramento nasal, ardor no local da injeção, coágulos no dispositivo.
Raro (pode ocorrer em até 1 em cada 1000 doentes)
Pode ocorrer reações alérgicas. Raramente, observa-se um aumento temporário nos resultados dos testes hepáticos (transaminases).
Nos doentes tratados com Octaplex para terapia de substituição, podem desenvolver anticorpos neutralizantes (inibidores) contra algum dos factores de coagulação presentes. Nesse caso, o tratamento de substituição não será muito eficaz.
Muito raro (pode ocorrer em até 1 em cada 10 000 doentes)
Foram observados casos de aumento da temperatura corporal (febre).
Existe um risco de formação de coágulos após a administração deste medicamento.
Frequência não conhecida (a frequência não pode ser estimada a partir dos dados disponíveis)
Reações alérgicas graves e choque, sensibilidade, tremores, insuficiência cardíaca, taquicardia, distúrbios da circulação, hipotensão, insuficiência respiratória, distúrbios da respiração, náuseas, urticária, erupções cutâneas, calafrios.
A heparina presente no medicamento pode causar uma redução súbita do número de plaquetas no sangue. Isso é uma reação alérgica denominada "trombocitopenia induzida por heparina do tipo II". Em casos raros, essa redução do número de plaquetas pode ocorrer 6-14 dias após o início do tratamento em doentes sem alergia prévia à heparina. Em doentes com alergia conhecida à heparina, essa mudança pode ocorrer dentro de algumas horas após o início do tratamento.
Deve interromper imediatamente o tratamento com Octaplex em doentes que apresentem essa reação alérgica. A esses doentes não deve ser administrado no futuro medicamentos que contenham heparina.
Informações sobre segurança viral, ver ponto 2.
Notificação de efeitos não desejados
Se ocorrerem algum efeito não desejado, incluindo quaisquer efeitos não desejados não mencionados neste folheto, deve informar o médico, farmacêutico ou enfermeiro. Os efeitos não desejados podem ser notificados diretamente para o Departamento de Monitorização de Efeitos Não Desejados de Medicamentos do Instituto Nacional de Farmacologia,
Al. Jerozolimskie 181C, 02-222 Varsóvia,
telefone: + 48 22 49 21 301, fax: + 48 22 49 21 309
e-mail: [email protected].
A notificação de efeitos não desejados pode ajudar a recolher mais informações sobre a segurança do medicamento.
5. COMO CONSERVAR OCTAPLEX
O medicamento deve ser conservado em um local fora do alcance das crianças.
Não use este medicamento após o prazo de validade impresso na embalagem. O prazo de validade é o último dia do mês indicado.
Não conserve em temperaturas acima de 25°C. Não congele. Conservar na embalagem original para proteger da luz.
O pó deve ser dissolvido apenas imediatamente antes da injeção. A estabilidade da solução foi demonstrada por um período de até 8 horas a 25°C. No entanto, para evitar contaminação, a solução deve ser utilizada imediatamente e apenas uma vez.
6. CONTEÚDO DA EMBALAGEM E OUTRAS INFORMAÇÕES
O que contém Octaplex no frasco e após reconstituição em 20 ml (500 UI)/40 ml (1000 UI)
de solvente
Os princípios ativos são:
| Nome do princípio ativo | Octaplex Conteúdo no frasco 500 UI | Octaplex Conteúdo no frasco 1000 UI | Octaplex Conteúdo em 1 ml de solução reconstituída |
| Proteína total: | 260–820 mg | 520–1640 mg |
|
| Princípios ativos | |||
| Factor de coagulação humana II | 280–760 UI | 560–1520 UI |
|
| Factor de coagulação humana VII | 180–480 UI | 360–960 UI |
|
| Factor de coagulação humana IX | 500 UI | 1000 UI | 25 UI/ml |
| Factor de coagulação humana X | 360–600 UI | 720–1200 UI |
|
| Outros princípios ativos | |||
| Proteína C | 260–620 UI | 520–1240 UI |
|
| Proteína S | 240–640 UI | 480–1280 UI |
|
A atividade específica do produto é ≥ 0,6 UI/mg, expressa como atividade do factor IX.
Os outros componentes são:
heparina, citrato de sódio di-hidratado , água para injeção.
Como é Octaplex e que conteúdo tem a embalagem
Octaplex é apresentado sob a forma de pó e solvente para solução para infusão. É um pó higroscópico, branco ou ligeiramente colorido, ou uma massa quebradiça num frasco de vidro.
O solvente é água para injeção fornecida num frasco de vidro. A solução reconstituída é clara ou ligeiramente opalescente e pode ser colorida.
Octaplex é vendido em uma caixa individual que contém:
- 1 frasco com pó para solução para infusão
- 1 frasco com solvente, água para injeção
- 1 conjunto de transferência Nextaro .
Responsável e fabricante
Octapharma (IP) SPRL
Allée de la Recherche 65
1070 Anderlecht
Bélgica
Para obter informações mais detalhadas, deve contactar o representante local do responsável:
Octapharma Portugal, Lda.
Rua do Centro Empresarial do Aeroporto, n.º 29, 1.º andar, sala 1
4470-177 Maia
Telefone: +351 229 405 010
Fax: +351 229 405 019
E-mail: [[email protected]](mailto:[email protected])
Fabricantes:
Octapharma Pharmazeutika Produktionsges.m.b.H.
Oberlaaer Str. 235
1100 Viena
Áustria
Octapharma Lingolsheim S.A.S.
72 Rue du Maréchal Foch
67380 Lingolsheim
França
Este medicamento está autorizado para comercialização nos países membros da Área Económica Europeia sob as seguintes designações:
Alemanha, Áustria, Bélgica, Bulgária, Croácia, Chipre, Dinamarca, Eslováquia, Eslovénia, Espanha, Estónia, Finlândia, França, Grécia, Hungria, Irlanda, Islândia, Itália, Letónia, Lituânia, Luxemburgo, Malta, Noruega, Países Baixos, Polónia, Portugal, Reino Unido, República Checa, Roménia, Suécia.
Data da última revisão do folheto: 06.07.2024 -------------------------------------------------------------------------------------------------------------------------
INFORMAÇÕES PARA PROFISSIONAIS DE SAÚDE
Informações gerais sobre o uso de Octaplex estão apresentadas no ponto 3.
As seguintes informações são destinadas apenas a profissionais de saúde:
Instruções para o tratamento
Deve ler todas as instruções e seguir em conformidade!
Durante as seguintes etapas, deve ser assegurada a esterilidade!
O produto dissolve-se rapidamente à temperatura ambiente.
A solução reconstituída deve ser transparente ou ligeiramente opalescente.
Não deve usar soluções turvas ou que contenham partículas sólidas.
Antes da administração, deve avaliar visualmente se a solução não contém partículas sólidas ou se a cor mudou.
Após a reconstituição, a solução deve ser utilizada imediatamente.
Todos os resíduos do produto não utilizado ou material utilizado devem ser eliminados de acordo com as regulamentações locais.
Posologia
Hemorragias e prevenção de hemorragias em caso de tratamento com antagonistas da vitamina K:
A dose depende do INR antes do tratamento e do peso corporal. A tabela apresenta as doses aproximadas (em UI/kg de peso corporal de produto reconstituído).
| INR antes do tratamento |
|
| > 6 |
| Dose de Octaplex (UI de factor IX) / kg de peso corporal | 25 | 35 | 50 |
A dose é determinada com base no peso corporal máximo, mas não excedendo, 100 kg. Por isso, em doentes com peso corporal acima de 100 kg, a dose máxima única (UI de factor IX) não deve exceder 2 500 UI para valores de INR de 2 – <4, 3 500 UI para valores de INR de 4 – 6 e 5 000 UI para valores de INR > 6.
- A dose é calculada com base em dados experimentais, e a recuperação e a duração do efeito podem variar, por isso é obrigatório monitorizar o INR durante o tratamento.
Hemorragias e prevenção de hemorragias durante procedimentos cirúrgicos em deficiências congénitas de factores de coagulação II e X dependentes de vitamina K, quando o produto do factor de coagulação específico não está disponível:
A dose necessária é calculada com base em dados experimentais, de modo que cerca de 1 UI de factor II ou X por kg de peso corporal causa um aumento da atividade do factor II ou X no sangue de, respetivamente, 0,02 e 0,017 UI/ml.
Instruções para a reconstituição:
- 1. Se necessário, leve o solvente (água para injeção) e o pó em frascos fechados à temperatura ambiente. Essa temperatura deve ser mantida durante a reconstituição. Se um banho de água for usado para aquecer, deve ter cuidado para evitar o contato da água com as tampas de borracha ou as rolhas dos frascos. A temperatura do banho de água não deve exceder 37°C.
- 2. Remova as tampas do tipo "flip-off" do frasco com pó e do frasco com solvente e desinfete as tampas de borracha.
- 3. Retire a tampa do invólucro externo do conjunto Nextaro . Coloque o frasco com solvente sobre uma superfície plana e segure-o firmemente. Sem remover o invólucro externo, coloque a parte azul do Nextaro sobre o frasco com solvente e pressione firmemente até ouvir um clique (fig. 1). Não gire durante a conexão! Segurando o frasco com solvente, retire cuidadosamente o invólucro externo do conjunto Nextaro , mantendo o conjunto Nextaro firmemente preso ao frasco com solvente (fig. 2)
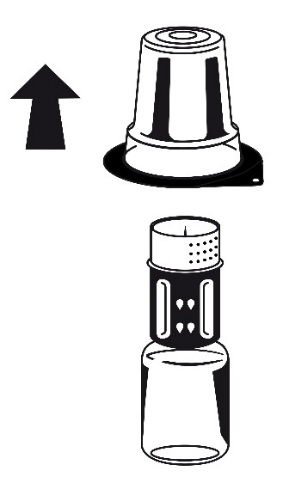
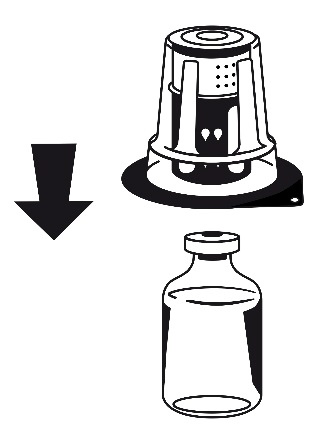
Fig. 2
Fig. 1
- 4. Coloque o frasco com pó sobre uma superfície plana e segure-o firmemente. Pegue o frasco com solvente com o conjunto Nextaro conectado e vire-o de cabeça para baixo. Coloque a parte transparente branca do conector Nextaro sobre o frasco com pó e pressione firmemente até ouvir um clique (fig. 3). Não gire durante a conexão! O solvente flui automaticamente para o frasco com pó.
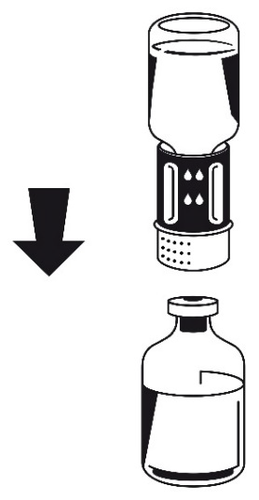
Fig. 3
- 5. Com os dois frascos ainda conectados, agite suavemente o frasco com pó até que o produto esteja dissolvido. Octaplex dissolve-se rapidamente à temperatura ambiente, dando uma solução transparente a ligeiramente azulada. Desrosqueie o Nextaro em duas partes (fig. 4).
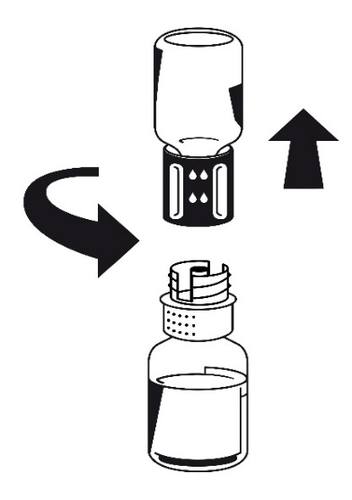
Jogue fora o frasco vazio com solvente com
a parte azul do Nextaro .
Fig. 4
Se o pó não estiver completamente dissolvido ou se formar uma substância sólida, não deve usar o produto.
Instruções para a infusão:
Como medida de precaução, deve verificar a frequência cardíaca do doente antes e durante a infusão do factor IX. Se
ocorrer um aumento significativo da frequência cardíaca, deve reduzir a velocidade da infusão ou interromper a administração.
- 1. Conecte uma seringa de 20 ml (no caso do frasco de 500 UI) ou 40 ml (no caso do frasco de 1000 UI) à conexão luer lock na parte branca do Nextaro . Vire o frasco de cabeça para baixo e aspire a solução para a seringa. Após a transferência da solução, segure firmemente o êmbolo da seringa (segurando para baixo) e retire a seringa do Nextaro . Jogue fora o Nextaro e o frasco vazio.
- 2. Desinfete adequadamente o local da injeção.
- 3. Administre a solução por via intravenosa com uma velocidade de 0,12 ml/kg/min (~3 UI/kg/min), até um máximo de 8 ml/min (~210 UI/min), em condições assépticas.
Não deve entrar sangue na seringa devido ao risco de formação de coágulos com fibrina.
O conjunto Nextaro é destinado a um uso único.
- País de registo
- Substância ativa
- Requer receita médicaSim
- Fabricante
- ImportadorOctapharma Pharmazeutika Produktions.ges.m.b.H. Octapharma S.A.S.
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a OctaplexForma farmacêutica: Pó, 1000 UISubstância ativa: coagulation factor IX, II, VII and X in combinationRequer receita médicaForma farmacêutica: Pó, 250 UISubstância ativa: coagulation factor IX, II, VII and X in combinationRequer receita médicaForma farmacêutica: Pó, 500 UISubstância ativa: coagulation factor IX, II, VII and X in combinationRequer receita médica
Alternativas a Octaplex noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a Octaplex em Espanha
Alternativa a Octaplex em Ukraine
Médicos online para Octaplex
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de Octaplex – sujeita a avaliação médica e regras locais.














