OCTAPLEX, 500 UI PÓ E SOLVENTE PARA SOLUÇÃO INJETÁVEL

Pergunte a um médico sobre a prescrição de OCTAPLEX, 500 UI PÓ E SOLVENTE PARA SOLUÇÃO INJETÁVEL

Como usar OCTAPLEX, 500 UI PÓ E SOLVENTE PARA SOLUÇÃO INJETÁVEL
Introdução
PROSPECTO: INFORMAÇÃO PARA O UTILIZADOR
OCTAPLEX500 UI, pó e dissolvente para solução para perfusão. Complexo de protrombina humana.
OCTAPLEX1000 UI, pó e dissolvente para solução para perfusão. Complexo de protrombina humana.
Leia todo o prospecto detenidamente antes de começar a usar este medicamento, porque contém informações importantes para si.
- Conservar este prospecto, pois pode ter que voltar a lê-lo.
- Se tiver alguma dúvida, consulte o seu médico, farmacêutico ou enfermeiro.
- Este medicamento foi-lhe prescrito apenas para si e não deve dá-lo a outras pessoas, mesmo que tenham os mesmos sintomas que si, pois pode prejudicá-las.
- Se experimentar efeitos adversos, consulte o seu médico, farmacêutico ou enfermeiro, mesmo que se trate de efeitos adversos que não aparecem neste prospecto. Ver secção 4.
Conteúdo do prospecto:
- O que é Octaplex e para que é utilizado
- O que necessita de saber antes de começar a usar Octaplex
- Como usar Octaplex
- Possíveis efeitos adversos
- Conservação de Octaplex
- Conteúdo do envase e informação adicional
1. O que é Octaplex e para que é utilizado
Octaplex pertence ao grupo de medicamentos denominado factores de coagulação. Contém factores de coagulação humanos II, VII, IX e X dependentes de vitamina K.
Octaplex é utilizado para tratar e prevenir hemorragias:
- Causadas por medicamentos chamados antagonistas de vitamina K (como a warfarina). Estes medicamentos bloqueiam o efeito da vitamina K e causam um défice dos factores de coagulação dependentes de vitamina K no seu organismo.
Octaplex é utilizado quando é necessária uma rápida correção do défice.
- Em pessoas que nascem com este défice dos factores de coagulação II e X, dependentes de vitamina K. É utilizado quando não se dispõe do produto de fator de coagulação específico purificado.
2. O que necessita de saber antes de começar a usar Octaplex
Não use Octaplex:
- Se é alérgico ao complexo de protrombina humano ou a algum dos outros componentes deste medicamento (incluídos na secção 6).
- Se é alérgico à heparina ou se a heparina lhe produziu alguma vez uma redução do nível de plaquetas no sangue.
- Se tem deficiência de IgA com anticorpos conhecidos contra a IgA.
Advertências e precauções:
- Peça o conselho de um médico especialista com experiência no tratamento dos distúrbios da coagulação, quando receber Octaplex.
- Se si tem um défice adquirido de factores de coagulação dependentes de vitamina K (por exemplo, o causado pelo tratamento com medicamentos antagonistas de vitamina K), só pode utilizar Octaplex se for necessária uma rápida correção do défice, como em hemorragias importantes ou em cirurgia de emergência. Noutros casos, costuma ser suficiente diminuir a dose de antagonistas de vitamina K e/ou a administração de vitamina K.
- Se si receber um medicamento antagonista de vitamina K (como warfarina), pode ter um risco maior de formar coágulos de sangue. Neste caso, o tratamento com Octaplex pode aumentar o risco.
- Se si nasceu com um défice dos factores de coagulação dependentes de vitamina K, o fator de coagulação específico deve ser utilizado em caso de estar disponível.
- Se ocorrer alguma reação alérgica ou de tipo anafiláctico, interromperão imediatamente a perfusão do medicamento e darão o tratamento apropriado.
- Existe um risco de trombose ou coagulação intravascular disseminada (doença grave com a qual se formam coágulos por todo o corpo) quando receber Octaplex (em particular se o tiver recebido com regularidade). A si será observado cuidadosamente em relação aos sinais ou sintomas de coagulação intravascular ou trombose.
Isso é especialmente importante se si tem uma história de doença cardíaca coronária, doença hepática, se si vai ser operado e também se Octaplex for dado a bebés muito pequenos.
- Não se dispõe de dados sobre o uso de Octaplex em caso de hemorragias durante o nascimento devido a défice de vitamina K em recém-nascidos.
Segurança viral
- Quando se administram medicamentos derivados de plasma ou sangue humano, há que levar a cabo certas medidas para evitar que as infecções passem aos pacientes. Tais medidas incluem uma cuidadosa seleção dos doadores de sangue e plasma que garanta a exclusão daqueles com risco de ser portadores de infecções e o análise dos sinais de vírus/infecções nas doações individuais e nas misturas de plasma. Os fabricantes de tais produtos também incluem etapas no processamento da sangue ou do plasma capazes de inativar ou eliminar os vírus. Apesar destas medidas, quando se administram medicamentos preparados a partir de sangue ou plasma humanos, não se pode excluir totalmente a possibilidade de transmissão de infecção. Isso também se refere a todos os vírus desconhecidos ou emergentes ou outros tipos de infecções.
As medidas tomadas são consideradas eficazes para vírus envoltos, como são o vírus de imunodeficiência humana (VIH), o vírus da hepatite B (VHB) e o vírus da hepatite C (VHC). As medidas tomadas podem ter um valor limitado contra vírus não envoltos, tais como o vírus da hepatite A (VHA) e o parvovirus B19. A infecção por parvovirus B19 pode ser grave para uma mulher grávida (infecção fetal) e para sujeitos com o sistema imunológico deprimido ou que sofrem alguns tipos de anemias (por exemplo, doença falciforme ou anemia hemolítica).
Recomenda-se encarecidamente que cada vez que se lhe administre uma dose de Octaplex, se anote o nome e número de lote do produto, com o fim de manter um vínculo com os lotes utilizados.
- Recomenda-se vacinar-se adequadamente (hepatite A e B) se a si lhe for administrado de forma regular ou repetida complexo de protrombina humana.
Crianças e adolescentes
Não se dispõe de dados sobre o uso de Octaplex em crianças e adolescentes.
Outros medicamentos e Octaplex
- Octaplex não se deve misturar com outros medicamentos.
- Octaplex bloqueia o efeito dos medicamentos antagonistas de vitamina K (como a Warfarina), mas não se conhecem interações com outros medicamentos.
- Octaplex pode afetar os resultados dos testes de coagulação que são sensíveis à heparina.
- Informe o seu médico ou farmacêutico se está a tomar ou tomou recentemente ou possa ter que tomar qualquer outro medicamento.
Gravidez e amamentação
- Octaplex só deve ser utilizado durante a gravidez e a amamentação se for claramente necessário. Consulte o seu médico ou farmacêutico antes de utilizar qualquer medicamento.
Condução e uso de máquinas:
Não se descreveu que Octaplex afete a capacidade de conduzir e usar máquinas.
Informação importante sobre alguns dos componentes de Octaplex
A heparina pode provocar reações alérgicas e diminuição no recuento de células sanguíneas que pode afetar o sistema de coagulação sanguínea. Os pacientes com antecedentes de reações alérgicas induzidas pela heparina devem evitar o uso de medicamentos que contenham heparina.
Este medicamento contém 75 ‑ 125 mg (frasco de 500 UI) ou 150 ‑ 250 mg (frasco de 1000 UI) de sódio (componente principal da sal de mesa/para cozinhar) por frasco. Isso equivale a 3,8 ‑ 6,3% ou 7,5 ‑ 12,5% da ingestão diária máxima de sódio recomendada para um adulto.
3. Como usar Octaplex
O tratamento com Octaplex deve ser supervisionado por um médico com experiência no tratamento dos distúrbios da coagulação do sangue.
- Primeiro, dissolva o pó em água.
- Depois, a solução é administrada através de uma veia (via intravenosa).
A quantidade de Octaplex que vai receber e a duração do seu tratamento dependerão de:
- a seriedade da sua doença
- a zona onde se localiza a hemorragia e a gravidade da mesma, e
- o seu estado geral.
Se usar mais Octaplex do que deve
Em caso de sobredose, aumenta o risco de desenvolver:
- complicações na coagulação (como ataque cardíaco e coágulos nas suas veias ou pulmões)
- coagulação intravascular disseminada (doença grave com a qual se formam coágulos por todo o corpo).
4. Possíveis efeitos adversos
Assim como todos os medicamentos, este medicamento pode produzir efeitos adversos, embora nem todas as pessoas os sofram.
Frequentes: (podem afetar até 1 de cada 10 pessoas)
Coágulos nos vasos sanguíneos
Pouco frequentes: (podem afetar até 1 de cada 100 pessoas)
Ansiedade, aumento na tensão arterial, sintomas semelhantes ao asma, tos com sangue, sangramento do nariz, queimadura na zona de injeção e coágulos no dispositivo.
Raros (podem afetar até 1 de cada 1.000 pessoas)
Podem produzir-se reações de tipo alérgico.
Raramente se observou um aumento temporário nos resultados das provas hepáticas (transaminases).
Os pacientes tratados com Octaplex para a terapia de substituição podem desenvolver anticorpos neutralizantes (inibidores) contra um ou mais dos factores de coagulação contidos. Se aparecerem esses inibidores, a terapia de substituição não será muito eficaz.
Muito raros (podem afetar até 1 de cada 10.000 )
Observou-se um aumento da temperatura (febre).
Existe um risco de coagulação do sangue após a administração deste medicamento.
Frequência não conhecida: (não pode ser estimada a partir dos dados disponíveis).
Reação alérgica grave e choque, hipersensibilidade, tremor, falha do coração, aumento na frequência cardíaca, falha da circulação do sangue, descida na pressão do sangue, falha respiratória, dificuldade para respirar, náuseas, vómitos, erupção cutânea, arrepios.
A heparina nesta preparação pode causar uma repentina queda do número de plaquetas no sangue. Esta é uma reação alérgica chamada “trombocitopenia tipo II induzida por heparina”. Raramente, em pacientes previamente não hipersensitivos à heparina, esta queda no número de plaquetas pode ocorrer entre 6 e 14 dias após o início do tratamento. Em pacientes com hipersensibilidade prévia, esta alteração pode desenvolver-se dentro das horas seguintes ao início do tratamento.
O tratamento com Octaplex deve parar imediatamente em pacientes que mostrem esta reação alérgica. Estes pacientes não devem receber medicamentos que contenham heparina no futuro.
Para informação sobre segurança viral, ver secção 2.
Comunicação de efeitos adversos
Se experimentar qualquer tipo de efeito adverso, consulte o seu médico, farmacêutico ou enfermeiro, mesmo que se trate de possíveis efeitos adversos que não aparecem neste prospecto. Também pode comunicá-los diretamente através do www.notificaRAM.es. Mediante a comunicação de efeitos adversos, si pode contribuir para fornecer mais informações sobre a segurança deste medicamento.
5. Conservação de Octaplex
Mantenha este medicamento fora da vista e do alcance das crianças.
Não utilize este medicamento após a data de validade que aparece na etiqueta. A data de validade é o último dia do mês que se indica.
Conservar o frasco no embalagem exterior para protegê-lo da luz e por debaixo de +25ºC. Não congelar.
O pó deve ser dissolvido sempre justo antes da injeção. A estabilidade da solução foi demonstrada durante um máximo de 8 horas a +25°C. No entanto, para prevenir a contaminação, a solução deve ser utilizada imediatamente e em uma única ocasião.
6. Conteúdo do envase e informação adicional
Composição de Octaplex por frasco e após reconstituição com 20 ml (500UI)/ 40 ml (1000UI) de dissolvente:
Os princípios ativos são:
Nome do componente | Octaplex Quantidade por 500UI frasco | Octaplex Quantidade por 1000UI frasco | OCTAPLEX Quantidade por mL de solução reconstituída |
Proteínas totais: | 260 - 820 mg | 520 - 1640 mg | 13 - 41 mg/ml |
Princípios ativos | |||
Fator II de coagulação humano | 280 - 760 UI | 560 - 1520 UI | 14- 38 UI/ml |
Fator VII de coagulação humano | 180 - 480 UI | 360 - 960 UI | 9 - 24 UI/ml |
Fator IX de coagulação humano | 500 UI | 1000 UI | 25 UI/ml |
Fator X de coagulação humano | 360 - 600 UI | 720 - 1200 UI | 18 - 30 UI/ml |
Outros componentes ativos | |||
Proteína C | 260 - 620 UI | 520 - 1240 UI | 13 - 31 UI/ml |
Proteína S | 240- 640 UI | 480 - 1280 UI | 12- 32 UI/ml |
A atividade específica do Fator IX é ? 0,6 UI/mg de proteínas.
Os demais componentes são heparina, citrato trissódico di-hidrato e água para injeção.
Aspecto do produto e conteúdo do envase
Octaplex é apresentado como um pó e dissolvente para solução para perfusão. É um pó higroscópico branco ou ligeiramente colorido ou uma massa friável em um frasco de vidro. O dissolvente é água para injeção e é fornecido em um frasco de vidro. A solução reconstituída é transparente ou ligeiramente opalescente e pode apresentar cor.
Octaplex é apresentado em um estojo que contém:
-1 frasco com pó para solução injetável.
-1 frasco com o dissolvente, água para injeção
-1 equipamento de transferência Nextaro®.
Titular da autorização de comercialização:
Octapharma S.A.
Avda. Castilla, 2. (P.E. San Fernando)
Ed. Dublin – 2ª Planta
28830 San Fernando de Henares
Madrid
Responsável pela fabricação:
Octapharma Pharmazeutika Produktionsges.m.b.H.Oberlaaer Str. 2351100 ViennaÁustria
ou
Octapharma Lingolsheim S.A.S.
72 Rue du Maréchal Foch
67380 Lingolsheim
França
Este medicamento está autorizado nos estados membros do Espaço Económico Europeu com os seguintes nomes:
Áustria, Bélgica, Bulgária, Chipre, Croácia, Dinamarca, Estónia, Finlândia, França, Alemanha, Hungria, Islândia, Irlanda, Letónia, Lituânia, Luxemburgo, Malta, Holanda, Noruega, Polónia, Portugal, República de Eslovénia, República de Eslováquia, Espanha, Reino Unido: Octaplex
República Checa, Suécia: Ocplex
Itália e Roménia: Pronativ
Data da última revisão deste prospecto: 06/2024
INSTRUÇÕES PARA PROFISSIONAIS DO SETOR SANITÁRIO
A informação geral sobre como usar Octaplex é dada na secção 3.
A seguinte informação é dirigida apenas ao profissional sanitário:
Instruções para o tratamento
Leia todas as instruções e siga-as cuidadosamente.
Durante o procedimento que se descreve a seguir, deve seguir-se uma técnica asséptica.
O produto é reconstituído rapidamente à temperatura ambiente.
A solução reconstituída deve ser clara ou ligeiramente opalescente. Não utilizar soluções turvas ou que apresentem sedimentos. Os produtos reconstituídos devem ser inspecionados visualmente para detectar a possível presença de partículas e a possível decoloração antes da sua administração.
Uma vez reconstituída a solução, deve ser utilizada imediatamente.
Todo o produto não utilizado ou material de desperdício deve ser eliminado de acordo com as exigências locais.
Dosagem:
Hemorragia e prevenção da hemorragia durante o tratamento com antagonistas de vitamina K:
A dose dependerá do Rácio Internacional Normalizado (INR) prévio ao tratamento e do peso corporal. Na seguinte tabela são fornecidas as doses aproximadas (unidades/kg peso corporal do produto reconstituído).
INR prévio ao tratamento | 2 – < 4 | 4 – 6 | > 6 |
Dose de Octaplex (unidades† de fator IX)/kg de peso corporal) | 25 | 35 | 50 |
† Unidades refere-se a unidades internacionais (UI).
A dose baseia-se no peso corporal até um máximo de 100 kg. Por conseguinte, para pacientes que pesem mais de 100 kg, a dose única máxima (UI de fator IX) não deve ser superior a 2500 UI para um INR de 2 - < 4, 3500 UI para um INR de 4 - 6 e 5000 UI para um INR > 6.
Como estas recomendações são empíricas e que a recuperação e a duração do efeito podem variar, é obrigatório monitorizar o INR durante o tratamento.
Hemorragia e profilaxia perioperatória em défice congénito dos factores de coagulação II e X quando não se dispõe do produto de fator de coagulação específico:
O cálculo da dose necessária para o tratamento baseia-se no dado empírico de que aproximadamente 1 UI de fator II ou X por kg de peso corporal aumenta a atividade plasmática do fator II ou X em 0,02 e 0,017 UI/ml, respectivamente.
?Unidades necessárias = peso corporal (kg) x aumento desejado do fator X (UI/mL) x 60
onde 60 (ml/kg) é o inverso da recuperação estimada.
?Unidades necessárias = peso corporal (kg) x aumento desejado do fator II (UI/mL) x 50
Se a recuperação individual for conhecida, deve ser utilizado este valor no cálculo.
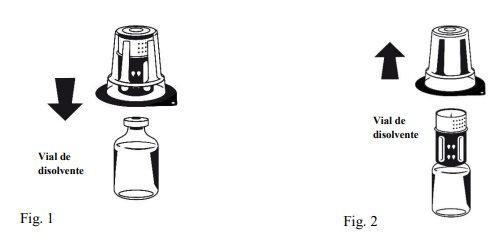
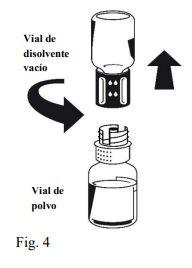
Instruções para a reconstituição:
| |
Octaplex se dissolve rapidamente à temperatura ambiente para dar uma solução incolor ou ligeiramente azulada. Desenrosque as duas partes do Nextaro® (Fig. 4). Descarte o frasco de diluente vazio com a parte azul do Nextaro®. | |
Se o concentrado não se dissolver completamente ou se formar um agregado, não deve ser utilizada a preparação.
Instruções para a perfusão:
Como medida de precaução, deve-se medir o pulso dos pacientes antes e durante a perfusão. Se se produzir um marcado aumento no pulso, deve-se reduzir a velocidade da perfusão ou interromper a administração.
Uma vez que a solução tenha sido transferida, segure com firmeza o êmbolo da seringa (mantendo-o para baixo) e extraia a seringa do Nextaro®. Descarte o Nextaro® e o frasco vazio. |
- Desinfete adequadamente a zona onde se vai aplicar a injeção.
- Injete a solução intravenosamente a uma velocidade de 0,12 ml/kg/min (≈ 3 unidades/kg/min), até uma velocidade máxima de 8 ml/min (≈ 210 unidades/min), utilizando uma técnica asséptica.
Não deve haver fluxo de sangue para a seringa devido ao risco de formação de coágulos de fibrina. O Nextaro® é de um só uso.
A informação detalhada e atualizada deste medicamento está disponível na página web da Agência Española del Medicamento y Productos Sanitarios (AEMPS)
http://www.aemps.gob.es/
- País de registo
- Substância ativa
- Requer receita médicaSim
- Fabricante
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a OCTAPLEX, 500 UI PÓ E SOLVENTE PARA SOLUÇÃO INJETÁVELForma farmacêutica: INJETÁVEL, 1000 UI/frascoSubstância ativa: coagulation factor IX, II, VII and X in combinationFabricante: Csl Behring GmbhRequer receita médicaForma farmacêutica: INJETÁVEL, 500 UISubstância ativa: coagulation factor IX, II, VII and X in combinationFabricante: Csl Behring GmbhRequer receita médicaForma farmacêutica: INJETÁVEL, 250 UISubstância ativa: coagulation factor IX, II, VII and X in combinationFabricante: Prothya Biosolutions Netherlands B.V.Requer receita médica
Alternativas a OCTAPLEX, 500 UI PÓ E SOLVENTE PARA SOLUÇÃO INJETÁVEL noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a OCTAPLEX, 500 UI PÓ E SOLVENTE PARA SOLUÇÃO INJETÁVEL em Polónia
Alternativa a OCTAPLEX, 500 UI PÓ E SOLVENTE PARA SOLUÇÃO INJETÁVEL em Ukraine
Médicos online para OCTAPLEX, 500 UI PÓ E SOLVENTE PARA SOLUÇÃO INJETÁVEL
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de OCTAPLEX, 500 UI PÓ E SOLVENTE PARA SOLUÇÃO INJETÁVEL – sujeita a avaliação médica e regras locais.