
Beriplex P/n 250
Pergunte a um médico sobre a prescrição de Beriplex P/n 250

Como usar Beriplex P/n 250
Folheto para o Paciente
Beriplex P/N 250
Pó e solvente para solução injetável de complexo de protrombina humana
Deve ler atentamente o folheto antes de tomar o medicamento, pois contém informações importantes para o paciente.
- Deve guardar este folheto para poder relê-lo novamente se necessário
- Deve consultar um médico ou farmacêutico se tiver mais alguma dúvida
- Este medicamento foi prescrito exclusivamente para si. Não o deve dar a outros
- O medicamento pode prejudicar outras pessoas, mesmo que tenham os mesmos sintomas que o seu
- Se ocorrerem efeitos indesejados, incluindo quaisquer efeitos indesejados não mencionados neste folheto, deve informar o seu médico ou farmacêutico. Ver ponto 4.
Índice do folheto:
- 1. O que é o medicamento Beriplex P/N 250 e para que é utilizado
- 2. Informações importantes antes de tomar o medicamento Beriplex P/N 250
- 3. Como tomar o medicamento Beriplex P/N 250
- 4. Efeitos indesejados
- 5. Como conservar o medicamento Beriplex P/N 250
- 6. Conteúdo da embalagem e outras informações
1. O que é o medicamento Beriplex P/N 250 e para que é utilizado
O que é o Beriplex P/N 250
O Beriplex P/N 250 está disponível como pó e solvente para solução injetável. É um pó branco ou ligeiramente colorido ou uma massa congelada quebradiça. A solução reconstituída é para injeção intravenosa.
O Beriplex P/N 250 é produzido a partir de plasma humano (parte líquida do sangue) e contém fatores de coagulação humanos II, VII, IX e X. Os concentrados que contêm os fatores de coagulação acima mencionados são chamados de produtos do complexo de protrombina. Os fatores de coagulação dependentes de vitamina K - II, VII, IX e X - desempenham um papel importante no processo de coagulação. A falta de qualquer um dos fatores de coagulação mencionados pode fazer com que o sangue não coagule tão rapidamente quanto deveria e aumente o risco de sangramento. A reposição dos fatores de coagulação II, VII, IX e X através da administração do medicamento Beriplex P/N 250 leva à correção do mecanismo de coagulação.
Para que é utilizado o Beriplex P/N 250
O Beriplex P/N 250 é utilizado para prevenir (durante cirurgias) e tratar sangramentos causados por deficiência adquirida ou congênita de fatores de coagulação dependentes de vitamina K (II, VII, IX e X) no sangue, quando um medicamento que contenha um fator de coagulação específico não estiver disponível.
2. Informações importantes antes de tomar o medicamento Beriplex P/N 250
No ponto abaixo, estão incluídas informações que o paciente e o médico devem ler antes de tomar o medicamento Beriplex P/N 250.
Quando não tomar o medicamento Beriplex P/N 250:
se o paciente tiver alergia a substâncias ativas ou a qualquer um dos outros componentes deste medicamento (listados no ponto 6).
Deve informar o médico sobre alergias a medicamentos ou alimentos.
- se houver risco aumentado de formação de coágulos (pacientes com risco de coagulação intravascular disseminada)
- em caso de reação alérgica à heparina, que cause redução do número de plaquetas (trombocitopenia induzida por heparina, TIH tipo II).
Deve informar o médico ou farmacêutico se tiver alguma dessas condições.
Advertências e precauções
Antes de iniciar o tratamento com o medicamento Beriplex, deve discutir com o médico ou farmacêutico.
- Em caso de deficiência adquirida de fatores de coagulação dependentes de vitamina K. Isso pode ser causado pela ingestão de medicamentos que bloqueiam a ação da vitamina K. O Beriplex P/N 250 só deve ser utilizado em caso de necessidade de correção rápida do nível de fatores de coagulação do complexo de protrombina, por exemplo, em caso de sangramentos graves ou cirurgias de emergência.
- Em caso de deficiência congênita de qualquer um dos fatores de coagulação dependentes de vitamina K, deve-se utilizar, sempre que possível, um medicamento que contenha um fator de coagulação específico.
- Em caso de reação alérgica ou anafilática (reação alérgica grave que causa dificuldade respiratória ou tontura):
A administração do medicamento Beriplex P/N 250 deve ser interrompida imediatamente (por exemplo, parar a injeção).
- Se houver risco aumentado de formação de coágulos nos vasos sanguíneos (trombose), especialmente nos seguintes casos:
- em pacientes após ataque cardíaco (com doença coronariana diagnosticada ou infarto do miocárdio)
- em pacientes com doenças hepáticas
- em pacientes logo antes e depois de cirurgias
- em recém-nascidos
- em pacientes com risco aumentado de formação de coágulos (pacientes com risco de tromboembolismo ou coagulação intravascular disseminada, ou deficiência de inibidores de coagulação)
- Se houver risco aumentado de distúrbios de coagulação causados por aumento do consumo de plaquetas ou fatores de coagulação. O tratamento com o medicamento Beriplex P/N 250 pode ser iniciado após a conclusão do tratamento da doença subjacente.
- Redução da produção de plaquetas induzida por heparina (trombocitopenia induzida por heparina, TIH tipo II). A heparina, uma proteína que dissolve coágulos sanguíneos, é um componente do medicamento Beriplex. A redução significativa do número de plaquetas pode estar relacionada a:
- formação de coágulos nos vasos sanguíneos das pernas,
- aumento do risco de formação de coágulos,
- em alguns casos, com erupções cutâneas no local da injeção,
- equimoses e
- aparecimento de fezes escuras. Nesses casos, a ação da heparina pode ser prejudicada (tolerância à heparina). Se ocorrerem esses sintomas, deve-se interromper imediatamente a administração do medicamento e consultar um médico. No futuro, não deve-se tomar medicamentos que contenham heparina.
- Uma forma especial de inflamação renal foi relatada após o tratamento de pacientes com hemofilia B com inibidores do fator IX. Esses pacientes tinham histórico de reações alérgicas.
O médico deve considerar os benefícios do tratamento com o medicamento Beriplex P/N 250 em relação ao risco de ocorrência das complicações mencionadas.
Segurança contra vírus
Quando os medicamentos são obtidos a partir de sangue humano ou plasma, são utilizadas várias medidas para evitar a transmissão de agentes infecciosos ao paciente. Essas medidas incluem:
- seleção apropriada de doadores de sangue e plasma para evitar a transmissão de agentes infecciosos,
- teste de doadores individuais e de pools de plasma para detectar vírus e outras infecções,
- inclusão de etapas no processo de fabricação para inativar ou remover vírus.
Apesar da utilização dessas medidas de segurança, não é possível excluir completamente o risco de doenças infecciosas ao utilizar medicamentos obtidos a partir de sangue humano ou plasma, devido à possibilidade de transmissão de agentes infecciosos. Isso se aplica também a patógenos desconhecidos e outros tipos de infecções.
As medidas utilizadas são consideradas eficazes contra vírus envelopados, como o vírus da imunodeficiência humana (HIV, vírus que causa a AIDS), vírus da hepatite B, vírus da hepatite C (hepatite viral) e parvovirus B19.
O médico pode recomendar a vacinação contra a hepatite viral A e B se o paciente receber regularmente medicamentos obtidos a partir de plasma humano.
É altamente recomendável que, a cada administração do medicamento Beriplex P/N 250, seja registrada a nome e o lote do medicamento nos registros médicos para documentar os lotes de medicamento utilizados.
Beriplex P/N 250 e outros medicamentos
- Deve informar o médico ou farmacêutico sobre todos os medicamentos que está tomando atualmente ou recentemente, bem como sobre medicamentos que planeja tomar.
- O Beriplex P/N 250 pode inibir a ação de antagonistas da vitamina K. Não há interações conhecidas com outros medicamentos.
- O medicamento Beriplex P/N 250 não deve ser misturado com outros medicamentos, exceto aqueles mencionados no ponto 6.
Gravidez, amamentação e fertilidade
- Se estiver grávida, amamentando ou suspeitar que está grávida, ou se planeja engravidar, deve consultar um médico ou farmacêutico antes de tomar este medicamento.
- Em mulheres grávidas ou em período de amamentação, o medicamento Beriplex P/N 250 deve ser utilizado apenas em casos justificados.
- Não há dados disponíveis sobre o efeito na fertilidade.
Condução de veículos e operação de máquinas
Não há estudos adequados que documentem o efeito do medicamento na condução de veículos e operação de máquinas.
Beriplex P/N 250 contém sódio
O Beriplex P/N 250 contém até 343 mg de sódio (aproximadamente 15 milimoles) em 100 ml. Essa quantidade deve ser considerada em pacientes com dieta controlada de sódio.
3. Como tomar o medicamento Beriplex P/N 250
O tratamento deve ser iniciado sob supervisão de um médico experiente no tratamento desses distúrbios.
Posologia
A dose recomendada de fatores II, VII, IX e X, bem como a duração do tratamento, depende de vários fatores, como peso corporal, gravidade e curso da doença, localização e intensidade do sangramento, e necessidade de prevenir sangramentos durante cirurgias ou procedimentos diagnósticos (ver ponto "Informações destinadas apenas ao pessoal médico").
Em caso de dúvidas sobre a administração do medicamento, deve-se consultar um médico ou farmacêutico.
Superdose
Durante o tratamento, o médico deve monitorar regularmente os parâmetros de coagulação.
A administração de doses elevadas de concentrado de fatores de coagulação do complexo de protrombina foi associada a infarto do miocárdio, desenvolvimento de coagulação intravascular disseminada e formação de coágulos nos vasos sanguíneos em pacientes com risco aumentado de desenvolver esses distúrbios.
4. Efeitos indesejados
Como qualquer medicamento, o Beriplex P/N 250 pode causar efeitos indesejados, embora não todos os pacientes os experimentem.
Os seguintes efeitos indesejados foram observados frequentemente (em menos de 1 em 10 pacientes):
- Risco aumentado de formação de coágulos (ver ponto 2)
- Dor de cabeça
- Febre
Os seguintes efeitos indesejados foram observados não muito frequentemente (em menos de 1 em 100 pacientes):
- Sensibilidade ou reações alérgicas (ver ponto 2)
A frequência de ocorrência dos seguintes efeitos indesejados é desconhecida (não pode ser estimada com base nos dados disponíveis):
- Sangramentos graves devido à coagulação excessiva
- Reações anafiláticas com choque incluído (ver ponto 2)
- Formação de anticorpos circulantes que inibem um ou mais fatores de coagulação
Crianças e adolescentes
Não há dados disponíveis sobre a administração do medicamento Beriplex em crianças e adolescentes.
Notificação de efeitos indesejados
Se ocorrerem efeitos indesejados, incluindo quaisquer efeitos indesejados não mencionados neste folheto, deve-se informar o médico ou farmacêutico. Os efeitos indesejados podem ser notificados diretamente ao Departamento de Monitoramento de Efeitos Indesejados de Produtos Farmacêuticos da Agência Nacional de Vigilância Sanitária
Endereço:
Telefone:
Fax:
Site:
Os efeitos indesejados também podem ser notificados ao titular da autorização de comercialização.
A notificação de efeitos indesejados pode ajudar a coletar mais informações sobre a segurança do medicamento.
5. Como conservar o medicamento Beriplex P/N 250
- O medicamento deve ser conservado em local não acessível a crianças.
- Não utilizar o medicamento Beriplex P/N 250 após a data de validade impressa na embalagem e rótulo.
- Não conservar a uma temperatura superior a 25°C.
- Não congelar.
- A ampola deve ser conservada na embalagem exterior para proteger da luz.
- O Beriplex P/N 250 não contém conservantes, o produto reconstituído deve ser utilizado imediatamente.
6. Conteúdo da embalagem e outras informações
O que contém o Beriplex P/N 250
O Beriplex P/N 250 contém 200 - 310 UI de fator IX humano por ampola.
A substância ativa do medicamento é:
Concentrado de fatores de coagulação humanos II, VII, IX e X, proteínas C e S.
Os outros componentes são:
Antitrombina III humana, heparina, albumina humana, cloreto de sódio, citrato de sódio, HCl ou NaOH (em pequenas quantidades para ajustar o pH).
Solvente : Água para injeção.
Como é o medicamento Beriplex P/N 250 e o que contém a embalagem
O Beriplex P/N 250 é um pó branco ou ligeiramente colorido e é fornecido com água para injeção como solvente. O pó deve ser reconstituído em 10 ml de água para injeção.
A solução reconstituída deve ser transparente ou ligeiramente opalescente, o que significa que pode apresentar um brilho quando observada à luz, e não deve conter partículas sólidas.
Embalagens disponíveis
A embalagem com o medicamento na dose de 250 UI contém:
- 1 ampola de pó
- 1 ampola de água para injeção de 10 ml
- 1 sistema de transferência 20/20 com filtro
Nome e endereço do titular da autorização de comercialização e do fabricante:
CSL Behring GmbH
Emil-von-Behring-Str. 76
35041 Marburg
Alemanha
Este medicamento está autorizado para comercialização nos países membros da Área Econômica Europeia sob as seguintes denominações:
Áustria
Beriplex P/N 250 I.E. Pó e solvente para solução injetável
Dinamarca
Confidex
Finlândia
Confidex 250 IU pó e solvente para solução injetável
França
Confidex 250 UI pó e solvente para solução injetável
Alemanha
Beriplex P/N 250
Irlanda
Beriplex P/N 250 pó e solvente para solução injetável
Países Baixos
Beriplex P/N 250 IE pó e solvente para solução injetável
Noruega
Confidex 250 IU pó e solvente para solução injetável
Polônia
Beriplex P/N 250
Suécia
Confidex 250 IE pó e solvente para solução injetável
Reino Unido
Beriplex P/N 250 IU pó e solvente para solução injetável
Data da última atualização do folheto:
Informações destinadas apenas ao pessoal médico
Composição qualitativa e quantitativa
O Beriplex P/N 250 contém nominalmente as seguintes quantidades de UI de fatores de coagulação humanos, conforme apresentado na tabela abaixo:
| Nome do componente | Conteúdo após reconstituição (UI/ml) | Conteúdo em uma ampola de Beriplex P/N 250 (UI) |
| Substâncias ativas | ||
| Fator II de coagulação sanguínea humano |
|
|
| Fator VII de coagulação sanguínea humano |
|
|
| Fator IX de coagulação sanguínea humano |
|
|
| Fator X de coagulação sanguínea humano |
|
|
| Outras substâncias ativas | ||
| Proteína C |
| 150 -450 |
| Proteína S |
|
|
O conteúdo de proteína total após reconstituição é de 6-14 mg/ml na solução.
A atividade específica do fator IX é de 2,5 UI por mg de proteína total.
A atividade de todos os fatores de coagulação, bem como a das proteínas C e S (antígenos), foi testada de acordo com os padrões internacionais atuais da OMS.
Posologia e modo de administração Posologia
Abaixo estão apresentadas apenas as diretrizes gerais de posologia.
A dose e a frequência de administração devem ser calculadas individualmente para cada paciente.
Os intervalos entre as doses devem ser ajustados com base nos valores do período de meia-vida dos fatores de coagulação do complexo de protrombina.
A dose individual é determinada com base na monitorização regular da atividade no soro dos fatores de coagulação individuais ou com base nos resultados de testes laboratoriais que avaliam a atividade geral do complexo de protrombina (INR, teste de Quick) e na monitorização contínua do estado clínico do paciente.
Em caso de intervenções cirúrgicas maiores, é necessário um monitoramento cuidadoso do tratamento de substituição (testes para fatores de coagulação individuais e testes gerais para fatores de coagulação do complexo de protrombina).
- Sangramentos e profilaxia de sangramentos perioperatórios devido ao tratamento com antagonistas da vitamina K:
A dose do medicamento depende do valor do INR antes do início do tratamento e do valor do INR que o paciente deve atingir.
O valor do INR antes do tratamento deve ser medido no menor tempo possível antes da administração do medicamento para permitir o cálculo da dose apropriada do produto.
A tabela abaixo fornece as doses aproximadas (ml/kg de peso corporal de produto reconstituído e UI de fator IX/kg de peso corporal) para atingir a normalização do INR (ou seja, INR ≤ 1,3) em diferentes valores iniciais de INR.
| Valor do INR antes do tratamento | 2,0 – 3,9 | 4,0 – 6,0 | > 6,0 |
| Dose aproximada em ml/kg de peso corporal | 1 | 1,4 | 2 |
| Dose aproximada em UI de fator IX/kg de peso corporal | 25 | 35 | 50 |
A posologia é calculada com base no peso corporal, desde que não exceda 100 kg.
Em pacientes com peso corporal superior a 100 kg, a dose máxima única (UI de fator IX) não deve exceder 2500 UI para valores de INR de 2,0 a 3,9; 3500 UI para valores de INR de 4,0 a 6,0; e 5000 UI para valores de INR > 6,0.
A normalização dos distúrbios hemostáticos devido ao tratamento com antagonistas da vitamina K é geralmente alcançada após aproximadamente 30 minutos após a injeção.
A administração concomitante de vitamina K deve ser considerada em pacientes que recebem Beriplex para reverter rapidamente a ação dos antagonistas da vitamina K, pois o efeito da vitamina K é geralmente alcançado após 4-6 horas.
A administração repetida de Beriplex em pacientes que necessitam de reversão rápida da ação dos antagonistas da vitamina K não é apoiada por estudos clínicos e, portanto, não é recomendada.
Essas recomendações são baseadas em estudos clínicos realizados em um número limitado de indivíduos.
É necessário monitorar o valor do INR durante o tratamento, pois a eficácia e a duração da ação podem variar entre pacientes.
- Sangramentos e profilaxia perioperatória em pacientes com deficiências congênitas de fatores de coagulação dependentes de vitamina K, quando a administração de um medicamento que contenha um fator de coagulação específico não é possível
O cálculo da dose necessária de concentrado de fatores de coagulação do complexo de protrombina é baseado em estudos clínicos:
- 1 UI de fator IX por kg de peso corporal aumenta a atividade do fator IX no soro em 1,3% (0,013 UI/ml) em relação à norma,
- 1 UI de fator VII por kg de peso corporal aumenta a atividade do fator VII no soro em 1,7% em relação à norma (0,017 UI/ml),
- 1 UI de fator II por kg de peso corporal aumenta a atividade do fator II no soro em 1,9% em relação à norma (0,019 UI/ml),
- 1 UI de fator X por kg de peso corporal aumenta a atividade do fator X no soro em 1,9% em relação à norma (0,019 UI/ml).
A dose do fator de coagulação é expressa em unidades internacionais (UI), de acordo com o padrão internacional para cada fator de coagulação aprovado pela Organização Mundial da Saúde (OMS).
A atividade do fator de coagulação no soro é expressa em porcentagem (em relação ao soro humano normal) ou em unidades internacionais (de acordo com o padrão internacional para o fator de coagulação específico no soro).
Uma unidade internacional (UI) de atividade do fator de coagulação é igual à atividade desse fator contida em 1 ml de soro humano normal.
Por exemplo, o cálculo da dose necessária de fator X é baseado na observação empírica de que 1 UI de fator X por kg de peso corporal aumenta a atividade do fator X no soro em 0,019 UI/ml.
A dose necessária é calculada usando a seguinte fórmula:
Número de unidades necessárias = peso corporal (kg) x aumento desejado da atividade do fator X (UI/ml) x 53,
onde 53 (ml/kg) é o inverso do valor estimado de recuperação.
Se o valor individual de recuperação for conhecido, deve ser utilizado para os cálculos.
Os cálculos baseados em dados de indivíduos saudáveis forneceriam um valor mais baixo da dose necessária.
Os dados do produto são baseados em estudos clínicos realizados em voluntários saudáveis (N = 15), na reversão da ação dos antagonistas da vitamina K no tratamento de sangramentos graves ou na profilaxia de sangramentos perioperatórios (N = 98, N = 43).
Crianças e adolescentes
A segurança e eficácia do medicamento Beriplex P/N 250 em crianças e adolescentes não foram estabelecidas em estudos clínicos controlados.
Idosos
A posologia e o modo de administração em idosos (> 65 anos) são os mesmos que os recomendados para a população em geral.
Modo de administração Instruções gerais
- A solução deve ser transparente ou ligeiramente opalescente. Após a filtração e a retirada da solução reconstituída (ver abaixo), antes da administração, deve-se verificar se não contém partículas visíveis a olho nu ou descoloração. Não deve ser administrada solução turva ou que contenha resíduos ou partículas.
- A reconstituição e a retirada da ampola devem ser realizadas em condições assépticas.
Reconstituição
Deve-se levar o solvente à temperatura ambiente.
Certificar-se de que as tampas das ampolas de pó e solvente sejam removidas, limpar as rolhas de borracha com um antisséptico e deixar as rolhas secarem antes de abrir o pacote Mix2Vial.
1 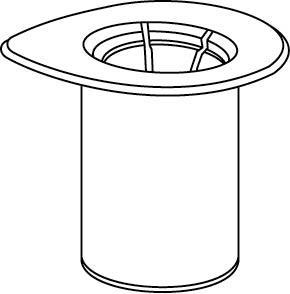 |
|
2 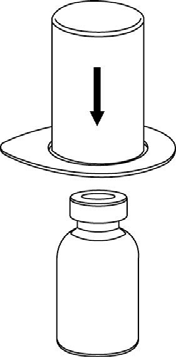 |
|
3 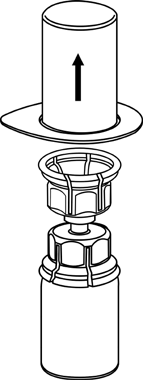 |
|
4 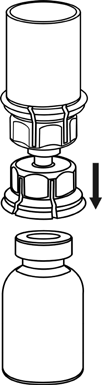 |
|
5 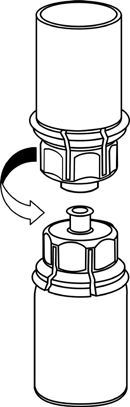 |
|
6 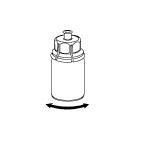 |
|
7 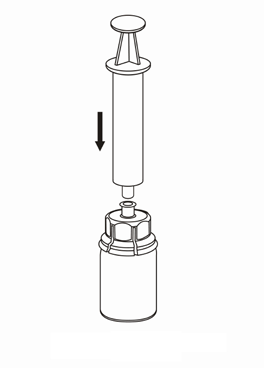 |
|
Retirada e administração
8 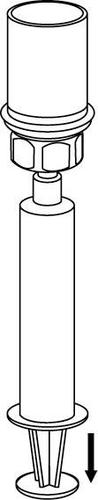 |
|
9 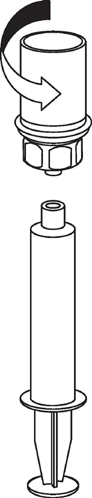 |
|
Deve-se ter cuidado para que o sangue não entre na seringa cheia de produto, pois isso pode causar uma reação dos fatores de coagulação presentes no produto e formar coágulos de fibrina, que podem ser administrados ao paciente.
Se for necessário administrar mais de uma ampola do produto Beriplex, é possível combinar várias ampolas para administração como uma infusão única, utilizando um conjunto de administração disponível no mercado.
A solução do produto Beriplex não deve ser diluída.
A solução reconstituída deve ser administrada por via intravenosa (não mais rápido do que 8 ml/min*).
Qualquer resíduo não utilizado do produto ou seus descartes deve ser eliminado de acordo com as regulamentações locais.
Advertências e precauções especiais de uso
Não há dados clínicos disponíveis sobre o uso do medicamento Beriplex P/N 250 em sangramentos pós-parto devido à deficiência de vitamina K em recém-nascidos.
_____________________________________________________
*Nos estudos clínicos do Beriplex, pacientes com peso inferior a 70 kg tinham uma dose recomendada com uma velocidade máxima de infusão de 0,12 ml/kg/min (abaixo de 8 ml/min).
Observações sobre o monitoramento da contagem de plaquetas:
Deve-se monitorar rigorosamente a contagem de plaquetas.
Interações com outros medicamentos e outras formas de interação
Em caso de realização de testes de coagulação sensíveis à presença de heparina, em pacientes que recebem altas doses de fatores de coagulação do complexo de protrombina, os resultados dos testes devem levar em conta a dose de heparina contida no produto.
- País de registo
- Substância ativa
- Requer receita médicaSim
- ImportadorCSL Behring GmbH
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a Beriplex P/n 250Forma farmacêutica: Pó, 1000 UISubstância ativa: coagulation factor IX, II, VII and X in combinationRequer receita médicaForma farmacêutica: Pó, 500 UISubstância ativa: coagulation factor IX, II, VII and X in combinationRequer receita médicaForma farmacêutica: Pó, 500 UISubstância ativa: coagulation factor IX, II, VII and X in combinationRequer receita médica
Alternativas a Beriplex P/n 250 noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a Beriplex P/n 250 em Испания
Alternativa a Beriplex P/n 250 em Украина
Médicos online para Beriplex P/n 250
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de Beriplex P/n 250 – sujeita a avaliação médica e regras locais.














