
Numeta G13%e Preterm

Pergunte a um médico sobre a prescrição de Numeta G13%e Preterm

Como usar Numeta G13%e Preterm
Folheto informativo para o utilizador
NUMETA G13%E Pré-termo, emulsão para infusão
Deve ler atentamente o conteúdo do folheto antes de administrar o medicamento, pois contém
informações importantes para o doente.
- Deve conservar este folheto para poder relê-lo se necessário.
- Em caso de dúvidas, deve consultar o médico do seu filho, farmacêutico ou enfermeira.
- Se o seu filho apresentar algum efeito secundário, incluindo quaisquer efeitos secundários não mencionados neste folheto, deve informar o médico assistente ou enfermeira. Ver ponto 4.
Índice do folheto
- 1. O que é o medicamento NUMETA G13%E Pré-termo e para que é utilizado
- 2. Informações importantes antes de administrar o medicamento NUMETA G13%E Pré-termo ao seu filho
- 3. Como administrar o medicamento NUMETA G13%E Pré-termo
- 4. Efeitos secundários possíveis
- 5. Como conservar o medicamento NUMETA G13%E Pré-termo
- 6. Conteúdo do pacote e outras informações
1. O que é o medicamento NUMETA G13%E Pré-termo e para que é utilizado
O medicamento NUMETA G13%E Pré-termo é uma emulsão especial para nutrição destinada a recém-nascidos prematuros. É administrado através de um tubo inserido numa veia do seu filho, quando o seu filho não pode ingerir todos os nutrientes necessários por via oral.
- solução de glicose a 50%;
- solução pediátrica de aminoácidos com eletrólitos a 5,9%;
- emulsão lipídica a 12,5%.
Consoante as necessidades do seu filho, duas ou três dessas soluções são misturadas no saco antes da administração ao seu filho.
2. Informações importantes antes de administrar o medicamento NUMETA G13%E Pré-termo ao seu filho
Quando o medicamento NUMETA G13%E Pré-termo não deve ser administrado ao seu filho:
Em caso de soluções de glicose e aminoácidos com eletrólitos misturadas no saco (“2 em 1”):
- se o seu filho for alérgico a ovos, soja, amendoins ou a qualquer um dos outros componentes deste medicamento ou aos componentes do recipiente (listados no ponto 6);
- se o organismo do seu filho não puder utilizar os componentes de construção das proteínas;
- se o sangue do seu filho contiver uma grande concentração de qualquer um dos eletrólitos presentes no medicamento NUMETA G13%E Pré-termo;
- o medicamento NUMETA G13%E Pré-termo (ou outras soluções contendo cálcio) não deve ser administrado simultaneamente com ceftriaxona (antibiótico), mesmo que sejam utilizadas linhas de infusão separadas. Existe o risco de formação de partículas no sangue do recém-nascido, que podem levar à morte.
- se o seu filho tiver hiperglicemia (concentração de açúcar no sangue particularmente elevada).
Em caso de soluções com glicose, aminoácidos com eletrólitos e emulsão lipídica misturadas no saco (“3 em 1”):
Em todos os casos mencionados acima para o medicamento “2 em 1” e, além disso:
- se o seu filho apresentar uma concentração particularmente elevada de lipídios no sangue.
Em todos os casos, o médico decide a administração do medicamento, tendo em conta a idade, o peso e o estado clínico do seu filho. O médico também considerará os resultados de todos os exames realizados.
Precauções e advertências
Antes de iniciar a administração do medicamento NUMETA G13%E Pré-termo, deve discutir com o médico assistente ou enfermeira.
Reações alérgicas:
A infusão deve ser interrompida imediatamente se ocorrerem quaisquer sinais ou sintomas de reação alérgica (como febre, suor, calafrios, dor de cabeça, erupções cutâneas ou dificuldades respiratórias). Este medicamento contém óleo de soja, que pode causar reações de sensibilidade em casos raros. Em algumas pessoas alérgicas a proteínas de amendoim, também foi observada sensibilidade ao óleo de soja.
Risco de formação de depósitos com ceftriaxona (antibiótico):
O antibiótico ceftriaxona não deve ser misturado ou administrado simultaneamente com qualquer solução contendo cálcio (incluindo o medicamento NUMETA G13%E Pré-termo) por via de infusão intravenosa.
Formação de pequenas partículas nos vasos sanguíneos nos pulmões:
Dificuldades respiratórias também podem ser um sinal de que se formaram pequenas partículas que bloqueiam os vasos sanguíneos nos pulmões (depósitos nos vasos pulmonares). Se o seu filho apresentar dificuldades respiratórias, deve informar o médico ou enfermeira. Eles decidirão sobre as medidas apropriadas.
Infecção e septicemia:
O médico estará atento para detectar sinais de infecção. A utilização de técnicas assépticas (procedimentos que protegem contra microorganismos) ao inserir e manter o cateter e ao preparar a mistura nutricional pode reduzir o risco de infecção.
Síndrome de sobrecarga lipídica:
Durante a administração de medicamentos semelhantes, foi relatada a ocorrência de síndrome de sobrecarga lipídica.
Alterações nos níveis de substâncias químicas no sangue:
O médico verificará e monitorizará o estado dos fluidos do seu filho, a composição química do sangue e os níveis de outras substâncias durante o tratamento com o medicamento NUMETA G13%E Pré-termo.
Monitorização e ajuste:
O médico estará atento e ajustará a administração do medicamento NUMETA G13%E Pré-termo às necessidades individuais do seu filho, especialmente nas seguintes situações:
- estados graves pós-traumáticos;
- diabetes grave;
- choque;
- ataque cardíaco;
- infecção grave;
- certos tipos de coma.
Uso com precaução:
O medicamento NUMETA G13%E Pré-termo deve ser utilizado com precaução se o seu filho apresentar:
- edema pulmonar (líquido nos pulmões) ou insuficiência cardíaca;
- distúrbios graves da função hepática;
- distúrbios da absorção de nutrientes;
- concentração elevada de açúcar no sangue;
- problemas renais;
- distúrbios graves do metabolismo (quando o processo de decomposição de substâncias não ocorre normalmente);
- distúrbios da coagulação do sangue.
O estado dos fluidos no organismo do seu filho, os resultados dos exames hepáticos e (ou) outros resultados dos exames de sangue serão verificados cuidadosamente.
Interacções do medicamento NUMETA G13%E Pré-termo com outros medicamentos
Deve informar o médico sobre todos os medicamentos que o seu filho está a tomar atualmente ou recentemente, bem como sobre os medicamentos que serão administrados.
O medicamento NUMETA G13%E Pré-termo não deve ser administrado simultaneamente com:
- ceftriaxona(antibiótico), mesmo que sejam utilizadas linhas de infusão separadas, devido ao risco de formação de partículas sólidas;
- sangueatravés do mesmo conjunto de infusão, devido ao risco de pseudoaglutinação (glóbulos vermelhos que se aglutinam);
- ampicilina, fosfenitoína ou furosemidaatravés da mesma linha de infusão, devido ao risco de formação de partículas sólidas.
Anticoagulantes como a warfarina:
O médico estará atento se o seu filho estiver a tomar anticoagulantes como a warfarina. Estes medicamentos são utilizados para prevenir a coagulação do sangue.
Exames laboratoriais:
Os lipídios presentes nesta emulsão podem afetar os resultados de certos exames laboratoriais.
Interacções do medicamento NUMETA G13%E Pré-termo com medicamentos que podem afetar os níveis de potássio/metabolismo:
O medicamento NUMETA G13%E Pré-termo contém potássio. Concentrações elevadas de potássio no sangue podem causar arritmias cardíacas.
3. Como administrar o medicamento NUMETA G13%E Pré-termo
O medicamento NUMETA G13%E Pré-termo deve ser sempre administrado ao seu filho de acordo com as recomendações do médico.
Grupo etário
O medicamento NUMETA G13%E Pré-termo foi projetado para atender às necessidades nutricionais de recém-nascidos prematuros.
Administração
Este medicamento é uma emulsão para infusão. É administrado através de um tubo de plástico inserido numa veia do braço ou numa grande veia no peito do seu filho.
Dose e duração do tratamento
O médico decidirá a dose do medicamento e por quanto tempo será administrado. A dose depende das necessidades nutricionais do seu filho.
Administração de uma dose maior do que a recomendada do medicamento NUMETA G13%E Pré-termo ao seu filho
Sintomas
Uma dose excessiva do medicamento ou uma administração demasiado rápida pode causar:
- náuseas (enjoo);
- vômitos;
- convulsões;
- distúrbios eletrolíticos (quantidades anormais de eletrólitos no sangue);
- sintomas de hipervolemia (volume aumentado de sangue circulante, excesso de líquido nos vasos sanguíneos);
- acidose (aumento da acidez do sangue). Nesses casos, a infusão deve ser interrompida imediatamente. O médico decidirá se são necessárias medidas adicionais.
A sobrecarga de lipídios presentes no medicamento NUMETA G13%E Pré-termo pode levar à ocorrência de “síndrome de sobrecarga lipídica”, que geralmente desaparece após a interrupção da infusão.
4. Efeitos secundários possíveis
Como qualquer medicamento, o medicamento NUMETA G13%E Pré-termo pode causar efeitos secundários, embora não todos os doentes os experimentem.
Notificação de efeitos secundários
Se o seu filho apresentar algum efeito secundário, deve consultar o médico ou enfermeira.
5. Como conservar o medicamento NUMETA G13%E Pré-termo
O medicamento deve ser conservado num local fora do alcance das crianças, quando não estiver a ser administrado.
Não deve ser utilizado após o prazo de validade impresso no saco e na embalagem exterior (MM/AAAA). O prazo de validade é o último dia do mês indicado.
Não congelar.
Conservar no saco de proteção.
Os medicamentos não devem ser eliminados na canalização ou nos contentores de lixo doméstico. Deve perguntar ao farmacêutico como eliminar os medicamentos de que já não precisa. Este procedimento ajudará a proteger o ambiente.
6. Conteúdo do pacote e outras informações
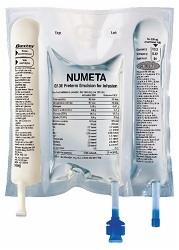
Como é o medicamento NUMETA G13%E Pré-termo e que conteúdo tem o pacote
O medicamento NUMETA G13%E Pré-termo está num saco tricamarado. O conteúdo de cada saco é estéril e consiste em solução de glicose, solução de aminoácidos para crianças com eletrólitos e emulsão lipídica, conforme descrito abaixo.
| Tamanho do recipiente | 50% solução de glicose | 5,9% solução de aminoácidos com eletrólitos | 12,5% emulsão lipídica |
| 300 ml | 80 ml | 160 ml | 60 ml |
Aspeto antes da preparação:
- As soluções nos compartimentos que contêm aminoácidos e glicose são transparentes, incolores ou ligeiramente amareladas
- A emulsão lipídica é um líquido homogêneo e branco leitoso
Aspeto após a preparação:
- As soluções para infusão “2 em 1” (aminoácidos/eletrólitos e glicose) são transparentes, incolores ou ligeiramente amareladas
- A emulsão para infusão “3 em 1” é homogênea e branca leitosa
O saco tricamarado é um saco plástico multicamada.
Para proteger contra o contacto com o ar, o saco NUMETA G13%E Pré-termo está embalado num saco de proteção que protege contra a entrada de oxigénio, que também contém um absorvente de oxigénio e um indicador de oxigénio.
Tamanho dos pacotes
sacos de 300 ml: 10 sacos em caixa de cartão
1 saco de 300 ml
Nem todos os tipos de embalagens podem estar disponíveis.
Responsável e fabricante
Responsável
Baxter Portugal, Unipessoal Lda.
Rua do Centro Empresarial do Porto, 27, 1º
4200-467 Porto
Fabricante
Baxter S.A.
Boulevard René Branquart 80
7860 Lessines
Bélgica
Este medicamento está autorizado para comercialização nos países membros do Espaço Económico Europeu sob as seguintes designações:
| País | Designação |
| Áustria | Numeta G 13 % E Emulsion zur Infusion |
| Alemanha | Numeta G 13 % E Emulsion zur Infusion |
| Bélgica | NUMETA G13%E, émulsion pour perfusion |
| França | NUMETAH G13%E PREMATURES, émulsion pour perfusion |
| Dinamarca | Numeta G13E |
| Noruega | Numeta G13E |
| Suécia | Numeta G13E |
| República Checa | NUMETA G 13 % E |
| Grécia | NUMETA Preterm G 13 E |
| Países Baixos | NUMETA G13%E emulsie voor infusie |
| Irlanda | Numeta G13%E Preterm, Emulsion for Infusion |
| Malta | Numeta G13%E Preterm, Emulsion for Infusion |
| Reino Unido | Numeta G13%E Preterm, Emulsion for Infusion |
| Itália | NUMETA G13E emulsione per infusione |
| Finlândia | Numeta G13E infuusioneste, emulsio |
| Polónia | NUMETA G13%E Preterm |
| Portugal | Numeta G13%E |
| Espanha | NUMETA G13%E, emulsión para perfusión |
Data da última revisão do folheto: Maio 2024
Informações destinadas apenas a profissionais de saúde
*Em alguns casos, este medicamento pode ser administrado em casa pelos pais ou outros cuidadores.
Se for esse o caso, os pais/cuidadores devem ler as informações abaixo.
Não deve adicionar componentes adicionais ao saco sem verificar previamente a compatibilidade.
Isso pode causar a formação de partículas sólidas ou a desestabilização da emulsão lipídica.
Isso pode levar ao bloqueio dos vasos sanguíneos.
O medicamento NUMETA G13%E Pré-termo deve atingir a temperatura ambiente antes da administração.
Antes da administração do medicamento NUMETA G13%E Pré-termo, o saco deve ser preparado como mostrado abaixo.
Deve verificar se o saco não está danificado.
O saco só pode ser utilizado se não estiver danificado.
Abaixo estão indicadas as características de um saco não danificado:
- As divisórias estão intactas. Isso é indicado pela falta de mistura do conteúdo de qualquer uma das três câmaras.
- As soluções que contêm aminoácidos e glicose são transparentes, incolores ou ligeiramente amareladas, sem partículas visíveis.
- A emulsão lipídica é um líquido homogêneo com aspeto branco leitoso.
Antes de abrir o saco de proteção, deve verificar a cor do indicador de oxigénio.
- Deve compará-la com a cor de referência impressa ao lado do símbolo OK e mostrada na área impressa da etiqueta do indicador.
- Não deve utilizar o medicamento se a cor do indicador de oxigénio não corresponder à cor de referência impressa ao lado do símbolo OK.













Figura 1
Figura 2
Preparação da emulsão misturada:
- Antes de romper as soldas, deve verificar se o medicamento atingiu a temperatura ambiente.
- Colocar o saco sobre uma superfície plana e limpa.
Ativação do saco tricamarado (mistura de 3 soluções abrindo as 2 soldas separadoras)
Passo 1: Começar a dobrar o saco a partir do lado com o gancho.
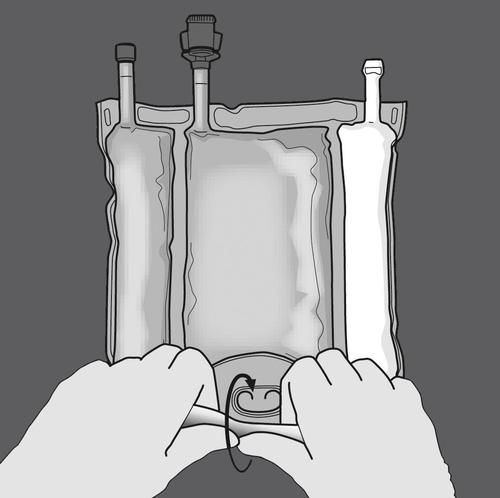
Passo 2: Pressionar até que as soldas se abram.
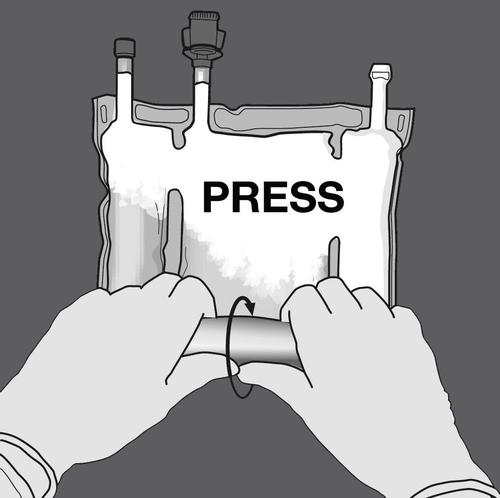
PRESSIONAR
Passo 3: Mudar a direção, dobrando o saco em direção ao gancho.
PRESSIONAR
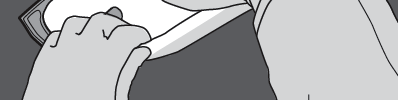

Passo 4: Girar o saco pelo menos três vezes para misturar bem o conteúdo.

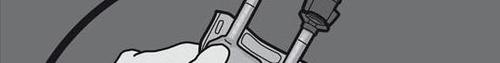






Passo 5: Retirar a tampa de proteção do local de administração e conectar o conjunto de infusão.








Ativação do saco bicamarado (mistura de 2 soluções abrindo a solda separadora entre os compartimentos que contêm aminoácidos e glicose)
Passo 1: Para misturar apenas 2 soluções, deve dobrar o saco, começando pelo canto superior (com o gancho) ao lado da solda que separa as soluções.
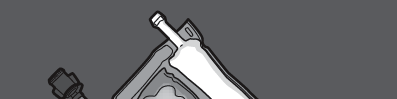
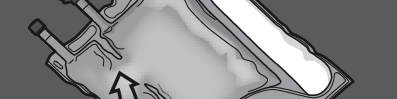
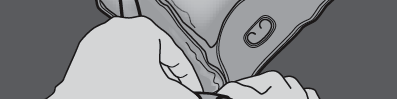
PRESSIONAR

Passo 2: Colocar o saco de modo que o compartimento com a emulsão lipídica fique mais perto de si.
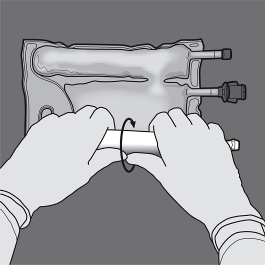
Passo 3: Pressionar com uma mão e dobrar o saco em direção aos tubos.

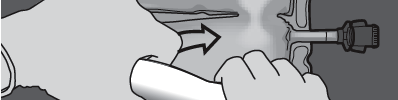
PRESSIONAR


Passo 4: Mudar a direção, dobrando o saco em direção à extremidade superior (com o gancho).

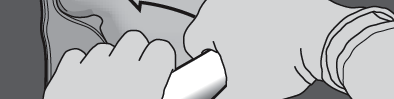
PREPARAÇÃO


Passo 5: Girar o saco pelo menos três vezes para misturar completamente o conteúdo.
A solução misturada deve ser transparente, incolor ou ligeiramente amarelada.







Passo 6: Remover a tampa de proteção do local de administração do medicamento e introduzir o conjunto de administração intravenosa.








Dentro da primeira hora, a velocidade de fluxo deve ser aumentada gradualmente. A velocidade de fluxo da administração deve ser ajustada com base nos seguintes fatores:
- dose administrada;
- volume diário consumido;
- tempo de duração da infusão.
Método de administração:
Em caso de uso em recém-nascidos e crianças abaixo de 2 anos, a solução (em sacos e conjuntos de administração) deve ser protegida da luz até o final da administração.
Para a administração do medicamento NUMETA G13%E Preterm, recomenda-se o uso de um filtro de 1,2 micra.
Devido à alta osmolalidade, o medicamento NUMETA G13%E Preterm não diluído pode ser administrado apenas por via central.
A diluição adequada do medicamento NUMETA G13%E Preterm com água para injeção reduz a osmolalidade e permite a infusão em um vaso periférico.
A fórmula abaixo apresenta o efeito da diluição na osmolalidade do medicamento.
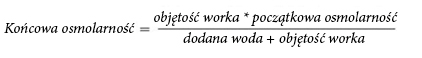
Na tabela abaixo, são apresentados exemplos de osmolalidade de sacos de duas câmaras e três câmaras ativados após a adição de água para injeção:
| Aminocidos e glicose (saco W2K ativado) | Aminocidos, glicose e lipídios (saco W3K ativado) | |
| Volume inicial no saco (ml) | 240 | 300 |
| Osmolalidade inicial (mOsm/l aproximadamente) | 1400 | 1150 |
| Volume de água adicionado (ml) | 240 | 300 |
| Volume final após adição (ml) | 480 | 600 |
| Osmolalidade após adição (mOsm/l aproximadamente) | 700 | 575 |
Adição de componentes adicionais:
A exposição à luz de soluções para nutrição parenteral, especialmente após a mistura com minerais traços e (ou) vitaminas, pode ter um efeito adverso nos resultados clínicos em recém-nascidos, devido à formação de peróxidos e outros produtos de degradação.
Em caso de uso em recém-nascidos e crianças abaixo de 2 anos, o medicamento NUMETA G13%E Preterm deve ser protegido da luz ambiente até o final da administração.
Componentes adicionais compatíveis podem ser adicionados à mistura reconstituída através do local de injeção (após a abertura das soldas rompíveis e após a mistura do conteúdo de duas ou três câmaras).
Vitaminas também podem ser adicionadas à câmara que contém glicose antes da reconstituição da mistura (antes da abertura das soldas rompíveis e antes da mistura das soluções e emulsões).
São possíveis adições de soluções prontas de minerais traços (identificados como TE1 e TE4),
vitaminas (identificados como liofilizado V1 e emulsão V2) e eletrólitos em quantidades específicas
apresentados nas Tabelas 1-4.
- 1.Compatibilidade com TE4, V1 e V2
Tabela 1: Compatibilidade 3-em-1 (saco W3K ativado) com diluição em água e sem diluição
| Para 300 ml (após mistura de 3 câmaras, com lipídios) | ||||||
| Adição sem diluição | Adição com diluição | |||||
| Componentes adicionais | Quantidade contida | Quantidade máxima adicionada | Quantidade máxima total | Quantidade contida | Quantidade máxima adicionada | Quantidade máxima total |
| Sódio (mmol) | 6,6 | 5,0 | 11,6 | 6,6 | 5,0 | 11,6 |
| Potássio (mmol) | 6,2 | 4,2 | 10,4 | 6,2 | 4,2 | 10,4 |
| Magnésio (mmol) | 0,47 | 0,83 | 1,3 | 0,47 | 0,83 | 1,3 |
| Cálcio (mmol) | 3,8 | 3,5 | 7,3 | 3,8 | 3,5 | 7,3 |
| Fosfatos* (mmol) | 3,8 | 2,5 | 6,3 | 3,8 | 2,5 | 6,3 |
| Minerais traços e vitaminas | 15 ml TE4 + 1,5 frascos V1 + 25 ml V2 | 15 ml TE4 + 1,5 frascos V1 + 25 ml V2 | 15 ml TE4 + 1,5 frascos V1 + 25 ml V2 | 15 ml TE4 + 1,5 frascos V1 + 25 ml V2 | ||
| Água para injeção | 300 ml | 300 ml | ||||
Tabela 2: Compatibilidade 2-em-1 (saco W2K ativado) com diluição em água e sem diluição
| Para 240 ml (após mistura de 2 câmaras, sem lipídios) | ||||||
| Adição sem diluição | Adição com diluição | |||||
| Componentes adicionais | Quantidade contida | Quantidade máxima adicionada | Quantidade máxima total | Quantidade contida | Quantidade máxima adicionada | Quantidade máxima total |
| Sódio (mmol) | 6,4 | 17,6 | 24 | 6,4 | 0,0 | 6,4 |
| Potássio (mmol) | 6,2 | 17,8 | 24 | 6,2 | 0,0 | 6,2 |
| Magnésio (mmol) | 0,47 | 2,13 | 2,6 | 0,47 | 0,0 | 0,47 |
| Cálcio (mmol) | 3,8 | 3,5 | 7,3 | 3,8 | 0,0 | 3,8 |
| Fosfatos* (mmol) | 3,2 | 4,0 | 7,2 | 3,2 | 0,0 | 3,2 |
| Minerais traços e vitaminas | 2,5 ml TE4 + ¼ frasco V1 | 2,5 ml TE4 + ¼ frasco V1 | 2,5 ml TE4 + ¼ frasco V1 | 2,5 ml TE4 + ¼ frasco V1 | ||
| Água para injeção | 240 ml | 240 ml |
- 2.Compatibilidade com TE1, V1 e V2Tabela 3: Compatibilidade 3-em-1 (saco W3K ativado) com diluição em água e sem diluição
| Para 300 ml (após mistura de 3 câmaras, com lipídios) | ||||||
| Adição sem diluição | Adição com diluição | |||||
| Componentes adicionais | Quantidade contida | Quantidade máxima adicionada | Quantidade máxima total | Quantidade contida | Quantidade máxima adicionada | Quantidade máxima total |
| Sódio (mmol) | 6,6 | 5,0 | 11,6 | 6,6 | 0,0 | 6,6 |
| Potássio (mmol) | 6,2 | 4,2 | 10,4 | 6,2 | 0,0 | 6,2 |
| Magnésio (mmol) | 0,47 | 0,83 | 1,3 | 0,47 | 0,0 | 0,47 |
| Cálcio (mmol) | 3,8 | 1,9 | 5,7 | 3,8 | 0,0 | 3,8 |
| Fosfatos* (mmol) | 3,8 | 2,5 | 6,3 | 3,8 | 0,0 | 3,8 |
| Minerais traços e vitaminas | 2,5 ml TE1 + ¼ frasco V1 + 2,5 ml V2 | 2,5 ml TE1 + ¼ frasco V1 + 2,5 ml V2 | 2,5 ml TE1 + ¼ frasco V1 + 2,5 ml V2 | 2,5 ml TE1 + ¼ frasco V1 + 2,5 ml V2 | ||
| Água para injeção | 300 ml | 300 ml | ||||
Tabela 4: Compatibilidade 2-em-1 (saco W2K ativado) com diluição em água e sem diluição
| Para 240 ml (após mistura de 2 câmaras, sem lipídios) | ||||||
| Adição sem diluição | Adição com diluição | |||||
| Componentes adicionais | Quantidade contida | Quantidade máxima adicionada | Quantidade máxima total | Quantidade contida | Quantidade máxima adicionada | Quantidade máxima total |
| Sódio (mmol) | 6,4 | 17,6 | 24 | 6,4 | 0,0 | 6,4 |
| Potássio (mmol) | 6,2 | 17,8 | 24 | 6,2 | 0,0 | 6,2 |
| Magnésio (mmol) | 0,47 | 2,13 | 2,6 | 0,47 | 0,0 | 0,47 |
| Cálcio (mmol) | 3,8 | 3,5 | 7,3 | 3,8 | 0,0 | 3,8 |
| Fosfatos* (mmol) | 3,2 | 4,0 | 7,2 | 3,2 | 0,0 | 3,2 |
| Minerais traços e vitaminas | 2,5 ml TE1 + ¼ frasco V1 | 2,5 ml TE1 + ¼ frasco V1 | 2,5 ml TE1 + ¼ frasco V1 | 2,5 ml TE1 + ¼ frasco V1 | ||
| Água para injeção | 240 ml | 240 ml | ||||
A composição dos preparados contendo vitaminas e minerais traços é apresentada nas Tabelas 5 e 6.
Tabela 5: Composição do preparado pronto contendo minerais traços:
Tabela 6: Composição do preparado pronto contendo vitaminas:
Adição de componentes adicionais:
- Devem ser mantidas as condições assépticas.
- Preparar o local de injeção no saco.
- Perfurar o local de injeção e injetar os componentes adicionais com uma agulha para injeção ou dispositivo de preparação de medicamentos.
- Misturar o conteúdo do saco com os componentes adicionais.
Preparação da infusão:
- Devem ser mantidas as condições assépticas.
- Suspender o saco.
- Remover o protetor plástico do porto de administração do medicamento.
- Introduzir a agulha do conjunto de infusão no porto de administração do medicamento com um movimento decidido.
Administração da infusão:
- Apenas para uso único.
- Administrar o medicamento apenas após a ruptura das soldas entre as duas ou três câmaras e após a mistura do conteúdo das duas ou três câmaras.
- Deve-se garantir que na emulsão pronta do saco de três câmaras ativado para infusão não ocorra separação de fases ou no saco de duas câmaras para infusão não haja partículas sólidas.
- Recomenda-se o uso imediato após a abertura das soldas rompíveis. O medicamento NUMETA G13%E Preterm não deve ser armazenado para a próxima infusão.
- Não conectar sacos parcialmente usados.
| Composição por frasco | TE1 (10 ml) | TE4 (10 ml) |
| Zinco | 38,2 µmol ou 2,5 mg | 15,3 µmol ou 1 mg |
| Selênio | 0,253 µmol ou 0,02 mg | 0,253 µmol ou 0,02 mg |
| Cobre | 3,15 µmol ou 0,2 mg | 3,15 µmol ou 0,2 mg |
| Iodo | 0,0788 µmol ou 0,01 mg | 0,079 µmol ou 0,01 mg |
| Flúor | 30 µmol ou 0,57 mg | |
| Manganês | 0,182 µmol ou 0,01 mg | 0,091 µmol ou 0,005 mg |
| Composição por frasco | V1 | V2 |
| Vitamina B1 | 2,5 mg | |
| Vitamina B2 | 3,6 mg | |
| Nicotinamida | 40 mg | |
| Vitamina B6 | 4,0 mg | |
| Ácido pantotênico | 15,0 mg | |
| Biotina | 60 µg | |
| Ácido fólico | 400 µg | |
| Vitamina B12 | 5,0 µg | |
| Vitamina C | 100 mg | |
| Vitamina A | 2300 UI | |
| Vitamina D | 400 UI | |
| Vitamina E | 7 UI | |
| Vitamina K | 200 µg |
- Para evitar a formação de um embolo aéreo causado pelo ar residual contido no primeiro saco, não conectar sacos em série.
- Para a administração do medicamento NUMETA G13%E Preterm, recomenda-se o uso de um filtro de 1,2 micra.
- Em caso de uso em recém-nascidos e crianças abaixo de 2 anos, deve-se proteger da luz até o final da administração. A exposição do medicamento NUMETA G13%E Preterm à luz ambiente, especialmente após a mistura com minerais traços e (ou) vitaminas, pode causar a formação de peróxidos e outros produtos de degradação, o que pode ser reduzido protegendo da luz.
- Todos os resíduos de medicamento não utilizado ou seus resíduos, bem como todo o conjunto de uso único necessário, devem ser eliminados adequadamente.
Prazo de validade após a mistura das soluções
O medicamento deve ser usado imediatamente após a abertura das soldas rompíveis entre as duas ou três câmaras.
Estudos de estabilidade das misturas foram realizados por 7 dias a uma temperatura de 2°C a 8°C, e subsequentemente
48 horas a 30°C.
Prazo de validade após a adição de componentes adicionais (eletrólitos, minerais traços, vitaminas, água)
Para os componentes adicionais específicos, foi demonstrada a estabilidade física do medicamento NUMETA por 7 dias a uma temperatura de 2°C a 8°C, e subsequentemente por 48 horas a 30°C.
As informações sobre esses componentes adicionais estão no ponto 6.6 da Bula do Medicamento.
Do ponto de vista microbiológico, o medicamento deve ser usado imediatamente. Se não for usado imediatamente, o tempo e as condições de armazenamento até o momento de sua aplicação são de responsabilidade do usuário, mas não deve exceder 24 horas a uma temperatura de 2°C a 8°C, a menos que
a preparação/dissolução/adução de componentes adicionais tenha sido realizada em condições assépticas controladas e validadas.
Não use o medicamento NUMETA G13%E Preterm se o saco estiver danificado. Abaixo estão listadas as características de um saco danificado:
- As soldas rompíveis estão abertas
- Alguma das câmaras contém uma mistura de soluções
- As soluções contendo aminocidos e glicose não são transparentes, incolores ou ligeiramente amareladas e (ou) contêm partículas visíveis
- A emulsão lipídica não é um líquido homogêneo de aparência leitosa.
Os medicamentos não devem ser jogados na rede de esgotos ou em recipientes de lixo doméstico. É necessário perguntar ao farmacêutico o que fazer com os medicamentos que não são mais necessários. Esse procedimento ajudará a proteger o meio ambiente.
O que contém o medicamento NUMETA G13%E Preterm
Substâncias ativas:
| Substância ativa | Saco W2K ativado (240 ml) | Saco W3K ativado (300 ml) |
| Câmara com aminocidos | ||
| Alanina | 0,75 g | 0,75 g |
| Arginina | 0,78 g | 0,78 g |
| Ácido aspártico | 0,56 g | 0,56 g |
| Cisteína | 0,18 g | 0,18 g |
| Ácido glutâmico | 0,93 g | 0,93 g |
| Glicina | 0,37 g | 0,37 g |
| Histidina | 0,35 g | 0,35 g |
| Isolucina | 0,62 g | 0,62 g |
| Leucina | 0,93 g | 0,93 g |
| Lisina monohidratada (corespondente à lisina) | 1,15 g (1,03 g) | 1,15 g (1,03 g) |
| Metionina | 0,22 g | 0,22 g |
| Ornitina cloridratada (corespondente à ornitina) | 0,30 g (0,23 g) | 0,30 g (0,23 g) |
| Fenilalanina | 0,39 g | 0,39 g |
| Prolina | 0,28 g | 0,28 g |
| Serina | 0,37 g | 0,37 g |
| Taurina | 0,06 g | 0,06 g |
| Treonina | 0,35 g | 0,35 g |
| Triptofano | 0,19 g | 0,19 g |
| Tirosina | 0,07 g | 0,07 g |
| Valina | 0,71 g | 0,71 g |
| Octanoato de potássio | 0,61 g | 0,61 g |
| Clorato de cálcio di-hidratado | 0,55 g | 0,55 g |
| Octanoato de magnésio tetra-hidratado | 0,10 g | 0,10 g |
| Glicerofosfato de sódio monohidratado | 0,98 g | 0,98 g |
| Câmara com glicose | ||
| Glicose monohidratada (corespondente à glicose anidra) | 44,00 g (40,00 g) | 44,00 g (40,00 g) |
| Câmara com lipídios | ||
| Óleo de oliva purificado (aprox. 80%) + óleo de soja purificado (aprox. 20%) | 7,5 g | |
A solução após a mistura/emulsão contém os seguintes componentes:
| Composição | ||||
| Saco W2K ativado | Saco W3K ativado | |||
| Por unidade de volume (ml) Azoto (g) Aminocidos (g) Glicose (g) Lipídios (g) Valor energético Valor energético total (kcal) | 240 1,4 9,4 40,0 0 198 | 100 0,59 3,9 16,7 0 82 | 300 1,4 9,4 40,0 7,5 273 | 100 0,47 3,1 13,3 2,5 91 |
| Valor energético não proteico (kcal) Valor energético da glicose (kcal) Valor energético lipídico (kcal) Valor energético não proteico/azoto (kcal/g N) Valor energético lipídico/valor energético não proteico (%) Valor energético lipídico/valor energético total (%) Eletrólitos Sódio (mmol) Potássio (mmol) Magnésio (mmol) Cálcio (mmol) Fosfatosb (mmol) Octanatos (mmol) Jablonatos (mmol) Cloratos (mmol) | 160 160 0 113 Não aplic. Não aplic. 6,4 6,2 0,47 3,8 3,2 7,2 3,2 9,3 | 67 67 0 113 Não aplic. Não aplic. 2,7 2,6 0,20 1,6 1,3 3,0 1,3 3,9 | 235 160 75 165 32 28 6,6 6,2 0,47 3,8 3,8 7,2 3,2 9,3 | 78 53 25 165 32 28 2,2 2,1 0,16 1,3 1,3 2,4 1,1 3,1 |
| pH (aproximadamente) Osmolalidade aproximada (mOsm/l) | 5,5 1400 | 5,5 1400 | 5,5 1150 | 5,5 1150 |
Neste, o valor energético dos fosfolipídios do ovo para injeção.
Neste, os fosfatos dos fosfolipídios do ovo para injeção, componente da emulsão lipídica.
Outros componentes:
Ácido L-málico
Ácido clorídrico
Fosfolipídios do ovo para injeção
Glicerol
Oleato de sódio
Hidróxido de sódio
Água para injeção
para ajustar o pH
Baxter, Numeta, Numetzah e Numetah são marcas registradas da Baxter International Inc.
- País de registo
- Substância ativa
- Requer receita médicaSim
- Fabricante
- ImportadorBaxter S.A.
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a Numeta G13%e PretermForma farmacêutica: Solução, -Substância ativa: combinationsNão requer receita médicaForma farmacêutica: Solução, -Substância ativa: combinationsNão requer receita médicaForma farmacêutica: Solução, -Substância ativa: combinationsNão requer receita médica
Alternativas a Numeta G13%e Preterm noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a Numeta G13%e Preterm em Espanha
Alternativa a Numeta G13%e Preterm em Ukraine
Médicos online para Numeta G13%e Preterm
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de Numeta G13%e Preterm – sujeita a avaliação médica e regras locais.














