
Multimel N6-900e
Pergunte a um médico sobre a prescrição de Multimel N6-900e

Como usar Multimel N6-900e
Folheto de informação para o utilizador
Multimel N6-900 E, emulsão para infusão
Deve ler atentamente o folheto antes de tomar o medicamento, pois contém informações
importantes para o paciente.
- Deve conservar este folheto para poder relê-lo se necessário.
- Se tiver alguma dúvida adicional, deve consultar um médico ou enfermeiro.
- Se o paciente apresentar algum efeito adverso, incluindo quaisquer efeitos adversos não mencionados neste folheto, deve informar o médico ou enfermeiro. Ver ponto 4.
Índice do folheto:
- 1. O que é Multimel N6-900 E e para que é utilizado
- 2. Informações importantes antes de tomar o medicamento Multimel N6-900 E
- 3. Como tomar Multimel N6-900 E
- 4. Efeitos adversos possíveis
- 5. Como conservar o medicamento Multimel N6-900 E
- 6. Conteúdo do pacote e outras informações
1. O que é Multimel N6-900 E e para que é utilizado
Multimel N6-900 E é uma emulsão para infusão. É embalado em um saco tricamarado.
A primeira câmara contém uma solução de glicose com cálcio, a segunda câmara contém uma emulsão lipídica e a
terceira câmara contém uma solução de aminoácidos com eletrólitos.
Grupo farmacoterapêutico: líquidos para nutrição parenteral/misturas.
Multimel N6-900 E é administrado para nutrição intravenosa de adultos e crianças com mais de 2 anos de idade, quando a nutrição oral não é adequada.
Multimel N6-900 E deve ser administrado apenas sob supervisão médica.
2. Informações importantes antes de tomar o medicamento Multimel N6-900 E
Quando não tomar o medicamento Multimel N6-900 E:
- em caso de prematuros, lactentes e crianças com menos de 2 anos de idade;
- se o paciente tiver alergia a ovos, soja, proteínas de amendoim, milho/produtos que contenham milho (ver também o ponto "Advertências e precauções" abaixo) ou a qualquer um dos outros componentes do medicamento Multimel N6-900 E;
- se a administração de alguns aminoácidos causar uma reação anormal no organismo do paciente;
- se o paciente tiver um nível muito alto de lipídios no sangue (hiperlipidemia);
- -se o paciente tiver hiperglicemia grave (nível muito alto de açúcar no sangue);
- se o sangue do paciente contiver um nível anormalmente alto de qualquer um dos eletrólitos (sódio, potássio, magnésio, cálcio e (ou) fósforo).
Em cada caso, o médico tomará a decisão de administrar o medicamento com base em fatores como idade, peso corporal do paciente e seu estado clínico, considerando os resultados dos exames realizados.
Advertências e precauções
Antes de iniciar a administração do medicamento Multimel N6-900 E, deve discutir com o médico ou enfermeiro.
A administração excessivamente rápida de soluções para nutrição parenteral total pode resultar em morte.
Se ocorrerem sintomas ou sinais de reação alérgica, como febre, calafrios, erupção cutânea ou dificuldade para respirar, suor excessivo, náuseas e dor de cabeça, a infusão deve ser interrompida imediatamente. O medicamento contém óleo de soja e fosfatídeos de ovo. As proteínas de soja e ovo podem causar reações de sensibilidade. Foram observadas reações alérgicas cruzadas entre as proteínas de soja e amendoim.
O medicamento Multimel N6-900 E contém glicose derivada do milho, que pode causar reações de sensibilidade se o paciente tiver alergia ao milho ou produtos que contenham milho (ver também o ponto "Quando não tomar o medicamento Multimel N6-900 E" acima).
Dificuldades para respirar também podem ser um sinal de formação de pequenas partículas, bloqueando os vasos sanguíneos nos pulmões (sedimento nos vasos pulmonares). Deve informar o médico ou enfermeiro se ocorrerem dificuldades para respirar. Eles decidirão sobre as medidas a serem tomadas.
O antibiótico ceftriaxona não pode ser misturado ou administrado simultaneamente com qualquer solução que contenha cálcio e seja administrada por gotejamento intravenoso (incluindo Multimel N6-900 E).
Esses medicamentos não podem ser administrados simultaneamente, mesmo por linhas de infusão ou locais de punção diferentes.
No entanto, Multimel N6-900 E e ceftriaxona podem ser administrados sequencialmente, um após o outro, se as linhas de infusão forem trocadas ou limpas cuidadosamente com solução fisiológica de cloreto de sódio entre as infusões, para evitar a formação de sedimento (formação de partículas de sal ceftriaxona-cálcio).
O médico verificará e monitorará os níveis de triglicerídeos (um tipo de lipídio encontrado no sangue).
Alguns medicamentos e doenças podem aumentar o risco de infecção ou septicemia (presença de bactérias no sangue). Um risco especial de infecção ou septicemia existe após a inserção de um cateter (cateter venoso) na veia do paciente. O médico monitorará cuidadosamente o paciente para detectar qualquer sinal de infecção. Pacientes que necessitam de nutrição parenteral (administração de substâncias nutricionais por meio de um tubo inserido na veia) podem estar mais propensos a desenvolver infecção devido ao seu estado clínico. A utilização de técnica asséptica (livre de germes) durante a inserção e manutenção do cateter e durante a preparação do medicamento para nutrição pode reduzir o risco de infecção.
Deve informar o médico:
- sobre doenças renais graves. Também deve informar o médico se o paciente está sendo submetido a diálise (rim artificial) ou outros métodos de limpeza do sangue;
- sobre doença hepática grave;
- sobre distúrbios da coagulação do sangue;
- sobre disfunção adrenal (insuficiência adrenal). As glândulas adrenais são glândulas com forma triangular localizadas no topo dos rins;
- sobre insuficiência cardíaca;
- sobre doença pulmonar;
- sobre retenção de líquidos no organismo (hiperhidratação);
- sobre falta de líquidos no organismo (desidratação);
- sobre diabetes não tratada (nível alto de açúcar no sangue);
- sobre infarto do miocárdio ou choque devido à falha cardíaca aguda;
- sobre acidose metabólica grave (pH do sangue muito ácido);
- sobre septicemia generalizada (presença de bactérias no sangue);
- sobre coma.
Se o paciente for uma criança, o médico verificará cuidadosamente o estado de hidratação e (ou) parâmetros sanguíneos.
Durante a administração do medicamento Multimel e medicamentos semelhantes, foram relatados casos de síndrome de sobrecarga lipídica. A capacidade reduzida ou limitada do organismo de eliminar os lipídios contidos no medicamento Multimel N6-900 E pode resultar em "síndrome de sobrecarga lipídica" (ver ponto 4 - "Efeitos adversos possíveis").
Não deve adicionar componentes adicionais ao saco sem verificar previamente a compatibilidade. Isso pode causar a formação de partículas ou perturbar a estabilidade da emulsão lipídica. Isso pode causar obstrução dos vasos sanguíneos.
Se o nível de glicose no sangue aumentar excessivamente, o médico deve ajustar a velocidade de administração do medicamento Multimel N6-900 E ou administrar insulina ao paciente.
Em casos de desnutrição grave que exigem a administração de componentes nutricionais por via intravenosa, é recomendável iniciar a nutrição parenteral lentamente e com cautela.
Antes de iniciar a infusão, deve corrigir as alterações no equilíbrio hidroeletrolítico e metabólico do paciente. O médico monitorará o estado do paciente durante a terapia e pode alterar a dosagem ou, se achar necessário, recomendar componentes nutricionais adicionais, como vitaminas, eletrólitos e oligoelementos.
Durante a administração do medicamento, o médico realizará exames clínicos e laboratoriais para verificar a eficácia e controlar a segurança da administração do medicamento. Se o paciente receber o medicamento por várias semanas, os exames de sangue serão realizados regularmente. Esses exames são particularmente necessários em casos de doenças como insuficiência hepática, insuficiência renal, doença em que os aminoácidos não podem ser processados corretamente pelo organismo, doença em que o sangue tem um pH muito ácido, doença em que o nível de lipídios e colesterol é maior do que o normal, diabetes, anemia ou dificuldades para controlar a coagulação do sangue.
Se durante a infusão ocorrer dor, ardor, rigidez, inchaço ou alterações na pele no local da infusão ou vazamento da infusão, deve informar o médico ou enfermeiro. A administração será interrompida imediatamente e reiniciada em outra veia.
Crianças
Se o paciente for uma criança, deve ter cuidado especial para administrar a dose correta.
Pode ser necessário um suplemento adicional de vitaminas e oligoelementos, dependendo da dose utilizada e do tempo de administração. Devido à maior sensibilidade das crianças ao risco de infecção, também devem ser tomadas medidas de precaução aumentadas.
Multimel N6-900E e outros medicamentos
Deve informar o médico ou enfermeiro sobre todos os medicamentos que o paciente está tomando atualmente ou recentemente, bem como sobre os medicamentos que o paciente planeja tomar.
Não deve administrar o medicamento Multimel N6-900 E simultaneamente com sangue pelo mesmo conjunto de infusão.
Multimel N6-900 E contém cálcio. Não deve ser administrado com o antibiótico ceftriaxona ou pela mesma linha de infusão, pois podem se formar partículas. Se o mesmo conjunto de administração for utilizado para esses medicamentos, o conjunto deve ser limpo cuidadosamente.
O óleo de oliva e o óleo de soja presentes no medicamento Multimel N6-900 E contêm vitamina K. Normalmente, isso não afeta a ação de medicamentos anticoagulantes, como a cumarina. No entanto, se o paciente estiver tomando medicamentos anticoagulantes, deve informar o médico.
Os lipídios presentes nessa emulsão podem interferir nos resultados de alguns exames laboratoriais, desde que as amostras de sangue sejam coletadas antes da eliminação dos lipídios (os lipídios são normalmente eliminados após cerca de 5-6 horas após a interrupção da administração).
Multimel N6-900 E com eletrólitos contém potássio. Deve ter cuidado especial em pacientes que estejam tomando diuréticos, inibidores da enzima conversora de angiotensina (ECA), antagonistas do receptor de angiotensina II (medicamentos utilizados na hipertensão) ou imunossupressores.
Esses medicamentos podem causar um aumento nos níveis de potássio no sangue.
Gravidez e amamentação
Se a paciente estiver grávida ou amamentando, acredita que possa estar grávida ou planeja ter um filho, deve consultar um médico antes de usar este medicamento.
3. Como tomar Multimel N6-900 E
Multimel N6-900 E pode ser administrado apenas a adultos e crianças com mais de 2 anos de idade.
É uma emulsão para infusão administrada por um tubo de plástico apenas na veia central do paciente.
O tratamento pode ser continuado por tanto tempo quanto necessário, dependendo do estado clínico do paciente.
Multimel N6-900 E é destinado apenas para uso único.
Dosagem - Adultos
A dosagem é determinada pelo médico com base nas necessidades individuais e no estado clínico do paciente.
A dosagem máxima diária é de 40 ml/kg de peso corporal. Por exemplo: para um paciente com 70 kg de peso, a dosagem máxima diária não deve exceder 2800 ml de emulsão para infusão (40 ml de emulsão para infusão multiplicado por 70 kg).
Dosagem - Crianças com mais de 2 anos de idade
A dose do medicamento utilizada em crianças e o período de administração são determinados pelo médico. Isso depende da idade, peso corporal, crescimento, estado clínico, volume diário de líquidos e necessidade de energia e azoto.
Administração de uma dose maior do que a recomendada de Multimel N6-900 E
Se o paciente receber uma dose excessiva do medicamento ou uma infusão muito rápida, os aminoácidos presentes podem contribuir para um aumento da acidose no sangue e um aumento do volume de líquidos no sistema circulatório. A glicose presente no medicamento pode aumentar o nível de glicose no sangue e na urina, e os lipídios presentes na emulsão podem aumentar o nível de triglicerídeos no sangue. A administração de uma quantidade excessiva do medicamento Multimel N6-900 E pode causar náuseas, vômitos, calafrios, dor no peito, dor de cabeça, batimentos cardíacos irregulares ou acelerados e distúrbios eletrolíticos. Nesse caso, a infusão deve ser interrompida imediatamente.
Em alguns casos graves, para ajudar os rins do paciente a eliminar o excesso do medicamento, o médico pode usar diálise por um período.
Para evitar tais situações, o médico monitora regularmente o estado do paciente e verifica os parâmetros sanguíneos.
Se tiver alguma dúvida sobre a administração do medicamento, deve consultar um médico.
4. Efeitos adversos possíveis
Como qualquer medicamento, este medicamento pode causar efeitos adversos, embora não todos os pacientes os experimentem.
Se ocorrerem alguma alteração no bem-estar durante o tratamento ou após a sua interrupção, deve informar o médico ou enfermeiro imediatamente.
Os exames realizados pelo médico durante a administração do medicamento visam minimizar o risco de efeitos adversos.
Se ocorrerem sintomas ou sinais de reação alérgica, como febre, calafrios, erupção cutânea ou dificuldade para respirar, suor excessivo, náuseas e dor de cabeça, a infusão deve ser interrompida imediatamente.
Foram relatados os seguintes efeitos adversos durante a administração do medicamento Multimel:
- reações alérgicas
Frequência: desconhecida(não pode ser estimada com base nos dados disponíveis)
- constricção das vias respiratórias, respiração sibilante e (ou) tosse (constricção brônquica, como parte de uma reação alérgica)
- tremores
- diarreia, náuseas, vômitos
- vermelhidão cutânea anormal (rubor), suor excessivo
- dor nas extremidades, cãibras musculares
- vazamento da infusão para os tecidos circundantes (extravasamento), que pode causar inchaço/edema no local da infusão, dor, irritação e inflamação da veia, vermelhidão/ calor, perda local de tecido, necrose do tecido ou bolhas
- febre, calafrios, estado inflamatório
- diminuição ou limitação da capacidade de eliminar os lipídios contidos no medicamento Multimel N6-900 E pode causar "síndrome de sobrecarga lipídica". Isso pode ser devido à superdose, mas também pode ocorrer no início da infusão, mesmo quando o medicamento é administrado de acordo com as instruções. Isso está relacionado a um piora súbita do estado clínico do paciente. Caracteriza-se por um nível alto de lipídios no sangue, febre, esteatose hepática (nível alto de lipídios no fígado) e (ou) aumento do fígado. Também pode ocorrer anemia (diminuição do número de glóbulos vermelhos, que pode resultar em palidez, fraqueza ou falta de ar), diminuição do número de glóbulos brancos e plaquetas, distúrbios da coagulação do sangue e (ou) coma. Essa síndrome geralmente desaparece após a interrupção da infusão da emulsão lipídica.
Foram relatados os seguintes efeitos adversos para medicamentos semelhantes:
Frequência desconhecida (não pode ser estimada com base nos dados disponíveis)
- formação de pequenas partículas, que pode levar à obstrução dos vasos sanguíneos nos pulmões (sedimento nos vasos pulmonares), causando embolia pulmonar e dificuldade para respirar (insuficiência respiratória)
- diminuição do número de plaquetas (diminuição do número de glóbulos responsáveis pela coagulação do sangue, o que pode causar sangramento, como sangramento nasal)
- dificuldade para eliminar a bile (colestase), aumento do fígado, icterícia (amarelamento da pele ou da parte branca dos olhos devido a distúrbios hepáticos ou sanguíneos)
- hipersensibilidade
- aumento da atividade das enzimas hepáticas, aumento do nível de lipídios no sangue (aumento do nível de triglicerídeos no sangue), aumento do nível de bilirrubina no sangue
- aumento do nível de azoto no sangue (azotemia)
Em crianças, foram relatados casos de diminuição do número de glóbulos brancos e plaquetas.
Notificação de efeitos adversos
Se ocorrerem efeitos adversos, incluindo quaisquer efeitos adversos não mencionados no folheto, deve informar o médico ou enfermeiro. Os efeitos adversos podem ser notificados diretamente ao Departamento de Monitoramento de Efeitos Adversos de Produtos Farmacêuticos da Agência Reguladora de Produtos Farmacêuticos, Dispositivos Médicos e Produtos Biocidas:
Al. Jerozolimskie 181 C
PL 02-222 Varsóvia
Tel.: + 48 22 49 21 301
Fax: + 48 22 49 21 309
Site: https://smz.ezdrowie.gov.pl
Os efeitos adversos também podem ser notificados ao titular da autorização de comercialização.
A notificação de efeitos adversos pode ajudar a coletar mais informações sobre a segurança do medicamento.
5. Como conservar o medicamento Multimel N6-900 E
O medicamento deve ser conservado em um local não visível e inacessível a crianças.
Não deve usar este medicamento após a data de validade impressa no recipiente e na embalagem exterior. A data de validade é o último dia do mês indicado.
Não congelar.
Conservar na embalagem protetora.
Conservar na caixa exterior para proteger da luz.
Os medicamentos não devem ser jogados na canalização ou nos recipientes de lixo doméstico. Deve perguntar ao farmacêutico como descartar os medicamentos que não são mais utilizados. Essa ação ajudará a proteger o meio ambiente.
6. Conteúdo do pacote e outras informações
O que contém o medicamento Multimel N6-900 E
Substâncias ativas presentes em cada saco com emulsão pronta:
Substâncias ativas 1000 ml 1500 ml 2000 ml 2500 ml
Óleo de oliva purificado e
óleo de soja purificado*
100,00 g
L-alanina
7,04 g
10,56 g
14,08 g
17,60 g
L-arginina
3,91 g
5,87 g
7,82 g
9,78 g
Glicina
3,50 g
5,26 g
7,01 g
8,76 g
L-histidina
1,63 g
2,45 g
3,26 g
4,08 g
L-isoleucina
2,04 g
3,06 g
4,08 g
5,10 g
40,00 g
60,00 g
80,00 g
L-leucina
2,48 g
3,73 g
4,97 g
6,21 g
L-lisina
1,97 g
2,96 g
3,94 g
4,93 g
(equivalente a cloreto de lisina)
(2,46 g)
(3,70 g)
(4,93 g)
(6,16 g)
L-metionina
1,36 g
2,04 g
2,72 g
3,40 g
L-fenilalanina
1,90 g
2,86 g
3,81 g
4,76 g
L-prolina
2,31 g
3,47 g
4,62 g
5,78 g
L-serina
1,70 g
2,55 g
3,40 g
4,25 g
L-treonina
1,43 g
2,14 g
2,86 g
3,57 g
L-triptofano
0,61 g
0,92 g
1,22 g
1,53 g
L-tirosina
0,14 g
0,20 g
0,27 g
0,34 g
L-valina
1,97 g
2,96 g
3,94 g
4,93 g
Octato de sódio tri-hidratado
2,45 g
3,67 g
4,90 g
6,12 g
Glicerofosfato de sódio penta-hidratado
2,14 g
3,22 g
4,29 g
5,36 g
Cloruro de potássio
1,79 g
2,68 g
3,58 g
4,47 g
Cloruro de magnésio hexa-hidratado
0,45 g
0,67 g
0,90 g
1,12 g
Glicose
(equivalente a glicose mono-hidratada)
300,00 g
(330,00 g)
Cloruro de cálcio di-hidratado
0,30 g
0,44 g
0,59 g
0,74 g
Valor energético total (kcal)
1015
1525
2030
2540
Valor energético não proteico (kcal)
880
1320
1760
2200
120,00 g
(132,00 g)
180,00 g
(198,00 g)
240,00 g
(264,00 g)
Os outros componentes são fosfatídeos de ovo purificados, glicerol, oleato de sódio, hidróxido de sódio, ácido acético glacial, ácido clorídrico, água para injeção.
Como é o medicamento Multimel N6-900 E e o que o pacote contém
Multimel N6-900 E é uma emulsão para infusão fornecida em um saco tricamarado, que é um saco de plástico multicamada. A camada interna (de contato) do saco é feita de polímeros (mistura de copolímeros de poliolefinas) e é compatível com o conteúdo do saco (soluções de aminoácidos, soluções de glicose e emulsões lipídicas) e os aditivos permitidos, e permite a criação de soldas frágeis. Os polímeros usados para fazer a camada de revestimento são produzidos a partir de EVA (acetato de polietileno-vinil) e copolímero de poliéster.
Antes de misturar o conteúdo das 3 câmaras do saco, a primeira câmara contém um líquido homogêneo com aparência leitosa (emulsão lipídica), enquanto as duas outras câmaras (contendo solução de aminoácidos com eletrólitos e solução de glicose com cálcio) contêm soluções incolores ou ligeiramente amareladas, praticamente sem partículas visíveis. Após a mistura, Multimel N6-900 E é uma emulsão para infusão com aparência de líquido leitoso homogêneo.
O saco é colocado em uma embalagem protetora, que protege contra o oxigênio, e contém um sachê que absorve oxigênio.
Tamanhos do pacote
saco de 1000 ml: 6 sacos em uma caixa de papelão
saco de 1500 ml: 4 sacos em uma caixa de papelão
saco de 2000 ml: 4 sacos em uma caixa de papelão
saco de 2500 ml: 2 sacos em uma caixa de papelão
Nem todos os tamanhos de pacotes podem estar disponíveis no mercado.
Titular da autorização de comercialização:
Para obter informações sobre o medicamento Multimel N6-900 E, deve contatar o representante do titular da autorização de comercialização:
Baxter Polska Sp. z o.o.
ul. Kruczkowskiego 8
00-380 Varsóvia
Fabricante:
Baxter S.A.
Boulevard René Branquart 80
7860 Lessines
Bélgica
Data da última atualização do folheto: 06.03.2020
--------------------------------------------------------------------------------------------------------------
Informações destinadas apenas ao pessoal médico especializado:
Multimel N6-900 E, emulsão para infusão
1. COMPOSIÇÃO QUANTITATIVA
Após a mistura do conteúdo das 3 câmaras, a mistura tem a forma de uma emulsão homogênea com aparência leitosa.
A emulsão pronta, após a mistura, contém os seguintes componentes nos sacos de diferentes tamanhos:
** Incluindo fosfatos presentes na emulsão lipídica
2. DOSAGEM E MODO DE ADMINISTRAÇÃO
A dosagem é determinada com base no gasto energético, estado clínico do paciente, peso corporal e capacidade de metabolizar os componentes do produto Multimel N6-900 E, bem como da quantidade de componentes energéticos ou proteicos adicionais administrados por via oral ou enteral; portanto, também é necessário escolher o tamanho do saco adequadamente.
A administração pode ser continuada por tanto tempo quanto necessário, dependendo do estado clínico do paciente.
Não deve exceder a dosagem máxima diária em adultos ou em crianças e adolescentes. Devido à composição fixa do saco multicamada,
a satisfação de todas as necessidades nutricionais do paciente pode não ser possível. Pode ocorrer uma situação clínica em que o paciente precise de uma quantidade diferente de componentes nutricionais do que a disponível na composição fixa do saco.
Como regra geral, não deve exceder a dose de 3 g de aminoácidos/kg de peso corporal por dia e (ou) 17 g de glicose/kg de peso corporal por dia e (ou) 3 g de lipídios/kg de peso corporal por dia e (ou) 100 ml de líquido/kg de peso corporal por dia, com exceção de casos especiais.
Multimel é destinado apenas para uso único.
O tempo recomendado para a infusão no caso de nutrição parenteral é de 12 a 24 horas.
Dosagem e velocidade de infusão - Adultos
A necessidade média de azoto é de 0,16 a 0,35 g/kg de peso corporal por dia (cerca de 1 a 2 g de aminoácidos/kg de peso corporal por dia).
A necessidade energética varia dependendo do estado de nutrição do paciente e do nível de catabolismo. Em média, é de 20 a 40 kcal/kg de peso corporal por dia.
Dosagem máxima diária:
Para o produto Multimel N6-900 E:A dosagem máxima diária é de 40 ml/kg de peso corporal (o que equivale a 1,36 g de aminoácidos, 4,8 g de glicose, 1,6 g de lipídios, 1,28 mmol de sódio e 0,96 mmol de potássio/kg de peso corporal),
ou seja, 2800 ml de emulsão para infusão para um paciente com 70 kg de peso.
Velocidade máxima de infusão
Como regra geral, não deve exceder a velocidade de infusão de 0,10 g de aminoácidos/kg de peso corporal por hora e (ou) 0,25 g de glicose/kg de peso corporal por hora e (ou) 0,15 g de lipídios/kg de peso corporal por hora, com exceção de casos especiais.
Para o produto Multimel N6-900 E:Como regra geral, não deve exceder a velocidade de infusão de 2 ml/kg de peso corporal por hora, ou seja, 0,07 g de aminoácidos, 0,24 g de glicose e 0,08 g de lipídios/kg de peso corporal por hora.
Dosagem e velocidade de infusão - Crianças com mais de 2 anos de idade e adolescentes
Não foram realizados estudos em crianças e adolescentes.
A dosagem é determinada com base na quantidade de líquidos ingeridos e na necessidade diária de azoto.
A dose deve ser corrigida com base no estado de hidratação da criança.
A necessidade diária de líquidos, azoto e energia diminui constantemente com a idade.
As diretrizes para a velocidade máxima de infusão por hora e o volume diário para crianças e adolescentes são:
Multimel N6-900 E:
Dosagem máxima diária:
| Componente | 2 a 11 anos | 12 a 18 anos | ||
| Dose máxima diária recomendadaa | Dose máxima diária de MULTIMEL N6-900 Eb | Dose máxima diária recomendadaa | Dose máxima diária de MULTIMEL N6-900 Eb | |
| Líquidos (ml/kg de peso corporal/dia) |
| 45 |
| 45 |
| Aminoácidos (g/kg de peso corporal/dia) |
| 1,5 |
| 1,5 |
| Glicose (g/kg de peso corporal/dia) | 1,4 – 8,6 | 5,4 | 0,7 – 5,8 | 5,4 |
| Lipídios (g/kg de peso corporal/dia) | 0,5 – 3 | 1,8 | 0,5 – 2 (até 3) | 1,8 |
| Valor energético total (kcal/kg de peso corporal/dia) | 30-75 | 45,7 | 20-55 | 45,7 |
| Sódio (mmol/kg de peso corporal/dia) | 1-3 | 1,4 | 1-3 | 1,4 |
| Potássio (mmol/kg de peso corporal/dia) | 1-3 | 1,1 | 1-3 | 1,1 |
Velocidade máxima por hora
| Componente | 2 a 11 anos | 12 a 18 anos | ||
| Velocidade máxima por horaa | Velocidade máxima por hora de MULTIMEL N6-900 Eb | Velocidade máxima por horaa | Velocidade máxima por hora de MULTIMEL N6-900 Eb | |
| Líquidos (ml/kg de peso corporal/hora) | Não se aplica | 3,0 | Não se aplica | 2,0 |
| Aminoácidos (g/kg de peso corporal/hora) | 0,20 | 0,10 | 0,12 | 0,06 |
| Glicose (g/kg de peso corporal/hora) | 0,36 | 0,36 | 0,24 | 0,24 |
| Lipídios (g/kg de peso corporal/hora) | 0,13 | 0,12 | 0,13 | 0,08 |
Via de administração
Multimel N6-900 E deve ser administrado por via intravenosa, na veia central.
A velocidade de infusão deve ser ajustada com base na dose administrada, características da mistura final, volume total previsto para ser administrado em 24 horas e duração da infusão.
3. PRECAUÇÕES E ADVERTÊNCIAS ESPECIAIS
4. INFORMAÇÕES PRÁTICAS SOBRE A PREPARAÇÃO PARA
USO DO PRODUTO MÉDICO E ELIMINAÇÃO DE SEUS RESÍDUOS
O produto Multimel N6-900 E deve ser usado apenas se:
- o saco não estiver danificado
- as soldas não estiverem danificadas
- as soluções de aminoácidos e glicose estiverem claras, incolores ou ligeiramente amareladas, praticamente sem partículas visíveis
- a emulsão lipídica for um líquido homogêneo com aparência leitosa.
Antes de usar, o produto Multimel N6-900 E deve ser levado à temperatura ambiente.
A administração deve ser feita apenas após a ruptura das soldas que separam as 3 câmaras do saco e a mistura do conteúdo das 3 câmaras, como mostrado abaixo.
Deve-se garantir que a emulsão pronta para infusão não apresente sinais de separação de fases.
1. 2. 3.



Rasgar o pacote de proteção
da parte superior.
Remover a parte frontal
do pacote de proteção para
expor o saco Multimel N6-900 E. Jogar fora
o pacote de proteção e o pacote
de absorção de oxigênio.
Colocar o saco em uma superfície
plana, horizontal e limpa, com
o suporte voltado para cima.
4. 5. 6.
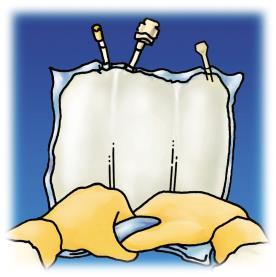
Levantar o saco segurando pelo
suporte para remover o líquido
da parte superior do saco.
Rolar firmemente o saco com
as duas mãos, começando da
parte superior do saco, até
romper as soldas (aproximadamente
metade do comprimento delas).
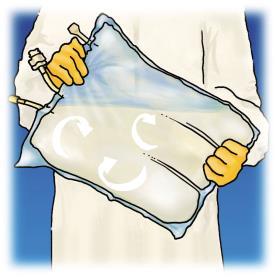
Misturar o conteúdo do saco,
girando-o pelo menos 3 vezes.
Deve-se garantir que a mistura
seja homogênea e que não ocorra
separação de fases.
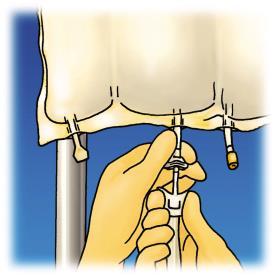
Suspender o saco. Remover
a cobertura plástica do local
de inserção da agulha do conjunto
de infusão.
Empurrar firmemente a agulha
do conjunto de infusão.
Após a abertura do saco, o conteúdo deve ser usado imediatamente. Não se deve armazenar o saco aberto para uma infusão posterior.
Não se deve reconectar sacos parcialmente usados.
Não se deve conectar sacos em série para evitar embolia aérea causada pelo ar residual contido no primeiro saco.
Apenas para uso único. Todos os resíduos do produto não utilizado ou seus resíduos e todo o conjunto de infusão devem ser destruídos.
Não se deve armazenar sacos parcialmente usados e jogar fora todos os componentes do conjunto após o uso.
Componentes adicionais
Não se deve adicionar outros produtos ou substâncias medicinais a nenhuma das câmaras do saco ou à emulsão pronta, sem verificar previamente a compatibilidade e a estabilidade da mistura resultante (especialmente a estabilidade da emulsão lipídica).
O produto Multimel N6-900 E pode ser usado sem a adição de componentes ou, se necessário, após a adição de eletrólitos, minerais ou vitaminas.
A capacidade do saco é suficiente para permitir a adição de componentes adicionais, como vitaminas, eletrólitos e minerais. Todos os componentes adicionais (incluindo vitaminas) podem ser adicionados à emulsão pronta (após a ruptura das soldas e a mistura do conteúdo das 3 câmaras).
As vitaminas também podem ser adicionadas à câmara com solução de glicose antes da preparação da emulsão pronta (antes da ruptura das soldas e a mistura das soluções e emulsões).
Em caso de adição de componentes ao produto, antes da administração na veia periférica, deve-se medir a osmolalidade final da mistura.
Para o produto Multimel N6-900 E, podem ser adicionados:
- eletrólitos: deve-se considerar a quantidade de eletrólitos já presentes no saco; foi demonstrada a estabilidade da mistura contendo até 150 mmol de sódio, 150 mmol de potássio, 5,6 mmol de magnésio, 5 mmol de cálcio por litro de mistura de três componentes;
- fosfatos orgânicos: foi demonstrada a estabilidade da mistura contendo até 15 mmol de fosfatos adicionados por saco.
Minerais e vitaminas: foi demonstrada a estabilidade após a adição de produtos de vitaminas e minerais disponíveis no mercado (contendo até 1 mg de ferro). A compatibilidade com outros componentes adicionais está disponível a pedido.
Os componentes adicionais devem ser adicionados por pessoal qualificado em condições assépticas.
Os componentes adicionais são adicionados através do local de injeção usando uma agulha:
- preparar o local de injeção;
- inserir a agulha no local de injeção e injetar;
- misturar o conteúdo do saco com os componentes adicionados.
Interações com outros medicamentos
Não foram realizados estudos de interação com o produto Multimel.
O produto Multimel N6-900 E contém vitamina K, naturalmente presente nas emulsões lipídicas. A quantidade de vitamina K nas doses recomendadas do produto Multimel N6-900 E não deve afetar a ação dos derivados da cumarina.
Não se deve misturar ou administrar ceftriaxona simultaneamente com soluções intravenosas que contenham cálcio, incluindo o produto Multimel N6-900 E, pela mesma linha de infusão, devido ao risco de precipitação de sais de cálcio da ceftriaxona.
A ceftriaxona e as soluções que contenham cálcio podem ser administradas sequencialmente, uma após a outra, se as linhas de infusão forem usadas em locais diferentes ou se as linhas de infusão forem trocadas ou lavadas cuidadosamente entre as infusões com solução fisiológica de cloreto de sódio, a fim de evitar a formação de depósitos.
Devido à presença de potássio no produto Multimel N6-900 E, deve-se ter cuidado ao usá-lo em pacientes tratados com diuréticos poupadores de potássio (por exemplo, amilorida, espironolactona, triamtereno), inibidores da conversão da angiotensina (ECA), antagonistas do receptor da angiotensina II ou medicamentos imunossupressores: tacrolimo e ciclosporina, devido ao risco de hipercalemia.
Os lipídios presentes nesta emulsão podem interferir nos resultados de alguns exames laboratoriais (por exemplo, bilirrubina, desidrogenase láctica, saturação de oxigênio, hemoglobina glicada), desde que as amostras de sangue sejam coletadas antes da eliminação dos lipídios (os lipídios são geralmente eliminados após cerca de 5-6 horas após a interrupção da administração).
Incompatibilidades farmacêuticas
Não se deve administrar esta emulsão para infusão simultaneamente com sangue pelo mesmo conjunto de infusão.
O produto Multimel N6-900 E contém íons de cálcio, que representam um risco adicional de coagulação e formação de depósitos em sangue anticoagulado/conservado com citratos ou componentes sanguíneos.
A causa da incompatibilidade pode ser, por exemplo, a acididade excessiva (pH baixo) ou a presença inadequada de cátions divalentes (Ca e Mg), o que pode afetar negativamente a estabilidade da emulsão lipídica.
Como no caso de todas as misturas para nutrição parenteral, deve-se considerar o conteúdo de cálcio e fósforo. O excesso de cálcio ou fósforo, especialmente na forma de sais minerais, pode levar à formação de depósitos de fosfato de cálcio.
Deve-se verificar a compatibilidade do produto com as soluções administradas simultaneamente pela mesma linha de infusão, cateter ou cânula.
Não se deve misturar ou administrar ceftriaxona simultaneamente com soluções intravenosas que contenham cálcio, incluindo o produto Multimel N6-900 E, pela mesma linha de infusão (por exemplo, conexão do tipo Y), devido ao risco de precipitação de sais de cálcio da ceftriaxona (ver item "Interações").
5. PRAZO DE VALIDADE
2 anos, se o pacote de proteção não estiver danificado.
Recomenda-se que o produto seja usado imediatamente após a abertura das soldas que separam as 3 câmaras. No entanto, foi demonstrado que a emulsão pronta é estável por 7 dias a uma temperatura de +2 °C a +8 °C e, em seguida, por 48 horas a uma temperatura não superior a +25 °C.
Após a adição de componentes (eletrólitos, minerais, vitaminas) à emulsão pronta Multimel N6-900 E (ver seção anterior), a emulsão pronta mantém a estabilidade química e física por 7 dias a uma temperatura de 2 °C a 8 °C e, em seguida, por 48 horas a uma temperatura abaixo de 25 °C. Do ponto de vista microbiológico, cada mistura pronta contendo componentes adicionais deve ser usada imediatamente. Caso contrário, o tempo e as condições de armazenamento da mistura até o uso são de responsabilidade do usuário. No entanto, as misturas preparadas não devem ser armazenadas por mais de 24 horas a uma temperatura de 2-8 °C, a menos que a adição de componentes tenha sido realizada em condições assépticas controladas e validadas.
- País de registo
- Substância ativa
- Requer receita médicaNão
- Fabricante
- ImportadorBaxter S.A.
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a Multimel N6-900eForma farmacêutica: Solução, -Substância ativa: combinationsNão requer receita médicaForma farmacêutica: Solução, -Substância ativa: combinationsNão requer receita médicaForma farmacêutica: Solução, -Substância ativa: combinationsNão requer receita médica
Alternativas a Multimel N6-900e noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a Multimel N6-900e em Espanha
Alternativa a Multimel N6-900e em Ukraine
Médicos online para Multimel N6-900e
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de Multimel N6-900e – sujeita a avaliação médica e regras locais.














