

Maxitrol

Pergunte a um médico sobre a prescrição de Maxitrol

Como usar Maxitrol
Folheto incluído na embalagem: informação para o paciente
Atenção! Guarde o folheto! Informação na embalagem primária em língua estrangeira.
Maxitrol
(1 mg + 3500 UI + 6000 UI)/ml, gotas para os olhos, suspensão
Dexametasona + Sulfato de Neomicina + Sulfato de Polimixina B
Deve ler atentamente o conteúdo do folheto antes de usar o medicamento, pois contém informações importantes para o paciente.
- Deve guardar este folheto para poder relê-lo se necessário.
- Em caso de dúvidas, deve consultar um médico, farmacêutico ou enfermeiro.
- Este medicamento foi prescrito especificamente para uma pessoa. Não deve ser dado a outros. O medicamento pode prejudicar outra pessoa, mesmo que os sintomas da doença sejam os mesmos.
- Se o paciente desenvolver algum efeito colateral, incluindo qualquer efeito colateral não listado neste folheto, deve informar o médico, farmacêutico ou enfermeiro. Ver ponto 4.
Índice do folheto:
- 1. O que é o medicamento Maxitrol e para que é usado
- 2. Informações importantes antes de usar o medicamento Maxitrol
- 3. Como usar o medicamento Maxitrol
- 4. Possíveis efeitos colaterais
- 5. Como armazenar o medicamento Maxitrol
- 6. Conteúdo da embalagem e outras informações
1. O que é o medicamento Maxitrol e para que é usado
O medicamento Maxitrol é usado para tratar doenças inflamatórias dos olhos, que podem ser acompanhadas
de infecção.A inflamação do olho pode ser causada por infecção ou outros fatores
que afetam o olho ou lesões oculares.
O Maxitrol é um medicamento composto que contém componentes antibacterianos e corticosteroides.
Os corticosteroides (neste caso, dexametasona) são usados para prevenir e reduzir
inflamações oculares. Os medicamentos antibacterianos presentes nas gotas (neste caso, sulfato de neomicina
e sulfato de polimixina B) são ativos contra a maioria das bactérias patogênicas
que causam infecções oculares.
2. Informações importantes antes de usar o medicamento Maxitrol
Quando não usar o medicamento Maxitrol:
- se o paciente tiver alergiaao sulfato de neomicina, sulfato de polimixina B, dexametasona ou a qualquer um dos outros componentes deste medicamento (listados no ponto 6),
- se o paciente tiver:
- ceratite por herpes, varicela, sarampo ou qualquer outra infecção viral ocular,
- infecção fúngica ocular,
- infecção parasitária ocular não tratada,
- infecção tuberculosa ocular,
- infecção piogênica ocular não tratada.
Advertências e precauções
Para uso exclusivo nos olhos.
- Em alguns pacientes, pode ocorrer sensibilidade ao uso tópico de antibióticos aminoglicosídeos, como a neomicina. Se ocorrerem sintomas de sensibilidade, deve-se interromper o uso do medicamento e procurar um médico imediatamente (ver ponto 4). As reações de sensibilidade podem ocorrer na forma de coceira ou vermelhidão local, reações alérgicas graves (anafilaxia) ou reações cutâneas graves. Essas reações cutâneas podem ocorrer durante o uso de outros antibióticos tópicos ou sistêmicos da mesma família (aminoglicosídeos).
- Além disso, o uso tópico de neomicina pode causar vermelhidão, irritação e desconforto ocular.
- Os pacientes que desenvolveram sintomas de sensibilidade ao uso tópico de neomicina também podem desenvolver sensibilidade a outros antibióticos.
- Se o paciente estiver usando outros antibióticos durante o tratamento com Maxitrol, deve procurar um médico, pois o uso concomitante de Maxitrol com outros antibióticos pode causar efeitos colaterais graves.
- Os pacientes que usam corticosteroides oculares por períodos prolongados podem desenvolver: - pressão ocular aumentada. A pressão ocular deve ser monitorada regularmente durante o uso deste medicamento. Isso é especialmente importante em crianças, pois o aumento da pressão ocular causado por corticosteroides pode ser maior e ocorrer mais cedo em crianças do que em adultos. O paciente deve procurar um médico, especialmente em casos de crianças. O risco de aumento da pressão ocular e (ou) catarata também é maior em pacientes com predisposição (por exemplo, diabéticos). - desenvolvimento do síndrome de Cushing causado pelo medicamento que entra na corrente sanguínea. O paciente deve procurar um médico se desenvolver inchaço e aumento de peso, especialmente no tronco e face, pois são geralmente os primeiros sintomas da doença conhecida como síndrome de Cushing. A supressão da função adrenal pode ocorrer após a interrupção do uso prolongado ou intensivo de Maxitrol. O paciente deve procurar um médico antes de interromper o tratamento. Esse risco é especialmente importante em crianças e pacientes tratados com ritonavir ou cobicistat.
- Se ocorrer infecção ocular ou piora dos sintomas, o paciente deve procurar um médico imediatamente. Os pacientes que usam Maxitrol podem ter imunidade reduzida a infecções oculares, incluindo infecções bacterianas e fúngicas resistentes a antibióticos.
- Os pacientes que usam corticosteroides e anti-inflamatórios não esteroides concomitantemente podem desenvolver problemas de cicatrização de lesões oculares.
- Se o paciente tiver doenças que causem afinamento da córnea ou esclera, deve informar o médico.
Se o paciente desenvolver visão turva ou outros distúrbios da visão, deve procurar um médico.
Se o paciente tiver glaucoma, o tratamento deve ser limitado a duas semanas, a menos que o médico prescreva de outra forma.
O medicamento deve ser usado por tanto tempo quanto prescrito pelo médico.Se os sintomas da doença piorarem ou não melhorarem, o paciente deve consultar um médico.
Crianças
A segurança e eficácia do uso de Maxitrol em crianças não foram documentadas, portanto, não é recomendado o uso em crianças.
Maxitrol e outros medicamentos
O paciente deve informar o médico ou farmacêutico sobre todos os medicamentos que está usando atualmente ou recentemente, bem como sobre os medicamentos que planeja usar, incluindo os medicamentos sem prescrição.
Especially, o paciente deve informar o médico se estiver usando:
- anti-inflamatórios não esteroides tópicos. O uso concomitante de um medicamento esteroide e um anti-inflamatório não esteroide pode causar problemas de cicatrização de lesões oculares;
- ritonavir ou cobicistat, pois podem aumentar a concentração de dexametasona no sangue.
Se o paciente estiver usando outras gotas ou pomadas oculares, deve manter um intervalo de pelo menos 5 minutos entre as doses. As pomadas oculares devem ser usadas por último.
Gravidez, amamentação e fertilidade
Se a paciente estiver grávida ou amamentando, acredita que possa estar grávida ou planeja ter um filho, deve consultar um médico ou farmacêutico antes de usar este medicamento.
O medicamento não é recomendado durante a gravidez ou amamentação.
Condução de veículos e uso de máquinas
O Maxitrol não tem ou tem um efeito insignificante na capacidade de conduzir veículos e usar máquinas.
Por um período após a administração de Maxitrol, a visão pode estar turva. O paciente não deve conduzir veículos ou usar máquinas até que esse efeito desapareça.
Maxitrol gotas para os olhos contém cloreto de benzalcônio
O medicamento contém 0,04 mg de cloreto de benzalcônio por mililitro (0,04 mg/ml).
O cloreto de benzalcônio pode ser absorvido por lentes de contato macias e alterar sua coloração. O paciente deve remover as lentes de contato antes de usar as gotas e esperar pelo menos 15 minutos antes de recolocá-las.
O cloreto de benzalcônio também pode causar irritação ocular, especialmente em pessoas com síndrome do olho seco ou distúrbios da córnea (camada transparente da frente do olho). Se ocorrerem sensações anormais no olho, coceira ou dor após o uso do medicamento, o paciente deve procurar um médico.
3. Como usar o medicamento Maxitrol
O medicamento Maxitrol deve ser usado sempre de acordo com as instruções do médico. Em caso de dúvidas, o paciente deve consultar um médico ou farmacêutico.
O Maxitrol é destinado exclusivamentepara uso nos olhos; uma embalagem do medicamento deve ser usada por apenasum paciente.
Se, após a remoção da tampa, o anel de segurança estiver solto, deve ser removido antes de usar o medicamento.
Recomenda-se fechar a pálpebra e pressionar suavemente o ducto nasolacrimal (canal lacrimal) com o dedo. Isso ajuda a reduzir a absorção do medicamento para a corrente sanguínea após a administração em forma de gotas para os olhos.
Dose recomendada
Em doenças de curso leve, use 1 a 2 gotas no(s) saco(s) conjuntival(is) 4 a 6 vezes ao dia.
Em casos graves, use 1 a 2 gotas a cada hora. O medicamento deve ser usado em doses cada vez menores à medida que os sintomas da inflamação desaparecem, e o tratamento deve ser interrompido após a resolução dos sintomas.
O médico determinará a duração do tratamento. O paciente não deve interromper o tratamento prematuramente.
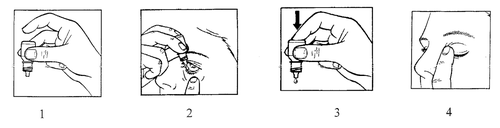
- 1. Preparar a garrafa de Maxitrol e um espelho.
- 2. Lavar as mãos.
- 3. Agitar a garrafa.
- 4. Remover a tampa.
- 5. Segurar a garrafa com a mão e direcioná-la para cima com a base, segurando com o polegar e o dedo médio (figura 1).
- 6. Inclinar a cabeça para trás. Puxar a pálpebra inferior para baixo com um dedo limpo, de modo a formar uma "bolsa" entre a pálpebra e o globo ocular. A gota deve cair nessa bolsa (figura 2).
- 7. Aproximar a ponta da garrafa do olho. Para facilitar, pode-se usar um espelho.
8. Não tocar a ponta do aplicador no olho, pálpebra, área ao redor dos olhos ou outras superfícies.
Não seguir essa recomendação pode causar infecção das gotas.
- 9. Pressionar suavemente a base da garrafa para fazer com que uma gota única de Maxitrol saia (figura 3).
- 10. Após a instilação de Maxitrol, remover o dedo que segurava a pálpebra inferior. Fechar o olho e pressionar o canto do olho perto do nariz com o dedo (figura 4). Isso ajuda a prevenir a absorção do medicamento para a corrente sanguínea.
- 11. Se for necessário administrar gotas em ambos os olhos, repetir as etapas acima para o segundo olho.
- 12. Fechar a garrafa imediatamente após o uso.
- 13. Deve-se usar uma garrafa de Maxitrol por vez.
Se a gota não atingir o olho,deve-se repetir a tentativa de instilação correta.
Uso de dose maior do que a recomendada de Maxitrol
Em caso de superdose local de Maxitrol, deve-se lavar o olho(s) com água morna.
Não deve-se usar o medicamento até a próxima dose programada.
Omissão da dose de Maxitrol
Se o paciente esquecer uma dose, deve tomar a próxima dose programada. No entanto, se faltar pouco tempo para a próxima dose, a dose esquecida deve ser omitida e o paciente deve retornar ao esquema de dosagem normal. Não devetomar uma dose dupla para compensar a dose esquecida.
Em caso de dúvidas adicionais sobre o uso deste medicamento, o paciente deve consultar um médico ou farmacêutico.
4. Possíveis efeitos colaterais
Como qualquer medicamento, este medicamento pode causar efeitos colaterais, embora não todos os pacientes os desenvolvam.
Se o paciente desenvolver reações alérgicas, incluindo erupções cutâneas, inchaço facial, lábios, língua e (ou)
garganta, que podem causar dificuldade para respirar ou engolir, ou desenvolver outros efeitos colaterais graves, deve interromper o uso de Maxitrol e procurar um médico ou o departamento de emergência do hospital mais próximo.
Durante o uso de Maxitrol, foram observados os seguintes efeitos colaterais:
Pouco comuns(pode ocorrer em menos de 1 em 1000 pacientes): ceratite, aumento da pressão intraocular, coceira nos olhos, desconforto nos olhos, irritação nos olhos.
Frequência desconhecida(frequência não pode ser estimada com base nos dados disponíveis):
hipersensibilidade, dor de cabeça, ceratite ulcerativa, visão turva, hipersensibilidade à luz, dilatação da pupila, ptose, dor nos olhos, inchaço nos olhos, sensação de corpo estranho nos olhos, hiperemia nos olhos, lacrimejamento aumentado, reações cutâneas graves (síndrome de Stevens-Johnson), visão turva, hirsutismo (especialmente em mulheres), fraqueza muscular e perda de massa muscular, estrias roxas na pele, hipertensão, irregularidades menstruais ou amenorreia, alterações nos níveis de proteína e cálcio no organismo, supressão do crescimento em crianças e adolescentes, e inchaço e ganho de peso, especialmente no tronco e face (doença conhecida como síndrome de Cushing) (ver ponto 2 "Advertências e precauções").
Notificação de efeitos colaterais
Se ocorrerem qualquer efeito colateral, incluindo qualquer efeito colateral não listado neste folheto, o paciente deve informar o médico, farmacêutico ou enfermeiro. Os efeitos colaterais podem ser notificados diretamente ao Departamento de Monitoramento de Efeitos Colaterais de Medicamentos da Agência Reguladora de Medicamentos, Produtos para a Saúde e Produtos Biocidas, Al. Jerozolimskie 181C, 02-222 Varsóvia, telefone: +48 22 49 21 301, fax: +48 22 49 21 309, site: https://smz.ezdrowie.gov.pl.
A notificação de efeitos colaterais pode ajudar a coletar mais informações sobre a segurança do medicamento.
Se qualquer um dos sintomas se agravar ou se ocorrerem outros sintomas não listados neste folheto, o paciente deve informar o médico.
5. Como armazenar o medicamento Maxitrol
Para evitar a contaminação das gotas, a garrafa deve ser descartada após 4 semanas da primeira abertura. A data de abertura da garrafa deve ser anotada no espaço indicado abaixo.
Data de primeira abertura:
O medicamento deve ser armazenado em um local não visível e inacessível a crianças.
Não armazenar em temperaturas acima de 25°C.
Não armazenar na geladeira ou congelar.
Armazenar na embalagem original para proteger da luz.
Armazenar a garrafa bem fechada.
Não deve-se usar este medicamento após a data de validade indicada na embalagem. A data de validade indica o último dia do mês indicado.
Os medicamentos não devem ser jogados na canalização ou em lixeiras domésticas. O paciente deve perguntar ao farmacêutico como descartar os medicamentos que não são mais usados. Essa ação ajudará a proteger o meio ambiente.
6. Conteúdo da embalagem e outras informações
O que contém o medicamento Maxitrol
Os princípios ativos do medicamento são:
Dexametasona 1 mg/ml (0,1% p/v)
Sulfato de Neomicina 3500 UI/ml (3500 IU/ml)
Sulfato de Polimixina B 6000 UI/ml (6000 IU/ml)
Os excipientes são: cloreto de sódio, polissorbato 20, cloreto de benzalcônio, hipromelose (E 464),
água purificada.
Para o medicamento, são adicionadas quantidades mínimas de ácido clorídrico e (ou) hidróxido de sódio para manter o pH dentro do limite normal.
Como é o medicamento e o que a embalagem contém
O Maxitrol gotas para os olhos é uma suspensão não transparente de cor branca a amarelo-clara.
Está disponível em uma garrafa de polietileno de baixa densidade (LDPE) com um aplicador (LDPE) e uma tampa branca de polipropileno (PP), em uma caixa de papelão.
Para obter informações mais detalhadas, o paciente deve consultar o responsável pelo medicamento ou o importador paralelo.
Responsável pelo medicamento na Irlanda, país de exportação:
Novartis Ireland Limited
Vista Building
Elm Park
Merrion Road, Ballsbridge
Dublin 4, Irlanda
Fabricante:
Novartis Farmacéutica, S.A., Gran Via de les Corts Catalanes, 764, 08013 Barcelona, Espanha
Novartis Manufacturing NV, Rijksweg 14, 2870 Puurs-Sint-Amands, Bélgica
Siegfried El Masnou, S.A., Camil Fabra, 58, El Masnou, 08320 Barcelona, Espanha
Novartis Pharma GmbH, Roonstrasse 25, 90429 Nuremberga, Alemanha
Importador paralelo:
InPharm Sp. z o.o.
ul. Strumykowa 28/11
03-138 Varsóvia
Reembalado por:
InPharm Sp. z o.o. Services sp. k.
ul. Chełmżyńska 249
04-458 Varsóvia
Número da autorização na Irlanda, país de exportação:PA0896/019/001
Número da autorização de importação paralela:451/21
Data de aprovação do folheto: 03.06.2025
[Informação sobre marca registrada]
- País de registo
- Substância ativa
- Requer receita médicaNão
- Titular da Autorização de Introdução no Mercado (AIM, MAH)Novartis Ireland Ltd
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a MaxitrolForma farmacêutica: Gotas, (3 mg + 1 mg)/mlSubstância ativa: dexamethasone and antiinfectivesFabricante: Rafarm S.A.Requer receita médicaForma farmacêutica: Gotas, (5 mg + 1 mg)/mlSubstância ativa: dexamethasone and antiinfectivesFabricante: Dr. Gerhard Mann Chem. - Pharm. Fabrik GmbHRequer receita médicaForma farmacêutica: Pomada, (5 mg + 0.3 mg)/gSubstância ativa: dexamethasone and antiinfectivesFabricante: Dr. Gerhard Mann Chem. - Pharm. Fabrik GmbHRequer receita médica
Alternativas a Maxitrol noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a Maxitrol em Ukraina
Alternativa a Maxitrol em Hiszpania
Médicos online para Maxitrol
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de Maxitrol – sujeita a avaliação médica e regras locais.














