

MAXITROL 3.500 UI/mL + 6.000 UI/mL + 1 mg/mL COLÍRIO EM SUSPENSÃO

Pergunte a um médico sobre a prescrição de MAXITROL 3.500 UI/mL + 6.000 UI/mL + 1 mg/mL COLÍRIO EM SUSPENSÃO

Como usar MAXITROL 3.500 UI/mL + 6.000 UI/mL + 1 mg/mL COLÍRIO EM SUSPENSÃO
Introdução
Prospecto: informação para o utilizador
MAXITROL 3.500 UI/ml + 6.000 UI/ml + 1 mg/ml colírio em suspensão
Neomicina / Polimixina B / Dexametasona
Leia todo o prospecto atentamente antes de começar a usar este medicamento, porque contém informações importantes para si.
- Conserva este prospecto, porque pode ter que voltar a lê-lo.
- Se tiver alguma dúvida, consulte o seu médico ou farmacêutico.
- Este medicamento foi prescrito apenas para si, e não deve dá-lo a outras pessoas, embora tenham os mesmos sintomas que si, porque pode prejudicá-las.
- Se experimentar efeitos adversos, consulte o seu médico ou farmacêutico, mesmo que se trate de efeitos adversos que não aparecem neste prospecto. Ver secção 4.
Conteúdo do prospecto:
- O que é MAXITROL e para que se utiliza
- O que precisa saber antes de começar a usar MAXITROL
- Como usar MAXITROL
- Possíveis efeitos adversos
- Conservação de MAXITROL
- Conteúdo do envase e informação adicional
1. O que é MAXITROL e para que se utiliza
É um colírio que combina dois antibióticos que oferecem uma atividade antibacteriana de amplo espectro juntamente com a atividade anti-inflamatória de um corticosteroide (dexametasona), para tratar certas infecções microbianas do segmento anterior do olho.
Os antibióticos são utilizados para tratar infecções bacterianas e não servem para tratar infecções virais.
É importante que siga as instruções relativas à dose, ao intervalo de administração e à duração do tratamento indicadas pelo seu médico.
Não guarde nem reutilize este medicamento. Se uma vez finalizado o tratamento lhe sobrar antibiótico, devolva-o à farmácia para a sua correta eliminação. Não deve deitar os medicamentos pelo esgoto nem para o lixo.
Este medicamento está indicado no tratamento das inflamações do olho infecciosas que requeiram corticoides quando seja necessária profilaxia antibiótica.
2. O que precisa saber antes de começar a usar MAXITROL
Não use Maxitrol
- Se é alérgico à neomicina, polimixina B, dexametasona ou a algum dos outros componentes deste medicamento (incluídos na secção 6).
- Se pensa que tem:
- Queratite por herpes simplex, varicela, varicela/herpes zoster ou qualquer outra infecção do olho causada por vírus.
- Tuberculose do olho.
- Doenças fúngicas do olho
- Antecedentes de glaucoma pessoal ou familiar.
Advertências e precauções
Consulte o seu médico ou farmacêutico antes de começar a usar Maxitrol.
- Apenas utilize este medicamento nos seus olhos.
- Se com este medicamento lhe aparecerem sintomas de reação alérgica, interrompa o tratamento e consulte o seu médico. As reações alérgicas podem variar desde picazón localizado ou enrubescimento da pele até reações alérgicas graves (reação anafiláctica) ou reações graves da pele. Estas reações alérgicas podem ocorrer com outros antibióticos tópicos ou sistémicos da mesma família (aminoglicosídeos).
- O uso deste medicamento pode produzir molestia, irritação e enrubescimento da pele.
- Se ao mesmo tempo está utilizando outro tratamento antibiótico, consulte o seu médico.
- Se utilizar este medicamento durante um período longo de tempo, pode:
- tornar-se mais sensível a infecções do olho
- sofrer aumento da pressão no olho(s). Durante o uso deste medicamento, deverá controlar regularmente a pressão do olho. Isto é especialmente importante em pacientes pediátricos, pois o risco de hipertensão ocular induzida por corticosteroides pode ser maior em crianças e pode ocorrer mais rapidamente do que em adultos. O risco de pressão intraocular elevada e/ou formação de cataratas induzida por corticosteroides é maior em pacientes propensos (p. ex., diabetes)
- desenvolver cataratas
- Desenvolver o síndrome de Cushing devido a que o medicamento chegue até ao sangue. Consulte o seu médico se sofre inchaço e aumento de peso à volta do tronco e na face, pois estas são, por norma, as primeiras manifestações do síndrome. Pode produzir-se uma supressão da função da glândula adrenal após interromper um tratamento intensivo ou a longo prazo com Maxitrol. Consulte o seu médico antes de interromper o tratamento por sua conta. Estes riscos são especialmente importantes em crianças e pacientes tratados com medicamentos que contêm ritonavir ou cobicistat.
- Consulte o seu médico ou farmacêutico se sofre um distúrbio causante de adelgaçamento dos tecidos do olho antes de utilizar este medicamento.
- Se os seus sintomas pioram ou voltam repentinamente, por favor, contacte o seu médico. Com o uso deste medicamento pode tornar-se mais sensível a infecções oculares.
- Entre em contacto com o seu médico se apresenta visão borrosa ou outras alterações visuais.
- Os esteroides aplicados no olho podem retardar a cura de feridas do mesmo. Também se sabe que os AINEs (Anti-inflamatórios Não Esteroideos) oftálmicos enlentecem ou retardam a cicatrização. O uso concomitante de AINEs e esteroides oftálmicos pode aumentar o potencial de problemas de cicatrização.
- Se utiliza lentes de contacto:
- Levar lentes de contacto (duras ou macias) não é recomendado durante o tratamento de uma inflamação ou infecção do olho.
Outros medicamentos e Maxitrol
Informa ao seu médico ou farmacêutico se está utilizando, utilizou recentemente ou pudesse ter que utilizar qualquer outro medicamento.
Informa ao seu médico se está utilizando AINEs oftálmicos. O uso concomitante de esteroides e AINEs oftálmicos pode aumentar os problemas de cicatrização da córnea.
Informa ao seu médico se está utilizando ritonavir ou cobicistat, pois pode provocar um aumento da quantidade de dexametasona no sangue.
Gravidez, lactação e fertilidade
Se está grávida ou em período de lactação, acredita que possa estar grávida ou tem intenção de engravidar, consulte o seu médico ou farmacêutico antes de utilizar este medicamento.
Este medicamento não é recomendado durante a gravidez nem a lactação.
Condução e uso de máquinas
Pode notar que a sua visão se torna borrosa durante um tempo após aplicar o colírio. Não conduza nem utilize máquinas até que este efeito desapareça.
Maxitrol contém cloreto de benzalconio
Este medicamento contém 0,04 mg de cloreto de benzalconio em cada ml.
O cloreto de benzalconio pode ser absorvido pelas lentes de contacto macias, alterando a sua cor. Retire as lentes de contacto antes de usar este medicamento e espere 15 minutos antes de voltar a colocá-las.
O cloreto de benzalconio pode causar irritação ocular, especialmente se padece de olho seco ou outras doenças da córnea (camada transparente da zona frontal do olho). Consulte o seu médico se sente uma sensação estranha, picazón ou dor no olho após usar este medicamento.
3. Como usar MAXITROL
Siga exatamente as instruções de administração deste medicamento indicadas pelo seu médico ou farmacêutico. Em caso de dúvida, consulte novamente o seu médico ou farmacêutico.
Este medicamento apenas deve ser utilizado como gotas para os olhos.
A dose recomendada é:
Uso em adultos (incluídos pacientes de idade avançada)
Instilar 1 ou 2 gotas no saco conjuntival 4 ou 6 vezes ao dia. A dose pode ser reduzida após 3 ou 4 dias se se obtiver uma resposta satisfatória.
Uso em crianças
Não há dados disponíveis.
Recomendações de uso:
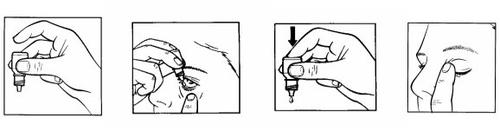
1 2 3 4
- Lave as mãos.
- Coja o frasco (envase conta-gotas).
- Agite bem antes de usar.
- Depois de abrir o frasco pela primeira vez, deve retirar o anel de plástico do precinto se estiver solto.
- Sostenha o frasco, boca para baixo, entre os dedos (figura 1).
- Incline a cabeça para trás. Separe suavemente a pálpebra do olho com um dedo até que se forme uma bolsa entre a pálpebra e o seu olho, na qual deverá cair a gota (figura 2).
- Aproxime a ponta do frasco do olho. Pode ser-lhe útil um espelho.
- Não toque no olho ou na pálpebra, zonas próximas nem outras superfícies com o conta-gotas. As gotas poderiam contaminar-se.
- Aperte suavemente a base do frasco com o dedo índice para que caia uma gota de cada vez (figura 3).
- Depois de utilizar este medicamento, solte a pálpebra, feche o olho e pressione suavemente com o dedo o bordo do olho junto à nariz. Isto ajuda a evitar que este medicamento passe para o resto do corpo (figura 4).
- Se se aplicam gotas em ambos os olhos, repita todos os passos anteriores com o outro olho.
- Feche bem o frasco imediatamente após utilizar o produto.
Se uma gota cair fora do olho, tente novamente.
Se está utilizando outros medicamentos oftálmicos, espere pelo menos 5 minutos entre a administração deste medicamento e os outros medicamentos oftálmicos. As pomadas oftálmicas devem ser administradas por último.
Se usa mais Maxitrol do que deve,pode eliminá-lo lavando os olhos com água morna. Não se aplique mais gotas até a próxima dose.
Em caso de sobredose ou ingestão acidental, consulte imediatamente o seu médico ou farmacêutico ou ligue para o Serviço de Informação Toxicológica, telefone: 91 562 04 20, indicando o medicamento e a quantidade utilizada.
Se esqueceu de usar Maxitrol,aplique uma única dose assim que se dê conta e continue com a próxima dose que estava prevista. No entanto, se já é quase a hora da próxima dose, não se aplique a dose esquecida e continue com a próxima dose do seu regime habitual. Não se aplique uma dose dupla para compensar as doses esquecidas.
Se tiver alguma outra dúvida sobre o uso deste medicamento, pergunte ao seu médico ou farmacêutico.
4. Possíveis efeitos adversos
Como todos os medicamentos, este medicamento pode produzir efeitos adversos, embora nem todas as pessoas os sofram.
Os efeitos adversos são classificados por frequências, que são definidas como: muito frequentes (podem afetar mais de 1 de cada 10 pessoas); frequentes (podem afetar até 1 de cada 10 pessoas); pouco frequentes (podem afetar até 1 de cada 100 pessoas); raros (podem afetar até 1 de cada 1.000 pessoas); muito raros (podem afetar até 1 de cada 10.000 pessoas); frequência não conhecida (não pode ser estimada a partir dos dados disponíveis).
Foram notificados os seguintes efeitos adversos com este medicamento:
Efeitos adversos pouco frequentes (podem afetar até 1 de cada 100 pessoas):
- Efeitos no olho: inflamação da superfície do olho, aumento da pressão no olho,
picazón no olho, molestia no olho, irritação do olho,
Foram observados os seguintes efeitos adversos durante a experiência pós-comercialização deste medicamento. Não se conhece a frequência (não pode ser estimada a partir dos dados disponíveis):
- Efeitos no olho: úlcera corneal, visão borrosa, sensibilidade à luz, aumento no tamanho da pupila, queda da pálpebra, dor no olho, inchaço no olho, sensação anormal no olho, enrubescimento do olho, aumento na produção de lágrimas.
- Efeitos gerais: alergia, dor de cabeça, reações graves na pele (Síndrome de Stevens-Johnson).
Problemas hormonais: crescimento excessivo de pelo corporal (particularmente nas mulheres), fraqueza e desgaste muscular, estrias moradas na pele do corpo, aumento da pressão arterial, menstruações irregulares ou ausentes, alterações nos níveis de proteínas e cálcio do corpo, atraso no crescimento em crianças e adolescentes e inchaço e aumento de peso do corpo e da face (síndrome de Cushing) (ver secção 2, "Advertências e precauções").
Comunicação de efeitos adversos
Se experimentar qualquer tipo de efeito adverso, consulte o seu médico ou farmacêutico, mesmo que se trate de possíveis efeitos adversos que não aparecem neste prospecto. Também pode comunicá-los diretamente através do Sistema Espanhol de Farmacovigilância de Medicamentos de Uso Humano: https://www.notificaRAM.es.Mediante a comunicação de efeitos adversos, você pode contribuir para proporcionar mais informações sobre a segurança deste medicamento.
5. Conservação de MAXITROL
Mantenha este medicamento fora da vista e do alcance das crianças.
Não utilize este medicamento após a data de validade que aparece no frasco e na caixa após CAD. A data de validade é o último dia do mês que se indica.
Não conserve a uma temperatura superior a 25ºC. Não refrigerar.
Para evitar infecções, deve deitar o frasco 4 semanas após tê-lo aberto pela primeira vez.
Anote a data de abertura do frasco no recuadro reservado para esta finalidade na caixa.
Os medicamentos não devem ser deitados pelos esgotos nem para o lixo. Deposite os envases e os medicamentos que não precisa no Ponto SIGRE da farmácia. Em caso de dúvida, pergunte ao seu farmacêutico como se livrar dos envases e dos medicamentos que não precisa. Deste modo, ajudará a proteger o meio ambiente.
6. Conteúdo do envase e informação adicional
Composição de Maxitrol
- Os princípios ativos são sulfato de neomicina, sulfato de polimixina B e dexametasona. Um ml de suspensão contém 3.500 UI de sulfato de neomicina, 6.000 UI de sulfato de polimixina B e 1 mg de dexametasona.
- Os demais componentes são cloreto de benzalconio, cloreto de sódio, polissorbato 20 (E-432), hipromelosa (E 464), ácido clorídrico concentrado e/ou hidróxido de sódio e água purificada.
Aspecto do produto e conteúdo do envase
Maxitrol é um líquido (branco ou ligeiramente amarelado) que se apresenta em um envase que contém um frasco de plástico de 5 ml com um tampão de rosca.
Titular da autorização de comercialização
Novartis Farmacêutica, S.A.
Gran Via de les Corts Catalanes, 764
08013 – Barcelona, Espanha
Responsável pela fabricação
Siegfried El Masnou, S.A.
C/ Camil Fabra, 58
08320 El Masnou – Barcelona, Espanha
ou
Novartis Farmacêutica, S.A.
Gran Via de les Corts Catalanes, 764
08013 Barcelona, Espanha
ou
Novartis Pharma GmbH
Roonstrasse 25
90429 Nuremberga, Alemanha
ou
Novartis Manufacturing NV
Rijsksweg 14
2870 Puurs-Sint-Amands
Bélgica
Data da última revisão deste prospecto: Janeiro 2019
A informação detalhada deste medicamento está disponível na página Web da Agência Espanhola de Medicamentos e Produtos Sanitários (AEMPS) http://www.aemps.gob.es/
- País de registo
- Substância ativa
- Requer receita médicaSim
- Fabricante
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a MAXITROL 3.500 UI/mL + 6.000 UI/mL + 1 mg/mL COLÍRIO EM SUSPENSÃOForma farmacêutica: COLÍRIO, 1 mg/ml + 5 mg/mlSubstância ativa: dexamethasone and antiinfectivesFabricante: Santen OyRequer receita médicaForma farmacêutica: COLÍRIO, 3 mg/ml + 1 mg/mlSubstância ativa: dexamethasone and antiinfectivesFabricante: Sifi S.P.A.Requer receita médicaForma farmacêutica: COLÍRIO, 3mg/ml + 1mg/mlSubstância ativa: dexamethasone and antiinfectivesFabricante: Sifi S.P.A.Requer receita médica
Alternativas a MAXITROL 3.500 UI/mL + 6.000 UI/mL + 1 mg/mL COLÍRIO EM SUSPENSÃO noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a MAXITROL 3.500 UI/mL + 6.000 UI/mL + 1 mg/mL COLÍRIO EM SUSPENSÃO em Polónia
Alternativa a MAXITROL 3.500 UI/mL + 6.000 UI/mL + 1 mg/mL COLÍRIO EM SUSPENSÃO em Ukraine
Médicos online para MAXITROL 3.500 UI/mL + 6.000 UI/mL + 1 mg/mL COLÍRIO EM SUSPENSÃO
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de MAXITROL 3.500 UI/mL + 6.000 UI/mL + 1 mg/mL COLÍRIO EM SUSPENSÃO – sujeita a avaliação médica e regras locais.














