
Antithrombin Iii Nf Takeda

Pergunte a um médico sobre a prescrição de Antithrombin Iii Nf Takeda

Como usar Antithrombin Iii Nf Takeda
Folheto informativo para o utilizador
Antithrombin III NF Takeda, 50 UI/ml, pó e solvente para solução para infusão
humana antitrombina III de origem plasmática
Deve ler atentamente o conteúdo do folheto antes de tomar o medicamento, pois contém informações importantes para o doente.
- Deve guardar este folheto para poder relê-lo se necessário.
- Em caso de dúvidas, deve consultar o médico ou farmacêutico.
- Se o doente apresentar algum efeito secundário, incluindo qualquer efeito secundário não mencionado neste folheto, deve informar o médico ou farmacêutico. Ver ponto 4.
Índice do folheto
- 1. O que é Antithrombin III NF Takeda e para que é utilizado
- 2. Informações importantes antes de tomar Antithrombin III NF Takeda
- 3. Como tomar Antithrombin III NF Takeda
- 4. Efeitos secundários possíveis
- 5. Como conservar Antithrombin III NF Takeda
- 6. Conteúdo do pacote e outras informações
1. O que é Antithrombin III NF Takeda e para que é utilizado
Antithrombin III NF Takeda é apresentado sob a forma de pó branco ou amarelado-pálido
com solvente associado para solução para infusão.
Antithrombin III NF Takeda está disponível em embalagens contendo:
- 500 UI de antitrombina III e 10 ml de solvente ou
- 1000 UI de antitrombina III e 20 ml de solvente
Antithrombin III NF Takeda pertence a um grupo farmacoterapêutico conhecido como agentes
antitrombóticos.
Antithrombin III NF Takeda é utilizado no tratamento de deficiência congénita ou adquirida de
antitrombina III, sendo que a deficiência adquirida pode ocorrer no decurso de muitas perturbações
clínicas.
2. Informações importantes antes de tomar Antithrombin III NF Takeda
Quando não tomar Antithrombin III NF Takeda
- se o doente for alérgico à antitrombina III ou a qualquer outro componente deste medicamento (listados no ponto 6)
- em doentes com trombocitopenia induzida por heparina (i.e., redução do número de plaquetas) na história
Precauções e advertências
Identificabilidade
Para melhorar a identificabilidade de produtos biológicos, deve registar-se claramente
o nome e o número de série do produto administrado.
- Deve informar o médico assistente se ocorrerem os primeiros sintomas de reação alérgica (por exemplo, urticária, incluindo urticária generalizada, pressão no peito, respiração sibilante, hipotensão e choque anafilático). Sintomas graves podem exigir tratamento de emergência.
- Deve informar o médico se o doente estiver a tomar ou tiver tomado recentemente medicamentos que contenham heparina (por exemplo, no tratamento de trombose), pois a ação da antitrombina é significativamente potenciada pela heparina.
- Antithrombin III NF Takeda é produzido a partir de plasma humano. No caso da administração de medicamentos obtidos a partir de sangue ou plasma humano, não é possível excluir completamente a transmissão de agentes infecciosos. Isso também se aplica a patógenos ainda desconhecidos. No entanto, o risco de transmissão de agentes infecciosos é minimizado por meio da seleção cuidadosa de doadores e plasma, testes de bancos de plasma e procedimentos de inativação/remoção de vírus.
Crianças
Não administrar este medicamento a crianças com menos de 6 anos, pois a segurança e eficácia não foram estabelecidas nesta faixa etária.
Antithrombin III NF Takeda e outros medicamentos
Deve informar o médico sobre todos os medicamentos que o doente está a tomar atualmente ou
recentemente, bem como sobre os medicamentos que o doente planeia tomar.
Deve informar o médico sobre os medicamentos que contenham heparina (por exemplo, no tratamento de trombose) que o doente está a tomar atualmente ou recentemente, pois a ação da antitrombina é significativamente potenciada pela heparina.
Gravidez, amamentação e fertilidade
Deve informar o médico se a paciente está grávida ou a amamentar. O médico decidirá se
é possível administrar Antithrombin III NF Takeda durante a gravidez ou amamentação.
Se a paciente estiver grávida ou a amamentar, acredita que possa estar grávida ou planeia ter
um filho, deve consultar o médico ou farmacêutico antes de tomar este medicamento.
Condução de veículos e utilização de máquinas
Embora não tenha sido observado qualquer efeito na capacidade de conduzir veículos ou operar máquinas, não é possível excluir tal efeito. Portanto, recomenda-se que o doente não conduza veículos ou opere máquinas sem consultar previamente o médico.
Antithrombin III NF Takeda contém sódio
500 UI/10 ml
O medicamento contém 37,7 mg de sódio (principal componente do sal de cozinha) em cada frasco. Isso corresponde a 1,9%
da dose diária máxima recomendada pela OMS de 2 g de sódio para adultos.
1000 UI/20 ml
O medicamento contém 75,5 mg de sódio (principal componente do sal de cozinha) em cada frasco. Isso corresponde a 3,8%
da dose diária máxima recomendada pela OMS de 2 g de sódio para adultos.
3. Como tomar Antithrombin III NF Takeda
Antithrombin III NF Takeda será administrado exclusivamente sob supervisão médica. A dose
dependerá do peso corporal e das necessidades individuais do doente. O médico assistente determinará
a dose a ser administrada. Antithrombin III NF Takeda será administrado por infusão intravenosa.
Administração de uma dose maior do que a recomendada de Antithrombin III NF Takeda
Não foram relatados sintomas de superdose de antitrombina.
Omissão da administração de Antithrombin III NF Takeda
Não se aplica.
Interrupção da administração de Antithrombin III NF Takeda
Não se aplica.
4. Efeitos secundários possíveis
Como qualquer medicamento, este medicamento pode causar efeitos secundários, embora não
ocorram em todos. Os efeitos secundários observados após a comercialização de Antithrombin III NF Takeda incluem hipersensibilidade, reação anafilática, tremores e ondas de calor.
- Hipersensibilidade ou reações alérgicas, como: angioedema, ardor e picadas no local da infusão, calafrios, ondas de calor, urticária generalizada, cefaleia, erupção cutânea pruriginosa, hipotensão, sonolência, náuseas, ansiedade, taquicardia, sensação de opressão no peito, formigamento, vômitos, respiração sibilante foram observados raramente, mas podem ser graves o suficiente para causar reação anafilática (incluindo choque).
- Em casos raros, foi observada febre.
- Em casos raros, pode ocorrer trombocitopenia (i.e., redução do número de plaquetas), que é mediada por anticorpos induzidos por heparina. Foi observada uma redução do número de plaquetas abaixo de 100.000/µl ou uma redução do número de plaquetas em 50%.
Se algum efeito secundário piorar ou ocorrer algum efeito secundário não mencionado neste folheto, deve informar o médico.
Notificação de efeitos secundários
Se ocorrerem algum efeito secundário, incluindo qualquer efeito secundário não mencionado no folheto, deve informar o médico ou farmacêutico. Os efeitos secundários podem ser notificados diretamente ao Departamento de Monitorização de Efeitos Secundários de Medicamentos da Agência Reguladora de Medicamentos:
Al. Jerozolimskie 181C
02-222 Warszawa
Tel.: + 48 22 49 21 301
Fax: + 48 22 49 21 309
Site da internet: https://smz.ezdrowie.gov.pl
Os efeitos secundários também podem ser notificados ao titular da autorização de comercialização.
A notificação de efeitos secundários pode ajudar a obter mais informações sobre a segurança do medicamento.
5. Como conservar Antithrombin III NF Takeda
Manter o medicamento fora do alcance e da vista das crianças.
Manter na geladeira (2°C a 8°C). Não congelar.
Manter no embalagem original para proteger da luz.
Não usar este medicamento após o prazo de validade impresso na etiqueta e embalagem de cartão após EXP. O prazo de validade é o último dia do mês indicado.
Não usar este medicamento se a solução estiver turva ou contiver depósitos.
Os medicamentos não devem ser jogados na canalização ou lixeiras domésticas. Deve perguntar ao farmacêutico como eliminar os medicamentos que já não sejam necessários. Este procedimento ajudará a proteger o meio ambiente.
6. Conteúdo do pacote e outras informações
O que contém Antithrombin III NF Takeda
- O princípio ativo do medicamento é a antitrombina III humana de origem plasmática
- Os outros componentes são glicose, cloreto de sódio, citrato de sódio di-hidratado e tris (hidroximetil) aminometano
Como é Antithrombin III NF Takeda e o que o pacote contém
Antithrombin III NF Takeda é apresentado sob a forma de pó para solução para infusão
contendo nominalmente 500 UI (ou 1000 UI) de antitrombina de origem plasmática humana
em frasco e solvente.
500 UI/10 ml
Após reconstituição em 10 ml de água estéril para injeção, o medicamento contém aproximadamente 50 UI/ml (500 UI/10 ml)
de antitrombina III humana de origem plasmática.
1000 UI/20 ml
Após reconstituição em 20 ml de água estéril para injeção, o medicamento contém aproximadamente 50 UI/ml
(1000 UI/20 ml) de antitrombina III humana de origem plasmática.
Antithrombin III NF Takeda é um pó liofilizado amarelado-pálido ou verde-pálido.
Cada embalagem também contém:
- 1 agulha de transferência
- 1 agulha com filtro
- 1 agulha de ventilação
- 1 agulha de uso único
- 1 conjunto para infusão
Titular da autorização de comercialização e fabricante
Titular da autorização de comercialização
Takeda Pharma, S.A.
Rua Prosta, 68
00-838 Varsóvia
Fabricante
Takeda Manufacturing Austria AG
Industriestrasse 67
1221 Viena, Áustria
Data da última atualização do folheto: ------------------------------------------------------------------------------------------------------------------------
Informações destinadas exclusivamente a profissionais de saúde:
Posologia e modo de administração
O tratamento deve ser conduzido sob supervisão de um médico com experiência no tratamento de doentes com deficiência de antitrombina.
Posologia
No caso de deficiência congénita de antitrombina, a dose deve ser individualizada para cada doente e levar em conta a história familiar de eventos tromboembólicos, fatores de risco atuais e resultados de exames laboratoriais.
A posologia e a duração da terapia de substituição na deficiência adquirida dependem do nível de antitrombina no plasma, da presença de sintomas de consumo aumentado, da causa da perturbação e da gravidade do estado clínico do doente. Em cada caso, a dose e a frequência de administração devem ser determinadas com base nos resultados laboratoriais e na avaliação do estado clínico do doente e da resposta ao tratamento.
A quantidade de unidades de antitrombina é expressa em unidades internacionais (UI), que se referem ao padrão atual da OMS para antitrombina. A atividade da antitrombina no plasma é expressa em percentagem (em relação ao plasma humano normal) ou em unidades internacionais (em relação ao Padrão Internacional de antitrombina no plasma).
A atividade de uma unidade internacional (UI) de antitrombina corresponde à quantidade de antitrombina contida em 1 ml de plasma humano normal. O cálculo da dose necessária de antitrombina baseia-se nos dados empíricos de que a administração de 1 UI de antitrombina por quilograma de peso corporal aumenta a atividade da antitrombina no plasma em aproximadamente 2%.
A dose inicial é calculada de acordo com a seguinte fórmula:
Quantidade necessária = peso corporal (kg) x (Nível objetivo - atividade atual de antitrombina [%]) x 0,5
O nível objetivo de atividade da antitrombina no plasma depende da avaliação do estado clínico do doente.
Após a determinação da indicação para a substituição da antitrombina, uma dose única deve garantir o alcance do nível objetivo de atividade da antitrombina no plasma e, subsequentemente, manter esse nível.
A dose administrada deve ser determinada e controlada com base nas medições da atividade da antitrombina, que devem ser realizadas pelo menos duas vezes ao dia até que o estado do doente se estabilize e, subsequentemente, uma vez ao dia, preferencialmente pouco antes da próxima infusão. A correção da dose deve levar em conta tanto o consumo aumentado de antitrombina quanto os resultados laboratoriais e os sintomas clínicos. Durante o tratamento, a atividade da antitrombina deve ser mantida acima de 80%, a menos que as condições clínicas exijam um nível diferente.
A dose média inicial na deficiência congénita é de 30-50 UI/kg de peso corporal.
Posteriormente, a dose e a frequência de administração, bem como a duração do tratamento, devem ser adaptadas com base nos resultados laboratoriais e no estado clínico do doente.
Crianças e adolescentes
A segurança e eficácia de Antithrombin III NF Takeda não foram estabelecidas em crianças com menos de 6 anos. Portanto, não se recomenda a administração deste medicamento nesta faixa etária.
Modo de administração
Administrar por via intravenosa. A velocidade máxima de infusão é de 5 ml/min.
Precauções especiais para a eliminação e preparação do medicamento para administração
Antithrombin III NF Takeda deve ser reconstituído imediatamente antes da administração, pois o produto não contém conservantes.
Deve usar-se apenas o conjunto de infusão fornecido. Durante a preparação da solução, devem ser utilizadas técnicas assépticas. A solução preparada deve ser utilizada imediatamente após a preparação.
Antes da administração, deve verificar-se se o medicamento reconstituído não contém partículas insolúveis e se não sofreu alteração de cor. A solução deve ser clara ou ligeiramente opalescente. Não deve ser administrada soluções turvas ou que contenham depósitos.
Não armazenar na geladeira após a reconstituição.
Preparação da solução:
- 1. Levar o frasco fechado contendo o solvente (água para injeção) à temperatura ambiente (máx. 37°C).
- 2. Retirar as cápsulas protetoras dos frascos contendo o pó e o solvente (fig. A) e desinfetar as rolhas de borracha dos dois frascos.
- 3. Retirar a tampa protetora de uma das extremidades da agulha de transferência, girando e puxando (fig. B). Introduzir a extremidade exposta da agulha no batoque de borracha do frasco contendo o solvente (fig. C).
- 4. Retirar a tampa protetora da outra extremidade da agulha de transferência, tendo o cuidado de não tocar na parte exposta.
- 5. Inverter o frasco contendo o solvente e introduzir a extremidade livre da agulha de transferência no batoque do frasco contendo o pó (fig. D). O solvente será aspirado para o frasco contendo o pó por sucção.
- 6. Separar os dois frascos, retirando a agulha do frasco contendo o pó (fig. E). Agitar suavemente o frasco para acelerar a dissolução.
- 7. Após a dissolução completa do pó, introduzir a agulha de ventilação fornecida (fig. F) e a espuma formada desaparecerá. Retirar a agulha de ventilação.
Administração:
- 8. Retirar a cobertura da agulha com filtro fornecida, girando e puxando, e colocá-la na seringa estéril de uso único. Aspirar a solução para a seringa (fig. G).
- 9. Desconectar a agulha com filtro da seringa e, após colocar a agulha de uso único (ou o conjunto de infusão fornecido), administrar a solução por via intravenosa, lentamente (velocidade máxima de administração: 5 ml/min).
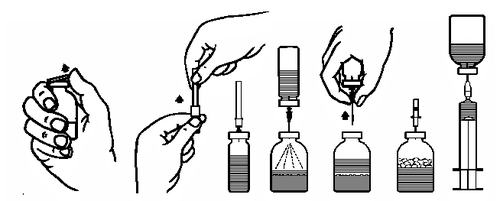
fig. A fig. B
fig. C fig. D
fig. E fig. F fig. G
Qualquer resíduo não utilizado do medicamento ou resíduos deve ser eliminado de acordo com as regulamentações locais.
Incompatibilidades farmacêuticas
O medicamento não deve ser misturado com outros medicamentos.
Precauções e advertências especiais para a administração
Como no caso de outros medicamentos que contenham proteínas administrados por infusão intravenosa, a administração de Antithrombin III NF Takeda pode causar reações de hipersensibilidade do tipo alérgico.
A hipersensibilidade e as reações anafiláticas foram relatadas após a comercialização do produto Antithrombin III NF Takeda. Em alguns casos, podem evoluir para reação anafilática grave (incluindo choque anafilático).
Durante a infusão, os doentes devem ser monitorizados de perto e observados atentamente para detectar qualquer sinal de efeitos secundários. Deve informar o doente sobre os primeiros sintomas de reação de hipersensibilidade, como: erupção cutânea pruriginosa, urticária generalizada, sensação de opressão no peito, respiração sibilante, hipotensão e choque anafilático. Se esses sintomas ocorrerem após a administração do medicamento, o doente deve contactar o médico assistente.
Em caso de choque, deve ser administrado tratamento padrão.
Takeda é uma marca registada da Takeda Pharmaceutical Company Limited.
- País de registo
- Substância ativa
- Requer receita médicaNão
- Fabricante
- ImportadorTakeda Manufacturing Austria AG
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a Antithrombin Iii Nf TakedaForma farmacêutica: Pó, 500 UISubstância ativa: antithrombin IIIFabricante: Instituto Grifols S.A.Não requer receita médicaForma farmacêutica: Pó, 1000 UISubstância ativa: antithrombin IIIFabricante: Instituto Grifols S.A.Não requer receita médicaForma farmacêutica: Pó, 50 UI/mlSubstância ativa: antithrombin IIIFabricante: Takeda Manufacturing Austria AGNão requer receita médica
Alternativas a Antithrombin Iii Nf Takeda noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a Antithrombin Iii Nf Takeda em Украина
Alternativa a Antithrombin Iii Nf Takeda em Испания
Médicos online para Antithrombin Iii Nf Takeda
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de Antithrombin Iii Nf Takeda – sujeita a avaliação médica e regras locais.














