ZARZIO 30 MU/0,5 ml SOL. INY. O PARA PERFUSION EN JERINGA PRECARGADA


Cómo usar ZARZIO 30 MU/0,5 ml SOL. INY. O PARA PERFUSION EN JERINGA PRECARGADA
Traducción generada por IA
Este contenido ha sido traducido automáticamente y se ofrece solo con fines informativos. No sustituye la consulta con un profesional sanitario.
Ver originalContenido del prospecto
Introducción
Prospecto: información para el usuario
Zarzio30MU/0,5ml solución inyectable o para perfusión en jeringa precargadaZarzio48MU/0,5ml solución inyectable o para perfusión en jeringa precargada
filgrastim
Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene información importante para usted.
- Conserve este prospecto, ya que puede tener que volver a leerlo.
- Si tiene alguna duda, consulte a su médico, farmacéutico o enfermero.
- Este medicamento se le ha recetado solamente a usted, y no debe dárselo a otras personas aunque tengan los mismos síntomas que usted, ya que puede perjudicarles.
- Si experimenta efectos adversos, consulte a su médico, farmacéutico o enfermero, incluso si se trata de efectos adversos que no aparecen en este prospecto. Ver sección 4.
Contenido del prospecto
- Qué es Zarzio y para qué se utiliza
- Qué necesita saber antes de empezar a usar Zarzio
- Cómo usar Zarzio
- Posibles efectos adversos
- Conservación de Zarzio
- Contenido del envase e información adicional
- Instrucciones de uso
1. Qué es Zarzio y para qué se utiliza
Zarzio es un factor de crecimiento de los glóbulos blancos (factor estimulante de las colonias de granulocitos) y pertenece a un grupo de medicamentos denominados citocinas. Los factores de crecimiento son proteínas que se producen de manera natural en el organismo pero también se pueden elaborar mediante biotecnología para su uso como medicamentos. Zarzio actúa haciendo que la médula ósea produzca más glóbulos blancos.
Una reducción del número de glóbulos blancos (neutropenia) se puede producir por motivos diversos y hace que su cuerpo tenga menos posibilidades de luchar contra las infecciones. Zarzio estimula la médula ósea para producir rápidamente nuevos glóbulos blancos.
Zarzio se puede utilizar:
- para aumentar el número de glóbulos blancos tras el tratamiento con quimioterapia para ayudar a prevenir infecciones;
- para aumentar el número de glóbulos blancos tras un trasplante de médula ósea para ayudar a prevenir infecciones;
- antes de someterse a quimioterapia de altas dosis para que la médula ósea produzca más células madre que se pueden recoger y que se le pueden devolver al organismo después del tratamiento. Éstas se pueden extraer de usted mismo o de un donante. Las células madre regresarán después a la médula ósea y producirán células sanguíneas;
- para aumentar el número de glóbulos blancos si padece neutropenia crónica grave para ayudarle a prevenir infecciones;
- en pacientes con infección VIH avanzada para ayudar a reducir el riesgo de infecciones.
2. Qué necesita saber antes de empezar a usar Zarzio
No use Zarzio
- si es alérgico al filgrastim o a alguno de los demás componentes de este medicamento (incluidos en la sección 6).
Advertencias y precauciones
Consulte a su médico, farmacéutico o enfermero antes de empezar a usar Zarzio.
Informe a su médico antes de iniciar el tratamiento si tiene:
- osteoporosis (enfermedad de los huesos);
- anemia de células falciformes ya que Zarzio puede provocar crisis de células falciformes.
Informe a su médico inmediatamente durante el tratamiento con Zarzio, si:
- siente dolor en la parte superior izquierda del abdomen, dolor en el lado izquierdo inferior de la caja torácica o dolor en el extremo del hombro izquierdo [estos pueden ser síntomas de un aumento de tamaño del bazo (esplenomegalia) o de una posible ruptura del mismo].
- tiene sangrados o hematomas (moratones) inusuales [estos pueden ser síntomas de una disminución de las plaquetas sanguíneas (trombocitopenia), con la consiguiente reducción de la capacidad de la sangre para formar coágulos].
- presenta signos repentinos de alergia, como erupción, picazón o habones urticariales en la piel, hinchazón de la cara, los labios, la lengua u otras partes del cuerpo, respiración difícil, sonido silbante que se produce al respirar (sibilancia) o dificultad para respirar, ya que podrían ser signos de una reacción alérgica grave (hipersensibilidad).
- presenta hinchazón en la cara o en los tobillos, sangre en la orina o si su orina es de color marrón o si advierte que orina menos de lo habitual (glomerulonefritis).
- presenta síntomas de inflamación de la aorta (el vaso sanguíneo grande que transporta sangre desde el corazón hasta el resto del cuerpo); esto se ha notificado en casos raros en pacientes con cáncer y donantes sanos. Los síntomas pueden incluir fiebre, dolor abdominal, malestar general, dolor de espalda y marcadores inflamatorios aumentados. Informe a su médico si presenta estos síntomas.
Pérdida de respuesta a filgrastim
Si sufre pérdida de respuesta al tratamiento con filgrastim o ésta no se mantiene, su médico estudiará los motivos, por ejemplo, si ha producido anticuerpos que neutralizan la actividad de filgrastim.
Es posible que su médico desee vigilarle atentamente; ver sección 4 del prospecto.
Si es usted un paciente con neutropenia crónica grave, puede tener riesgo de desarrollar un cáncer de la sangre (leucemia, síndrome mielodisplásico [SMD]). Debe consultar con su médico sobre su riesgo de desarrollar cáncer de sangre y qué pruebas se deben hacer. Si desarrolla o es probable que desarrolle cáncer de sangre, no debe usar Zarzio a menos que se lo indique su médico.
Si es donante de células madre, debe usted tener entre 16 y 60 años de edad.
Tenga especial cuidado con otros productos que estimulan los glóbulos blancos.
Zarzio pertenece a un grupo de medicamentos que estimulan la producción de glóbulos blancos. El profesional sanitario que le atienda siempre debe registrar en su historial el producto exacto que está usando.
Otros medicamentos y Zarzio
Informe a su médico o farmacéutico si está tomando, ha tomado recientemente o pudiera tener que tomar cualquier otro medicamento.
Embarazo, lactancia y fertilidad
Zarzio no se ha probado en mujeres embarazadas o en periodo de lactancia.
No se recomienda utilizar Zarzio durante el embarazo.
Es importante que informe a su médico si:
- está embarazada o en periodo de lactancia,
- cree que puede estarlo o
- planea quedarse embarazada.
Si se queda embarazada durante el tratamiento con Zarzio, informe a su médico.
A menos que su médico le indique otra cosa, debe interrumpir la lactancia si usa Zarzio.
Conducción y uso de máquinas
La influencia de Zarzio sobre la capacidad para conducir y utilizar máquinas es pequeña. Este medicamento puede causar mareos. Es aconsejable esperar a ver cómo se siente después de usar Zarzio y antes de conducir o utilizar maquinaria.
Zarzio contiene sorbitol y sodio
Zarzio contiene sorbitol (E 420).
El sorbitol es una fuente de fructosa. Si usted (o su hijo) padecen intolerancia hereditaria a la fructosa (IHF), una enfermedad genética rara, no deben recibir este medicamento. Los pacientes con IHF no pueden descomponer la fructosa, lo que puede provocar efectos adversos graves.
Consulte con su médico antes de recibir este medicamento si usted (o su hijo) padecen IHF o no pueden tomar alimentos o bebidas dulces porque les produce mareos, vómitos o efectos desagradables como hinchazón, calambres en el estómago o diarrea.
Este medicamento contiene menos 1 mmol de sodio (23 mg) por unidad de dosis volumen; esto es, esencialmente “exento de sodio”.
3. Cómo usar Zarzio
Siga exactamente las instrucciones de administración de este medicamento indicadas por su médico. En caso de duda, consulte de nuevo a su médico, enfermero o farmacéutico.
¿Cómo se administra Zarzio y qué cantidad debo usar?
Zarzio se administra habitualmente como una inyección diaria en el tejido situado justo debajo de la piel (es lo que se llama una inyección subcutánea). También se puede administrar como una inyección diaria lenta en la vena (lo que se conoce como perfusión intravenosa). La dosis habitual varía en función de su enfermedad y peso. Su médico le indicará la cantidad de Zarzio que debe usar.
Pacientes a los que se realiza un trasplante de médula ósea después de la quimioterapia:
Generalmente recibirá la primera dosis de Zarzio al menos 24 horas después de la quimioterapia y al menos 24 horas después de la realización del trasplante de médula ósea.
Usted, o las personas que lo cuidan, pueden recibir formación sobre cómo administrar inyecciones subcutáneas para que pueda continuar el tratamiento en su domicilio. No obstante, no debe intentarlo hasta que un profesional sanitario le haya enseñado primero correctamente cómo hacerlo.
¿Durante cuánto tiempo deberé usar Zarzio?
Deberá usar Zarzio hasta que su recuento de glóbulos blancos sea normal. Se le harán análisis de sangre periódicos para controlar el número de glóbulos blancos de su cuerpo. Su médico le indicará durante cuánto tiempo necesitará utilizar Zarzio.
Uso en niños
Zarzio se utiliza para tratar a niños que reciben quimioterapia o que tienen un recuento de glóbulos blancos muy bajo (neutropenia). La dosis para niños que reciben quimioterapia es igual que para adultos.
Administración de dosis pequeñas
No debe inyectar una dosis inferior a 0,3 ml con la jeringa precargada, ya que no se puede medir con precisión debido a que las marcas de graduación de 0,1 y 0,2 ml no son visibles.
Si fuera necesario, la solución inyectable se puede diluir.
Si usa más Zarzio del que debe
No aumente la dosis que su médico le ha indicado. Si cree que se ha inyectado más del que debe, contacte con su médico lo antes posible.
Si olvidó usar Zarzio
Si olvidó una inyección, o la cantidad inyectada es demasiado pequeña, contacte con su médico lo antes posible. No use una dosis doble para compensar las dosis olvidadas.
Si tiene cualquier otra duda sobre el uso de este medicamento, pregunte a su médico, farmacéutico o enfermero.
4. Posibles efectos adversos
Al igual que todos los medicamentos, este medicamento puede producir efectos adversos, aunque no todas las personas los sufran.
Informe a su médico inmediatamentedurante el tratamiento:
- si tiene una reacción alérgica que incluye debilidad, disminución de la presión arterial, dificultad respiratoria, hinchazón de la cara (anafilaxia), erupción cutánea, erupción con picor (urticaria), hinchazón de la cara, los labios, la lengua o la garganta (angioedema) y dificultad para respirar (disnea).
- si tiene tos, fiebre y dificultades respiratorias (disnea), ya que podrían ser signos de un síndrome de distrés respiratorio agudo (SDRA).
- si tiene dolor en la parte superior izquierda del abdomen, dolor en el lado izquierdo inferior de la caja torácica o dolor en el extremo del hombro, ya que podría haber algún problema en el bazo [aumento del tamaño del bazo (esplenomegalia)] o ruptura del bazo].
- si está en tratamiento para la neutropenia crónica grave y tiene sangre en la orina (hematuria). Su médico puede realizarle análisis de orina regularmente en el caso de que presente este efecto adverso o en el caso de tener proteínas en la orina (proteinuria).
- si experimenta alguno o una combinación de los siguientes efectos adversos:
- inflamación o hinchazón, que puede estar asociado con orinar con una menor frecuencia, dificultad para respirar, hinchazón y sensación de plenitud en abdomen y una sensación general de cansancio. Estos síntomas generalmente se desarrollan muy rápidamente.
Estos pueden ser síntomas de una enfermedad llamada “síndrome de fuga capilar” y que puede causar que la sangre se escape de los vasos sanguíneos pequeños hacia otros lugares de su cuerpo y necesite atención médica urgente.
- si experimenta una combinación de alguno de los siguientes síntomas:
- fiebre, o escalofríos, o si siente mucho frío, frecuencia cardíaca alta, confusión o desorientación, dificultad para respirar, dolor fuerte o molestias y piel sudorosa o húmeda.
Estos pueden ser síntomas de una enfermedad llamada “sepsis” (o "septicemia"), una infección grave en la que se produce una respuesta inflamatoria de todo el organismo que puede poner en peligro la vida y que necesita atención médica urgente.
- si experimenta lesión renal (glomerulonefritis). Se ha observado lesión renal en pacientes tratados con filgrastim. Llame inmediatamente a su médico si presenta hinchazón en la cara o en los tobillos, sangre en la orina o si su orina es de color marrón o si advierte que orina menos de lo habitual.
Un efecto adverso frecuente de filgrastim es dolor en los músculos o en los huesos (dolor musculoesquelético), que se puede aliviar tomando analgésicos comunes. Los pacientes que se someten a un trasplante de células madre o de médula ósea, pueden padecer la enfermedad de injerto contra el huésped (EICH). Ésta es una reacción de las células del donante contra el paciente que recibe el trasplante, cuyos signos y síntomas incluyen erupción en las palmas de las manos o plantas de los pies y úlceras y llagas en la boca, intestino, hígado, piel, o en los ojos, pulmones, vagina y articulaciones. En donantes de células madre sanos se observa muy frecuentemente un aumento en los glóbulos blancos de la sangre (leucocitosis) y una disminución de las plaquetas reduciéndose la capacidad de coagulación de la sangre (trombocitopenia), ambos serán vigilados por su médico.
Efectos adversos muy frecuentes(pueden afectar a más de 1 de cada 10 personas)
- disminución de las plaquetas, reduciéndose la capacidad de coagulación de la sangre (trombocitopenia)
- recuento bajo de glóbulos rojos (anemia)
- dolor de cabeza
- diarrea
- vómitos
- náuseas
- debilitamiento o pérdida de cabello inusual (alopecia)
- cansancio (fatiga)
- irritación e hinchazón de la mucosa digestiva que va de la boca al ano (inflamación de la mucosa)
- fiebre (pirexia)
Efectos adversos frecuentes(pueden afectar hasta 1 de cada 10 personas)
- inflamación de los pulmones (bronquitis)
- infección del tracto respiratorio superior
- infección urinaria
- disminución del apetito
- problemas para dormir (insomnio)
- mareo
- pérdida de sensibilidad, especialmente en la piel (hipoestesia)
- hormigueo o entumecimiento de las manos o los pies (parestesia)
- tensión arterial baja (hipotensión)
- tensión arterial alta (hipertensión)
- tos
- tos con sangre (hemoptisis)
- dolor en la boca y garganta (dolor orofaríngeo)
- hemorragia nasal (epistaxis)
- estreñimiento
- dolor bucal
- aumento de tamaño del hígado (hepatomegalia)
- erupción
- enrojecimiento de la piel (eritema)
- espasmos musculares
- dolor al orinar (disuria)
- dolor en el pecho
- dolor
- debilidad generalizada (astenia)
- malestar general
- hinchazón de las manos y los pies (edema periférico)
- aumento de algunas enzimas de la sangre
- cambios en los parámetros bioquímicos de la sangre
- reacción transfusional
Efectos adversos poco frecuentes(pueden afectar hasta 1 de cada 100 personas)
- aumento de los glóbulos blancos (leucocitosis)
- reacción alérgica (hipersensibilidad)
- rechazo de la médula ósea trasplantada (enfermedad del injerto contra el huésped)
- altas concentraciones de ácido úrico en sangre, lo cual puede causar gota (hiperuricemia) [elevación del ácido úrico en sangre]
- lesión hepática causada por la obstrucción de las venas pequeñas del hígado (enfermedad venooclusiva)
- funcionamiento anormal de los pulmones, causando falta de aliento (insuficiencia respiratoria)
- hinchazón o líquido en los pulmones (edema pulmonar)
- inflamación de los pulmones (enfermedad pulmonar intersticial)
- anomalías radiológicas de los pulmones (infiltración pulmonar)
- sangrado del pulmón (hemorragia pulmonar)
- falta de absorción de oxígeno en los pulmones (hipoxia)
- exantema irregular (exantema maculopapuloso)
- enfermedad que produce una disminución de la densidad de los huesos, lo que los hace más débiles, más frágiles y más propensos a romperse (osteoporosis)
- reacción en el lugar de la inyección
Efectos adversos raros(pueden afectar hasta 1 de cada 1.000 personas):
- dolor intenso en los huesos, el pecho, el intestino o las articulaciones (anemia de células falciformes con crisis)
- reacción alérgica repentina potencialmente mortal (reacción anafiláctica)
- dolor e hinchazón de las articulaciones, similar a la gota (pseudogota)
- un cambio en la forma que el cuerpo regula los líquidos corporales que puede causar hinchazón (alteraciones del volumen de líquidos)
- inflamación de los vasos sanguíneos de la piel (vasculitis cutánea)
- úlceras dolorosas de color rojo oscuro con halo inflamatorio en las extremidades y, a veces, la cara y el cuello que cursan con fiebre (síndrome de Sweet)
- empeoramiento de la artritis reumatoide
- cambio anormal en la orina
- reducción de la densidad ósea
- inflamación de la aorta (el vaso sanguíneo grande que transporta sangre desde el corazón hasta el resto del cuerpo), ver sección 2
- formación de células sanguíneas fuera de la médula ósea (hematopoyesis extramedular)
Comunicación de efectos adversos
Si experimenta cualquier tipo de efecto adverso, consulte a su médico, farmacéutico o enfermero, incluso si se trata de posibles efectos adversos que no aparecen en este prospecto. También puede comunicarlos directamente a través del sistema nacional de notificación incluido en el Apéndice V. Mediante la comunicación de efectos adversos usted puede contribuir a proporcionar más información sobre la seguridad de este medicamento.
5. Conservación de Zarzio
Mantener este medicamento fuera de la vista y del alcance de los niños.
No utilice este medicamento después de la fecha de caducidad que aparece en la caja y en la etiqueta de la jeringa después de CAD y EXP, respectivamente. La fecha de caducidad es el último día del mes que se indica.
Conservar en nevera (entre 2 °C y 8 °C).
Conservar la jeringa precargada en el embalaje exterior para protegerla de la luz.
La congelación accidental no provocará daños en Zarzio.
La jeringa puede sacarse de la nevera y dejarse a temperatura ambiente durante un periodo único de hasta 8 días (pero a una temperatura no superior a 25 ºC). Después de este periodo, el producto no se debe volver a refrigerar y se debe desechar.
No utilice este medicamento si observa decoloración, turbidez o partículas; debe ser un líquido transparente, entre incoloro y ligeramente amarillento.
Los medicamentos no se deben tirar por los desagües ni a la basura. Pregunte a su farmacéutico cómo deshacerse de los envases y de los medicamentos que ya no necesita. De esta forma, ayudará a proteger el medio ambiente.
6. Contenido del envase e información adicional
Composición de Zarzio
- El principio activo es filgrastim.
Zarzio 30 MU/0,5 ml solución inyectable o para perfusión en jeringa precargada: cada jeringa precargada contiene 30 MU de filgrastim en 0,5 ml, que corresponden a 60 MU/ml.
Zarzio 48 MU/0,5 ml solución inyectable o para perfusión en jeringa precargada: cada jeringa precargada contiene 48 MU de filgrastim en 0,5 ml, que corresponden a 96 MU/ml.
- Los demás componentes son ácido glutámico, sorbitol (E 420), polisorbato 80 , hidróxido de sodio y agua para preparaciones inyectables. Ver sección 2 “Zarzio contiene sorbitol y sodio”.
Aspecto del producto y contenido del envase
Zarzio es una solución inyectable o para perfusión transparente y de aspecto incoloro a ligeramente amarillento, que se suministra en jeringa precargada que contiene 0.5 ml de solución.
Zarzio se encuentra disponible en envases de 1, 3, 5 o 10 jeringas precargadas de vidrio (vidrio tipo I) con un tope del émbolo (goma bromobutílica), una aguja de acero inoxidable de calibre 29 con protector automático de la aguja y un capuchón de la aguja (elastómero termoplástico).
La jeringa precargada lleva impresas marcas desde 0,1 ml a 1 ml; no obstante, no está diseñada para medir volúmenes inferiores a 0,3 ml debido al mecanismo de resorte.
Puede que solamente estén comercializados algunos tamaños de envases.
Titular de la autorización de comercialización
Sandoz GmbH
Biochemiestr. 10
6250 Kundl
Austria
Responsable de la fabricación
Sandoz GmbH
Biochemiestr. 10
6336 Langkampfen
Austria
Novartis Pharmaceutical Manufacturing GmbH
Biochemiestrasse 10
6336 Langkampfen
Austria
Pueden solicitar más información respecto a este medicamento dirigiéndose al representante local del titular de la autorización de comercialización:
België/Belgique/Belgien Sandoz nv/sa Tél/Tel: +32 2 722 97 97 | Lietuva Sandoz Pharmaceuticals d.d filialas Tel: +370 5 2636 037 |
| Luxembourg/Luxemburg Sandoz nv/sa (Belgique/Belgien) Tél/Tel.: +32 2 722 97 97 |
Ceská republika Sandoz s.r.o. Tel: +420 234 142 222 | Magyarország Sandoz Hungária Kft. Tel.: +36 1 430 2890 |
Danmark/Norge/Ísland/Sverige Sandoz A/S Tlf/Sími/Tel: +45 63 95 10 00 | Malta Sandoz Pharmaceuticals d.d. Tel: +35699644126 |
Deutschland Hexal AG Tel: +49 8024 908 0 | Nederland Sandoz B.V. Tel: +31 36 52 41 600 |
Eesti Sandoz d.d. Eesti filiaal Tel: +372 665 2400 | Österreich Sandoz GmbH Tel: +43 5338 2000 |
Ελλáδα SANDOZ HELLAS ΜΟΝΟΠΡΟΣΩΠΗ Α.Ε. Τηλ: +30 216 600 5000 | Polska Sandoz Polska Sp. z o.o. Tel.: +48 22 209 70 00 |
España Sandoz Farmacéutica, S.A. Tel: +34 900 456 856 | Portugal Sandoz Farmacêutica Lda. Tel: +351 21 000 86 00 |
France Sandoz SAS Tél: +33 1 49 64 48 00 | România Sandoz Pharmaceuticals SRL Tel: +40 264 50 15 00 |
Hrvatska Sandoz d.o.o. Tel: +385 1 23 53 111 | Slovenija Sandoz farmacevtska družba d.d. Tel: +386 1 580 29 02 |
Ireland Rowex Ltd. Tel: + 353 27 50077 | Slovenská republika Sandoz d.d. - organizacná zložka Tel: +421 2 48 20 0600 |
Italia Sandoz S.p.A. Tel: +39 02 96541 | Suomi/Finland Sandoz A/S Puh/Tel: +358 10 6133 400 |
Κúπρος SANDOZ HELLAS ΜΟΝΟΠΡΟΣΩΠΗ Α.Ε. Τηλ: +30 216 600 5000 | United Kingdom (Northern Ireland) Sandoz GmbH (Austria) Tel: +43 5338 2000 |
Latvija Sandoz d.d. Latvia filiale Tel: +371 67 892 006 |
Fecha de la última revisión de este prospecto: {MM/AAAA}
La información detallada de este medicamento está disponible en la página web de la Agencia Europea de Medicamentos: http://www.ema.europa.eu/.
-------------------------------------------------------------------------------------------------------------------------
- Instrucciones de uso
Siga estas instrucciones como ayuda para evitar una posible infección.
Es importante que no intente administrarse la inyección o ponérsela a otra persona sin que antes su médico, profesional de enfermería o farmacéutico le haya explicado cómo hacerlo. Lea todas las instrucciones antes de administrar una inyección. Cada blíster sellado contiene una única jeringa precargada.
Cada jeringa precargada contiene 30 MU/0,5 ml o 48 MU/0,5 ml de filgrastim.
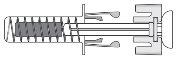
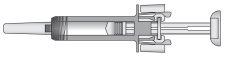
Figura 7-1 Jeringa precargada de Zarzio con protector de la aguja
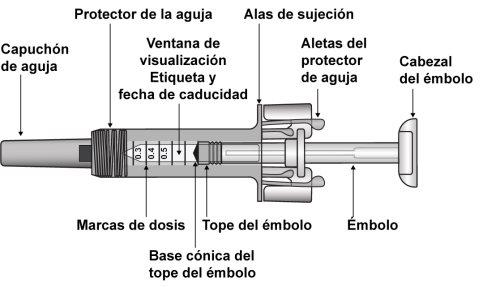
Después de que se haya inyectado la medicación, el protector de la aguja se activará para cubrir la aguja. El protector de la aguja está diseñado para proteger a los profesionales sanitarios, cuidadores y pacientes de lesiones debido a pinchazos accidentales con la aguja después de la inyección.
Material adicional necesario para la inyección:
gasa
objetos punzantes
|
|
Información importante sobre seguridad
Precaución: Mantener la jeringa precargada fuera del alcance de los niños.
- No abra la caja exterior hasta que esté preparado para utilizar la jeringa precargada.
- No utilice la jeringa precargada si el sello del blíster está roto, ya que usarla podría no ser seguro para usted.
- No utilice la jeringa precargada si hay líquido en la bandeja de plástico. No utilice la jeringa precargada si falta el capuchón de la aguja o no está bien colocado. En todos estos casos, devuelva el envase completo del producto a la farmacia.
- No intente inyectar una dosis inferior a 0,3 ml con una jeringa precargada. No se puede medir con exactitud una dosis inferior a 0,3 ml con la jeringa precargada de Zarzio, ya que las marcas de graduación de 0,1 y 0,2 ml no son visibles en el cilindro de la jeringa.
- No deje nunca la jeringa precargada desatendida donde otras personas puedan manipularla.
- Noagite la jeringa precargada.
- Tenga cuidado de no tocar las aletas del protector de la aguja antes de su uso. Si se tocan las aletas, el protector de la aguja puede activarse antes de tiempo.
- No retire el capuchón de la aguja hasta justo antes de administrar la inyección.
- La jeringa precargada no se puede reutilizar. Deseche inmediatamente la jeringa precargada utilizada.
- No utilice la jeringa si se ha caído sobre una superficie dura o después de retirar el capuchón de la aguja.
Conservación de la jeringa precargada de Zarzio
- Conserve la jeringa precargada en su caja exterior para protegerlo de la luz. Consérvela en la nevera entre 2 °C y 8 °C (36 °F y 46 °F). Nocongelar.
- Recuerde sacar el blíster de la nevera y dejar que se atempere durante 15-30 minutos para que alcance la temperatura ambiente antes de preparar la jeringa para la inyección.
- No utilice la jeringa precargada después de la fecha de caducidad que aparece en la caja exterior o en la etiqueta de la jeringa. Si ha caducado, devuelva el envase completo a la farmacia.
- La jeringa se puede sacar de la nevera y dejar a temperatura ambiente durante un único periodo de 8 días como máximo (pero no por encima de 25 °C). Al final de este periodo, el producto no se podrá volver a meter en la nevera y se debe desechar.
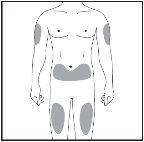
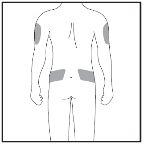
Lugar de la inyección
Figura7-3Lugares de la inyección
| El lugar de la inyección es el lugar del cuerpo en el que va a usar la jeringa precargada.
|
|
|
Preparación de la jeringa precargada de Zarzio para su uso
- Saque de la nevera el blíster que contiene la jeringa precargada y déjelo sin abrirdurante aproximadamente 15-30 minutos para que pueda alcanzar la temperatura ambiente.
- Cuando esté listo para usar la jeringa precargada, abra el blíster y lávese bien las manos con agua y jabón.
- Limpie el sitio de inyección con un hisopo con alcohol.
- Saque la jeringa precargada del blíster sosteniéndola por la parte central, como se muestra en la figura 7-4. No agarre el vástago del émbolo ni el capuchón de la aguja.
Figura7-4Retire la jeringa precargada del blíster
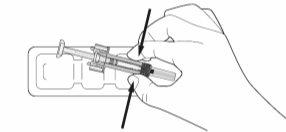
- Compruebe que el protector transparente de plástico de la aguja está situado sobre el cilindro de la jeringa de vidrio. Si el protector transparente de la aguja está cubriendo el capuchón de la aguja (como se muestra en la figura 7-5), la jeringa se habrá activado; NO utilice esta jeringa y tome una nueva. En la figura 7-6 se muestra una jeringa lista para usar.
Figura7-5NO UTILICE
| En esta configuración, el protector de la aguja está ACTIVADO: NO UTILICE la jeringa precargada |
Figura7-6Lista para usar
| En esta configuración, el protector de la aguja NO ESTÁ ACTIVADO y la jeringa está lista para usar. |
- Inspeccione la jeringa precargada. El líquido debe ser transparente. El color puede ser de incoloro a ligeramente amarillento. NO UTILICE la jeringa precargada si observa partículas o cambios de color; devuelva a la farmacia la jeringa precargada y el envase en el que viene.
- NO UTILICE la jeringa precargada si está rota o se ha activado el protector de la aguja. En todos estos casos, devuelva el envase completo del producto a la farmacia.
Cómo utilizar la jeringa precargada
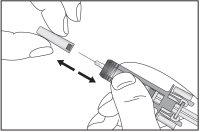
Figura7-7Retire el capuchón de la aguja
| Tire con cuidado del capuchón de la aguja para retirarlo de la jeringa precargada. Deseche el capuchón. Es posible que vea una gota de líquido en el extremo de la aguja. Esto es normal. |
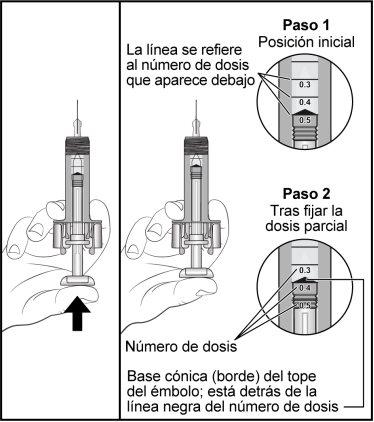
Sujete la jeringa como se muestra en la figura, presione lentamente el émbolo para expulsar el medicamento sobrante hasta que el borde de la base cónica del tope del émbolo quede alineado con la marca de la jeringa correspondiente a la dosis prescrita. El siguiente ejemplo es para una dosis de 0,4 ml. Tenga cuidado de no tocar las aletas del protector de la aguja antes de usarla. El protector de la aguja puede activarse antes de tiempo. Compruebe de nuevo que la jeringa precargada tiene la dosis correcta de Zarzio. Llame al médico o profesional de enfermería si tiene problemas para medir o inyectar la dosis de Zarzio. | |
Figura7-8Ejemplo particular para una dosis de 0,4ml
| |
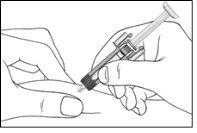
Figura7-9Inserte la aguja
| Pellizque suavemente la piel en el lugar de la inyección e inserte la aguja como se muestra en la figura. Empuje la aguja todo el recorrido para asegurarse de que se administra todo el medicamento. |
Figura7-10 Presione el émbolo
| Sujetando la jeringa precargada como se muestra, presione lentamenteel émbolo hasta que llegue al tope, de modo que el cabezal del émbolo quede completamente entre las aletas del protector de la aguja. Mantenga el émbolo completamente presionado mientras sostiene la jeringa en su lugar durante 5 segundos. |
Figura7-11 Retire la aguja
| Mantenga el émbolo completamente presionadomientras extrae con cuidado la aguja del lugar de la inyección. |
Figura7-12Suelte el émbolo
| Suelte el émbolo lentamente y deje que el protector de la aguja cubra automáticamente la aguja expuesta. Es posible que haya una pequeña cantidad de sangre en el lugar de la inyección. Puede hacer presión con una bola de algodón o una gasa sobre el lugar de la inyección durante 10 segundos. No frote el lugar de la inyección. Si es necesario, puede poner una tirita. |
Instrucciones de eliminación
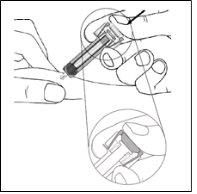
Figura7-13Eliminación
| Deseche la jeringa usada en un recipiente para objetos punzantes (recipiente con cierre, resistente a las perforaciones). Por su salud y seguridad, y la de otras personas, las agujas y las jeringas usadas nunca se debenreutilizar. |
-------------------------------------------------------------------------------------------------------------------------
Esta información está destinada únicamente a profesionales sanitarios:
La solución debe inspeccionarse visualmente antes del uso. Tan sólo se deben utilizar soluciones transparentes sin partículas. La exposición accidental a temperaturas de congelación no afecta de forma adversa a la estabilidad de Zarzio.
Zarzio no contiene conservantes: en vista del posible riesgo de contaminación microbiológica, las jeringas de Zarzio son para un solo uso.
Dilución previa a la administración (opcional)
Zarzio se puede diluir, si es necesario, en una solución glucosa de 50 mg/ml (al 5%). Zarzio no debe diluirse con soluciones de cloruro sódico.
No se recomienda en ningún caso diluir a concentraciones finales < 0,2 MU/ml (2 microgramos/ml).
En los pacientes tratados con filgrastim diluido a concentraciones < 1,5 MU/ml (15 microgramos/ml), debe añadirse albúmina sérica humana (ASH) hasta una concentración final de 2 mg/ml.
Ejemplo: si el volumen de inyección final es de 20 ml y la dosis total de filgrastim inferior a 30 MU (300 microgramos), deben agregarse 0,2 ml de una solución de albúmina sérica humana de 200 mg/ml (al 20%) Ph. Eur.
Diluido en una solución glucosa de 50 mg/ml (al 5%), filgrastim es compatible con el vidrio y con diversos plásticos, incluidos el cloruro de polivinilo, la poliolefina (un copolímero de polipropileno y polietileno) y el polipropileno.
Tras la dilución: se ha demostrado que, durante el uso, la solución diluida para perfusión permanece fisicoquímicamente estable durante 24 horas a 2 – 8 °C. Desde el punto de vista microbiológico, el producto debe utilizarse inmediatamente. Si no se utiliza de forma inmediata, los tiempos de almacenamiento durante el uso y las condiciones previas al mismo son responsabilidad del usuario y normalmente no debe sobrepasar las 24 horas a 2 – 8 °C, a menos que la dilución se haya realizado en condiciones de asepsia validadas y controladas.
Uso de la jeringa precargada con protector de seguridad para la aguja
El protector de seguridad para la aguja cubre ésta tras haber realizado la inyección con el fin de prevenir pinchazos accidentales. Ello no afecta a la forma de utilizar la jeringa. Empujar el émbolo lenta y uniformemente hasta que se haya administrado la totalidad de la dosis y el émbolo no pueda seguir avanzando. Retirar la jeringa manteniendo la presión sobre el émbolo. El protector de seguridad para la aguja cubrirá ésta una vez que se suelte el émbolo.
Eliminación
La eliminación del medicamento no utilizado y de todos los materiales que hayan estado en contacto con él se realizará de acuerdo con la normativa local.
- País de registro
- Principio activo
- Requiere recetaSí
- Fabricante
- Esta información es de carácter general y no sustituye la consulta con un profesional sanitario.
- Alternativas a ZARZIO 30 MU/0,5 ml SOL. INY. O PARA PERFUSION EN JERINGA PRECARGADAForma farmacéutica: INYECTABLE, 12 MU/0,2 mlPrincipio activo: FilgrastimFabricante: Accord Healthcare S.L.U.Requiere recetaForma farmacéutica: INYECTABLE, 0,3 mg / jeringa precargadaPrincipio activo: FilgrastimFabricante: Accord Healthcare S.L.U.Requiere recetaForma farmacéutica: INYECTABLE, 0,3 mg / jeringa precargadaPrincipio activo: FilgrastimFabricante: Accord Healthcare S.L.U.Requiere receta
Médicos online para ZARZIO 30 MU/0,5 ml SOL. INY. O PARA PERFUSION EN JERINGA PRECARGADA
Comenta la dosis, los posibles efectos secundarios, interacciones, contraindicaciones o la revisión de receta de ZARZIO 30 MU/0,5 ml SOL. INY. O PARA PERFUSION EN JERINGA PRECARGADA, sujeto a valoración médica y a la normativa local.
Preguntas frecuentes