VABYSMO 120 MG/ML SOLUCION PARA INYECCION EN JERINGA PRECARGADA

Cómo usar VABYSMO 120 MG/ML SOLUCION PARA INYECCION EN JERINGA PRECARGADA
Traducción generada por IA
Este contenido ha sido traducido automáticamente y se ofrece solo con fines informativos. No sustituye la consulta con un profesional sanitario.
Ver originalContenido del prospecto
Introducción
Prospecto: información para el paciente
Vabysmo 120mg/ml solución inyectable en jeringa precargada
faricimab
Este medicamento está sujeto a seguimiento adicional, lo que agilizará la detección de nueva información sobre su seguridad. Puede contribuir comunicando los efectos adversos que pudiera usted tener. La parte final de la sección 4 incluye información sobre cómo comunicar estos efectos adversos.
Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene información importante para usted.
- Conserve este prospecto, ya que puede tener que volver a leerlo.
- Si tiene alguna duda, consulte a su médico.
- Si experimenta efectos adversos, consulte a su médico, incluso si se trata de efectos adversos que no aparecen en este prospecto. Ver sección 4.
Contenido del prospecto
- Qué es Vabysmo y para qué se utiliza
- Qué necesita saber antes de empezar a usar Vabysmo
- Cómo usar Vabysmo
- Posibles efectos adversos
- Conservación de Vabysmo
- Contenido del envase e información adicional
1. Qué es Vabysmo y para qué se utiliza
Qué es Vabysmo y para qué se utiliza
Vabysmo contiene el principio activo faricimab, que pertenece a un grupo de medicamentos llamados agentes antineovascularización.
Vabysmo se inyecta en el ojo por su médico para tratar trastornos oculares en adultos llamados:
- degeneración macular asociada a la edad neovascular (exudativa) (DMAEn),
- alteración en la visión debida al edema macular diabético (EMD).
- alteración en la visión debida a edema macular a causa de un bloqueo de las venas retinianas (oclusión de la rama venosa retiniana (ORVR) u oclusión de la vena central de la retina (OVCR)).
Estos trastornos afectan a la mácula, la parte central de la retina (la capa sensible a la luz en la parte de atrás del ojo) que es responsable de la visión fina y central. La DMAEn se produce por el crecimiento de vasos sanguíneos anormales que permiten el filtrado de sangre y fluido dentro de la mácula, y el EMD se produce por vasos sanguíneos agujereados que causan hinchazón de la mácula. La OVCR es el bloqueo del vaso sanguíneo principal (vena) que transporta la sangre desde la retina y la ORVR es el bloqueo de una de las ramas más pequeñas de la vena principal. Debido al aumento en la presión dentro de las venas, hay una fuga de fluido a la retina, lo que provoca hinchazón de la mácula (edema macular).
Cómo funciona Vabysmo
Vabysmo reconoce y bloquea específicamente la actividad de unas proteínas conocidas como angiopoyetina-2 y factor de crecimiento endotelial vascular A. Cuando estas proteínas están presentes a niveles superiores al normal, pueden causar el crecimiento de vasos sanguíneos anormales y/o daño en los vasos normales, con fuga dentro de la mácula, causando hinchazón o daño que puede afectar negativamente a la visión de la persona. Uniéndose a estas proteínas, Vabysmo puede bloquear sus acciones y prevenir el crecimiento anormal de los vasos, la fuga y la hinchazón. Vabysmo puede mejorar la enfermedad y/o enlentecer el empeoramiento de la enfermedad y de esta forma mantener, o incluso mejorar, su visión.
2. Qué necesita saber antes de empezar a usar Vabysmo
No use Vabysmo:
- si es alérgico a faricimab o a alguno de los demás componentes de este medicamento (incluidos en la sección 6).
- si tiene una infección activa o sospecha de ésta en el ojo o alrededor del mismo.
- si tiene dolor o enrojecimiento en el ojo (inflamación ocular).
Si se encuentra en alguna de estas situaciones, informe a su médico. No le deben administrar Vabysmo.
Advertencias y precauciones
Consulte a su médico antes de empezar a usar Vabysmo:
- si tiene glaucoma (una enfermedad del ojo generalmente causada por presión alta en el ojo).
- si tiene historia de ver destellos, luces o partículas flotantes (puntos flotantes negros) y si tiene un aumento repentino en el tamaño y el número de partículas flotantes.
- si ha sufrido cirugía ocular en las últimas 4 semanas o si la cirugía ocular está planeada para las próximas 4 semanas.
- si ha tenido alguna vez alguna enfermedad ocular o tratamiento ocular.
Consulte a su médico inmediatamente si:
- presenta pérdida repentina de la visión.
- presenta signos de una posible infección o inflamación ocular, como empeoramiento del enrojecimiento del ojo, dolor ocular, aumento del malestar ocular, visión borrosa o disminuida, un aumento del número de pequeñas partículas en la visión, sensibilidad incrementada a la luz.
Además, es importante que sepa que:
- la seguridad y eficacia de Vabysmo cuando se administra en ambos ojos a la vez no ha sido estudiada y usarlo de esta forma puede conllevar a un aumento del riesgo de experimentar efectos adversos.
- las inyecciones con Vabysmo pueden causar un aumento temporal en la presión del ojo (presión intraocular) en algunos pacientes dentro de los 60 minutos después de la inyección. Su médico vigilará esto después de cada inyección.
- Su médico comprobará si tiene otros factores de riesgo que puedan aumentar la posibilidad de desgarro o desprendimiento de una de las capas de la parte posterior del ojo (desprendimiento o desgarro de retina, y desprendimiento o desgarro del epitelio pigmentario de la retina), en cuyo caso Vabysmo se le administrará con precaución.
Cuando se administran algunos medicamentos que funcionan de forma similar a Vabysmo, se sabe que existe un riesgo de coágulos de sangre que bloquean los vasos sanguíneos (acontecimientos tromboembólicos arteriales), que pueden causar un ataque al corazón o un ictus. Dado que una pequeña cantidad del medicamento entra en la sangre, existe el riesgo teórico de estos episodios después de la inyección de Vabysmo dentro del ojo.
La experiencia es limitada en el tratamiento de:
- pacientes con infecciones activas.
- pacientes con DMAEn y pacientes con oclusión de la vena de la retina (OVR) de 85 años y mayores.
- pacientes con EMD debido a diabetes tipo I.
- diabéticos con valores medios de azúcar en sangre elevados (hemoglobina glicosilada superior al 10%).
- diabéticos con enfermedad ocular provocada por la diabetes, conocida como retinopatía diabética proliferativa.
- diabéticos con presión sanguínea alta, superior a 140/90 mmHg y enfermedad de vasos sanguíneos.
- pacientes con EMD que reciben inyecciones en intervalo inferior a 8 semanas durante un largo periodo de tiempo.
La experiencia es limitada en el tratamiento de pacientes que reciben inyecciones en intervalos inferiores a 8 semanas durante un largo periodo de tiempo y estos pacientes pueden tener un mayor riesgo de efectos adversos.
No hay experiencia en el tratamiento de:
- diabéticos o pacientes con OVR con alta presión sanguínea no controlada.
Si algo de lo anterior le sucede, su médico tendrá en cuenta esta falta de información en el momento de tratarle con Vabysmo.
Niños y adolescentes
No ha sido estudiado el uso de Vabysmo en niños y adolescentes porque la DMAEn, el EMD y OVR ocurren principalmente en adultos.
Otros medicamentos y Vabysmo
Informe a su médico si está utilizando, ha utilizado recientemente o pudiera tener que utilizar cualquier otro medicamento.
Embarazo ylactancia
Vabysmo no se ha estudiado en mujeres embarazadas. Vabysmo no debe usarse en el embarazo a no ser que el beneficio potencial para el paciente supere el riesgo potencial del niño no nacido.
Si está embarazada o en periodo de lactancia, cree que podría estar embarazada o tiene intención de quedarse embarazada, consulte a su médico antes de utilizar este medicamento.
No se recomienda la lactancia durante el tratamiento con Vabysmo porque se desconoce si Vabysmo se excreta en la leche humana.
Las mujeres que pudieran quedarse embarazadas deben usar un método anticonceptivo eficaz durante el tratamiento y durante al menos tres meses después de acabar tratamiento con Vabysmo. Si se queda embarazada o piensa que está embarazada durante el tratamiento, informe rápidamente a su médico.
Conducción y uso de máquinas
Después de la inyección de Vabysmo, puede sufrir problemas temporales de visión (por ejemplo, visión borrosa). No conduzca ni use máquinas mientras estos duren.
Vabysmo contiene sodio
Este medicamento contiene menos de 1 mmol de sodio (23 mg) por dosis, esto es, esencialmente “exento de sodio”.
Vabysmo contiene polisorbato
Este medicamento contiene 0,02 mg de polisorbato en cada dosis de 0,05 ml. Los polisorbatos pueden provocar reacciones alérgicas. Consulte a su médico si tiene alguna alergia conocida.
3. Cómo usar Vabysmo
Cómo se administra Vabysmo
La dosis recomendada es 6 mg de faricimab.
Degeneración macular asociada a la edad neovascular (exudativa) (DMAEn)
- Se le administrará una inyección cada mes durante los primeros 3 meses.
- Posteriormente, debe recibir inyecciones hasta cada 4 meses. Su médico determinará la frecuencia de las inyecciones basándose en el estado de su ojo.
Edema macular diabético (EMD) y edema macular secundario a la oclusión de la vena retiniana (oclusión de la rama venosa retiniana (ORVR) u oclusión de la vena central de la retina (OVCR))
- Se le administrará una inyección cada mes durante un mínimo de 3 meses.
- Posteriormente, puede recibir inyecciones menos frecuentemente. Su médico determinará la frecuencia de las inyecciones basándose en el estado de su ojo.
Forma de administración
Vabysmo se inyecta dentro del ojo (inyección intravítrea) por un médico experimentado en administrar inyecciones oculares.
Antes de la inyección, su médico usará un desinfectante ocular para limpiar su ojo cuidadosamente para prevenir la infección. Su médico la dará una gota ocular (anestésico local) para adormecer el ojo y reducir o prevenir el dolor de la inyección.
Cuánto dura el tratamiento con Vabysmo
Este es un tratamiento a largo plazo, posiblemente continuará durante meses o años. Su médico vigilará regularmente su estado para comprobar que el tratamiento está teniendo el efecto deseado. Dependiendo de cómo responda al tratamiento con Vabysmo, su médico le realizará un cambio a mayor o menor frecuencia de dosis.
Si pierde una dosis de Vabysmo
Si pierde una dosis, concierte una nueva cita con su médico tan pronto como sea posible.
Si interrumpe el tratamiento con Vabysmo
Hable con su médico antes de interrumpir el tratamiento. Interrumpir el tratamiento puede aumentar el riesgo de pérdida de visión y su visión puede empeorar.
Si tiene cualquier otra duda sobre el uso de este medicamento, pregunte a su médico.
4. Posibles efectos adversos
Al igual que todos los medicamentos, este medicamento puede producir efectos adversos, aunque no todas las personas los sufran.
Los efectos adversos con las inyecciones de Vabysmo son tanto por el medicamento como por el procedimiento de la inyección y pueden afectar al ojo mayormente.
Algunos efectos adversos pueden ser graves
Contacte con su médico inmediatamentesi tiene alguno de los siguientes síntomas, que son signos de reacciones alérgicas, inflamación o infecciones:
- dolor ocular, aumento del malestar, empeoramiento del enrojecimiento ocular, visión borrosa o disminuida, aumento en el número de pequeñas partículas en su visión, aumento en la sensibilidad a la luz – estos son signos de una posible infección ocular, inflamación o reacción alérgica.
- una disminución repentina o un cambio en la visión.
Otros posibles efectos adversos
Otros efectos adversos que pueden ocurrir después del tratamiento con Vabysmo incluyen aquellos listados más abajo.
Muchos de los efectos adversos son leves o moderados y generalmente desaparecerán dentro de una semana después de cada inyección.
Contacte con su médico si alguno de los siguientes efectos adversos llega a ser grave.
Muy frecuentes(pueden afectar a más de 1 de cada 10 personas):
- Ninguna
Frecuentes(pueden afectar a hasta 1 de cada 10 personas):
- Enturbiamiento del cristalino en el ojo (catarata)
- Desgarro de una de las capas de la parte posterior del ojo (desgarro del epitelio pigmentario de la retina, sólo en DMAEn)
- Desprendimiento de la sustancia similar a un gel que se encuentra dentro del ojo (desprendimiento vítreo)
- Aumento de la presión dentro del ojo (aumento de la presión intraocular)
- Sangrado de los pequeños vasos sanguíneos de la capa más externa del ojo (hemorragia conjuntival)
- Puntos que se mueven o sombras oscuras en su visión (partículas flotantes en el vítreo)
- Dolor ocular
Poco frecuentes(pueden afectar a hasta 1 de cada 100 personas):
- Inflamación grave o infección dentro del ojo (endoftalmitis)
- Inflamación de la sustancia gelatinosa dentro del ojo/ ojo rojo (vitritis)
- Inflamación del iris y su tejido adyacente en el ojo (iritis, iridociclitis, uveítis)
- Sangrado dentro del ojo (hemorragia vítrea)
- Malestar ocular
- Picor (prurito ocular)
- Desgarro de la retina (parte posterior del ojo que detecta la luz)
- Ojo rojo (hiperemia ocular/conjuntival)
- Sensación de tener algo en el ojo
- Visión borrosa
- Disminución de la nitidez en la visión (agudeza visual reducida)
- Dolor durante el procedimiento
- Desprendimiento de retina
- Aumento de la producción de lágrimas (lagrimeo aumentado)
- Rasguño de la córnea, daño de la parte transparente del globo ocular que cubre el iris (abrasión corneal)
- Irritación ocular
Raros(pueden afectar a hasta 1 de cada 1 000 personas):
- Disminución temporal de la nitidez en la visión (agudeza visual reducida transitoriamente)
- Enturbiamiento del cristalino debido a una lesión (catarata traumática)
Frecuencia no conocida
- Vasculitis retiniana (inflamación de los vasos sanguíneos del fondo del ojo)
- Vasculitis oclusiva retiniana (bloqueo de los vasos sanguíneos del fondo del ojo, normalmente en presencia de inflamación)
Cuando se administran algunos medicamentos que funcionan de forma similar a Vabysmo, se sabe que hay un riesgo de coágulos de sangre que bloquean los vasos sanguíneos (acontecimientos tromboembólicos arteriales) que pueden causar un ataque al corazón o un ictus. Dado que una pequeña cantidad del medicamento entra en la sangre, existe el riesgo teórico de estos episodios después de la inyección de Vabysmo dentro del ojo.
Comunicación de efectos adversos
Si experimenta cualquier tipo de efecto adverso, consulte a su médico, incluso si se trata de posibles efectos adversos que no aparecen en este prospecto. También puede comunicarlos directamente a través del sistema nacional de notificación incluido en el Apéndice V*. Mediante la comunicación de efectos adversos usted puede contribuir a proporcionar más información sobre la seguridad de este medicamento.
5. Conservación de Vabysmo
Su médico, farmacéutico o enfermero es responsable de conservar este medicamento y desechar correctamente cualquier producto no utilizado. La siguiente información está destinada a profesionales sanitarios.
Mantener este medicamento fuera de la vista y del alcance de los niños.
No utilice este medicamento después de la fecha de caducidad que aparece en la etiqueta y el envase después de EXP. La fecha de caducidad es el último día del mes que se indica.
Conservar en nevera (2 ºC - 8 ºC).
No congelar.
Mantener la bandeja sellada en el embalaje original para proteger la jeringa precargada de la luz.
La jeeringa precargada puede conservarse a temperatura ambiente, de 20 ºC a 25 ºC, en el embalaje original hasta 24 horas.
6. Contenido del envase e información adicional
Composición de Vabysmo
- El principio activo es faricimab. Un ml de solución inyectable contiene 120 mg de faricimab. Cada jeringa precargada contiene 21 mg de faricimab en 0,175 ml de solución. Esto proporciona una dosis aprovechable para liberar una dosis única de 0,05 ml de solución que contiene 6 mg de faricimab.
- Los demás componentes son: L-histidina, ácido acético al 30% (E 260), L-metionina, cloruro de sodio, sacarosa, polisorbato 20 (E 432), agua para preparaciones inyectables (ver Sección 2 “Vabysmo contiene sodio y polisorbato”).
Aspecto del producto y contenido del envase
Vabysmo 120 mg/ml solución inyectable (inyección) en jeringa precargada es una solución de clara a opalescente, de transparente a amarillo-pardusca.
El envase contiene una aguja de inyección con filtro de pared extrafina (calibre 30 x ½ pulgada, 0,30 mm x 12,7 mm, 5 µm), junto con una jeringa precargada para un único uso.
Titular de la autorización de comercialización y responsable de la fabricación
Roche Registration GmbH
Emil-Barell-Strasse 1
79639
Grenzach-Wyhlen
Alemania
Fabricante
Roche Pharma AG
Emil-Barell-Strasse 1
79639
Grenzach-Wyhlen
Alemania
Pueden solicitar más información respecto a este medicamento dirigiéndose al representante local del titular de la autorización de comercialización:
België/Belgique/Belgien N.V. Roche S.A. Tél/Tel: +32 (0) 2 525 82 11 | Lietuva UAB “Roche Lietuva” Tel: +370 5 2546799 |
| Luxembourg/Luxemburg (Voir/siehe Belgique/Belgien) |
Ceská republika Roche s. r. o. Tel: +420 - 2 20382111 | Magyarország Roche (Magyarország) Kft. Tel: +36 - 1 279 4500 |
Danmark Roche Pharmaceuticals A/S Tlf: +45 - 36 39 99 99 | Malta (See Ireland) |
Deutschland Roche Pharma AG Tel: +49 (0) 7624 140 | Nederland Roche Nederland B.V. Tel: +31 (0) 348 438050 |
Eesti Roche Eesti OÜ Tel: + 372 - 6 177 380 | Norge Roche Norge AS Tlf: +47 - 22 78 90 00 |
Ελλáδα Roche (Hellas) A.E. Τηλ: +30 210 61 66 100 | Österreich Roche Austria GmbH Tel: +43 (0) 1 27739 |
España Roche Farma S.A. Tel: +34 - 91 324 81 00 | Polska Roche Polska Sp.z o.o. Tel: +48 - 22 345 18 88 |
Francia Roche Tél: +33 (0) 1 47 61 40 00 | Portugal Roche Farmacêutica Química, Lda Tel: +351 - 21 425 70 00 |
Hrvatska Roche d.o.o Tel: +385 1 4722 333 | România Roche România S.R.L. Tel: +40 21 206 47 01 |
Ireland Roche Products (Ireland) Ltd. Tel: +353 (0) 1 469 0700 | Slovenija Roche farmacevtska družba d.o.o. Tel: +386 - 1 360 26 00 |
Ísland Roche Pharmaceuticals A/S c/o Icepharma hf Sími: +354 540 8000 | Slovenská republika Roche Slovensko, s.r.o. Tel: +421 - 2 52638201 |
Italia Roche S.p.A. Tel: +39 - 039 2471 | Suomi/Finland Roche Oy Puh/Tel: +358 (0) 10 554 500 |
| Sverige Roche AB Tel: +46 (0) 8 726 1200 |
Latvija Roche Latvija SIA Tel: +371 - 6 7039831 |
Fecha de la última revisión de este prospecto:
La información detallada de este medicamento está disponible en la página web de la Agencia Europea de Medicamentos: https://www.ema.europa.eu.
Esta información está destinada únicamente a profesionales sanitarios:
Instrucciones de uso para la jeringa precargada:
Antes de empezar: | |
Lea cuidadosamente todas las instrucciones antes de usar Vabysmo. | |
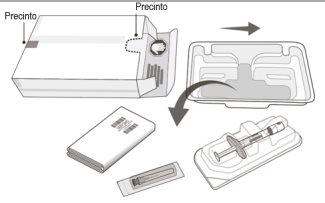
El envase de Vabysmo contiene: | |
Una jeringa precargada estéril en una bandeja sellada. La jeringa precargada es para un solo uso. | |
Una aguja de inyección con filtro estéril, calibre 30 x ½ pulgada, de pared extrafina con un filtro integrado en el conector. La aguja de inyección con filtro es para un solo uso. | |
Solo utilizar para la administración la aguja de inyección con filtro proporcionada, ya que se ha diseñado para asegurar un uso oftálmico seguro del medicamento | |
Vabysmo debe almacenarse en nevera a temperaturas entre 2 ºC y 8 ºC. | |
Nocongelar. | |
Deje que Vabysmo alcance temperatura ambiente, de 20 ºC a 25 ºC, antes de proceder con la administración. | |
Antes de su uso, mantener la bandeja sellada en el embalaje original para proteger la jeringa precargada de la luz. La jeringa precargada puede almacenarse a temperatura ambiente en el embalaje original hasta 24horas. | |
Vabysmo debe inspeccionarse visualmente antes de su administración. | |
Noutilice el envase si los precintos han sido manipulados. | |
Nolo use si el envase, la jeringa precargada, la aguja de inyección con filtro están caducadas, dañadas o han sido manipuladas. | |
Nolo utilice si falta la aguja de inyección con filtro. | |
Noretire la zona de sujeción para los dedos de la jeringa. | |
Nolo utilice si el capuchón de la jeringa se ha desprendido de la Luer lock. | |
Nolo use si se ven partículas, si tiene apariencia nubosa o si está decolorado. Vabysmo es una solución de clara a opalescente, de transparente a amarillo-pardusca. |
Contenido del envase | ||
Figura A | ||
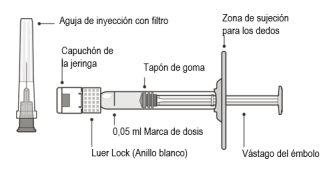
Descripción del producto | ||
Figura B | ||
Saque la jeringa de la bandeja de la jeringa (paso 1). Todos los pasos siguientes deben realizarse utilizando técnicas asépticas. | ||
Abra la bandeja y quite el tapón de la jeringa | ||
1 | Retire la tapa de la bandeja de la jeringa y extraiga la jeringa precargada de forma aséptica. | |
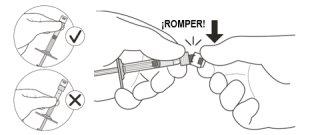
2 | Sostenga la jeringa por el anillo blanco y rompa el capuchón de la jeringa (ver Figura C). | |
Nogire el capuchón. | ||
Figura C | ||
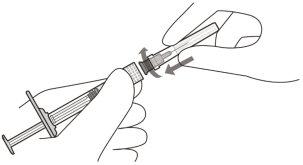
Una la aguja de inyección con filtro | ||
3 | Saque asépticamente la aguja de inyección con filtro de su envase. | |
4 | De forma aséptica y firme coloque la aguja de inyección con filtro en la jeringa Luer lock (ver Figura D). | |
Figura D | Solo utilizar para la administración la aguja de inyección con filtro proporcionada | |
5 | Retire con cuidado el capuchón de la aguja tirando de él en línea recta. | |
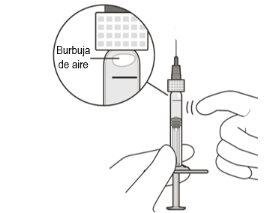
Eliminar las burbujas de aire | ||
6 | Mantenga la jeringa con la aguja apuntando hacia arriba. Compruebe la jeringa para asegurar que no hay burbujas de aire. | |
7 | Si hay burbujas de aire, golpee suavemente la jeringa con su dedo hasta que las burbujas asciendan hacia la parte superior (ver Figura E). | |
Figura E | ||
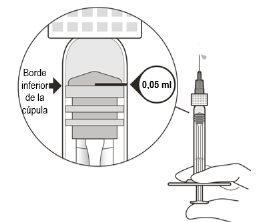
Ajustar la dosis del medicamento y eliminar el aire | ||
8 | Mantenga la jeringa a la altura del ojo y lentamenteempuje el vástago del émbolo hasta que el borde inferior de la cúpula del tapón de gomaquede alineado con la marca de dosis de 0,05 ml (ver Figura F). Esto eliminará el aire y el exceso de solución y ajustará la dosis a 0,05 ml. | |
Asegure que la inyección se adminsitra inmediatamentetras la preparación de la dosis. | ||
Figura F | ||
Procedimiento de inyección | ||
9 | El procedimiento de inyección debe realizarse bajo condiciones asépticas. Inyecte lentamentehasta que el tapón de goma alcance la parte inferior de la jeringa para liberar el volumen de 0,05 ml. Novuelva a tapar ni separe la aguja de inyección con filtro de la jeringa. La eliminación del medicamento no utilizado y de todos los materiales que hayan estado en contacto con él se realizará de acuerdo con la normativa local. |
- País de registro
- Principio activo
- Requiere recetaSí
- Fabricante
- Esta información es de carácter general y no sustituye la consulta con un profesional sanitario.
- Alternativas a VABYSMO 120 MG/ML SOLUCION PARA INYECCION EN JERINGA PRECARGADAForma farmacéutica: INYECTABLE, 120 MG/MLPrincipio activo: FaricimabFabricante: Roche Registration GmbhRequiere recetaForma farmacéutica: INYECTABLE, 40 mg/mlPrincipio activo: AfliberceptFabricante: Sandoz GmbhRequiere recetaForma farmacéutica: INYECTABLE, 40 mg/mlPrincipio activo: AfliberceptFabricante: Sandoz GmbhRequiere receta
Médicos online para VABYSMO 120 MG/ML SOLUCION PARA INYECCION EN JERINGA PRECARGADA
Comenta la dosis, los posibles efectos secundarios, interacciones, contraindicaciones o la revisión de receta de VABYSMO 120 MG/ML SOLUCION PARA INYECCION EN JERINGA PRECARGADA, sujeto a valoración médica y a la normativa local.
Preguntas frecuentes