
TEVAGRASTIM 48 MU/0,8 ml SOLUCION PARA INYECCION O PERFUSION

Cómo usar TEVAGRASTIM 48 MU/0,8 ml SOLUCION PARA INYECCION O PERFUSION
Traducción generada por IA
Este contenido ha sido traducido automáticamente y se ofrece solo con fines informativos. No sustituye la consulta con un profesional sanitario.
Ver originalContenido del prospecto
Introducción
Prospecto: información para el usuario
Tevagrastim 30 MUI/0,5 ml solución inyectable y para perfusión
Tevagrastim 48 MUI/0,8 ml solución inyectable y para perfusión
filgrastim
Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene información importante para usted.
- Conserve este prospecto, ya que puede tener que volver a leerlo.
- Si tiene alguna duda, consulte a su médico, farmacéutico o enfermero.
- Este medicamento se le ha recetado solamente a usted, y no debe dárselo a otras personas aunque tengan los mismos síntomas que usted, ya que puede perjudicarles.
- Si experimenta efectos adversos, consulte a su médico, farmacéutico o enfermero, incluso si se trata de efectos adversos que no aparecen en este prospecto. Ver sección 4.
Contenido del prospecto
- Qué es Tevagrastim y para qué se utiliza
- Qué necesita saber antes de empezar a usar Tevagrastim
- Cómo usar Tevagrastim
- Posibles efectos adversos
- Conservación de Tevagrastim
- Contenido del envase e información adicional
- Información para auto-inyectarse
- Esta información está destinada únicamente a profesionales del sector sanitario
1. Qué es Tevagrastim y para qué se utiliza
Qué es Tevagrastim
Tevagrastim es un factor de crecimiento de glóbulos blancos (factor estimulante de las colonias de granulocitos) y pertenece a un grupo de medicamentos llamados citocinas. Los factores de crecimiento son proteínas que se producen de manera natural en el cuerpo, pero también pueden producirse usando ingeniería genética para su uso como medicamento. Tevagrastim funciona haciendo que la médula ósea produzca más glóbulos blancos.
Para qué se utiliza Tevagrastim
Una reducción en el número de glóbulos blancos (neutropenia) se puede producir por varias razones y hace que su cuerpo sea menos eficaz a la hora de combatir las infecciones. Tevagrastim estimula la médula ósea para que produzca nuevos glóbulos blancos rápidamente.
Tevagrastim se puede utilizar:
- para aumentar el número de glóbulos blancos tras el tratamiento con quimioterapia para ayudar a prevenir infecciones;
- para aumentar el número de glóbulos blancos tras un trasplante de médula ósea para ayudar a prevenir infecciones;
- antes de la quimioterapia a dosis altas para hacer que la médula ósea produzca más células madre, que pueden ser recogidas y devueltas a su organismo después del tratamiento. Estas células se pueden recoger de usted o de un donante. Las células madre volverán entonces a la médula ósea y producirán células sanguíneas;
- para aumentar el número de glóbulos blancos si presenta neutropenia crónica grave para ayudar a prevenir infecciones;
- para ayudar a reducir el riesgo de infecciones en pacientes con infección avanzada por el VIH.
2. Qué necesita saber antes de empezar a usar Tevagrastim
No use Tevagrastim
- si es alérgico al filgrastim o a alguno de los demás componentes de este medicamento (incluidos en la sección 6).
Advertencias y precauciones
Consulte a su médico, farmacéutico o enfermero antes de empezar a usar Tevagrastim.
Informe a su médico antes de empezar el tratamiento si tiene:
- anemia de células falciformes, ya que este medicamento puede causar crisis de células falciformes;
- osteoporosis (enfermedad ósea).
Informe a su médico inmediatamente durante el tratamiento con Tevagrastim si:
- tiene signos repentinos de alergia, tales como erupción, picor o urticaria en la piel, hinchazón de la cara, labios, lengua u otras partes del cuerpo, falta de aliento, sibilancias o problemas al respirar, ya que podrían ser signos de una reacción alérgica grave (hipersensibilidad);
- presenta hinchazón en la cara o los tobillos, sangre en la orina u orina de color marrón o si nota que orina con menor frecuencia de lo habitual (glomerulonefritis);
- presenta dolor en la parte superior izquierda del vientre (dolor abdominal), dolor debajo de la caja torácica izquierda o en el extremo izquierdo del hombro (estos pueden ser síntomas de un bazo agrandado [esplenomegalia] o una posible rotura del bazo);
- nota sangrados o cardenales inusuales (estos pueden ser síntomas de una disminución de las plaquetas en sangre [trombocitopenia], con una capacidad reducida de la sangre para coagularse);
- tiene síntomas de inflamación de la aorta (el vaso sanguíneo grande que transporta sangre desde el corazón hasta el resto del cuerpo), esto rara vez se ha notificado en pacientes con cáncer y en donantes sanos. Los síntomas pueden incluir fiebre, dolor abdominal, malestar general, dolor de espalda y marcadores inflamatorios aumentados. Informe a su médico si presenta estos síntomas.
Pérdida de respuesta a filgrastim
Si experimenta una pérdida de respuesta o si no se consigue mantener la respuesta al tratamiento con filgrastim, su médico investigará las causas incluyendo si ha desarrollado anticuerpos que puedan neutralizar la actividad de filgrastim.
Puede que su médico quiera supervisarle estrechamente, ver sección 4 del prospecto.
Si usted es un paciente con neutropenia crónica grave, puede estar en riesgo de desarrollar cáncer de la sangre (leucemia, síndrome mielodisplásico [SMD]). Hable con su médico acerca de los riesgos de desarrollar cáncer de la sangre y de las pruebas que se deben realizar. Si desarrolla o es probable que desarrolle cáncer de la sangre, no debe utilizar Tevagrastim a menos que lo indique su médico.
Si usted es un donante de células madre, debe tener entre 16 y 60 años de edad.
Tenga especial cuidado con otros productos que estimulan los glóbulos blancos
Tevagrastim pertenece a un grupo de medicamentos que estimula la producción de glóbulos blancos. Su médico debe registrar siempre el producto exacto que esté utilizando.
Otros medicamentos y Tevagrastim
Informe a su médico o farmacéutico si está utilizando, ha utilizado recientemente o pudiera tener que utilizar cualquier otro medicamento.
Embarazo y lactancia
Tevagrastim no ha sido estudiado en mujeres embarazadas o en periodo de lactancia.
No se recomienda Tevagrastim durante el embarazo.
Es importante que informe a su médico si usted:
- está embarazada o en periodo de lactancia;
- cree que podría estar embarazada; o
- tiene intención de quedarse embarazada
Si se queda embarazada durante el tratamiento con Tevagrastim, informe a su médico. A menos que su médico le indique lo contrario, debe dejar de dar el pecho si utiliza Tevagrastim.
Conducción y uso de máquinas
La influencia de Tevagrastim sobre su capacidad para conducir y usar máquinas es pequeña. Este medicamento puede producir mareos. Es aconsejable esperar y ver cómo se siente tras la administración del medicamento antes de conducir o manejar maquinaria.
Tevagrastim contiene sorbitol
Este medicamento contiene 50 mg de sorbitol en cada ml.
Para administración por vía intravenosa
El sorbitol es una fuente de fructosa. Si usted (o su hijo) padecen intolerancia hereditaria a la fructosa (IHF), una enfermedad genética rara, usted (o su hijo) no deben recibir este medicamento. Los pacientes con IHF no pueden descomponer la fructosa, lo que puede causar efectos adversos graves. Consulte con su médico antes de recibir este medicamento si usted (o su hijo) padecen IHF o si su hijo no puede tomar alimentos o bebidas dulces porque les produce mareos, vómitos o efectos desagradables como hinchazón, calambres en el estómago o diarrea.
Tevagrastim contiene sodio
Este medicamento contiene menos de 1 mmol de sodio (23 mg) por jeringa precargada; esto es, esencialmente “exento de sodio”.
3. Cómo usar Tevagrastim
Siga exactamente las instrucciones de administración de este medicamento indicadas por su médico o farmacéutico. En caso de duda, consulte de nuevo a su médico o farmacéutico.
¿Cómo se administra Tevagrastim y cuánto debo tomar?
Tevagrastim se administra por lo general una vez al día como una inyección en el tejido justo debajo de la piel (conocida como inyección subcutánea). También se puede administrar una vez al día como una inyección lenta en la vena (conocida como perfusión intravenosa). La dosis habitual varía en función de su enfermedad y peso. Su médico le indicará la cantidad de Tevagrastim que debe tomar.
Pacientes con trasplante de médula ósea después de la quimioterapia:
Normalmente recibirá su primera dosis de Tevagrastim al menos 24 horas después de la quimioterapia y al menos 24 horas después de recibir su trasplante de médula ósea.
A usted o a las personas que le atienden se les puede enseñar a administrar inyecciones subcutáneas para que pueda continuar el tratamiento en su casa. Sin embargo, no debe intentarlo a menos que su profesional sanitario le haya entrenado de forma adecuada.
¿Cuánto tiempo tengo que tomar Tevagrastim?
Tendrá que tomar Tevagrastim hasta que su recuento de glóbulos blancos sea normal. Se le realizarán análisis de sangre periódicos para supervisar el número de glóbulos blancos en su cuerpo. Su médico le indicará cuanto tiempo necesita tomar Tevagrastim.
Uso en niños
Tevagrastim se utiliza para tratar a niños que están recibiendo quimioterapia o que presentan un recuento de glóbulos blancos bajo (neutropenia) grave. La dosis administrada a los niños que están recibiendo quimioterapia es la misma que para los adultos.
Si usa más Tevagrastim del que debe
No aumente la dosis que le ha recetado su médico. Si ha utilizado más Tevagrastim del que debe, póngase en contacto con su médico, o farmacéutico tan pronto como sea posible.
Si olvidó usar Tevagrastim
Si ha olvidado una inyección, o si se inyectó menos dosis, contacte con su médico tan pronto como sea posible. No tome una dosis doble para compensar las dosis olvidadas.
Si tiene cualquier otra duda sobre el uso de este medicamento, pregunte a su médico, farmacéutico o enfermero.
4. Posibles efectos adversos
Al igual que todos los medicamentos, este medicamento puede producir efectos adversos, aunque no todas las personas los sufran.
Efectos adversos importantes
Es importante que contacte a su médico inmediatamente:
- si experimenta una reacción alérgica, incluida debilidad, caída de la presión arterial, dificultad para respirar, hinchazón de la cara (anafilaxia), erupción cutánea, erupción cutánea con picor (urticaria), hinchazón de la cara, labios, boca, lengua o garganta (angioedema) y falta de aliento (disnea);
- si experimenta tos, fiebre y dificultad para respirar (disnea), ya que puede ser un signo del síndrome de dificultad respiratoria aguda (SDRA);
- si experimenta daño renal (glomerulonefritis). Se ha observado daño renal en pacientes que recibían filgrastim. Contacte con su médico inmediatamente si observa hinchazón en la cara o los tobillos, sangre en la orina u orina de color marrón, o nota que orina con menor frecuencia de lo habitual;
- si experimenta alguno o una combinación de los siguientes efectos adversos:
- hinchazón que puede estar asociada con orinar con una menor frecuencia, dificultad para respirar, hinchazón y sensación de plenitud abdominal y una sensación general de cansancio. Estos síntomas generalmente se desarrollan rápidamente.
Estos pueden ser síntomas de una enfermedad llamada “síndrome de fuga capilar” y que puede causar que la sangre se escape de un pequeño vaso sanguíneo hacia otros lugares de su cuerpo y necesite atención médica urgente.
- si experimenta una combinación de los siguientes síntomas:
- fiebre, escalofríos o sensación de mucho frío, frecuencia cardiaca alta, confusión o desorientación, dificultad para respirar, dolor extremo o malestar y piel húmeda o sudorosa.
Estos podrían ser síntomas de una afección llamada “sepsis” (también llamada “intoxicación sanguínea”), una infección grave con respuesta inflamatoria de todo el cuerpo que puede ser potencialmente mortal y requiere atención médica urgente;
- si experimenta dolor en la parte superior izquierda del vientre (dolor abdominal), dolor en el lado inferior izquierdo de la caja torácica o dolor en el extremo del hombro, ya que se podría tratar de algún problema con su bazo (agrandamiento del bazo [esplenomegalia] o rotura del bazo);
- si está siendo tratado por neutropenia crónica grave y tiene sangre en la orina (hematuria). Su médico le realizará análisis de orina periódicos si experimenta este efecto adverso o si se encuentran proteínas en su orina (proteinuria).
Un efecto adverso frecuente del uso de Tevagrastim es dolor en los músculos o huesos (dolor musculoesquelético), que se puede remediar tomando medicamentos habituales para aliviar el dolor (analgésicos). En los pacientes sometidos a un trasplante de células madre o de médula ósea, puede aparecer enfermedad del injerto contra huésped (EICH). Esta es una reacción de las células del donante contra el paciente que recibe el trasplante; los signos y síntomas incluyen erupciones en las palmas de las manos o las plantas de los pies, y úlceras y llagas en la boca, intestino, hígado, piel, ojos, pulmones, vagina y articulaciones.
En donantes sanos de células madre se puede observar un incremento de los glóbulos blancos (leucocitosis) y una disminución de las plaquetas que puede reducir la capacidad de su sangre para coagularse (trombocitopenia). Estos efectos serán vigilados por su médico.
Puede experimentar los siguientes efectos adversos:
Muy frecuentes(pueden afectar a más de 1 de cada 10 personas):
- Disminución de las plaquetas, lo que reduce la capacidad de la sangre de coagularse (trombocitopenia)
- Recuento bajo de glóbulos rojos (anemia)
- Dolor de cabeza
- Diarrea
- Vómitos
- Náuseas
- Pérdida o debilitamiento del cabello inusual (alopecia)
- Cansancio (fatiga)
- Irritación e hinchazón del revestimiento del tubo digestivo que va de la boca al ano (inflamación de la mucosa)
- Fiebre (pirexia)
Frecuentes(pueden afectar hasta 1 de cada 10 personas):
- Inflamación de los pulmones (bronquitis)
- Infección del tracto respiratorio superior
- Infección del tracto urinario
- Apetito disminuido
- Problemas para dormir (insomnio)
- Mareos
- Disminución de la sensibilidad, especialmente en la piel (hipoestesia)
- Hormigueo o entumecimiento de las manos o los pies (parestesia)
- Tensión arterial baja (hipotensión)
- Tensión arterial alta (hipertensión)
- Tos
- Tos con sangre (hemoptisis)
- Dolor en la boca y garganta (dolor orofaríngeo)
- Hemorragia nasal (epistaxis)
- Estreñimiento
- Dolor oral
- Aumento del tamaño del hígado (hepatomegalia)
- Erupción
- Enrojecimiento de la piel (eritema)
- Calambre muscular
- Dolor al orinar (disuria)
- Dolor en el pecho
- Dolor
- Debilidad generalizada (astenia)
- Sensación de malestar (malestar general)
- Hinchazón en manos y pies (edema periférico)
- Aumento de ciertas enzimas en la sangre
- Cambios en el análisis bioquímico de la sangre
- Reacción a la transfusión
Poco frecuentes(pueden afectar hasta 1 de cada 100 personas):
- Aumento de los glóbulos blancos de la sangre (leucocitosis)
- Reacción alérgica (hipersensibilidad)
- Rechazo del trasplante de médula ósea (enfermedad del injerto contra el huésped)
- Niveles altos de ácido úrico en la sangre, que pueden causar gota (hiperuricemia) (ácido úrico elevado en sangre)
- Daño hepático causado por el bloqueo de las pequeñas venas del hígado (enfermedad venooclusiva)
- Los pulmones no funcionan como deberían causando falta de aliento (insuficiencia respiratoria)
- Hinchazón o fluido en los pulmones (edema pulmonar)
- Inflamación de los pulmones (enfermedad pulmonar intersticial)
- Radiografías anormales de los pulmones (infiltración pulmonar)
- Sangrado de los pulmones (hemorragia pulmonar)
- Falta de absorción de oxígeno en los pulmones (hipoxia)
- Erupción cutánea irregular (erupción maculopapular)
- Enfermedad que hace que los huesos pierdan densidad haciéndolos más débiles, más frágiles y propensos a romperse (osteoporosis)
- Reacción en la zona de inyección
Raros(pueden afectar hasta 1 de cada 1.000 personas):
- Dolor intenso en los huesos, pecho, intestinos o articulaciones (anemia de células falciformes con crisis)
- Reacciones alérgicas repentinas y que pueden poner en peligro la vida (reacción anafiláctica)
- Hinchazón y dolor en las articulaciones, similar a la gota (pseudogota)
- Un cambio en la forma en que su cuerpo regula los fluidos corporales que puede resultar en hinchazón (alteraciones del volumen de fluidos)
- Inflamación de los vasos sanguíneos de la piel (vasculitis cutánea)
- Úlceras dolorosas, inflamadas y de color rojo oscuro en las extremidades y, a veces, en la cara y el cuello que cursan con fiebre (síndrome de Sweet)
- Empeoramiento de la artritis reumatoide
- Cambios inusuales en la orina
- Disminución de la densidad ósea
- Inflamación de la aorta (el vaso sanguíneo grande que transporta sangre desde el corazón hasta el resto del cuerpo), ver sección 2
Comunicación de efectos adversos
Si experimenta cualquier tipo de efecto adverso, consulte a su médico, farmacéutico o enfermero, incluso si se trata de posibles efectos adversos que no aparecen en este prospecto. También puede comunicarlos directamente a través del sistema nacional de notificación incluido en el Apéndice V. Mediante la comunicación de efectos adversos usted puede contribuir a proporcionar más información sobre la seguridad de este medicamento.
5. Conservación de Tevagrastim
Mantener este medicamento fuera de la vista y del alcance de los niños.
No utilice este medicamento después de la fecha de caducidad que aparece en la caja y en la jeringa precargada después de EXP. La fecha de caducidad es el último día del mes que se indica.
Conservar en nevera (entre 2 ºC y 8 ºC).
Dentro de su periodo de validez y para su uso ambulatorio, el medicamento puede sacarse de la nevera (2 ºC – 8 ºC) y almacenarse a una temperatura de hasta 25 ºC durante un único periodo de hasta 4 días. Si el medicamento no se ha usado en esos 4 días, se debe volver a refrigerar (2 ºC – 8 ºC) hasta la fecha de caducidad. Se deben eliminar las jeringas almacenadas a más de 8 ºC durante más de 4 días.
No utilice este medicamento si observa turbidez o partículas en el interior.
Los medicamentos no se deben tirar por los desagües. Pregunte a su farmacéutico cómo deshacerse de los envases y de los medicamentos que ya no necesita. De esta forma, ayudará a proteger el medio ambiente.
6. Contenido del envase e información adicional
Composición de Tevagrastim
- El principio activo es filgrastim. Cada ml de solución inyectable y para perfusión contiene 60 millones de unidades internacionales (MUI) (600 microgramos) de filgrastim.
Tevagrastim 30 MUI/0,5 ml: cada jeringa precargada contiene 30 millones de unidades internacionales [MUI] (300 microgramos) de filgrastim en 0,5 ml de solución.
Tevagrastim 48 MUI/0,8 ml: cada jeringa precargada contiene 48 millones de unidades internacionales [MUI] (480 microgramos) de filgrastim en 0,8 ml de solución.
- Los demás componentes son: hidróxido de sodio, ácido acético glacial, sorbitol, polisorbato 80, agua para preparaciones inyectables.
Aspecto del producto y contenido del envase
Tevagrastim es una solución inyectable y para perfusión en una jeringa precargada con o sin dispositivo de seguridad. Tevagrastim es una solución transparente e incolora. Cada jeringa precargada contiene 0,5 ml o 0,8 ml de solución.
Tevagrastim se suministra en envases de 1, 5 o 10 jeringas precargadas o en envases múltiples que contienen 10 jeringas precargadas (2 envases de 5) con aguja de inyección y con o sin protector de seguridad para la aguja. Puede que no se comercialicen todos los formatos.
Titular de la autorización de comercialización
TEVA GmbH
Graf-Arco-Strasse 3
89079 Ulm
Alemania
Responsable de la fabricación
Teva Pharma B.V.
Swensweg 5
2031 GA Haarlem
Países Bajos
Merckle GmbH
Graf-Arco-Straße 3
89079 Ulm
Alemania
Pueden solicitar más información respecto a este medicamento dirigiéndose al representante local del titular de la autorización de comercialización:
België/Belgique/Belgien Teva Pharma Belgium N.V./S.A./AG Tél/Tel: +32 38207373 | Lietuva UAB Teva Baltics Tel: +370 52660203 |
| Luxembourg/Luxemburg Teva Pharma Belgium N.V./S.A./AG Belgique/Belgien Tél/Tel: +32 38207373 |
Ceská republika Teva Pharmaceuticals CR, s.r.o. Tel: +420 251007111 | Magyarország Teva Gyógyszergyár Zrt. Tel: +36 12886400 |
Danmark Teva Denmark A/S Tlf: +45 44985511 | Malta Teva Pharmaceuticals Ireland L-Irlanda Tel: +44 2075407117 |
Deutschland TEVA GmbH Tel: +49 73140208 | Nederland Teva Nederland B.V. Tel: +31 8000228400 |
Eesti UAB Teva Baltics Eesti filiaal Tel: +372 6610801 | Norge Teva Norway AS Tlf: +47 66775590 |
Ελλáδα TEVA HELLAS Α.Ε. Τηλ: +30 2118805000 | Österreich ratiopharm Arzneimittel Vertriebs-GmbH Tel: +43 1970070 |
España Teva Pharma, S.L.U. Tel: +34 913873280 | Polska Teva Pharmaceuticals Polska Sp. z o.o. Tel: +48 223459300 |
France Teva Santé Tél: +33 155917800 | Portugal Teva Pharma - Produtos Farmacêuticos, Lda. Tel: +351 214767550 |
Hrvatska Pliva Hrvatska d.o.o. Tel: +385 13720000 | România Teva Pharmaceuticals S.R.L. Tel: +40 212306524 |
Ireland Teva Pharmaceuticals Ireland Tel: +44 2075407117 | Slovenija Pliva Ljubljana d.o.o. Tel: +386 15890390 |
Ísland Teva Pharma Iceland ehf. Sími: +354 5503300 | Slovenská republika TEVA Pharmaceuticals Slovakia s.r.o. Tel: +421 257267911 |
Italia Teva Italia S.r.l. Tel: +39 028917981 | Suomi/Finland Teva Finland Oy Puh/Tel: +358 201805900 |
Κúπρος TEVA HELLAS Α.Ε. Ελλáδα Τηλ: +30 2118805000 | Sverige Teva Sweden AB Tel: +46 42121100 |
Latvija UAB Teva Baltics filiale Latvija Tel: +371 67323666 | United Kingdom (Northern Ireland) Teva Pharmaceuticals Ireland Ireland Tel: +44 2075407117 |
Fecha de la última revisión de este prospecto:
La información detallada de este medicamento está disponible en la página web de la Agencia Europea de Medicamentos: http://www.ema.europa.eu.
- Información para auto-inyectarse
Esta sección contiene información de cómo administrarse a uno mismo una inyección de Tevagrastim. Es importante que no trate de administrarse una inyección sin haber recibido el curso necesario por su médico o enfermero. Si no está seguro de poder inyectarse o si tiene cualquier duda, consulte a su médico o enfermero.
Cómo auto-inyectarse Tevagrastim
Deberá inyectarse en el tejido justo bajo la piel. Esto se conoce como inyección subcutánea. La inyección deberá administrarse todos los días aproximadamente a la misma hora.
Equipo necesario para la administración
Para la administración de la inyección subcutánea, se necesita lo siguiente:
- una jeringa precargada de Tevagrastim,
- algodón o similar con alcohol.
Qué debo hacer antes de administrarme una inyección subcutánea de Tevagrastim
- Procurar administrar la inyección aproximadamente a la misma hora todos los días.
- Sacar la jeringa precargada de Tevagrastim del frigorífico.
- Comprobar la fecha de caducidad que indica la jeringa precargada (EXP). No usarla si la fecha es superior al último día del mes que aparece.
- Comprobar la apariencia de Tevagrastim. Debe ser un líquido transparente e incoloro. Si hay partículas en el interior, no debe utilizarlo.
- Para una inyección más cómoda, deje reposar la jeringa precargada durante 30 minutos a temperatura ambiente o tome la jeringa precargada con suavidad en sus manos durante unos minutos. No caliente Tevagrastim de otra manera (por ejemplo, no lo caliente en un microondas ni en agua caliente)
- Noretire la tapa de la jeringa hasta que este listo para la inyección
- Lávese las manos cuidadosamente.
- Buscar un lugar cómodo y bien iluminado y colocar todo lo necesario al alcance (la jeringa precargada de Tevagrastim y el algodón).
Cómo debo preparar mi inyección de Tevagrastim
Antes de inyectar Tevagrastim hay que:
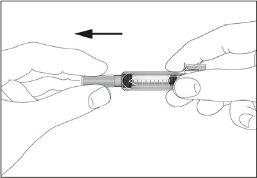
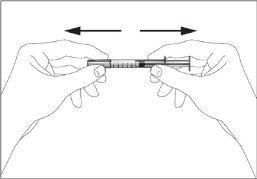
- Coger la jeringa y quitar la cubierta protectora de la aguja suavemente sin inclinarla. Separar tal como se indica en las imágenes 1 y 2. No toque la aguja ni empuje el embolo.
|
|
- Puede aparecer una pequeña burbuja de aire en la jeringa precargada. Si hay burbujas, de golpecitos con sus dedos en la jeringa hasta que las burbujas vayan al final de la jeringa. Con la jeringa apuntando hacia arriba extraiga el aire de la jeringa empujando el embolo.
- La jeringa tiene una escala. Empuje el embolo hasta el número (ml) de la jeringa que corresponde con la dosis de Tevagrastim prescrita por su médico.
- Compruebe de nuevo que la dosis de Tevagrastim es la correcta.
- Ahora puede utilizar la jeringa precargada.
En qué lugar debo poner la inyección
Los sitios más adecuados para la inyección son:
- la parte superior de los muslos; y
- el abdomen, excepto la zona alrededor del ombligo (ver imagen 3).
|
|
Si alguien le administra la inyección también podrá utilizar la parte posterior de sus antebrazos (ver imagen 4)
Para evitar el riesgo de dolor en un punto dado es mejor cambiar cada día el lugar de la inyección.
Cómo debo inyectarme
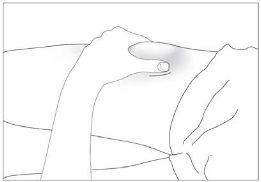
- Desinfecte el lugar de la inyección usando un algodón con alcohol y pellizcar la piel entre el pulgar y el índice, sin apretar (ver imagen 5).
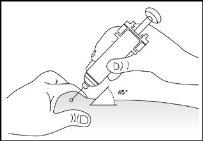
- Insertar completamente la aguja en la piel tal como le indicó su enfermero o médico (ver imagen 6).
- Tirar ligeramente del émbolo para asegurarse de que no se ha pinchado una vena. Si se ve sangre en la jeringa, retirar la aguja e insertarla en otro lugar.
- Manteniendo siempre la piel pellizcada, empujar el émbolo lenta y uniformemente hasta que se haya administrado la totalidad de la dosis y el émbolo no pueda seguir avanzando. ¡No liberar la presión sobre el émbolo!
- Inyecte únicamente la dosis prescrita por su médico.
- Tras inyectar el líquido, retirar la aguja manteniendo la presión sobre el émbolo y después soltar la piel.
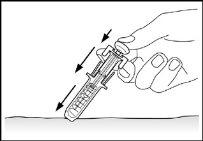
- Suelte el émbolo. El protector de seguridad para la aguja se moverá rápidamente para cubrirla (ver imagen 7).
 5
5
 6
6
 7
7
Recuerde
Si tiene cualquier duda, pida ayuda o consejos a su médico o su enfermero.
Cómo deshacerse de las jeringas usadas
- El protector de seguridad para la aguja previene las lesiones causadas por pinchazos con la aguja tras el uso, por lo que no se necesitan precauciones especiales de eliminación. Deposite la jeringa según las indicaciones del médico, enfermero o farmacéutico.
- Esta información está destinada únicamente a profesionales del sector sanitario
Tevagrastim no contiene conservantes. En vista de un posible riesgo de contaminación microbiana, las jeringas precargadas de Tevagrastim son para un solo uso.
La exposición accidental a temperaturas de congelación no afecta negativamente a la estabilidad de Tevagrastim.
Tevagrastim no debe diluirse con cloruro de sodio. Este medicamento no debe mezclarse con otros medicamentos excepto con los mencionados a continuación. La dilución de filgrastim puede ser adsorbida por el vidrio y materiales plásticos excepto si se diluye como se menciona a continuación.
Tevagrastim se puede diluir, si es necesario, en una solución para perfusión de glucosa 50 mg/ml (al 5 %). No se recomienda en ningún caso diluir a concentraciones finales inferiores a 0,2 MUI (2 μg) por ml. La solución debe inspeccionarse visualmente antes de usarla. Solamente deben utilizarse soluciones transparentes sin partículas. En pacientes tratados con filgrastim diluido a concentraciones inferiores de 1,5 MUI (15 μg) por ml, debe añadirse albúmina sérica humana (ASH) a una concentración final de 2 mg/ml. Ejemplo: si el volumen de inyección final es de 20 ml y la dosis total de filgrastim inferior a 30 MUI (300 μg), deben administrarse 0,2 ml de una solución de albúmina humana 200 mg/ml (al 20 %). Cuando se diluye Tevagrastim en una solución para perfusión de glucosa 50 mg/ml (al 5 %), es compatible con el vidrio y diversos plásticos como PVC, poliolefina (copolímero de polipropileno y polietileno) y polipropileno.
Tras la dilución: la estabilidad química y física de la solución diluida para perfusión ha sido demostrada durante 24 horas almacenada entre 2 y 8 ºC. Desde el punto de vista microbiológico, el producto debe ser usado inmediatamente. Si no se usa inmediatamente, el tiempo y las condiciones de almacenamiento de la solución diluida son responsabilidad del usuario y normalmente no deberían sobrepasar las 24 horas entre 2 y 8 ºC, a no ser que la dilución se haya realizado en condiciones de asepsia validadas y controladas.
Uso de la jeringa precargada con protector de seguridad para la aguja
El protector de seguridad para la aguja cubre ésta tras haber realizado la inyección con el fin de prevenir pinchazos accidentales. Ello no afecta a la forma de utilizar la jeringa. Empujar el émbolo lenta y uniformemente hasta que se haya administrado la totalidad de la dosis y el émbolo no pueda seguir avanzando. Retirar la jeringa manteniendo la presión sobre el émbolo. El protector de seguridad para la aguja cubrirá ésta una vez que se suelte el émbolo.
Eliminación
La eliminación del medicamento no utilizado y de todos los materiales que hayan estado en contacto con él, se realizará de acuerdo con la normativa local.
Prospecto: información para el usuario
Tevagrastim 30 MUI/0,5 ml solución inyectable y para perfusión
Tevagrastim 48 MUI/0,8 ml solución inyectable y para perfusión
filgrastim
Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene información importante para usted.
- Conserve este prospecto, ya que puede tener que volver a leerlo.
- Si tiene alguna duda, consulte a su médico, farmacéutico o enfermero.
- Este medicamento se le ha recetado solamente a usted, y no debe dárselo a otras personas aunque tengan los mismos síntomas que usted, ya que puede perjudicarles.
- Si experimenta efectos adversos, consulte a su médico, farmacéutico o enfermero, incluso si se trata de efectos adversos que no aparecen en este prospecto. Ver sección 4.
Contenido del prospecto
- Qué es Tevagrastim y para qué se utiliza
- Qué necesita saber antes de empezar a usar Tevagrastim
- Cómo usar Tevagrastim
- Posibles efectos adversos
- Conservación de Tevagrastim
- Contenido del envase e información adicional
- Información para auto-inyectarse
- Esta información está destinada únicamente a profesionales del sector sanitario
- Qué es Tevagrastim y para qué se utiliza
Qué es Tevagrastim
Tevagrastim es un factor de crecimiento de glóbulos blancos (factor estimulante de las colonias de granulocitos) y pertenece a un grupo de medicamentos llamados citocinas. Los factores de crecimiento son proteínas que se producen de manera natural en el cuerpo, pero también pueden producirse usando ingeniería genética para su uso como medicamento. Tevagrastim funciona haciendo que la médula ósea produzca más glóbulos blancos.
Para qué se utiliza Tevagrastim
Una reducción en el número de glóbulos blancos (neutropenia) se puede producir por varias razones y hace que su cuerpo sea menos eficaz a la hora de combatir las infecciones. Tevagrastim estimula la médula ósea para que produzca nuevos glóbulos blancos rápidamente.
Tevagrastim se puede utilizar:
- para aumentar el número de glóbulos blancos tras el tratamiento con quimioterapia para ayudar a prevenir infecciones;
- para aumentar el número de glóbulos blancos tras un trasplante de médula ósea para ayudar a prevenir infecciones;
- antes de la quimioterapia a dosis altas para hacer que la médula ósea produzca más células madre, que pueden ser recogidas y devueltas a su organismo después del tratamiento. Estas células se pueden recoger de usted o de un donante. Las células madre volverán entonces a la médula ósea y producirán células sanguíneas;
- para aumentar el número de glóbulos blancos si presenta neutropenia crónica grave para ayudar a prevenir infecciones;
- para ayudar a reducir el riesgo de infecciones en pacientes con infección avanzada por el VIH.
- Qué necesita saber antes de empezar a usar Tevagrastim
No use Tevagrastim
- si es alérgico al filgrastim o a alguno de los demás componentes de este medicamento (incluidos en la sección 6).
Advertencias y precauciones
Consulte a su médico, farmacéutico o enfermero antes de empezar a usar Tevagrastim.
Informe a su médico antes de empezar el tratamiento si tiene:
- anemia de células falciformes, ya que este medicamento puede causar crisis de células falciformes;
- osteoporosis (enfermedad ósea).
Informe a su médico inmediatamente durante el tratamiento con Tevagrastim si:
- tiene signos repentinos de alergia, tales como erupción, picor o urticaria en la piel, hinchazón de la cara, labios, lengua u otras partes del cuerpo, falta de aliento, sibilancias o problemas al respirar, ya que podrían ser signos de una reacción alérgica grave (hipersensibilidad);
- presenta hinchazón en la cara o los tobillos, sangre en la orina u orina de color marrón o si nota que orina con menor frecuencia de lo habitual (glomerulonefritis);
- presenta dolor en la parte superior izquierda del vientre (dolor abdominal), dolor debajo de la caja torácica izquierda o en el extremo izquierdo del hombro (estos pueden ser síntomas de un bazo agrandado [esplenomegalia] o una posible rotura del bazo);
- nota sangrados o cardenales inusuales (estos pueden ser síntomas de una disminución de las plaquetas en sangre [trombocitopenia], con una capacidad reducida de la sangre para coagularse);
- tiene síntomas de inflamación de la aorta (el vaso sanguíneo grande que transporta sangre desde el corazón hasta el resto del cuerpo), esto rara vez se ha notificado en pacientes con cáncer y en donantes sanos. Los síntomas pueden incluir fiebre, dolor abdominal, malestar general, dolor de espalda y marcadores inflamatorios aumentados. Informe a su médico si presenta estos síntomas.
Pérdida de respuesta a filgrastim
Si experimenta una pérdida de respuesta o si no se consigue mantener la respuesta al tratamiento con filgrastim, su médico investigará las causas incluyendo si ha desarrollado anticuerpos que puedan neutralizar la actividad de filgrastim.
Puede que su médico quiera supervisarle estrechamente, ver sección 4 del prospecto. Si usted es un paciente con neutropenia crónica grave, puede estar en riesgo de desarrollar cáncer de la sangre (leucemia, síndrome mielodisplásico [SMD]). Hable con su médico acerca de los riesgos de desarrollar cáncer de la sangre y de las pruebas que se deben realizar. Si desarrolla o es probable que desarrolle cáncer de la sangre, no debe utilizar Tevagrastim a menos que lo indique su médico.
Si usted es un donante de células madre, debe tener entre 16 y 60 años de edad.
Tenga especial cuidado con otros productos que estimulan los glóbulos blancos
Tevagrastim pertenece a un grupo de medicamentos que estimula la producción de glóbulos blancos. Su médico debe registrar siempre el producto exacto que esté utilizando.
Otros medicamentos y Tevagrastim
Informe a su médico o farmacéutico si está utilizando, ha utilizado recientemente o pudiera tener que utilizar cualquier otro medicamento.
Embarazo y lactancia
Tevagrastim no ha sido estudiado en mujeres embarazadas o en periodo de lactancia.
No se recomienda Tevagrastim durante el embarazo.
Es importante que informe a su médico si usted:
- está embarazada o en periodo de lactancia;
- cree que podría estar embarazada; o
- tiene intención de quedarse embarazada.
Si se queda embarazada durante el tratamiento con Tevagrastim, informe a su médico. A menos que su médico le indique lo contrario, debe dejar de dar el pecho si utiliza Tevagrastim.
Conducción y uso de máquinas
La influencia de Tevagrastim sobre su capacidad para conducir y usar máquinas es pequeña. Este medicamento puede producir mareos. Es aconsejable esperar y ver cómo se siente tras la administración del medicamento antes de conducir o manejar maquinaria.
Tevagrastim contiene sorbitol
Este medicamento contiene 50 mg de sorbitol en cada ml.
Para administración por vía intravenosa
El sorbitol es una fuente de fructosa. Si usted (o su hijo) padecen intolerancia hereditaria a la fructosa (IHF), una enfermedad genética rara, usted (o su hijo) no deben recibir este medicamento. Los pacientes con IHF no pueden descomponer la fructosa, lo que puede causar efectos adversos graves. Consulte con su médico antes de recibir este medicamento si usted (o su hijo) padecen IHF o si su hijo no puede tomar alimentos o bebidas dulces porque les produce mareos, vómitos o efectos desagradables como hinchazón, calambres en el estómago o diarrea.
Tevagrastim contiene sodio
Este medicamento contiene menos de 1 mmol de sodio (23 mg) por jeringa precargada; esto es, esencialmente “exento de sodio”.
- Cómo usar Tevagrastim
Siga exactamente las instrucciones de administración de este medicamento indicadas por su médico o farmacéutico. En caso de duda, consulte de nuevo a su médico o farmacéutico.
¿Cómo se administra Tevagrastim y cuánto debo tomar?
Tevagrastim se administra por lo general una vez al día como una inyección en el tejido justo debajo de la piel (conocida como inyección subcutánea). También se puede administrar una vez al día como una inyección lenta en la vena (conocida como perfusión intravenosa). La dosis habitual varía en función de su enfermedad y peso. Su médico le indicará la cantidad de Tevagrastim que debe tomar.
Pacientes con trasplante de médula ósea después de la quimioterapia:
Normalmente recibirá su primera dosis de Tevagrastim al menos 24 horas después de la quimioterapia y al menos 24 horas después de recibir su trasplante de médula ósea.
A usted o a las personas que le atienden se les puede enseñar a administrar inyecciones subcutáneas para que pueda continuar el tratamiento en su casa. Sin embargo, no debe intentarlo a menos que su profesional sanitario le haya entrenado de forma adecuada.
¿Cuánto tiempo tengo que tomar Tevagrastim?
Tendrá que tomar Tevagrastim hasta que su recuento de glóbulos blancos sea normal. Se le realizarán análisis de sangre periódicos para supervisar el número de glóbulos blancos en su cuerpo. Su médico le indicará cuanto tiempo necesita tomar Tevagrastim.
Uso en niños
Tevagrastim se utiliza para tratar a niños que están recibiendo quimioterapia o que presentan un recuento de glóbulos blancos bajo (neutropenia) grave. La dosis administrada a los niños que están recibiendo quimioterapia es la misma que para los adultos.
Si usa más Tevagrastim del que debe
No aumente la dosis que le ha recetado su médico. Si ha utilizado más Tevagrastim del que debe, póngase en contacto con su médico, o farmacéutico tan pronto como sea posible.
Si olvidó usar Tevagrastim
Si ha olvidado una inyección, o si se inyectó menos dosis, contacte con su médico tan pronto como sea posible. No tome una dosis doble para compensar las dosis olvidadas.
Si tiene cualquier otra duda sobre el uso de este medicamento, pregunte a su médico, farmacéutico o enfermero.
- Posibles efectos adversos
Al igual que todos los medicamentos, este medicamento puede producir efectos adversos, aunque no todas las personas los sufran.
Efectos adversos importantes
Es importante que contacte a su médico inmediatamente:
- si experimenta una reacción alérgica, incluida debilidad, caída de la presión arterial, dificultad para respirar, hinchazón de la cara (anafilaxia), erupción cutánea, erupción cutánea con picor (urticaria), hinchazón de la cara, labios, boca, lengua o garganta (angioedema) y falta de aliento (disnea);
- si experimenta tos, fiebre y dificultad para respirar (disnea), ya que puede ser un signo del síndrome de dificultad respiratoria aguda (SDRA);
- si experimenta daño renal (glomerulonefritis). Se ha observado daño renal en pacientes que recibían filgrastim. Contacte con su médico inmediatamente si observa hinchazón en la cara o los tobillos, sangre en la orina u orina de color marrón, o nota que orina con menor frecuencia de lo habitual;
- si experimenta alguno o una combinación de los siguientes efectos adversos:
- hinchazón que puede estar asociada con orinar con una menor frecuencia, dificultad para respirar, hinchazón y sensación de plenitud abdominal y una sensación general de cansancio. Estos síntomas generalmente se desarrollan rápidamente.
Estos pueden ser síntomas de una enfermedad llamada “síndrome de fuga capilar” y que puede causar que la sangre se escape de un pequeño vaso sanguíneo hacia otros lugares de su cuerpo y necesite atención médica urgente.
- si experimenta una combinación de los siguientes síntomas:
- fiebre, escalofríos o sensación de mucho frío, frecuencia cardiaca alta, confusión o desorientación, dificultad para respirar, dolor extremo o malestar y piel húmeda o sudorosa.
Estos podrían ser síntomas de una afección llamada “sepsis” (también llamada “intoxicación sanguínea”), una infección grave con respuesta inflamatoria de todo el cuerpo que puede ser potencialmente mortal y requiere atención médica urgente;
- si experimenta dolor en la parte superior izquierda del vientre (dolor abdominal), dolor en el lado inferior izquierdo de la caja torácica o dolor en el extremo del hombro, ya que se podría tratar de algún problema con su bazo (agrandamiento del bazo [esplenomegalia] o rotura del bazo);
- si está siendo tratado por neutropenia crónica grave y tiene sangre en la orina (hematuria). Su médico le realizará análisis de orina periódicos si experimenta este efecto adverso o si se encuentran proteínas en su orina (proteinuria).
Un efecto adverso frecuente del uso de Tevagrastim es dolor en los músculos o huesos (dolor musculoesquelético), que se puede remediar tomando medicamentos habituales para aliviar el dolor (analgésicos). En los pacientes sometidos a un trasplante de células madre o de médula ósea, puede aparecer enfermedad del injerto contra huésped (EICH). Esta es una reacción de las células del donante contra el paciente que recibe el trasplante; los signos y síntomas incluyen erupciones en las palmas de las manos o las plantas de los pies, y úlceras y llagas en la boca, intestino, hígado, piel, ojos, pulmones, vagina y articulaciones.
En donantes sanos de células madre se puede observar un incremento de los glóbulos blancos (leucocitosis) y una disminución de las plaquetas que puede reducir la capacidad de su sangre para coagularse (trombocitopenia). Estos efectos serán vigilados por su médico.
Puede experimentar los siguientes efectos adversos:
Muy frecuentes(pueden afectar a más de 1 de cada 10 personas):
- Disminución de las plaquetas, lo que reduce la capacidad de la sangre de coagularse (trombocitopenia)
- Recuento bajo de glóbulos rojos (anemia)
- Dolor de cabeza
- Diarrea
- Vómitos
- Náuseas
- Pérdida o debilitamiento del cabello inusual (alopecia)
- Cansancio (fatiga)
- Irritación e hinchazón del revestimiento del tubo digestivo que va de la boca al ano (inflamación de la mucosa)
- Fiebre (pirexia)
Frecuentes(pueden afectar hasta 1 de cada 10 personas):
- Inflamación de los pulmones (bronquitis)
- Infección del tracto respiratorio superior
- Infección del tracto urinario
- Apetito disminuido
- Problemas para dormir (insomnio)
- Mareos
- Disminución de la sensibilidad, especialmente en la piel (hipoestesia)
- Hormigueo o entumecimiento de las manos o los pies (parestesia)
- Tensión arterial baja (hipotensión)
- Tensión arterial alta (hipertensión)
- Tos
- Tos con sangre (hemoptisis)
- Dolor en la boca y garganta (dolor orofaríngeo)
- Hemorragia nasal (epistaxis)
- Estreñimiento
- Dolor oral
- Aumento del tamaño del hígado (hepatomegalia)
- Erupción
- Enrojecimiento de la piel (eritema)
- Calambre muscular
- Dolor al orinar (disuria)
- Dolor en el pecho
- Dolor
- Debilidad generalizada (astenia)
- Sensación de malestar (malestar general)
- Hinchazón en manos y pies (edema periférico)
- Aumento de ciertas enzimas en la sangre
- Cambios en el análisis bioquímico de la sangre
- Reacción a la transfusión
Poco frecuentes(pueden afectar hasta 1 de cada 100 personas):
- Aumento de los glóbulos blancos de la sangre (leucocitosis)
- Reacción alérgica (hipersensibilidad)
- Rechazo del trasplante de médula ósea (enfermedad del injerto contra el huésped)
- Niveles altos de ácido úrico en la sangre, que pueden causar gota (hiperuricemia) (ácido úrico elevado en sangre)
- Daño hepático causado por el bloqueo de las pequeñas venas del hígado (enfermedad venooclusiva)
- Los pulmones no funcionan como deberían causando falta de aliento (insuficiencia respiratoria)
- Hinchazón o fluido en los pulmones (edema pulmonar)
- Inflamación de los pulmones (enfermedad pulmonar intersticial)
- Radiografías anormales de los pulmones (infiltración pulmonar)
- Sangrado de los pulmones (hemorragia pulmonar)
- Falta de absorción de oxígeno en los pulmones (hipoxia)
- Erupción cutánea irregular (erupción maculopapular)
- Enfermedad que hace que los huesos pierdan densidad haciéndolos más débiles, más frágiles y propensos a romperse (osteoporosis)
- Reacción en la zona de inyección
Raros(pueden afectar hasta 1 de cada 1.000 personas):
- Dolor intenso en los huesos, pecho, intestinos o articulaciones (anemia de células falciformes con crisis)
- Reacciones alérgicas repentinas y que pueden poner en peligro la vida (reacción anafiláctica)
- Hinchazón y dolor en las articulaciones, similar a la gota (pseudogota)
- Un cambio en la forma en que su cuerpo regula los fluidos corporales que puede resultar en hinchazón (alteraciones del volumen de fluidos)
- Inflamación de los vasos sanguíneos de la piel (vasculitis cutánea)
- Úlceras dolorosas, inflamadas y de color rojo oscuro en las extremidades y, a veces, en la cara y el cuello que cursan con fiebre (síndrome de Sweet)
- Empeoramiento de la artritis reumatoide
- Cambios inusuales en la orina
- Disminución de la densidad ósea
- Inflamación de la aorta (el vaso sanguíneo grande que transporta sangre desde el corazón hasta el resto del cuerpo), ver sección 2
Comunicación de efectos adversos
Si experimenta cualquier tipo de efecto adverso, consulte a su médico, farmacéutico o enfermero, incluso si se trata de posibles efectos adversos que no aparecen en este prospecto. También puede comunicarlos directamente a través del sistema nacional de notificación incluido en el Apéndice V. Mediante la comunicación de efectos adversos usted puede contribuir a proporcionar más información sobre la seguridad de este medicamento.
- Conservación de Tevagrastim
Mantener este medicamento fuera de la vista y del alcance de los niños.
No utilice este medicamento después de la fecha de caducidad que aparece en la caja y en la jeringa precargada después de EXP. La fecha de caducidad es el último día del mes que se indica.
Conservar en nevera (entre 2 ºC y 8 ºC).
Dentro de su periodo de validez y para su uso ambulatorio, el medicamento puede sacarse de la nevera (2 ºC – 8 ºC) y almacenarse a una temperatura de hasta 25 ºC durante un único periodo de hasta 4 días. Si el medicamento no se ha usado en esos 4 días, se debe volver a refrigerar (2 ºC – 8 ºC) hasta la fecha de caducidad. Se deben eliminar las jeringas almacenadas a más de 8 ºC durante más de 4 días.
No utilice este medicamento si observa turbidez o partículas en el interior.
Los medicamentos no se deben tirar por los desagües. Pregunte a su farmacéutico cómo deshacerse de los envases y de los medicamentos que ya no necesita. De esta forma, ayudará a proteger el medio ambiente.
- Contenido del envase e información adicional
Composición de Tevagrastim
- El principio activo es filgrastim. Cada ml de solución para inyección y perfusión contiene 60 millones de unidades internacionales (MUI) (600 microgramos) de filgrastim.
Tevagrastim 30 MUI/0,5 ml: cada jeringa precargada contiene 30 millones de unidades internacionales [MUI] (300 microgramos) de filgrastim en 0,5 ml de solución.
Tevagrastim 48 MUI/0,8 ml: cada jeringa precargada contiene 48 millones de unidades internacionales [MUI] (480 microgramos) de filgrastim en 0,8 ml de solución.
- Los demás componentes son: hidróxido de sodio, ácido acético glacial, sorbitol, polisorbato 80, agua para preparaciones inyectables.
Aspecto del producto y contenido del envase
Tevagrastim es una solución para inyección y perfusión en una jeringa precargada. Tevagrastim es una solución transparente e incolora. Cada jeringa precargada contiene 0,5 ml o 0,8 ml de solución.
Tevagrastim se suministra en envases de 1, 5 o 10 jeringas precargadas o en envases múltiples que contienen 10 jeringas precargadas (2 envases de 5) con aguja de inyección y con o sin protector de seguridad para la aguja. Puede que no se comercialicen todos los formatos.
Titular de la autorización de comercialización
TEVA GmbH
Graf-Arco-Straße 3
89079 Ulm
Alemania
Responsable de la fabricación
Teva Pharma B.V.
Swensweg 5
2031 GA Haarlem
Países Bajos
Merckle GmbH
Graf-Arco-Straße 3
89079 Ulm
Alemania
Pueden solicitar más información respecto a este medicamento dirigiéndose al representante local del titular de la autorización de comercialización:
België/Belgique/Belgien Teva Pharma Belgium N.V./S.A./AG Tél/Tel: +32 38207373 | Lietuva UAB Teva Baltics Tel: +370 52660203 |
| Luxembourg/Luxemburg Teva Pharma Belgium N.V./S.A./AG Belgique/Belgien Tél/Tel: +32 38207373 |
Ceská republika Teva Pharmaceuticals CR, s.r.o. Tel: +420 251007111 | Magyarország Teva Gyógyszergyár Zrt. Tel: +36 12886400 |
Danmark Teva Denmark A/S Tlf: +45 44985511 | Malta Teva Pharmaceuticals Ireland L-Irlanda Tel: +44 2075407117 |
Deutschland TEVA GmbH Tel: +49 73140208 | Nederland Teva Nederland B.V. Tel: +31 8000228400 |
Eesti UAB Teva Baltics Eesti filiaal Tel: +372 6610801 | Norge Teva Norway AS Tlf: +47 66775590 |
Ελλáδα TEVA HELLAS Α.Ε. Τηλ: +30 2118805000 | Österreich ratiopharm Arzneimittel Vertriebs-GmbH Tel: +43 1970070 |
España Teva Pharma, S.L.U. Tel: +34 913873280 | Polska Teva Pharmaceuticals Polska Sp. z o.o. Tel: +48 223459300 |
France Teva Santé Tél: +33 155917800 | Portugal Teva Pharma - Produtos Farmacêuticos, Lda. Tel: +351 214767550 |
Hrvatska Pliva Hrvatska d.o.o. Tel: +385 13720000 | România Teva Pharmaceuticals S.R.L. Tel: +40 212306524 |
Ireland Teva Pharmaceuticals Ireland Tel: +44 2075407117 | Slovenija Pliva Ljubljana d.o.o. Tel: +386 15890390 |
Ísland Teva Pharma Iceland ehf. Sími: +354 5503300 | Slovenská republika TEVA Pharmaceuticals Slovakia s.r.o. Tel: +421 257267911 |
Italia Teva Italia S.r.l. Tel: +39 028917981 | Suomi/Finland Teva Finland Oy Puh/Tel: +358 201805900 |
Κúπρος TEVA HELLAS Α.Ε. Ελλáδα Τηλ: +30 2118805000 | Sverige Teva Sweden AB Tel: +46 42121100 |
Latvija UAB Teva Baltics filiale Latvija Tel: +371 67323666 | United Kingdom (Northern Ireland) Teva Pharmaceuticals Ireland Ireland Tel: +44 2075407117 |
Fecha de la última revisión de este prospecto:
La información detallada de este medicamento está disponible en la página web de la Agencia Europea de Medicamentos: http://www.ema.europa.eu.
- Información para auto-inyectarse
Esta sección contiene información de cómo administrarse a uno mismo una inyección de Tevagrastim. Es importante que no trate de administrarse una inyección sin haber recibido el curso necesario por su médico o enfermero. También es importante que disponga de una jeringa en un envase de seguridad a prueba de pinchazos. Si no esta seguro de poder inyectarse o si tiene cualquier duda, consulte a su médico o enfermero.
Es importante que deseche en un envase a prueba de pinchazos las jeringas usadas.
Cómo auto-inyectarse Tevagrastim
Deberá inyectarse en el tejido justo bajo la piel. Esto se conoce como inyección subcutánea. La inyección deberá administrarse todos los días aproximadamente a la misma hora.
Equipo necesario para la administración
Para la administración de la inyección subcutánea, se necesita lo siguiente:
- una jeringa precargada de Tevagrastim,
- algodón o similar con alcohol,
- un recipiente, a prueba de pinchazos (envase de plástico suministrado por un hospital o farmacia) para desechar las jeringas usadas de forma segura.
Qué debo hacer antes de administrarme una inyección subcutánea de Tevagrastim
- Procurar administrar la inyección aproximadamente a la misma hora todos los días.
- Sacar la jeringa precargada de Tevagrastim del frigorífico.
- Comprobar la fecha de caducidad que indica la jeringa precargada (EXP). No usarla si la fecha es superior al último día del mes que aparece.
- Comprobar la apariencia de Tevagrastim. Debe ser un líquido transparente e incoloro. Si hay partículas en el interior, no debe utilizarlo.
- Para una inyección más cómoda, deje reposar la jeringa precargada durante 30 minutos a temperatura ambiente o tome la jeringa precargada con suavidad en sus manos durante unos minutos. No caliente Tevagrastim de otra manera (por ejemplo, no lo caliente en un microondas ni en agua caliente)
- Noretire la tapa de la jeringa hasta que este listo para la inyección
- Lávese las manos cuidadosamente.
- Buscar un lugar cómodo y bien iluminado y colocar todo lo necesario al alcance (la jeringa precargada de Tevagrastim, algodón y el recipiente para desechos).
Cómo debo preparar mi inyección de Tevagrastim
Antes de inyectar Tevagrastim hay que:
- Coger la jeringa y quitar la cubierta protectora de la aguja suavemente sin inclinarla. Empujar el émbolo. Separar tal como se indica en las figuras 1 y 2. No toque la aguja ni empuje el embolo.
|
|
- Puede aparecer una pequeña burbuja de aire en la jeringa precargada. Si hay burbujas, de golpecitos con sus dedos en la jeringa hasta que las burbujas vayan al final de la jeringa. Con la jeringa apuntando hacia arriba extraiga el aire de la jeringa empujando el embolo.
- La jeringa tiene una escala. Empuje el embolo hasta el número (ml) de la jeringa que corresponde con la dosis de Tevagrastim prescrita por su medico.
- Compruebe de nuevo que la dosis de Tevagrastim es la correcta.
- Ahora puede utilizar la jeringa precargada.
En qué lugar debo poner la inyección
Los sitios más adecuados para la inyección son:
- la parte superior de los muslos; y
- el abdomen, excepto la zona alrededor del ombligo (ver imagen 3).
|
|
Si alguien le administra la inyección también podrá utilizar la parte posterior de sus antebrazos (ver imagen 4)
Para evitar el riesgo de dolor en un punto dado es mejor cambiar cada día el lugar de la inyección.
Cómo debo inyectarme
- Desinfecte el lugar de la inyección usando un algodón con alcohol y pellizcar la piel entre el pulgar y el índice, sin apretar (ver imagen 5).
- Insertar completamente la aguja en la piel tal como le indicó su enfermero o médico (ver imagen 6).
- Tirar ligeramente del émbolo para asegurarse de que no se ha pinchado una vena. Si se ve sangre en la jeringa, retirar la aguja e insertarla en otro lugar.
- Inyectar el líquido lenta y regularmente, manteniendo siempre la piel pellizcada.
- Inyecte únicamente la dosis prescrita por su médico.
- Tras inyectar el líquido, retirar la aguja y soltar la piel.
- Use solo una jeringa para una sola inyección. No utilice ningún resto de Tevagrastim sobrante de la jeringa.
|
|
Recuerde
Si tiene cualquier duda, pida ayuda o consejos a su médico o su enfermero.
Cómo desechar las jeringas usadas
- No volver a poner la cubierta protectora en las jeringas ya usadas.
- Poner las jeringas usadas en un recipiente de seguridad a prueba de pinchazos y guarde este recipiente fuera del alcance y de la vista de los niños.
- Deposite el recipiente lleno según las indicaciones del médico, enfermero o farmacéutico.
- Nunca tirar las jeringas usadas en el cubo de basura habitual.
- Esta información está destinada únicamente a profesionales del sector sanitario
Tevagrastim no contiene conservantes. En vista de un posible riesgo de contaminación microbiana, las jeringas precargadas de Tevagrastim son para un solo uso.
La exposición accidental a temperaturas de congelación no afecta negativamente a la estabilidad de Tevagrastim.
Tevagrastim no debe diluirse con cloruro de sodio. Este medicamento no debe mezclarse con otros medicamentos excepto con los mencionados a continuación. La dilución de filgrastim puede ser adsorbida por el vidrio y materiales plásticos excepto si se diluye como se menciona a continuación.
Tevagrastim se puede diluir, si es necesario, en una solución para perfusión de glucosa 50 mg/ml (al 5 %). No se recomienda en ningún caso diluir a concentraciones finales inferiores a 0,2 MUI (2 μg) por ml. La solución debe inspeccionarse visualmente antes de usarla. Solamente deben utilizarse soluciones transparentes sin partículas. En pacientes tratados con filgrastim diluido a concentraciones inferiores de 1,5 MUI (15 μg) por ml, debe añadirse albúmina sérica humana (ASH) a una concentración final de 2 mg/ml. Ejemplo: si el volumen de inyección final es de 20 ml y la dosis total de filgrastim inferior a 30 MUI (300 μg), deben administrarse 0,2 ml de una solución de albúmina humana 200 mg/ml (al 20 %). Cuando se diluye Tevagrastim en una solución para perfusión de glucosa 50 mg/ml (al 5 %), es compatible con el vidrio y diversos plásticos como PVC, poliolefina (copolímero de polipropileno y polietileno) y polipropileno.
Tras la dilución: la estabilidad química y física de la solución diluida para perfusión ha sido demostrada durante 24 horas almacenada entre 2 y 8 ºC. Desde el punto de vista microbiológico, el producto debe ser usado inmediatamente. Si no se usa inmediatamente, el tiempo y las condiciones de almacenamiento de la solución diluida son responsabilidad del usuario y normalmente no deberían sobrepasar las 24 horas entre 2 y 8 ºC, a no ser que la dilución se haya realizado en condiciones de asepsia validadas y controladas.
Uso de la jeringa precargada sin protector de seguridad para la aguja
Administrar la dosis según el protocolo estándar.
Eliminación
La eliminación del medicamento no utilizado y de todos los materiales que hayan estado en contacto con él, se realizará de acuerdo con la normativa local.
- País de registro
- Principio activo
- Requiere recetaSí
- Fabricante
- Esta información es de carácter general y no sustituye la consulta con un profesional sanitario.
- Alternativas a TEVAGRASTIM 48 MU/0,8 ml SOLUCION PARA INYECCION O PERFUSIONForma farmacéutica: INYECTABLE, 12 MU/0,2 mlPrincipio activo: FilgrastimFabricante: Accord Healthcare S.L.U.Requiere recetaForma farmacéutica: INYECTABLE, 0,3 mg / jeringa precargadaPrincipio activo: FilgrastimFabricante: Accord Healthcare S.L.U.Requiere recetaForma farmacéutica: INYECTABLE, 0,3 mg / jeringa precargadaPrincipio activo: FilgrastimFabricante: Accord Healthcare S.L.U.Requiere receta
Médicos online para TEVAGRASTIM 48 MU/0,8 ml SOLUCION PARA INYECCION O PERFUSION
Comenta la dosis, los posibles efectos secundarios, interacciones, contraindicaciones o la revisión de receta de TEVAGRASTIM 48 MU/0,8 ml SOLUCION PARA INYECCION O PERFUSION, sujeto a valoración médica y a la normativa local.
Preguntas frecuentes






 1
1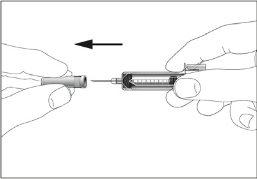 2
2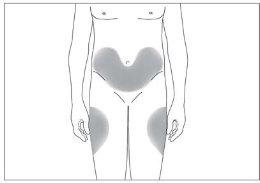 3
3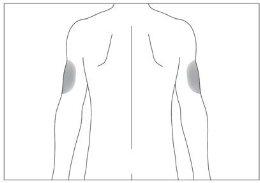 4
4
 1
1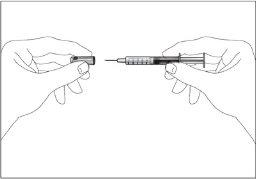 2
2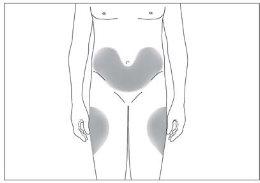 3
3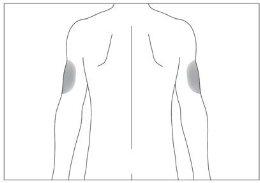 4
4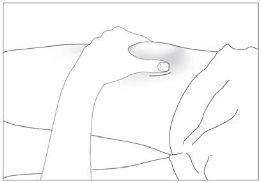 5
5 6
6
