
SUMATRIPTAN CFOURHEALTH 6 MG SOLUCION INYECTABLE EN PLUMA PRECARGADA EFG

Cómo usar SUMATRIPTAN CFOURHEALTH 6 MG SOLUCION INYECTABLE EN PLUMA PRECARGADA EFG
Traducción generada por IA
Este contenido ha sido traducido automáticamente y se ofrece solo con fines informativos. No sustituye la consulta con un profesional sanitario.
Ver originalContenido del prospecto
Introducción
Prospecto: información para el paciente
Sumatriptán CFOURHEALTH 6mg solución inyectable en pluma precargada EFG
Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene información importante para usted.
- Conserve este prospecto, ya que puede tener que volver a leerlo.
- Si tiene alguna duda, consulte a su médico o farmacéutico.
- Este medicamento se le ha recetado solamente a usted, y no debe dárselo a otras personas aunque tengan los mismos síntomas que usted, ya que puede perjudicarles.
- Si experimenta efectos adversos, consulte a su médico o farmacéutico, incluso si se trata de posibles efectos adversos que no aparecen en este prospecto. Ver sección 4.
Contenido del prospecto
- Qué es Sumatriptán CFOURHEALTH y para qué se utiliza
- Qué necesita saber antes de empezar a usar Sumatriptán CFOURHEALTH
- Cómo usar Sumatriptán CFOURHEALTH
- Posibles efectos adversos
- Conservación de Sumatriptán CFOURHEALTH
- Contenido del envase e información adicional
- Instrucciones de uso
1. Qué es Sumatriptán CFOURHEALTH y para qué se utiliza
Sumatriptán CFOURHEALTH contiene el principio activo sumatriptán, que pertenece a un grupo de medicamentos llamados triptanos (agonistas de los receptores 5-HT1).
Sumatriptán se utiliza para tratar la migraña y una rara afección llamada cefalea en brotes.
La causa de los síntomas de la migraña y la cefalea en brotes puede ser el ensanchamiento temporal de los vasos sanguíneos de la cabeza. Se cree que el sumatriptán reduce el ensanchamiento de estos vasos sanguíneos. Esto, a su vez, ayuda a quitar el dolor de cabeza y a aliviar otros síntomas, como la sensación de malestar (náuseas o vómitos) y la sensibilidad a la luz y al sonido.
2. Qué necesita saber antes de empezar a usar Sumatriptán CFOURHEALTH
No use Sumatriptán CFOURHEALTH
- si es alérgico al sumatriptán o a alguno de los demás componentes de este medicamento (incluidos en la sección 6).
- si tiene un problema cardíaco, como el estrechamiento de las arterias (cardiopatía isquémica) o dolores en el pecho (angina de pecho), o si ya ha sufrido un infarto
- si tiene problemas de circulación en las piernas o en los brazos que le provocan dolores parecidos a calambres cuando camina (enfermedad vascular periférica)
- si ha sufrido un ictus (también llamado accidente cerebrovascular o ACV) o un mini-ictus (también llamado accidente isquémico transitorio o AIT)
- si tiene una presión arterial no controlada leve o alta. Es posible que pueda utilizar Sumatriptán CFOURHEALTH si su presión arterial alta es leve y está siendo tratada
- si tiene una enfermedad hepática grave
- con otros medicamentos para la migraña, incluidos los que contienen ergotamina, o medicamentos similares como el maleato de metisergida; o cualquier triptano o agonista 5-HT1 (como el naratriptán, el rizatriptán o el zolmitriptán; ver sección «Otros medicamentos y Sumatriptán CFOURHEALTH».
- con cualquiera de los siguientes antidepresivos:
- IMAO (inhibidores de la monoaminoxidasa) o si ha tomado un IMAO en las últimas 2 semanas; ver sección «Otros medicamentos y Sumatriptán CFOURHEALTH».
Si alguno de estos casos le aplica:
Informe a su médico y no utilice Sumatriptán CFOURHEALTH.
Advertencias y precauciones
Consulte a su médico o farmacéutico antes de empezar a usar Sumatriptán CFOURHEALTH.
Factores de riesgo adicionales
- Si usted es un fumador empedernido o está utilizando un tratamiento sustitutivo con nicotina, y especialmente
- si usted es un hombre de más de 40 años, o
- si usted es una mujer que ha pasado por la menopausia
En casos muy raros, las personas han desarrollado afecciones cardíacas graves después de usar sumatriptán, aunque antes no tuvieran signos de enfermedad cardíaca. Si alguno de los puntos anteriores le es aplicable, podría significar que tiene un mayor riesgo de desarrollar una enfermedad cardíaca, así que:
- Informe a su médico para que pueda comprobar su función cardíaca antes de que se le recete Sumatriptán CFOURHEALTH.
Si tiene antecedentes de ataques epilépticos (convulsiones)
o si tiene otras afecciones que puedan hacer más probable que tenga un ataque (por ejemplo, una lesión en la cabeza o alcoholismo):
- Informe a su médico para que se le supervise más estrechamente.
Si ha tenido hipertensión arterial.
Sumatriptán puede no ser adecuado para usted.
- Informe a su médico o farmacéutico antes de empezar a usar Sumatriptán CFOURHEALTH.
Si tiene una enfermedad hepática o renal
Si cualquiera de estos casos le es aplicable:
- Informe a su médico o farmacéutico antes de empezar a usar Sumatriptán CFOURHEALTH.
Si es alérgico a los antibióticos llamados sulfonamidas
Si es así, también puede ser alérgico al sumatriptán. Si sabe que es alérgico a un antibiótico pero no está seguro de que sea una sulfonamida:
- Informe a su médico o farmacéutico antes de empezar a usar Sumatriptán CFOURHEALTH.
Si está tomando antidepresivos llamados ISRS
(Inhibidores selectivos de la recaptación de serotonina) o IRSN (inhibidores de la recaptación de serotonina y noradrenalina):
- Informe a su médico o farmacéutico antes de empezar a usar sumatriptán. Vea también «Otros medicamentos y Sumatriptán CFOURHEALTH», más abajo.
La jeringa de Sumatriptán CFOURHEALTH puede contener látex
El capuchón transparente protector de la aguja de la jeringa puede contener látex.
- Informe a su médico si es alérgico al látex.
Si utiliza Sumatriptán CFOURHEALTH con frecuencia
Utilizar Sumatriptán CFOURHEALTH con demasiada frecuencia puede empeorar sus dolores de cabeza.
- Informe a su médico si esto es aplicable a usted. Es posible que le recomiende que deje de usar sumatriptán.
Si siente dolor u opresión en el pecho después de usar Sumatriptán CFOURHEALTH
Estos efectos pueden ser intensos pero suelen pasar rápidamente. Si no se le pasan rápidamente, o se agravan, busque ayuda médica inmediatamente. La sección 4 (abajo) tiene más información sobre estos posibles efectos adversos.
Niños y adolescentes
Sumatriptán CFOURHEALTH no se recomienda para niños y adolescentes menores de 18 años. No se dispone de datos.
Personas de edad avanzada (mayores de 65 años)
Sumatriptán CFOURHEALTH no se recomienda para personas mayores de 65 años.
Otros medicamentos y Sumatriptán CFOURHEALTH
Informe a su médico o farmacéutico si está tomando, ha tomado recientemente o pudiera tener que tomar cualquier otro medicamento.
Algunos medicamentos no deben tomarse con Sumatriptán CFOURHEALTH y otros pueden causar efectos adversos si se toman con Sumatriptán CFOURHEALTH. Debe informar a su médico si está tomando:
- ergotamina - también utilizada para tratar la migraña, o medicamentos similares como el maleato de metisergida (ver sección 2 «No use Sumatriptán CFOURHEALTH»). No utilice Sumatriptán CFOURHEALTH al mismo tiempo que estos medicamentos. Deje de tomar estos medicamentos al menos 24 horas antes de usar Sumatriptán CFOURHEALTH. No vuelva a tomar ningún medicamento que contenga ergotamina o compuestos similares a la ergotamina durante al menos 6 horas después de usar Sumatriptán CFOURHEALTH.
- otros triptanos/agonistas de los receptores 5-HT1 (como naratriptán, rizatriptán y zolmitriptán), que también se utilizan para tratar la migraña, (ver sección 2 «No use Sumatriptán CFOURHEALTH»). No utilice Sumatriptán CFOURHEALTH al mismo tiempo que estos medicamentos. Deje de tomar estos medicamentos al menos 24 horas antes de usar Sumatriptán CFOURHEALTH. No tome otro triptano/agonista de los receptores 5-HT1 durante al menos 24 horas después de usar Sumatriptán CFOURHEALTH.
- Los IMAO utilizados para tratar la depresión. No utilice Sumatriptán CFOURHEALTH si los ha tomado en las últimas 2 semanas. Ver sección 2 «No use Sumatriptán CFOURHEALTH»
- Los ISRS y los IRSN que se utilizan para tratar la depresión. El uso de Sumatriptán CFOURHEALTH con estos medicamentos puede producir el síndrome serotoninérgico (un conjunto de síntomas que pueden incluir inquietud, confusión, sudoración, alucinaciones, aumento de los reflejos, espasmos musculares, escalofríos, aumento de los latidos del corazón y temblores). Informe a su médico inmediatamente si esto le afecta de esta manera.
- Hierba de San Juan (Hypericum perforatum). Tomar remedios de herbolario que contengan Hierba de San Juan mientras se usa Sumatriptán CFOURHEALTH puede hacer que sean más probables los efectos secundarios.
Embarazo y lactancia
Si está embarazada o en periodo de lactancia, cree que podría estar embarazada o tiene intención de quedarse embarazada, consulte a su médico o farmacéutico antes de utilizar este medicamento.
Únicamente existe información limitada sobre la seguridad del sumatriptán para las mujeres embarazadas, aunque hasta ahora no hay pruebas de que haya un mayor riesgo de defectos de nacimiento. Su médico le indicará si debe o no usar Sumatriptán CFOURHEALTH mientras está embarazada.
No amamante a su bebé durante 12 horas después de usar Sumatriptán CFOURHEALTH. Si se extrae leche materna durante este tiempo, deseche la leche y no se la dé a su bebé.
Conducción y uso de máquinas
Tanto los síntomas de la migraña como su medicamento pueden producirle somnolencia. Si está afectado, no conduzca ni maneje maquinaria.
Sumatriptán CFOURHEALTH contiene sodio
Este medicamento contiene menos de 1 mmol de sodio (23 mg) por 0,5 ml; esto es, esencialmente «exento de sodio».
3. Cómo usar Sumatriptán CFOURHEALTH
Siga exactamente las instrucciones de administración de este medicamento indicadas por su médico. En caso de duda, consulte de nuevo a su médico o farmacéutico.
Sumatriptán CFOURHEALTH es para vía subcutánea y suele inyectarse en la parte superior del brazo o el muslo.
Hay unaguía paso a pasopara el uso de la jeringa al final de este prospecto (ver sección 7 Instrucciones de uso).
Cuándo usar Sumatriptán CFOURHEALTH
- Es mejor utilizar sumatriptán en cuanto sienta que se avecina una migraña o una cefalea en brotes, aunque puede utilizarlo en cualquier momento durante un ataque.
- No utilice sumatriptán para tratar de prevenir un ataque, sólo hágalo después de que comiencen los síntomas de la migraña.
Cuánto utilizar
Adultos de 18 a 65 años
- La dosis habitual para adultos de 18 a 65 años con migraña o una cefalea en brotes es una inyección de 6 mg.
- Si los síntomas comienzan a reaparecer, puede aplicar una segunda inyección de Sumatriptán CFOURHEALTH si ha pasado al menos 1 hora desde la primera inyección.
- Si la primera inyección no tiene efecto, no utilice una nueva inyección ni ningún otro preparado inyectable de sumatriptán para el mismo ataque.
- Si Sumatriptán CFOURHEALTH no le proporciona ningún alivio, pida consejo a su médico o farmacéutico.
Si usa más Sumatriptán CFOURHEALTH del que debe
Usar demasiado sumatriptán podría enfermarle. Si ha utilizado más de dos inyecciones en 24 horas:
- Póngase en contacto con su médico para que le aconseje.
En caso de sobredosis o ingestión accidental, consulte inmediatamente a su médico o farmacéutico o llame al Servicio de Información Toxicológica, teléfono: 91 562 04 20, indicando el medicamento y la cantidad ingerida.
Si tiene otras dudas sobre el uso de este medicamento, pregunte a su médico o farmacéutico.
4. Posibles efectos adversos
Al igual que todos los medicamentos, este medicamento puede producir efectos adversos, aunque no todas las personas los sufran.
Algunos síntomas pueden ser causados por la propia migraña.
Reacción alérgica: busque la ayuda del médico inmediatamente
Se han producido los siguientes efectos adversos, pero se desconoce su frecuencia exacta.
- Los signos de la alergia incluyen sarpullido, urticaria (erupción con picor); sibilancias; párpados, cara o labios hinchados; colapso total.
Si tiene alguno de estos síntomas poco después de usar Sumatriptán CFOURHEALTH:
No lo use más. Póngase en contacto con un médico inmediatamente.
Muy frecuentes (pueden afectar a más de 1 de cada 10 personas)
- Dolor temporal en el lugar de la inyección
- Escozor o ardor, enrojecimiento, hinchazón, hematomas y sangrado en el lugar de la inyección
Frecuentes (pueden afectar a hasta 1 de cada 10 personas)
- Dolor, pesadez, presión u opresión en el pecho, la garganta u otras partes del cuerpo, o sensaciones inusuales, como entumecimiento, hormigueo y calor o frío. Estos efectos pueden ser intensos pero generalmente pasan rápidamente.
Si estos efectos continúan o se agravan (especialmente el dolor en el pecho):
Busque ayuda médica urgentemente. En un número muy pequeño de personas la causa de estos síntomas puede ser un ataque al corazón.
Otros efectos adversos frecuentes (pueden afectar a hasta 1 de cada 10 personas)
- Sentirse mareado (náuseas) o vomitar, aunque esto puede deberse a la propia migraña
- Cansancio o somnolencia
- Mareos, sensación de debilidad o sofocos
- Aumento temporal de la presión arterial
- Dificultad para respirar
- Músculos doloridos
Muy raros (pueden afectar a hasta 1 de cada 10.000 personas)
- Cambios en la función hepática. Si le hacen un análisis de sangre para comprobar su función hepática, dígale a su médico o enfermera que está usando sumatriptán.
Frecuencia no conocida (no puede estimarse a partir de los datos disponibles)
- Convulsiones/ataques epilépticos, temblores, espasmos musculares, rigidez de cuello
- Alteraciones visuales, como parpadeos, visión reducida, visión doble, pérdida de visión y, en algunos casos, incluso defectos permanentes (aunque pueden deberse a la propia crisis de migraña)
- Problemas cardíacos, en los que los latidos del corazón pueden ser más rápidos, más lentos o cambiar de ritmo, dolores en el pecho (angina de pecho) o ataque cardíaco
- Piel pálida y azulada y/o dolor en los dedos de las manos, los pies, las orejas, la nariz o la mandíbula en respuesta al frío o al estrés (fenómeno de Raynaud)
- Sensación de desmayo (la presión arterial puede bajar)
- Dolor en la parte inferior izquierda del estómago y diarrea con sangre (colitis isquémica)
- Diarrea
- Dolor en las articulaciones
- Sentirse ansioso
- Sudoración excesiva
- Si ha tenido una lesión reciente o si tiene una inflamación (como reumatismo o inflamación del colon) puede experimentar dolor o empeoramiento del dolor en el lugar de la lesión o inflamación.
- Dificultad para tragar
Comunicación de efectos adversos
Si experimenta cualquier tipo de efecto adverso, consulte a su médico o farmacéutico, incluso si se trata de posibles efectos adversos que no aparecen en este prospecto.
También puede comunicarlos directamente a través del
Sistema Español de Farmacovigilancia de Medicamentos de Uso Humano: www.notificaRAM.es
Mediante la comunicación de efectos adversos usted puede contribuir a proporcionar más información sobre la seguridad de este medicamento.
5. Conservación de Sumatriptán CFOURHEALTH
Mantener este medicamento fuera de la vista y del alcance de los niños.
No utilice este medicamento después de la fecha de caducidad que aparece en la caja de cartón y la pluma. La fecha de caducidad es el último día del mes que se indica.
No almacenar a temperatura superior a 25 °C. Conservar en el envase original para protegerlo de la luz.
Los medicamentos no se deben tirar por los desagües ni a la basura. Deposite los envases y los medicamentos que no necesita en el Punto SIGRE de la farmacia. Pregunte a su farmacéutico cómo deshacerse de los envases y de los medicamentos que ya no necesita. De esta forma, ayudará a proteger el medio ambiente
..
6. Contenido del envase e información adicional
Composición de Sumatriptán CFOURHEALTH
- El principio activo es sumatriptán. Cada pluma precargada con 0,5 ml de solución contiene 6 mg de sumatriptán (como succinato de sumatriptán).
- Los demás componentes son cloruro de sodio y agua para preparaciones inyectables.
Aspecto del producto y contenido del envase
Sumatriptán CFOURHEALTH es una solución transparente, entre incolora y amarillo pálido.
Pluma precargada compuesta por una jeringa de vidrio transparente tipo I de 1 ml de longitud, con reborde recortado y con aguja fija (calibre 29, de 12,7 milímetros y 5 biseles) cerrada con un capuchón rígido transparente de protección de la aguja, tapón estéril del émbolo en clorobutilo de color negro dentro de una caja de cartón.
Cada caja contiene 1, 2, 6 o 12 plumas precargadas.
Puede que solamente estén comercializados algunos tamaños de envases.
Titular de la autorización de comercialización
C4 health GmbH
Wildstraße 20
89522 Heidenheim
Alemania
Responsable de la fabricación
Hormosan Pharma GmbH
Hanauer Landstraße 139-143
60314 Frankfurt am Main
Alemania
Venipharm
4, bureaux de la Colline
92210 Saint-Cloud
Francia
Abcur AB
Bergaliden 11,
Helsinborg, 252 23,
Suecia
Este medicamento está autorizado en los Estados miembros del Espacio Económico Europeo con los siguientes nombres:
Alemania | Sumatriptan C4 health 6 mg Injektionslösung im Fertigpen |
Dinamarca | Sumatriptan C4 health |
Finlandia | Sumatriptan C4 HEALTH 6mg injektioneste, liuos, esitäytetty kynä |
Italia | Sumatriptan C4 Health |
Países Bajos | Sumatriptan C-Four 6 mg/0.5ml oplossing voor injectie in een voorgevulde pen |
Noruega | Sumatriptan CFOURHEALTH |
España | Sumatriptán CFOURHEALTH 6mg/0.5ml solución inyectable en pluma precargada EFG |
Suecia | Sumatriptan C4 Health |
Fecha de la última revisión de este prospecto: Octubre 2023.
La información detallada de este medicamento está disponible en la página web de la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) http://www.aemps.gob.es/
- Instrucciones de uso
CÓMO UTILIZAR LA PLUMA PRECARGADA | Figura 1 (vista frontal de la pluma precargada) |
Sumatriptán CFOURHEALTH | |
Esta sección explica cómo utilizar la pluma precargada de sumatriptán. Léala DOS veces antes de comenzar el primer paso. Si tiene alguna duda, consulte a su médico o farmacéutico. Sólo para uso en pacientes a quienes se les ha prescrito una dosis de 6 mg. | |
PRECAUCIONES: | |
| |
| |
| |
| |
Cómo utilizar la pluma precargada | |
| |
| |
No lo inyecte en zonas en las que la piel esté sensible, magullada, roja o dura. | Figura 2 |
| |
| |
| Figura 3 |
Cómo iniciar la inyección: | |
| |
| |
No mueva el inyector de la pluma precargada del lugar de la inyección. Siga sujetándolo firmemente contra la piel hasta que un «clic» audible señale el final de la inyección. Mantenga la pluma presionada sobre la piel durante otros 5 segundos para asegurarse de que se ha administrado la dosis completa (Fig. 4). | Figura 4 |
| Figura 5 |
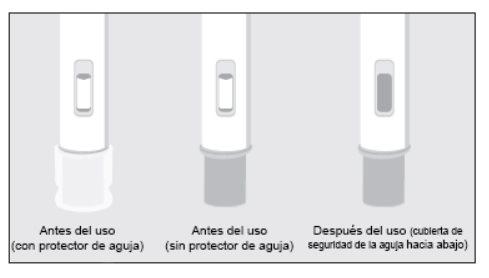
| |
Si la ventana de observación no es gris, no trate de volver a utilizar la pluma precargada. | |
NUNCA INTENTE UTILIZAR DOS VECES UNA PLUMA PRECARGADA | |
| Figura 6 |
Si sospecha que no ha recibido la dosis completa, no repita la inyección utilizando una nueva pluma precargada. | |
|
Figura 1
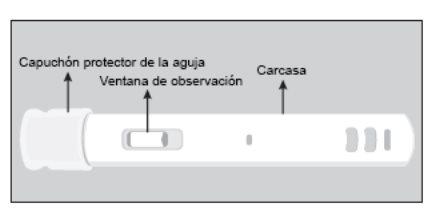
Figura 2
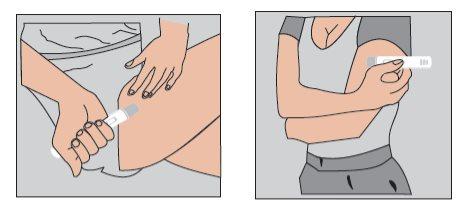
Figura 3
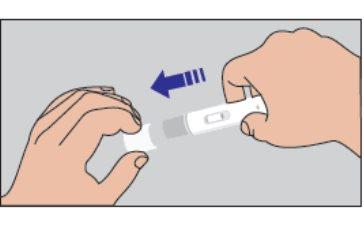
Figura 4
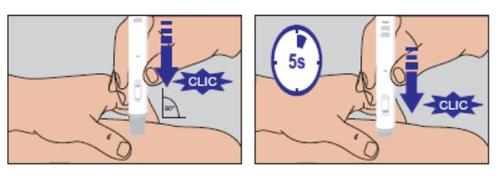
Figura 5
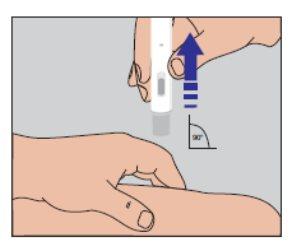
Figura 6
- País de registro
- Principio activo
- Requiere recetaSí
- Fabricante
- Esta información es de carácter general y no sustituye la consulta con un profesional sanitario.
- Alternativas a SUMATRIPTAN CFOURHEALTH 6 MG SOLUCION INYECTABLE EN PLUMA PRECARGADA EFGForma farmacéutica: PRODUCTO USO NASAL, 10 mgPrincipio activo: sumatriptánFabricante: Glaxosmithkline S.A.Requiere recetaForma farmacéutica: PRODUCTO USO NASAL, 20 mg sumatriptanPrincipio activo: sumatriptánFabricante: Glaxosmithkline S.A.Requiere recetaForma farmacéutica: INYECTABLE, 6 mgPrincipio activo: sumatriptánFabricante: Glaxosmithkline S.A.Requiere receta
Médicos online para SUMATRIPTAN CFOURHEALTH 6 MG SOLUCION INYECTABLE EN PLUMA PRECARGADA EFG
Comenta la dosis, los posibles efectos secundarios, interacciones, contraindicaciones o la revisión de receta de SUMATRIPTAN CFOURHEALTH 6 MG SOLUCION INYECTABLE EN PLUMA PRECARGADA EFG, sujeto a valoración médica y a la normativa local.
Preguntas frecuentes















