QDENGA POLVO Y DISOLVENTE PARA SOLUCION INYECTABLE EN JERINGA PRECARGADA

Cómo usar QDENGA POLVO Y DISOLVENTE PARA SOLUCION INYECTABLE EN JERINGA PRECARGADA
Traducción generada por IA
Este contenido ha sido traducido automáticamente y se ofrece solo con fines informativos. No sustituye la consulta con un profesional sanitario.
Ver originalContenido del prospecto
Introducción
Prospecto: información para el usuario
Qdenga polvo y disolvente para solución inyectable en jeringa precargada
Vacuna tetravalente contra el dengue (viva, atenuada)
Este medicamento está sujeto a seguimiento adicional, lo que agilizará la detección de nueva información sobre su seguridad. Puede contribuir comunicando los efectos adversos que pudiera usted tener. La parte final de la sección 4 incluye información sobre cómo comunicar estos efectos adversos.
Lea todo el prospecto detenidamente antes de que les vacunen a usted o a su hijo, porque contiene información importante para usted.
- Conserve este prospecto, ya que puede tener que volver a leerlo.
- Si tiene alguna duda, consulte a su médico, farmacéutico o enfermero.
- Este medicamento se le ha recetado solamente a usted o a su hijo, y no debe dárselo a otras personas.
- Si usted o su hijo experimentan efectos adversos, consulte a su médico, farmacéutico o enfermero, incluso si se trata de efectos adversos que no aparecen en este prospecto. Ver sección 4.
Contenido del prospecto
- Qué es Qdenga y para qué se utiliza
- Qué necesita saber antes de que usted o su hijo reciban Qdenga
- Cómo se administra Qdenga
- Posibles efectos adversos
- Conservación de Qdenga
- Contenido del envase e información adicional
1. Qué es Qdenga y para qué se utiliza
Qdenga es una vacuna. Se utiliza para ayudar a protegerle a usted o a su hijo contra el dengue. El dengue es una enfermedad causada por los serotipos 1, 2, 3 y 4 del virus del dengue. Qdenga contiene versiones debilitadas de estos 4 serotipos del virus del dengue, por lo que no puede causar la enfermedad.
Qdenga se administra a adultos, jóvenes y niños (a partir de los 4 años de edad).
Qdenga debe utilizarse de acuerdo con las recomendaciones oficiales.
Cómo funciona la vacuna
Qdenga estimula las defensas naturales del cuerpo (sistema inmunitario). Esto ayuda a proteger contra los virus que causan el dengue si el cuerpo, en el futuro, se expone a estos virus.
Qué es el dengue
El dengue está causado por un virus.
- El virus se transmite a través de mosquitos (mosquitos Aedes).
- Si un mosquito pica a una persona con dengue, puede transmitir el virus a las siguientes personas que pique.
El dengue no se transmite directamente de persona a persona.
Los signos de dengue incluyen fiebre, dolor de cabeza, dolor en la parte posterior de los ojos, dolor muscular y articular, sensibilidad o malestar (náuseas y vómitos), inflamación de los ganglios o erupción de la piel. Los signos de dengue suelen durar de 2 a 7 días. También puede estar infectado con el virus del dengue, pero no mostrar signos de enfermedad.
En ocasiones, el dengue puede ser lo suficientemente grave como para que usted o su hijo tengan que ir al hospital y, en raras ocasiones, puede causar la muerte. El dengue grave puede provocar fiebre alta y cualquiera de los siguientes síntomas: dolor abdominal (barriga) intenso, náuseas persistentes (vómitos), respiración acelerada, hemorragia grave, sangrado en el estómago, sangrado de las encías, sensación de cansancio, inquietud, coma, ataques (convulsiones) e disfunción orgánica.
2. Qué necesita saber antes de que usted o su hijo reciban Qdenga
Para asegurarse de que Qdenga es adecuado para usted o su hijo, es importante que informe a su médico, farmacéutico o enfermero si alguno de los siguientes puntos se aplican a usted o su hijo. Si hay algo que no entiende, pida a su médico, farmacéutico o enfermero que se lo explique.
No utilice Qdenga si usted o su hijo
- son alérgicos a los principios activos o a alguno de los demás componentes de Qdenga (incluidos en la sección 6).
- han tenido una reacción alérgica tras recibir Qdenga anteriormente. Los signos de una reacción alérgica pueden incluir una erupción que pica, dificultad para respirar e inflamación de la cara y la lengua.
- tienen un sistema inmunitario debilitado (las defensas naturales del organismo). Esto puede deberse a un defecto genético o a una infección por VIH.
- está tomando un medicamento que afecta al sistema inmunitario (como dosis altas de corticosteroides o quimioterapia). Su médico no utilizará Qdenga hasta 4 semanas después de que usted deje el tratamiento con este medicamento.
- está embarazada o en periodo de lactancia.
No utilice Qdenga si se da alguno de los casos anteriores.
Advertencias y precauciones
- Informe a su médico, farmacéutico o enfermero antes de recibir Qdenga si usted o su hijo:
- presentan una infección con fiebre. Puede ser necesario posponer la vacunación hasta la recuperación.
- alguna vez han tenido problemas de salud cuando se les administró una vacuna. Su médico considerará minuciosamente los riesgos y beneficios de la vacunación.
- alguna vez se han desmayado por una inyección. Pueden producirse mareos, desmayos y, en ocasiones, caídas (sobre todo en personas jóvenes) después o incluso antes de cualquier inyección con aguja.
Información importante acerca de la protección proporcionada
Como con cualquier vacuna, Qdenga puede no proteger a todos los que la reciban, y la protección puede disminuir con el tiempo. Aún puede contraer el dengue por las picaduras de mosquito, incluida la enfermedad grave del dengue. Debe seguir protegiéndose a sí mismo o a su hijo contra las picaduras de mosquitos incluso después de la vacunación con Qdenga.
Tras la vacunación, debe consultar a un médico si usted o su hijo creen que pueden tener una infección por dengue y presentan alguno de los siguientes síntomas: fiebre alta, dolor abdominal (barriga) intenso, vómitos persistentes, respiración rápida, encías sangrantes, cansancio, inquietud y sangre en el vómito.
Otras medidas de protección
Debe tomar precauciones para evitar las picaduras de mosquito. Esto incluye el uso de repelentes de insectos, ropa protectora y mosquiteras.
Niños pequeños
Los niños menores de 4 años de edad no deben recibir Qdenga.
Otros medicamentos y Qdenga
Qdenga puede administrarse junto con la vacuna contra la hepatitis A, la vacuna contra la fiebre amarilla o la vacuna contra el virus del papiloma humano en otro lugar de inyección (otra parte del cuerpo, normalmente el otro brazo) durante la misma visita.
Informe a su médico o farmacéutico si usted o su hijo están utilizando, han utilizado recientemente o pudieran tener que utilizar cualquier otro medicamento o vacuna.
En concreto, informe a su médico o farmacéutico si usted o su hijo están tomando alguna de las siguientes sustancias:
- Medicamentos que afectan a sus defensas naturales del cuerpo (sistema inmunitario) como dosis altas de corticosteroides o quimioterapia. En este caso, su médico no utilizará Qdenga hasta 4 semanas después de interrumpir el tratamiento. Esto se debe a que Qdenga podría no funcionar tan bien.
- Medicamentos denominados “inmunoglobulinas” o hemoderivados que contienen inmunoglobulinas, como sangre o plasma. En este caso, su médico no utilizará Qdenga hasta pasadas 6 semanas y, preferiblemente, hasta pasados 3 meses tras interrumpir el tratamiento. Esto se debe a que Qdenga podría no funcionar tan bien.
Embarazo y lactancia
No utilice Qdenga si usted o su hija están embarazadas o en periodo de lactancia. Si usted o su hija:
- están en edad fértil, deben tomar las precauciones necesarias para evitar el embarazo durante un mes después de la vacunación con Qdenga.
- creen que podrían estar embarazadas o están planeando tener un bebé, pregunten a su médico, farmacéutico o enfermero antes de utilizar Qdenga.
Conducción y uso de máquinas
Qdenga tiene una influencia pequeña sobre la capacidad para conducir y utilizar máquinas en los primeros días tras la vacunación.
Qdenga contiene sodio y potasio
Este medicamento contiene menos de 1 mmol de sodio (23 mg) por dosis de 0,5 ml; esto es, esencialmente “exento de sodio”.
Este medicamento contiene menos de 1 mmol (39 mg) de potasio por dosis de 0,5 ml; esto es, esencialmente “exento de potasio”.
3. Cómo se administra Qdenga
Qdenga se administra por el médico o enfermero como una inyección bajo la piel (inyección subcutánea) en la parte superior del brazo. No debe inyectarse en un vaso sanguíneo.
Usted o su hijo recibirán 2 inyecciones.
La segunda inyección se administra 3 meses después de la primera.
No existen datos de adultos mayores de 60 años de edad. Consulte a su médico para saber si Qdenga es beneficioso para usted.
Qdenga debe utilizarse de acuerdo con las recomendaciones oficiales.
Las instrucciones para la preparación de la vacuna para médicos y profesionales sanitarios figuran al final del prospecto.
Si usted o su hijo se saltan una inyección de Qdenga
- Si usted o su hijo se saltan una inyección programada, el médico decidirá cuándo administrar la inyección que falta. Es importante que usted o su hijo sigan las instrucciones del médico, farmacéutico o enfermero sobre la inyección de seguimiento.
- Si olvida o no puede volver en la hora programada, pregunte a su médico, farmacéutico o enfermero para que le aconseje.
Si tiene cualquier otra duda sobre el uso de esta vacuna, pregunte a su médico, farmacéutico o enfermero.
4. Posibles efectos adversos
Al igual que todos los medicamentos, Qdenga puede producir efectos adversos, aunque no todas las personas los sufran.
Reacción alérgica(anafiláctica)grave
Si se produce cualquiera de estos síntomas tras abandonar el lugar en el que usted o su hijo recibió una inyección, póngase en contacto con un médico de inmediato:
- dificultad para respirar
- lengua o labios azules
- erupción
- hinchazón de la cara o la garganta
- presión arterial baja que provoca mareos o desfallecimiento
- sensación repentina y grave de malestar o inquietud, acompañada de una bajada de tensión que provoca mareos y pérdida de consciencia, además de latidos acelerados asociados a la dificultad para respirar
Estos signos o síntomas (reacciones anafilácticas) suelen aparecer poco después de la administración de la inyección y mientras usted o su hijo todavía están en el centro o en la consulta del médico. También se pueden producir muy raramente después de recibir cualquier vacuna.
Los siguientes efectos adversos se han producido durante los estudios en niños, jóvenes y adultos.
Muy frecuentes(pueden afectar a más de 1 persona de cada 10):
- dolor en el lugar de la inyección
- dolor de cabeza
- dolor muscular
- enrojecimiento en el lugar de inyección
- sensación de malestar general
- debilidad
- infecciones de la nariz o la garganta
- fiebre
Frecuentes(pueden afectar hasta 1 de cada 10 personas):
- inflamación del lugar de inyección
- dolor o inflamación de la nariz o la garganta
- hematomas en el lugar de inyección
- picor en el lugar de inyección
- inflamación de la garganta y las amígdalas
- dolor articular
- enfermedad de tipo gripal
Poco frecuentes (pueden afectar hasta a 1 de cada 100 personas):
- diarrea
- náuseas
- dolor de estómago
- vómitos
- sangrado en el lugar de inyección
- sensación de mareo
- picor en la piel
- erupción cutánea, incluyendo erupciones en la piel con manchas o picor en la piel
- ronchas
- cansancio
- cambio del color de la piel en el lugar de inyección
- inflamación de las vías respiratorias
- goteo nasal
Muy raros(pueden afectar hasta a 1 de cada 10 000 personas):
- inflamación rápida debajo de la piel en zonas como el rostro, la garganta, los brazos y las piernas
Frecuencia no conocida(no puede estimarse a partir de los datos disponibles):
- reacción alérgica (anafiláctica) repentina y grave, con dificultad para respirar, hinchazón, vahído, latidos acelerados, sudoración y pérdida de consciencia
Otros efectos adversos en niños de 4 a 5 años de edad:
Muy frecuentes(pueden afectar a más de 1 persona de cada 10):
- disminución del apetito
- sensación de sueño
- irritabilidad
Comunicación de efectos adversos
Si experimenta cualquier tipo de efecto adverso, consulte a su médico, farmacéutico o enfermero, incluso si se trata de posibles efectos adversos que no aparecen en este prospecto. También puede comunicarlos directamente a través del sistema nacional de notificación incluido en el Apéndice V. Mediante la comunicación de efectos adversos usted puede contribuir a proporcionar más información sobre la seguridad de este medicamento.
5. Conservación de Qdenga
Mantener Qdenga fuera de la vista y del alcance de los niños.
No utilice Qdenga después de la fecha de caducidad que aparece en la caja después de CAD. La fecha de caducidad es el último día del mes que se indica.
Conservar en nevera (entre 2 ºC y 8 ºC).
No congelar.
Conservar la vacuna en el embalaje exterior.
Despues de mezclar (reconstitución) con el disolvente suministrado, Qdenga debe utilizarse inmediatamente. Si no se utiliza inmediatamente, Qdenga se debe utilizar en un plazo de 2 horas.
Los medicamentos no se deben tirar por los desagües ni a la basura. Pregunte a su farmacéutico cómo deshacerse de los envases y de los medicamentos que ya no necesita. De esta forma, ayudará a proteger el medio ambiente
6. Contenido del envase e información adicional
Qué contiene Qdenga
- Después de la reconstitución, una dosis (0,5 ml) contiene:
Virus del dengue serotipo 1 (vivo, atenuado)*: ≥ 3,3 log10 UFP**/dosis
Virus del dengue serotipo 2 (vivo, atenuado)#: ≥ 2,7 log10 UFP**/dosis
Virus del dengue serotipo 3 (vivo, atenuado)*: ≥ 4,0 log10 UFP**/dosis
Virus del dengue serotipo 4 (vivo, atenuado)*: ≥ 4,5 log10 UFP**/dosis
- Producido en células Vero mediante tecnología de ADN recombinante.. Genes de las proteínas de superficie específicas de cada serotipo, insertados en el esqueleto del dengue tipo 2. Este producto contiene organismos modificados genéticamente (OMG).
# Producido en células Vero por tecnología de ADN recombinante.
** UFP = unidades formadoras de placas
- Los demás ingredientes son: a,a-trehalosa dihidrato, poloxámero 407, albúmina de suero humano, dihidrogenofosfato de potasio, dihidrogenofosfato de sodio, cloruro potásico, cloruro de sodio, agua para preparaciones inyectables.
Aspecto de Qdenga y contenido del envase
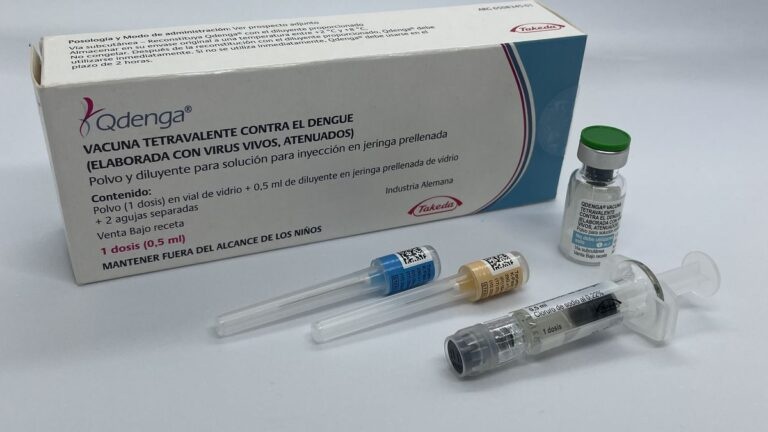
Qdenga es un polvo y disolvente para solución inyectable. Qdenga se suministra como polvo en un vial de dosis única y un disolvente en una jeringa precargada con 2 agujas aparte o sin aguja.
El polvo y el disolvente deben mezclarse antes de su uso.
Qdenga en polvo y disolvente para solución inyectable en jeringa precargada está disponible en envases de 1 o 5.
Puede que solamente estén comercializados algunos tamaños de envases.
El polvo es compacto para suspensión de color blanco a blanquecino.
El disolvente (0,22 % de solución de cloruro de sodio) es un líquido incoloro y transparente.
Tras la reconstitución, Qdenga es una solución transparente, de incolora a amarillo pálido, esencialmente sin partículas extrañas.
Titular de la autorización de comercialización y responsable de la fabricación
Titular de la autorización de comercialización
Takeda GmbH
Byk-Gulden-Str. 2
78467 Konstanz
Alemania
Responsable de la fabricación
Takeda GmbH
Production site Singen
Robert-Bosch-Str. 8
78224 Singen
Alemania
Pueden solicitar más información respecto a este medicamento dirigiéndose al representante local del titular de la autorización de comercialización:
België/Belgique/Belgien Takeda Belgium NV Tél/Tel: +32 2 464 06 11 | Lietuva Takeda, UAB Tel: +370 521 09 070 |
| Luxembourg/Luxemburg Takeda Belgium NV Tél/Tel: +32 2 464 06 11 |
Ceská republika Takeda Pharmaceuticals Czech Republic s.r.o. Tel: +420 234 722 722 | Magyarország Takeda Pharma Kft. Tel: +36 1 270 7030 |
Danmark Takeda Pharma A/S Tlf.: +45 46 77 10 10 | Malta Takeda HELLAS S.A. Tel: +30 210 6387800 |
Deutschland Takeda GmbH Tel: +49 (0) 800 825 3325 | Nederland Takeda Nederland B.V. Tel: +31 20 203 5492 |
Eesti Takeda Pharma AS Tel: +372 6177 669 | Norge Takeda AS Tlf: 800 800 30 |
Ελλáδα Takeda ΕΛΛΑΣ Α.Ε. Τηλ: +30 210 6387800 | Österreich Takeda Pharma Ges.m.b.H. Tel: +43 (0) 800-20 80 50 |
España Takeda Farmacéutica España S.A. Tel: +34 917 90 42 22 | Polska Takeda Pharma sp. z o.o. Tel: +48 22 306 24 47 |
Francia Takeda France SAS Tél: +33 1 40 67 33 00 | Portugal Takeda Farmacêuticos Portugal, Lda. Tel: +351 21 120 1457 |
Hrvatska Takeda Pharmaceuticals Croatia d.o.o. Tel: +385 1 377 88 96 | Ireland Takeda Products Ireland Ltd. Tel: 1800 937 970 |
România Takeda Pharmaceuticals SRL Tel: +40 21 335 03 91 | Slovenija Takeda Pharmaceuticals farmacevtska družba d.o.o. Tel: +386 (0) 59 082 480 |
Ísland Vistor hf. Sími: +354 535 7000 | Slovenská republika Takeda Pharmaceuticals Slovakia s.r.o. Tel: +421 (2) 20 602 600 |
Italia Takeda Italia S.p.A. Tel: +39 06 502601 | Suomi/Finland Takeda Oy Puh/Tel: 0800 774 051 |
Κúπρος Takeda ΕΛΛΑΣ Α.Ε. Τηλ: +30 2106387800 | Sverige Takeda Pharma AB Tel: 020 795 079 |
Latvija Takeda Latvia SIA Tel: +371 67840082 | Reino Unido (Irlanda del Norte) Takeda UK Ltd Tel: +44 (0) 3333 000 181 |
Fecha de la última revisión de este prospecto: Octubre 2024.
Otras fuentes de información
La información detallada de este medicamento está disponible en la página web de la Agencia Europea de Medicamentos: http://www.ema.europa.eu.
Esta información está destinada únicamente a profesionales sanitarios:
- Qdenga no debe mezclarse con otros medicamentos o vacunas en la misma jeringa.
- Qdenga no se debe administrar como inyección por vía intravascular bajo ninguna circunstancia.
- La vacunación debe realizarse mediante inyección subcutánea, preferiblemente en la parte superior del brazo, en el deltoides. Qdenga no debe administrarse como inyección intramuscular.
- Puede producirse síncope (desmayo) después, o incluso antes, de cualquier vacunación como respuesta psicógena a la inyección con aguja. Se deben establecer procedimientos para evitar lesiones por caídas y gestionar las reacciones sincopales.
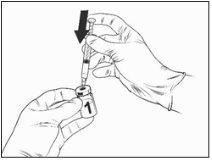
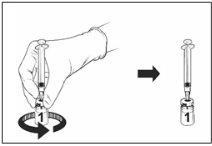
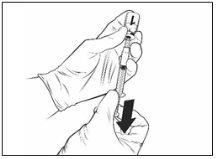
Instrucciones para la reconstitución de la vacuna con el disolvente presentado en la jeringa precargada:
Qdenga es una vacuna de 2 componentes que consiste en un vial que contiene la vacuna liofilizada y disolvente suministrado en la jeringa precargada. La vacuna liofilizada debe
reconstituirse con el disolvente antes de la administración.
Qdenga no debe mezclarse con otras vacunas en la misma jeringa.
Para reconstituir Qdenga, utilice solo el disolvente (solución de cloruro de sodio al 0,22 %) en la jeringa precargada suministrada con la vacuna, ya que no contiene conservantes ni otras sustancias antivíricas. Se debe evitar el contacto con conservantes, antisépticos, detergentes y otras sustancias antivíricas, ya que pueden inactivar la vacuna.
Retire el vial de la vacuna y el disolvente de la jeringa precargada de la nevera y colóquelos a temperatura ambiente durante aproximadamente 15 minutos.
Vial de vacuna liofilizada |
|
Vacuna reconstituida |
|
Tras la reconstitución, la solución resultante debe ser transparente, entre incolora y amarilla pálida, y básicamente sin partículas extrañas. Deseche la vacuna si se aprecian en ella partículas o cambios de color.
Vacuna reconstituida |
|
Qdenga se debe administrar inmediatamente tras la reconstitución. Se ha demostrado su estabilidad fisicoquímica durante el uso por un periodo de 2 horas a temperatura ambiente (hasta 32,5 ºC) desde el momento de la reconstitución del vial de la vacuna. Una vez transcurrido este período, la vacuna debe desecharse. No la vuelva a introducir en la nevera. Desde el punto de vista microbiológico, Qdenga debe utilizarse de inmediato. Si no se utiliza inmediatamente, los tiempos y condiciones de conservación serán responsabilidad del usuario.
La eliminación del medicamento no utilizado y de todos los materiales desechables se realizará de acuerdo con la normativa local.
- País de registro
- Principio activo
- Requiere recetaSí
- Fabricante
- Esta información es de carácter general y no sustituye la consulta con un profesional sanitario.
- Alternativas a QDENGA POLVO Y DISOLVENTE PARA SOLUCION INYECTABLE EN JERINGA PRECARGADAForma farmacéutica: INYECTABLE, 60 microgramos/dosis + 60 microgramos/dosisPrincipio activo: respiratory syncytial virus vaccinesFabricante: Pfizer Europe Ma EeigRequiere recetaForma farmacéutica: INYECTABLE, 0,5 MLPrincipio activo: respiratory syncytial virus vaccinesFabricante: Glaxosmithkline BiologicalsRequiere recetaForma farmacéutica: INYECTABLE, 50 µgPrincipio activo: respiratory syncytial virus vaccinesFabricante: Moderna Biotech Spain S.L.Requiere receta
Médicos online para QDENGA POLVO Y DISOLVENTE PARA SOLUCION INYECTABLE EN JERINGA PRECARGADA
Comenta la dosis, los posibles efectos secundarios, interacciones, contraindicaciones o la revisión de receta de QDENGA POLVO Y DISOLVENTE PARA SOLUCION INYECTABLE EN JERINGA PRECARGADA, sujeto a valoración médica y a la normativa local.
Preguntas frecuentes