
PHIVOR 3.500 UI ANTI XA/0,2 ML DE SOLUCION EN JERINGAS PRECARGAS

Cómo usar PHIVOR 3.500 UI ANTI XA/0,2 ML DE SOLUCION EN JERINGAS PRECARGAS
Traducción generada por IA
Este contenido ha sido traducido automáticamente y se ofrece solo con fines informativos. No sustituye la consulta con un profesional sanitario.
Ver originalContenido del prospecto
Introducción
Prospecto: información para el usuario
Phivor3.500 UI anti Xa/0,2 ml
solución inyectable en jeringas precargadas
Bemiparina sódica
Lea todo el prospecto detenidamente antes de empezar a usar este medicamento porque contiene información importante para usted.
- Conserve este prospecto, ya que puede tener que volver a leerlo.
- Si tiene alguna duda, consulte a su médico o farmacéutico.
- Este medicamento se le ha recetado solamente a usted, y no debe dárselo a otras personas aunque tengan los mismos síntomas que usted, ya que puede perjudicarles.
- Si experimenta efectos adversos, consulte a su médico o farmacéutico, incluso si se trata de efectos adversos que no aparecen en este prospecto. Ver sección 4.
En este prospecto:
- Qué es Phivor y para qué se utiliza
- Qué necesita saber antes de empezar a usar Phivor
- Cómo usar Phivor
- Posibles efectos adversos
- Conservación de Phivor
- Contenido del envase e información adicional
1. Qué es Phivor y para qué se utiliza
El principio activo de Phivor es bemiparina sódica, que pertenece a un grupo de medicamentos llamados anticoagulantes. Estos medicamentos ayudan a que la sangre no se coagule en las venas.
Phivor 3.500 UI se utiliza para: prevenir coágulos de sangre (por ejemplo, en venas de las piernas y/o de los pulmones) que puedan aparecer en pacientes sometidos a cirugía ortopédica (cadera, rodilla u otras operaciones de huesos) o en pacientes no sometidos a intervención quirúrgica pero que tengan riesgo moderado de sufrir coágulos.
También se utiliza para prevenir la formación de coágulos en el circuito de circulación extracorpórea durante la hemodiálisis.
2. Qué necesita saber antes de empezar a usar Phivor
No use Phivor
- Si es alérgico a bemiparina sódica, heparina o un producto similar (como enoxaparina, dalteparina, nadroparina) o a cualquiera de los demás componentes de este medicamento (incluidos en la sección 6).
- Si ha tenido alguna reacción alérgica después de haber sido tratado con algún medicamento que contenga heparina.
- Si es alérgico a alguna sustancia derivada del cerdo.
- Si padece Trombocitopenia Inducida por Heparina (TIH), una enfermedad que provoca un descenso importante en su cantidad de plaquetas (o, si como resultado de TIH, sufre otra enfermedad que se llama Coagulación Intravascular Diseminada (CID), en la que sus plaquetas se agruparían si utilizase Phivor).
- Si padece una enfermedad llamada endocarditis (inflamación de las paredes del corazón y de las válvulas cardíacas).
- Si padece algún tipo de trastorno que le provoca una tendencia a sangrar de forma excesiva.
- Si padece usted un trastorno grave de la función del hígado y/o del páncreas.
- Si sufre algún tipo de daño o lesión en sus órganos internos que pudiese implicar un alto riesgo de sangrado interno (por ejemplo, úlceras de estómago activa, aneurismas cerebrales [inflamación de las paredes de las arterias del cerebro] o tumores cerebrales).
- Si ha tenido una hemorragia cerebral.
- Si ha tenido o tiene una lesión o va a ser operado en el cerebro, en la médula espinal, en los ojos y/o en los oídos.
- Si está utilizando Phivor, no le podrán administrar anestesia epidural o espinal (un anestésico inyectado en la médula espinal) porque podría ser peligroso. Por lo tanto, asegúrese de que su médico sepa que está utilizando Phivor antes de cualquier operación.
Advertencias y precauciones
Consulte a su médico o farmacéutico antes de empezar a usar Phivor.
- Si está enfermo del hígado.
- Si está enfermo del riñón. Su médico podría considerar hacerle un seguimiento especial. En el caso de que su enfermedad del riñón fuera grave, su médico podría considerar necesario un ajuste de dosis.
- Si su tensión arterial es alta y/o difícil de controlar.
- Si ha tenido alguna vez úlcera de estómago que ya no está activa.
- Si tiene trombocitopenia, una enfermedad en la que hay menos plaquetas de las normales en sangre, que provoca moratones y que se sangre fácilmente.
- Si tiene piedras en el riñón y/o la vejiga.
- Si tiene algún tipo de enfermedad que provoca que sangre con facilidad.
- Si tiene problemas en los ojos debido a problemas en sus vasos sanguíneos.
- Si tiene diabetes.
- Si los resultados de sus análisis han mostrado que tiene los niveles de potasio en sangre elevados.
- Asegúrese por partida doble de que su médico sabe que está usando Phivor si le van a hacer una punción lumbar (un pinchazo en la parte más baja de la columna vertebral para hacerle análisis).
Uso de Phivor con otros medicamentos
Consulte a su médico si cree que pudiera estar utilizando:
- Cualquier medicamento que se inyecte en el músculo, porque estas inyecciones deben evitarse mientras esté en tratamiento con Phivor.
- Otros anticoagulantes como la warfarina y/o acenocumarol (antagonistas de la vitamina K), para tratar y/o prevenir los coágulos sanguíneos.
- Antiinflamatorios no esteroideos, como el ibuprofeno, por ejemplo, para la artritis.
- Corticoides como la prednisolona, para tratar enfermedades inflamatorias, como la artritis.
- Inhibidores plaquetarios, como la aspirina, ticlopidina o clopidogrel, para prevenir coágulos en la sangre.
- Medicamentos que puedan aumentar los niveles de potasio en sangre, como algunos diuréticos y antihipertensivos (usados para reducir la tensión arterial).
- Medicamentos para aumentar el volumen de la sangre, como el dextrano.
- Un medicamento inyectable para problemas de corazón que se llama nitroglicerina.
Comunique a su médico o farmacéutico si está utilizando, ha utilizado recientemente o podría tener que utilizar cualquier otro medicamento.
Análisis especiales que puede necesitar
- Algunos pacientes puede que necesiten tener controlado el nivel de plaquetas en su sangre. Su médico decidirá si es necesario y cuándo (por ejemplo, antes de iniciar tratamiento, el primer día de tratamiento, posteriormente cada 3 ó 4 días hasta finalizar el tratamiento).
- Si tiene determinadas enfermedades (diabetes, enfermedad de los riñones) o si está tomando medicamentos para no perder potasio, puede que su médico controle los niveles de potasio en su sangre.
Embarazo y lactancia
Si está embarazada o en periodo de lactancia, cree que podría estar embarazada o tiene intención de quedarse embarazada, consulta a su médico o farmacéutico antes de utilizar este medicamento.
Conducción y uso de máquinas
Phivor no afecta la capacidad de conducir y utilizar máquinas.
3. Cómo usar Phivor
Siga exactamente las instrucciones de administración de este medicamento indicadas por su médico. En caso de dudas, consulte de nuevo a su médico o farmacéutico.
La dosis recomendada es:
Prevención de la enfermedad tromboembólica en pacientes sometidos a cirugía ortopédica:
- Phivor 3.500 UI se administra generalmente por un médico o una enfermera por vía subcutánea (se inyecta por debajo de la piel, generalmente en un pliegue de piel del abdomen o en la parte alta de la cadera). Antes o después de la intervención se administrará una dosis del producto (el contenido de una jeringa). Los días siguientes se administrará una dosis (el contenido de una jeringa) cada día. Su médico le dirá cuánto tiempo le deben administrar este medicamento.
Prevención de la coagulación en el circuito de circulación extracorpórea durante la hemodiálisis:
- En los pacientes sometidos a sesiones de hemodiálisis Phivor 3.500 UI se administra generalmente inyectando una única dosis en forma de bolus (el contenido de una jeringa) en la línea arterial del circuito de diálisis.
Phivor se inyecta por debajo de la piel, generalmente en un pliegue de piel de un lado de la cintura (abdomen) o en la parte alta de la cadera. Normalmente, su médico o enfermera le pondrán la inyección en el hospital. Puede que necesite continuar recibiendo Phivor cuando vuelva a casa.
- Este medicamento nunca debe inyectarse en un músculo o mezclarse con ninguna otra inyección.
- Normalmente se administra una vez al día.
- Su médico le dirá cuánto tiempo le deben administrar este medicamento (normalmente de 7-10 días).
- Si su médico le ha dicho que usted mismo puede inyectarse este medicamento, siga cuidadosamente las instrucciones de su médico (Ver sección “¿Cómo me inyecto Phivor?”).
Ancianos(a partir de 65 años)
Reciben, por lo general, la misma dosis que otros pacientes adultos. Si tiene problemas de hígado, por favor, comuníqueselo a su médico, es posible que decida hacerle un seguimiento muy de cerca.
Si tiene problemas de riñón, por favor, comuníqueselo a su médico quien le hará un seguimiento muy de cerca. En caso de que su enfermedad del riñón sea grave, su médico podría considerar necesario un ajuste de dosis.
Uso en niños(menores de 18 años)
Phivor no está recomendado en niños.
¿Cómo me inyecto Phivor?
Phivor nunca se debe inyectar en un músculo porque podría provocar un sangrado dentro del músculo. Antes de ponerse su primera inyección, usted deberá recibir instrucciones sobre la forma correcta de utilizar este medicamento y sobre la técnica correcta de autoinyección. Estas instrucciones se las debe dar un médico u otro profesional sanitario debidamente cualificado.
Debe seguir estos pasos:
- Lávese bien las manos y siéntese o túmbese en una posición cómoda.
- Elija una zona de la cintura que esté, por lo menos, a 5 centímetros del ombligo y de cualquier cicatriz o moratón, y limpie bien la piel de esa zona.
- Utilice cada día sitios diferentes para la inyección, por ejemplo, primero en el lado izquierdo y la próxima vez en el derecho.
- Quite el capuchón que tapa la aguja de la jeringa de Phivor.
- Para mantener la aguja estéril, asegúrese de que no toca nada.
- La jeringa precargada ya está lista para usarla.
- Antes de la inyección, no empuje el vástago para eliminar las burbujas de aire, porque puede perder medicamento.
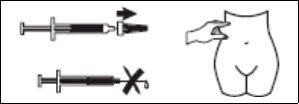
- Coja la jeringa con una mano y con la otra, usando los dedos índice y pulgar, coja un pellizco de la zona de piel que había limpiado para formar un pliegue.
- Introduzca la aguja entera en el pliegue de piel manteniendo la jeringa lo más erguida posible sobre la superficie del cuerpo, en un ángulo de 90º.
- Empuje el vástago asegurándose de que mantiene el pliegue de piel en la misma posición hasta que el vástago esté abajo del todo.
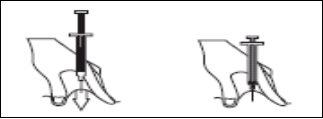
- Retire la jeringa del lugar de la inyección manteniendo el dedo sobre el vástago del émbolo y la jeringa erguida. Suelte el pliegue de piel.
- No frote la piel donde se ha puesto la inyección. Esto ayudará a evitar que salgan moratones.
- No trate de poner otra vez el capuchón en la jeringa. Deseche inmediatamente la jeringa arrojándola al contenedor de objetos punzantes más cercano (la aguja primero), cierre bien el contenedor con la tapa y póngalo fuera del alcance de los niños.
- Si estima que el efecto es demasiado fuerte (por ejemplo, porque experimenta un sangrado inesperado) o demasiado débil (por ejemplo, porque la dosis no parece funcionar) comuníqueselo a su médico o farmacéutico.
En algunos tamaños de envase, la jeringa precargada puede ser combinada con un dispositivo de seguridad el cual se activará después de la inyección para reducir el riesgo de lesiones por pinchazo de aguja.
Para jeringas con dispositivo de seguridad: Oriente la aguja lejos de usted y de cualquiera que esté presente, active el sistema de seguridad presionando firmemente sobre el vástago del émbolo. La funda protectora cubrirá automáticamente la aguja y se producirá un click audible que confirma la activación del dispositivo.
Deseche inmediatamente la jeringa arrojándola al contenedor de objetos punzantes más cercano (la aguja hacia dentro), cierre bien el contenedor con la tapa y póngalo fuera del alcance de los niños.
Si usa más Phivor del que debe
Es posible que pueda presentar algún tipo de sangrado. En tal caso, consulte inmediatamente a su médico o diríjase al servicio de urgencias del hospital más próximo, acompañado de este prospecto.
En caso de sobredosis o administración accidental, consulte al Servicio de Información Toxicológica. Teléfono 91 562 04 20.
Si olvidó utilizar Phivor
No tome una dosis doble para compensar la dosis olvidada. Consulte a su médico lo antes posible para que le indique qué es lo que debe hacer en estos casos.
Si interrumpe el tratamiento con Phivor
Consulte siempre con su médico antes de dejar de usar este medicamento.
Si tiene cualquier otra duda sobre el uso de este medicamento, pregunte a su médico o farmacéutico.
4. Posibles efectos adversos
Al igual que todos los medicamentos, este medicamento puede producir efectos adversos, aunque no todas las personas los sufran.
Deje de utilizar Phivor y consulte inmediatamente con su médico o enfermera (o vaya inmediatamente al servicio de urgencias del hospital más próximo), si sufre alguno de los siguientes efectos adversos:
Frecuentes(pueden afectar a entre 1 y 10 de cada 100 pacientes):
- Sangrado inusual o inesperado, por ejemplo, que haya sangre en la orina o heces, pudiendo ocasionar anemia hemorrágica.
Raros(pueden afectar a entre 1 y 10 de cada 1.000 pacientes):
- Descenso grave en el número de plaquetas (trombocitopenia tipo II), que puede llevar a la aparición de moratones, sangrado de encías, nariz y boca, erupciones.
- Daños en la piel (necrosis) en los puntos de inyección.
- Hematomas intra-espinales tras anestesia espinal o lumbar (dolor de espalda, entumecimiento y pérdida de fuerza o de sensibilidad en las piernas, incontinencia en intestino o la vejiga). Estos hematomas pueden ocasionar distintos grados de discapacidad, incluida parálisis durante tiempo prolongado o permanente.
- Reacciones alérgicas graves (subida de la temperatura del cuerpo, temblor, dificultad para respirar, hinchazón de las cuerdas vocales, mareo, sudoración, urticaria, erupción, picor, bajada de la tensión arterial, sofocos, enrojecimiento, síncope, contracción del tubo bronquial, hinchazón de la laringe).
Otros efectos adversos:
Muy frecuentes (afectan a más de 1 paciente de cada 10):
- Moratones, manchas en la piel, picor y algo de dolor en las áreas donde inyectó el medicamento.
Frecuentes (pueden afectar a entre 1 y 10 de cada 100 pacientes):
- Un aumento leve y transitorio de ciertas enzimas (transaminasas) en el hígado, que podría aparecer en los análisis de sangre.
Poco frecuentes (pueden afectar al menos a 10 de cada 1.000 pacientes):
- Reacciones alérgicas leves en la piel (sarpullido, erupción cutánea, urticaria, prurito, ronchas).
- Descenso leve y transitorio del número de plaquetas (trombocitopenia tipo I), que podría aparecer en los análisis de sangre.
Frecuencia no conocida (no puede estimarse a partir de los datos disponibles):
- Hiperpotasemia (aumento de los niveles de potasio en sangre).
- Fragilidad de huesos (osteoporosis) que se ha asociado al uso prolongado de tratamiento con heparina.
Comunicación de efectos adversos
Si experimenta cualquier tipo de efecto adverso, consulte a su médico o farmacéutico, incluso si se trata de posibles efectos adversos que no aparecen en este prospecto. También puede comunicarlos directamente a través del Sistema Español de Farmacovigilancia de Medicamentos de Uso Humano: https://www.notificaRAM.es.Mediante la comunicación de efectos adversos usted puede contribuir a proporcionar más información sobre la seguridad de este medicamento.
5. Conservación de Phivor
Mantener este medicamento fuera de la vista y del alcance de los niños.
No conservar a temperatura superior a 30ºC. No congelar.
No utilice este medicamento si observa:
- Que el envase protector está abierto.
- Que el envase protector está dañado.
- Que el medicamento contenido en la jeringa está turbio.
- Partículas pequeñas en el medicamento.
Una vez abierto el blister que contiene la jeringa, el medicamento debe ser utilizado inmediatamente.
Fecha de caducidad:
No utilice este medicamento después de la fecha de caducidad que aparece en el envase.
La fecha de caducidad es el último día del mes que se indica.
Eliminación
Este medicamento se presenta en jeringas para un sólo uso.
Deposite las jeringas usadas en un contenedor de residuos peligrosos.
No las guarde después de usarlas.
Los medicamentos no se deben tirar por los desagües ni a la basura. Pregunte a su farmacéutico cómo deshacerse de los envases y los medicamentos que ya no necesita. De esta forma, ayudará a proteger el medio ambiente.
6. Contenido del envase e información adicional
Composición de Phivor
El principio activo es: Bemiparina sódica 3.500 UI
Los demás componentes son: Agua para inyectables.
Aspecto del producto y contenido del envase
El medicamento contenido en las jeringas es una solución transparente, incolora o ligeramente amarillenta, sin partículas visibles.
Phivor 3.500 UI está disponible en cajas de 2, 10, 30 y 100 jeringas precargadas. Cada jeringa contiene 0,2 ml de solución. Cada jeringa de 0,2 ml proporciona una dosis de bemiparina sódica de 3.500 UI.
Puede que no se comercialicen todos los envases.
Titular de la autorización de comercialización y responsable de la fabricación
Titular de la autorización de comercialización
GINELADIUS, S.L.
C/ Rufino González 50, 28037 Madrid - España
Responsable de la fabricación
ROVI Pharma Industrial Services, S.A.
C/ Julián Camarillo, 35
28037 MADRID
LABORATORIOS FARMACÉUTICOS ROVI, S.A.
C/ Julián Camarillo, 35
28037 MADRID
Este medicamento está autorizado en los estados miembros del Espacio Económico Europeo con los siguientes nombres:
Ivor:Austria, Grecia, Italia, Portugal
Zibor:República Checa, Estonia, Hungría, Irlanda, Letonia, Lituania, Polonia, Eslovaquia, Eslovenia, Reino Unido.
Phivor:España
Fecha de la última revisión de este prospecto: 05/2023
La información detallada de este medicamento está disponible en la página web de la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) http://www.aemps.gob.es/
- País de registro
- Principio activo
- Requiere recetaSí
- Fabricante
- Esta información es de carácter general y no sustituye la consulta con un profesional sanitario.
- Alternativas a PHIVOR 3.500 UI ANTI XA/0,2 ML DE SOLUCION EN JERINGAS PRECARGASForma farmacéutica: INYECTABLE, 10000/IUPrincipio activo: bemiparinFabricante: Laboratorios Farmaceuticos Rovi S.A.Requiere recetaForma farmacéutica: INYECTABLE, 12.500/UIPrincipio activo: bemiparinFabricante: Laboratorios Farmaceuticos Rovi S.A.Requiere recetaForma farmacéutica: INYECTABLE, 2500/UIPrincipio activo: bemiparinFabricante: Laboratorios Farmaceuticos Rovi S.A.Requiere receta
Médicos online para PHIVOR 3.500 UI ANTI XA/0,2 ML DE SOLUCION EN JERINGAS PRECARGAS
Comenta la dosis, los posibles efectos secundarios, interacciones, contraindicaciones o la revisión de receta de PHIVOR 3.500 UI ANTI XA/0,2 ML DE SOLUCION EN JERINGAS PRECARGAS, sujeto a valoración médica y a la normativa local.
Preguntas frecuentes















