
KABIVEN EMULSION PARA PERFUSION
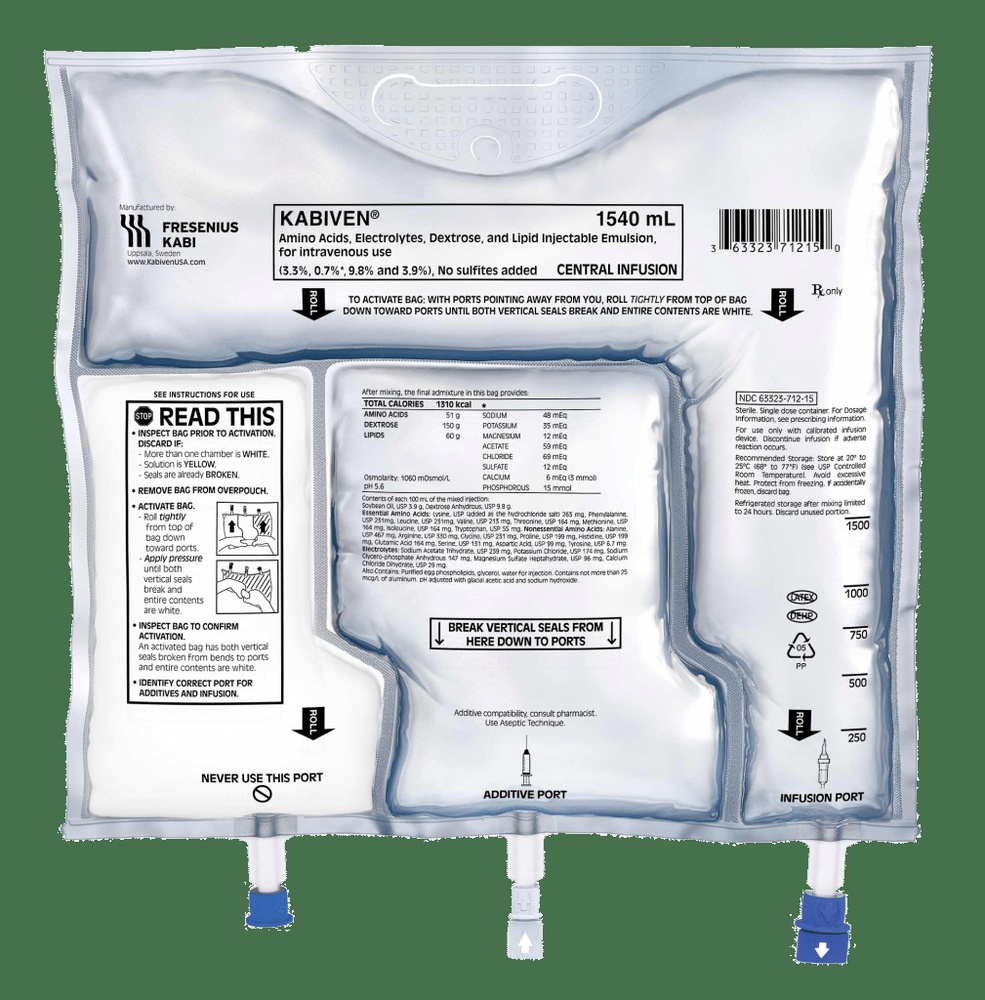

Cómo usar KABIVEN EMULSION PARA PERFUSION
Traducción generada por IA
Este contenido ha sido traducido automáticamente y se ofrece solo con fines informativos. No sustituye la consulta con un profesional sanitario.
Ver originalContenido del prospecto
Introducción
Prospecto: información para el paciente
Kabiven emulsión para perfusión
Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene información importante para usted:
- Conserve este prospecto, ya que puede tener que volver a leerlo.
- Si tiene alguna duda, consulte a su médico, farmacéutico o enfermero.
- Si experimenta efectos adversos, consulte a su médico, farmacéutico o enfermero, incluso si se trata de efectos adversos que no aparecen en este prospecto. Ver sección 4
Contenido del prospecto:
- Qué es Kabiven y para qué se utiliza
- Qué necesita saber antes de empezar a usar Kabiven
- Cómo usar Kabiven
- Posibles efectos adversos
- Conservación de Kabiven
- Contenido del envase e información adicional
-
1. Qué es Kabiven y para qué se utiliza
Kabiven se presenta en una bolsa de tres cámaras con sobrebolsa. Kabiven contiene los siguientes medicamentos: aminoácidos (componentes utilizados para construir proteínas), lípidos, glucosa y electrolitos. Proporciona energía (en forma de azúcar y lípidos) y aminoácidos a su flujo sanguíneo cuando no puede alimentarse normalmente.
Se utiliza como parte de una dieta intravenosa equilibrada, conjuntamente con sales, elementos traza y vitaminas para cumplir de forma completa con sus necesidades nutricionales.
2. Qué necesita saber antes de empezar a usa Kabiven
No use Kabiven:
- si es alérgico a alguna sustancia activa o a alguno de los componentes de este medicamento (listados en sección 6).
- si es alérgico a productos que contengan huevo, soja o cacahuete
- si tiene demasiadas sustancias grasas(como colesterol) en su sangre
- si tiene su función hepáticagravemente disminuida
- si sufre shock agudo(dando lugar a pérdida de sangre importante o reacción alérgica)
- si tiene alteraciones hemorrágicasasociadas con una situación conocida (como síndrome hemofagocitótico) o si su sangre no coagula adecuadamente
- si presenta una situación en la que su organismo tiene problemas en la utilización de proteínas o aminoácidos
- si tiene problemas graves en sus riñones
- si presenta hiperglicemia (demasiado azúcar en su sangre) que requiere la administración de más de 6 unidades de insulina por hora
- si tiene niveles elevados de electrolitos(sales) en su sangre
- si tiene acidosis metabólica(los niveles de ácido en sus líquidos corporales y tejidos son demasiado elevados)
- si presenta demasiado líquidoen su organismo (hiperhidratación)
- si tiene líquido en sus pulmones(edema pulmonar agudo)
- si está en coma
- si padece problemas de corazón
- si está deshidratadocon bajos niveles de sales
- si tiene sepsis grave(una situación en la que su organismo padece una infección grave)
Advertencias y precauciones
Informe a su médico antes de que se le administre Kabiven si tiene:
- función hepáticadisminuida
- diabetesdescompensada
- una situación en la que su organismo presenta problemas en la utilización de lípidosde forma adecuada
- alteración en los riñones
- cualquier problema en el páncreas
- problemas de tiroides– hipotiroidismo
- sepsis(una situación en la que su organismo sufre una infección)
- su organismo tiene problemas para la eliminación de electrolitos
- una situación en la que no hay suficiente oxígenoen sus células corporales
- osmolaridad sérica incrementada
Si durante la perfusión usted sufre fiebre, erupción cutánea, escalofríos o dificultad para respirar, informe al profesional sanitario inmediatamente. Estos síntomas pueden ser causados por una reacción alérgica o porque usted ha recibido demasiado medicamento (ver sección 4).
Este medicamento puede afectar a los resultados de otras pruebasque le realicen. Es importante que le comunique al médico que va a realizar las pruebas, que está recibiendo Kabiven.
Su médico puede realizarle de forma regular análisis de sangre para garantizar que su organismo está recibiendo Kabiven correctamente.
Niños
Kabiven no será administrado a recién nacidos o niños menores de dos años de edad.
Uso de Kabiven con otros medicamentos
Informe a su médico o farmacéutico, si está tomando, ha tomado recientemente o podría tener que tomar otros medicamentos.
Informe a su médico si está tomando
- un fármaco conocido como heparina que es utilizado para prevenir la formación de coágulos de sangre y para ayudar a la dispersión de los mismos
- warfarina como vitamina K1, que se encuentra en el aceite de soja y que podría afectar a la capacidad de coagulación de la sangre
- insulina para el tratamiento de la diabetes
Embarazo y lactancia
Si está embarazada o en periodo de lactancia, cree que podría estar embarazada o tiene intención de quedarse embarazada, consulte con su médico o farmacéutico antes de utilizar este medicamento. La seguridad de uso de Kabiven durante el embarazo y la lactancia no ha sido comprobada. Si es necesaria la nutrición a través de sus venas (nutrición parenteral) durante el embarazo o la lactancia, su médico le administrará Kabiven sólo después de una exhaustiva consideración.
Conducción y uso de máquinas
No se espera que Kabiven afecte la habilidad para conducir y usar maquinaria.
3. Cómo usar Kabiven
Recibirá su medicamento mediante perfusión sólo a través de una vena central. La dosis de Kabiven y qué tamaño de bolsa es utilizado, depende de su peso corporal en kilogramos y de la capacidad de su organismo para utilizar lípidos y azúcar. Kabiven será perfundido lentamente durante un período de 12-24 horas. Su médico decidirá la dosis correcta que debe recibir usted o su hijo. Puede ser monitorizado durante el tratamiento.
Niños
Kabiven no es adecuado para su uso en recién nacidos o en niños de menos de dos años de edad.
Si toma mas Kabiven del que debe
Es muy poco probable que reciba más perfusión de la que debería, ya que su médico o enfermera le monitorizarán durante el tratamiento. Los efectos de una sobredosis pueden incluir náuseas, vómitos, escalofríos y retención de líquidos. También se ha reportado hiperglicemia (demasiado azúcar en su sangre) y alteraciones de electrolitos. En el caso de sobredosis, existe el riesgo de recibir demasiados lípidos. Es el llamado “síndrome de sobrecarga lipídica”. Para más información, ver la sección 4 “Posibles efectos adversos”. Si usted experimenta cualquiera de los síntomas descritos arriba o cree que ha recibido demasiado Kabiven, informe a su médico o enfermera inmediatamente. La perfusión puede ser detenida inmediatamente o continuar a dosis reducida.
Si tiene cualquier duda relacionada con el uso de este producto, pregunte a su médico o enfermera.
4. Posibles efectos adversos
Al igual que todos los medicamentos, Kabiven puede producir efectos adversos, aunque no todas las personas los sufran.
Kabiven puede causar una reacción alérgica (muy raros, puede afectar hasta 1 de cada 10.000 pacientes). Informe a su médico inmediatamente si:
- aparece en su organismo una erupción cutánea con ronchas y picor
- usted tiene temperatura muy elevada
- usted tiene dificultades para respirar
Otros efectos adversos incluyen:
Efectos adversos frecuentes (puede afectar hasta 1 de cada 10 pacientes)
- ligero aumento de la temperatura corporal
Efectos adversos poco frecuentes (puede afectar hasta 1 de cada 100 pacientes)
- escalofríos
- cansancio
- dolor de estómago
- dolor de cabeza
- sensación de enfermedad
- aumento de los enzimas hepáticos. Su médico le indicará si esto ocurre
Muy raros (puede afectar hasta 1 de cada 10.000 pacientes)
- presión sanguínea elevada o baja
- dificultad para respirar
- erecciones prolongadas y dolorosas en hombres
- problemas en su sangre
Síndrome de sobrecarga lipídica
Esto podría ocurrir si su organismo tuviera problemas en la utilización de los lípidos, y usted hubiera recibido demasiado Kabiven. También puede ocurrir debido a un cambio repentino en su situación (como problemas en sus riñones o infección). Los síntomas posibles son fiebre, niveles elevados de lípidos en su sangre, en sus células y en sus tejidos, alteraciones en varios órganos y coma. Todos estos síntomas generalmente desaparecerán si la perfusión se detiene.
Comunicación de efectos adversos
Si experimenta cualquier tipo de efecto adverso, consulte a su médico, farmacéutico o enfermero, incluso si se trata de efectos adversos que no aparecen en este prospecto. También puede comunicarlos directamente a través del Sistema Español de Farmacovigilancia de Medicamentos de Uso Humano: www.notificaRAM.es. Mediante la comunicación de efectos adversos usted puede contribuir a proporcionar más información sobre la seguridad de este medicamento.
5. Conservación de Kabiven
Mantener este medicamento fuera de la vista y del alcance de los niños
Su médico o el farmacéutico del hospital son responsables de la correcta conservación, utilización y eliminación de la perfusión Kabiven. No conservar por encima de 25°C. No congelar y mantener siempre el envase en el contenedor externo.
La emulsión no debe ser utilizada después de la fecha de caducidad indicada en la etiqueta. Cualquier resto de emulsión sobrante debe ser retirada a través de los procedimientos hospitalarios autorizados.
.
6. Contenido del envase e información adicional
Composición de Kabiven
Kabiven está disponible en un sistema de bolsa de tres cámaras. Cada bolsa contiene los siguientes diferentes volúmenes dependiendo de los cuatro tamaños de envase:
2566 ml | 2053 ml | 1540 ml | 1026 ml | |
Glucosa (Glucosa 19 %) Aminoacidos y electrolitos (Vamin 18 Novum) Emulsión lipídica (Intralipid 20%) | 1316 ml 750 ml 500 ml | 1053 ml 600 ml 400 ml | 790 ml 450 ml 300 ml | 526 ml 300 ml 200 ml |
- Las sustancias activas son
Aceite de soja purificado Glucosa monohidrato Glucosa (anhidra) | 100 g 275 g 250 g | 80 g 220 g 200 g | 60 g 165 g 150 g | 40 g 110 g 100 g |
Aminoácidos Alanina Arginina Acido aspártico Acido glutámico Glicina Histidina Isoleucina Leucina Lisina Metionina Fenilalanina Prolina Serina Treonina Triptófano Tirosina Valina Cloruro cálcico 2H2O Correspondiente a Cloruro cálcico Glicerofosfato sódico (anhidro) Sulfato magnésico 7H2O Correspondiente a Sulfato magnésico Cloruro potásico Acetato sódico 3H2O Correspondiente a acetato sódico | 12,0 g 8,5 g 2,6 g 4,2 g 5,9 g 5,1 g 4,2 g 5,9 g 6,8 g 4,2 g 5,9 g 5,1 g 3,4 g 4,2 g 1,4 g 0,17 g 5,5 g 0,74 g 0,56 g 3,8 g 2,5 g 1,2 g 4,5 g 6,1 g 3,7 g | 9,6 g 6,8 g 2,0 g 3,4 g 4,7 g 4,1 g 3,4 g 4,7 g 5,4 g 3,4 g 4,7 g 4,1 g 2,7 g 3,4 g 1,1 g 0,14 g 4,4 g 0,59 g 0,44 g 3,0 g 2,0 g 0,96 g 3,6 g 4,9 g 2,9 g | 7,2 g 5,1 g 1,5 g 2,5 g 3,6 g 3,1 g 2,5 g 3,6 g 4,1 g 2,5 g 3,6 g 3,1 g 2,0 g 2,5 g 0,86 g 0,10 g 3,3 g 0,44 g 0,33 g 2,3 g 1,5 g 0,72 g 2,7 g 3,7 g 2,2 g | 4,8 g 3,4 g 1,0 g 1,7 g 2,4 g 2,0 g 1,7 g 2,4 g 2,7 g 1,7 g 2,4 g 2,0 g 1,4 g 1,7 g 0,57 g 0,07 g 2,2 g 0,29 g 0,22 g 1,5 g 0,99 g 0,48 g 1,8 g 2,5 g 1,5 g |
- Los otros ingredientes son
Fosfolípidos de huevo purificados
Glicerol
Hidróxido sódico
Ácido acético glacial
Agua para preparaciones inyectables.
Aspecto del producto y contenido del envase
Las soluciones de glucosa y aminoácidos son transparentes e incoloras o ligeramente amarillas, y la emulsión lipídica es blanca. Kabiven consiste en una bolsa de tres cámaras y una sobrebolsa. Entre la bolsa interna y la sobrebolsa se coloca un absorbente de oxígeno. La bolsa interna está separada en tres cámaras mediante soldaduras tipo peel. Los contenidos de las tres cámaras deben ser mezclados antes de su uso, mediante la apertura de las soldaduras peel.
Tamaños de envase
1 x 1026 ml, 4 x 1026 ml
1 x 1540 ml, 4 x 1540 ml
1 x 2053 ml, 4 x 2053 ml
1 x 2566 ml, 3 x 2566 ml
Puede que solamente estén comercializados algunos tamaños de envases.
Titular de la autorización de comercialización y responsable de la fabricación
Titular de la autorización de comercialización
Fresenius Kabi AB
SE-751 74 Uppsala, Suecia
Responsable de la fabricación
Fresenius Kabi AB
SE-751 74 Uppsala, Suecia
Este producto medicinal está autorizado en los estados miembros del Espacio Económico Europeo con los siguientes nombres:
Bélgica | Kabiven |
Dinamarca | Kabiven |
Finlandia | Kabiven |
Francia | Kabiven |
Alemania | Kabiven |
Grecia | Kabiven |
Islandia | Kabiven |
Irlanda | Kabiven |
Italia | Kabiven |
Luxemburgo | Kabiven |
Holanda | Kabiven |
Portugal | Kabiven |
España | Kabiven |
Suecia | Kabiven |
Reino Unido | Kabiven |
Fecha de la última revisión de este prospecto: Abril 2019
La información detallada y actualizada de este medicamento está disponible en la página Web de la Agencia Española del Medicamento y Productos Sanitarios (AEMPS) http://www.aemps.gob.es/
--------------------------------------------------------------------------------------------------------------------
Esta información está destinada únicamente a profesionales del sector sanitario
Advertencias y precauciones de uso
Para evitar el riesgo asociado a una velocidad de perfusión demasiado rápida, se recomienda llevar a cabo una perfusión continua y bien controlada, si es posible utilizando una bomba volumétrica.
Teniendo en cuenta el elevado riesgo de infección asociado al uso de una vena central, deben tomarse precauciones asépticas estrictas para evitar cualquier contaminación durante la inserción del catéter y la manipulación.
Deben monitorizarse los niveles séricos de glucosa, electrolitos y osmolaridad, así como el balance hídrico, el equilibrio ácido-base y los tests de enzimas hepáticos.
Ante cualquier signo o síntoma de reacción anafiláctica (como fiebre, escalofríos, erupción cutánea o disnea) debe interrumpirse inmediatamente la perfusión.
Kabiven no debe ser administrado simultáneamente con sangre en el mismo equipo de perfusión, debido al riesgo de pseudoaglutinación.
Método de administración
Vía intravenosa, perfusión en una vena central.
Velocidad de perfusión
La velocidad de perfusión máxima para glucosa es 0,25 g/kg pc/h.
La dosificación de aminoácidos no debería exceder 0,1 g/kg pc/h.
La dosificación de lípidos no debería superar 0,15 g/kg pc/h.
La velocidad de perfusión no debe exceder 2,6 ml/kg peso corporal/hora (correspondiente a 0,25 g de glucosa, 0,09 g de aminoácidos y 0,1 g de lípidos/kg peso corporal). El período de perfusión recomendado es de 12-24 horas.
Precauciones para la eliminación
No utilizar el envase si no está intacto. Utilizar sólo si las soluciones de glucosa y aminoácidos son transparentes e incoloras o ligeramente amarillas, y la emulsión lipídica es blanca y homogénea. Los contenidos de las tres cámaras separadas deben ser mezclados antes de su uso y previamente a cualquier adición realizada a través del puerto de aditivos.
Después de la separación de las soldaduras peel, la bolsa debe ser invertida varias veces, para garantizar una mezcla homogénea que no muestre evidencia de separación de fases.
Para un solo uso. Debe rechazarse cualquier mezcla sobrante después de la perfusión.
Compatibilidad
Existen datos de compatibilidad en cantidades definidas con los productos de marca Dipeptiven, Supliven, Glycophos, Vitalipid Adultos/Infantil y Soluvit y genéricos de electrolitos en concentraciones definidas. Cuando se realicen adiciones de electrolitos, deben tenerse en cuenta las cantidades ya presentes en la bolsa para satisfacer las necesidades clínicas del paciente. Los datos generados apoyan las adiciones a la bolsa activada de según la tabla de resumen que se muestra a continuación:
Rango de compatibilidad estable durante 8 días, es decir, 6 días de almacenamiento a 2-8 °C seguidos de 48 horas a 20-25 °C
Unidades | Contenido total máximo | ||||
Tamaño de la bolsa Kabiven | ml | 1026 | 1540 | 2053 | 2566 |
Aditivo | Volumen | ||||
Dipeptiven | ml | 0 - 200 | 0 - 300 | 0 - 300 | 0 - 300 |
Supliven | ml | 0 - 10 | 0 - 10 | 0 - 20 | 0 - 20 |
Soluvit | vial | 0 - 1 | 0 - 1 | 0 - 2 | 0 - 2 |
Vitalipid Adulto/Infantil | ml | 0 - 10 | 0 - 10 | 0 - 20 | 0 - 20 |
Límite electrolitos1 | Cantidad por bolsa | ||||
Sodio | mmol | ≤ 154 | ≤ 231 | ≤ 308 | ≤ 385 |
Potasio | mmol | ≤ 154 | ≤ 231 | ≤ 308 | ≤ 385 |
Calcio | mmol | ≤ 5 | ≤ 7,5 | ≤ 10 | ≤ 12,5 |
Magnesio | mmol | ≤ 5 | ≤ 7,5 | ≤ 10 | ≤ 12,5 |
Fosfato orgánico (Glycophos) | mmol | ≤ 15 | ≤ 22,5 | ≤ 30 | ≤ 37,5 |
- incluye las cantidades de todos los productos
Nota: Esta tabla pretende indicar compatibilidad. No es una guía de dosificación. En el caso de los productos con nombre comercial, antes de prescribirlos, consulte la ficha técnica aprobada.
Existen datos sobre la compatibilidad con otros aditivos y el tiempo de conservación de las diferentes mezclas, disponibles bajo petición.
Las adiciones deben realizarse asépticamente.
La eliminación del medicamento no utilizado y de todos los materiales que hayan estado en contacto con él, se realizará de acuerdo con la normativa local.
Caducidad después de mezclar las cámaras de la bolsa
Después de la apertura de las soldaduras peel, se ha demostrado una estabilidad química y física de la bolsa de tres cámaras mezclada, de 48 horas a 20-25 °C incluyendo duración de administración. Desde un punto de vista microbiológico, el producto debería utilizarse inmediatamente. Si no es utilizado inmediatamente, el tiempo de conservación hasta su utilización y las condiciones previstas a su uso son responsabilidad del usuario y normalmente no excederán las 24 horas a 2-8 °C, a menos que la mezcla se haya realizado en condiciones asépticas controladas y validadas.
Caducidad después de la mezcla con aditivos
Después de romper las soldaduras peel y mezclar las tres soluciones, pueden realizarse adiciones a través del puerto de adición de medicamentos. Se ha demostrado la estabilidad fisicoquímica en uso de la bolsa de tres cámaras mezclada con aditivos durante un máximo de 8 días, es decir, 6 días a 2-8 °C seguidos de 48 horas a 20-25 °C, incluida la duración de la administración.
Desde un punto de vista microbiológico, el producto debería utilizarse inmediatamente después de realizar las adiciones. Si no es utilizado inmediatamente, el tiempo de conservación hasta su utilización y las condiciones previas a su uso son responsabilidad del usuario y normalmente no deberían ser superiores a 24 horas a 2-8 ?C, a menos que la mezcla se haya realizado en condiciones asépticas controladas y validadas.
Instrucciones de uso Kabiven
La bolsa
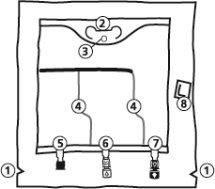
- Muescas en la sobrebolsa
- Colgador
- Anilla para colgar la bolsa
- Soldaduras peel
- Puerto sin salida (sólo se usa durante la Fabricación)
- Puerto de adición
- Puerto de perfusión
- Absorbente de oxígeno
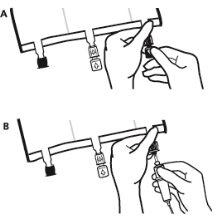
- Extracción de la sobrebolsa
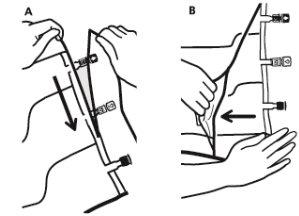
- Para extraer la sobrebolsa, sujetarla en posición horizontal y rasgar por la muesca hacia los puertos a lo largo del borde superior (A).
- Entonces, simplemente rasgar a lo largo del envase; separar la sobrebolsa y desecharla junto con el absorbente de oxígeno (B).
- Mezcla
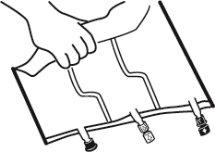
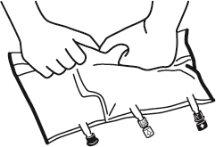
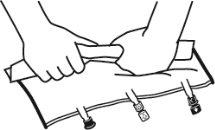
- Colocar la bolsa en una superficie plana.
- Enrollar la bolsa desde la parte del colgador hacia la parte de los puertos, primero con la mano derecha y a continuación aplicando una presión constante con la mano izquierda hasta que las soldaduras verticales se hayan abierto. Las soldaduras peel verticales se abren debido a la presión del líquido. Las soldaduras peel también pueden ser abiertas antes de retirar la sobrebolsa.
Nota:los líquidos se mezclan fácilmente aunque la soldadura horizontal permanezca cerrada.
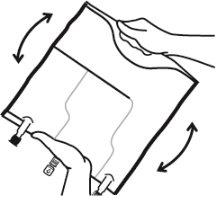
- Mezclar los contenidos de las tres cámaras invirtiendo la bolsa tres veces hasta que los componentes estén completamente mezclados.
- Finalización de la preparación
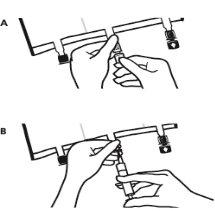
- Colocar la bolsa de nuevo sobre una superficie plana. Poco antes de inyectar los aditivos, romper el puerto de adición blanco por la marca en forma de flecha (A).
Nota:La membrana del puerto de aditivos es estéril
- Sujetar la base del puerto de aditivos. Insertar la aguja, inyectar los aditivos (de compatibilidad conocida) por el centro del punto de inyección (B).
- Mezclar completamente entre cada adición, invirtiendo la bolsa tres veces. Utilizar jeringas con agujas de calibre 18-23 y una longitud máxima de 40 mm.
- Poco antes de insertar el set de perfusión, romper el puerto de perfusión azul por la marca en forma de flecha (A).
Nota:La membrana del puerto de perfusión es estéril
- Usar un equipo de perfusión no venteado o cerrar la entrada del aire del equipo venteado.
- Sujetar la base del puerto de perfusión.
- Introducir el punzón a través del puerto de perfusión. El punzón deberá estar totalmente insertado para asegurar su retención.
Nota:La parte interna del puerto de perfusión es estéril
- Colgado de la bolsa
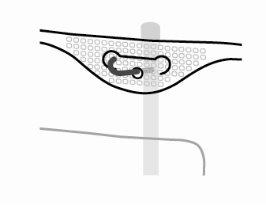
Colgar la bolsa por la anilla que hay bajo el colgador.
- País de registro
- Principio activo
- Requiere recetaSí
- Fabricante
- Esta información es de carácter general y no sustituye la consulta con un profesional sanitario.
- Alternativas a KABIVEN EMULSION PARA PERFUSIONForma farmacéutica: INYECTABLE PERFUSION, 3,92 g / 1,26 g / 7,21 g / 3,36 g / 4,2 g / 5,11 g / 2,94 g / 2,8 g / 4,76 g / 5,07 g / 4,06 g / 14,49 g / 0,28 g / 8,05 g / 3,5 g / 200 gPrincipio activo: combinationsFabricante: Baxter S.L.Requiere recetaForma farmacéutica: INYECTABLE PERFUSION, 3,5 g / 200 g / 5,22 g / 1,88 g / 3,92 g / 1,26 g / 7,21 g / 3,36 g / 4,2 g / 5,11 g / 2,94 g / 2,8 g / 662 mg / 1,02 g / 4,76 g / 5,15 g / 5,07 g / 4,06 g / 14,49 g / 0,28 g / 8,05 gPrincipio activo: combinationsFabricante: Baxter S.L.Requiere recetaForma farmacéutica: INYECTABLE PERFUSION, 4,25 g / 300 g / 5,22 g / 1,54 g / 4,76 g / 1,53 g / 8,76 g / 4,08 g / 5,1 g / 6,2 g / 3,57 g / 3,4 g / 662 mg / 1,02 g / 5,78 g / 5,94 g / 6,16 g / 4,93 g / 17,6 g / 0,34 g / 9,78 gPrincipio activo: combinationsFabricante: Baxter S.L.Requiere receta
Médicos online para KABIVEN EMULSION PARA PERFUSION
Comenta la dosis, los posibles efectos secundarios, interacciones, contraindicaciones o la revisión de receta de KABIVEN EMULSION PARA PERFUSION, sujeto a valoración médica y a la normativa local.
Preguntas frecuentes















