ILARIS 150 MG/ML SOLUCION INYECTABLE

Cómo usar ILARIS 150 MG/ML SOLUCION INYECTABLE
Traducción generada por IA
Este contenido ha sido traducido automáticamente y se ofrece solo con fines informativos. No sustituye la consulta con un profesional sanitario.
Ver originalContenido del prospecto
Introducción
Prospecto: información para el usuario
Ilaris 150mg/ml solución inyectable
canakinumab
Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene información importante para usted.
- Conserve este prospecto, ya que puede tener que volver a leerlo.
- Si tiene alguna duda, consulte a su médico, farmacéutico o enfermero.
- Este medicamento se le ha recetado solamente a usted, y no debe dárselo a otras personas aunque tengan los mismos síntomas que usted, ya que puede perjudicarles.
- Si experimenta efectos adversos, consulte a su médico, farmacéutico o enfermero, incluso si se trata de efectos adversos que no aparecen en este prospecto. Ver sección 4.
Además de este prospecto, se le entregará una tarjeta para el paciente, que contiene información de seguridad importante que necesita antes y durante el tratamiento con Ilaris.
Contenido del prospecto
- Qué es Ilaris y para qué se utiliza
- Qué necesita saber antes de empezar a usar Ilaris
- Cómo usar Ilaris
- Posibles efectos adversos
- Conservación de Ilaris
- Contenido del envase e información adicional
1. Qué es Ilaris y para qué se utiliza
Qué es Ilaris
Ilaris contiene el principio activo canakinumab, un anticuerpo monoclonal que pertenece al grupo de los medicamentos denominados inhibidores de interleucinas. En el organismo bloquea la actividad de una sustancia llamada interleucina-1 beta (IL-1 beta), que se encuentra a niveles elevados en las enfermedades inflamatorias.
Para qué se utiliza Ilaris
Ilaris se utiliza para el tratamiento de las siguientes enfermedades inflamatorias:
- Síndromes de fiebre periódica:
- síndromes periódicos asociados a la criopirina (CAPS*)
- síndrome periódico asociado al receptor del factor de necrosis tumoral (TRAPS*)
- síndrome de hiperinmunoglobulina D (HIDS*)/deficiencia de mevalonato quinasa (MKD*)
- fiebre mediterránea familiar (FMF).
- Enfermedad de Still incluyendo la enfermedad de Still del adulto (ESA) y la artritis ideopática juvenil sistémica (AIJS)
- Gota artrítica
(*) por sus siglas en inglés
A continuación se incluye más información sobre estas enfermedades.
Síndromes de fiebre periódica
Ilaris se utiliza en adultos y niños a partir de 2 años para tratar las siguientes enfermedades:
- Síndromes periódicos asociados a la criopirina (CAPS) – es un grupo de enfermedades autoinflamatorias, que incluye:
- síndrome de Muckle-Wells (MWS)
- enfermedad neonatal multisistémica inflamatoria (NOMID), también conocida como síndrome infantil neurológico, cutáneo y articular crónico (CINCA)
- manifestaciones graves del síndrome autoinflamatorio familiar inducido por el frío (FCAS) / urticaria familiar fría (FCU) que presente signos y síntomas más allá de la erupción de la piel de tipo urticaria inducido por el frío.
- Síndrome periódico asociado al receptor del factor de necrosis tumoral (TRAPS)
- Síndrome de hiperinmunoglobulina D (HIDS)/deficiencia de mevalonato quinasa (MKD)
- Fiebre Mediterránea familiar (FMF): Ilaris se utiliza para tratar la FMF. Ilaris se puede utilizar junto con colchicina, si es apropiado.
En pacientes con síndromes de fiebre periódica (CAPS, TRAPS, HIDS/MKD y FMF), el organismo produce demasiada IL-1 beta. Esto puede causar fiebre, dolor de cabeza, fatiga, erupción cutánea o dolores en las articulaciones y músculos. Mediante el bloqueo de la actividad de IL-1 beta, Ilaris puede mejorar estos síntomas.
Enfermedad de Still
Ilaris se utiliza en pacientes adultos, adolescentes y niños a partir de los 2 años de edad para el tratamiento de la enfermedad de Still activa incluyendo la enfermedad de Still del adulto (ESA) y la artritis idiopática juvenil sistémica (AIJS) cuando los otros tratamientos no hayan funcionado bien. Ilaris puede utilizarse sólo o en combinación con metrotrexato.
La enfermedad de Still que incluye AIJS y ESA es una enfermedad inflamatoria que puede provocar dolor, hinchazón e inflamación de una o más articulaciones, así como sarpullido y fiebre. La proteina pro-inflamatoria IL-1beta juega un importante papel en la inflamación de la enfermedad de Still. Ilaris puede mejorar los signos y síntomas de la enfermedad de Still bloqueando la actividad de IL-1beta.
Gota artrítica
Ilaris se utiliza en adultos para tratar los síntomas de ataques frecuentes de gota artrítica si otros tratamientos no han funcionado suficientemente bien.
La gota artrítica está causada por la formación de cristales de urato. Estos cristales de urato causan una producción excesiva de IL-1 beta, que a su vez pueden provocar un repentino dolor grave, enrojecimiento, calor, e hinchazón de las articulaciones (conocido como ataque de gota). Mediante el bloqueo de IL-1 beta, Ilaris puede conseguir mejorar estos síntomas.
2. Qué necesita saber antes de empezar a usar Ilaris
No use Ilaris
- si es alérgico al canakinumab o a alguno de los demás componentes de este medicamento (incluidos en la sección 6)
- si tiene, o sospecha que tiene, una infección grave y activa
Advertencias y precauciones
Consulte a su médico antes de empezar a usar Ilaris, si se encuentra en alguna de las siguientes situaciones:
- si padece alguna infección en la actualidad o si ha tenido infecciones repetidas o sufre alguna enfermedad tal como nivel bajo de góbulos blancos que le hace más vulnerable a tener infecciones
- si tiene o alguna vez ha tenido tuberculosis o contacto directo con una persona con una infección activa de tuberculosis. Su médico puede comprobar si tiene tuberculosis utilizando una prueba específica
- si tiene signos de un trastorno del hígado tales como coloración amarilla en la piel y los ojos, náuseas, pérdida del apetito, color oscuro en la orina y heces blanquecinas
- si tiene que ponerse alguna vacuna. Se recomienda evitar ser vacunado con un tipo de vacuna (también conocida como vacuna atenuada) mientras está usando Ilaris (ver también «Uso de Ilaris con otros medicamentos»).
- Este medicamento contiene 0,4 mg de polisorbato 80 en cada 1 ml de solución inyectable. Los polisorbatos pueden causar reacciones alérgicas. Informe a su médico si usted o su hijo tienen cualquier alergia conocida.
Consulte a su médico inmediatamente
- si alguna vez ha presentado una erupción generalizada atípica o descamación cutánea después de tomar Ilaris.
Rara vez se ha notificado una reacción cutánea grave, DRESS (reacción medicamentosa con eosinofilia y síntomas sistémicos), asociada al tratamiento con Ilaris, sobre todo en pacientes con artritis idiopática juvenil sistémica (AIJs). Solicite atención médica de inmediato si observa una erupción generalizada atípica, que puede aparecer junto con fiebre alta y aumento de tamaño de los ganglios linfáticos.
Enfermedad de Still
- Los pacientes con enfermedad de Still pueden desarrollar una enfermedad llamada síndrome de activación macrofágica (SAM) que puede causar la muerte. Su médico le hará un seguimiento de los posibles factores desencadenantes de SAM, que incluyen infecciones y re-activación de la enfermedad de Still (empeoramiento).
Trazabilidad
Cada vez que usted/su hijo reciba un nuevo envase de Ilaris, es importante que anote el nombre del medicamento y la fecha de administración junto con el número de lote y que conserve esta información en un lugar seguro.
Niños y adolescentes
- CAPS,TRAPS, HIDS/MKD, FMFy AIJS:Ilaris se puede utilizare en niños a partir de 2 años de edad.
- Gota artrítica:Ilaris no está recomendado para niños o adolescentes menores de 18 años de edad.
Otros medicamentos e Ilaris
Informe a su médico, farmacéutico o enfermero si está utilizando, ha utilizado recientemente o pudiera tener que utilizar cualquier otro medicamento.
- Vacunas atenuadas: se recomienda evitar ser vacunado con un tipo de vacuna conocida como vacuna atenuada mientras está en tratamiento con Ilaris. Puede que su médico necesite comprobar su historial de vacunaciones y darle aquellas vacunas que no ha recibido antes de iniciar el tratamiento con Ilaris. Si es necesario que le administren una vacuna atenuada después de iniciar el tratamiento con Ilaris, coméntelo con su médico. Una vacuna atenuada debe administrarse normalmente 3 meses después de su última inyección de Ilaris y 3 meses antes de la siguiente.
- Medicamentos conocidos como los inhibidores del factor de necrosis tumoral (TNF), tales como etanercept, adalimumab o infliximab. Éstos se utilizan principalmente en enfermedades reumáticas y autoinmunes. No deben utilizarse con Ilaris porque puede aumentar el riesgo de infecciones.
Embarazo y lactancia
Si está embarazada o en periodo de lactancia, cree que podría estar embarazada o tiene intención de quedarse embarazada, consulte a su médico o farmacéutico antes de utilizar este medicamento.
- Debe evitar quedar embarazada y se recomienda utilizar medidas anticonceptivas adecuadas mientras esté tomando Ilaris y durante al menos tres meses después de la última administración. Es importante que informe a su médico si está embarazada, si puede estar embarazada o si está planeando tener un bebé. Su médico le informará acerca del riesgo potencial de utilizar Ilaris durante el embarazo.
- Si recibe canakinumab mientras está embarazada, es importante que informe al pediatra o enfermero antes de que le administren alguna vacuna a su bebé. Su bebé no debe recibir vacunas vivas hasta al menos 16 semanas después de que usted haya recibido su última dosis de canakinumab antes del parto.
- Se desconoce si Ilaris pasa a la leche materna. Su médico le informará acerca de los riesgos potenciales de utilizar Ilaris antes de dar el pecho.
Conducción y uso de máquinas
El tratamiento con Ilaris puede producirle una sensación de que todo da vueltas (mareo o vértigo) o cansancio intenso (astenia). Esto se debe tener en cuenta cuando evalue su capacidad para realizar tareas que requieren juicio o habilidades motoras. Si nota la sensación de que todo le da vueltas o se siente cansado, no conduzca ni use herramientas o máquinas hasta que se sienta de nuevo bien.
3. Cómo usar Ilaris
Siga exactamente las instrucciones de administración de este medicamento indicadas por su médico. En caso de duda, consulte de nuevo a su médico, farmacéutico o enfermero.
Mantenga a su médico informado de su enfermedad y de cualquier síntoma antes de utilizar o que se le administre Ilaris (ver sección 2). Su médico puede decidir posponer o interrumpir su tratamiento, solo cuando sea necesario.
Ilaris se debe utilizar por vía subcutánea. Esto significa que se inyecta con una aguja corta dentro del tejipo adiposo por debajo de la piel.
Si tiene gota artrítica, un médico con formación especializada supervisará su tratamiento. Ilaris solo debe ser inyectado por un profesional sanitario.
Si tiene CAPS, TRAPS, HIDS/MKD, FMF o enfermedad de Still (ESA o AIJS), se puede inyectar usted mismo con Ilaris después de recibir una formación adecuada, o puede inyectársela un cuidador.
Cuánto Ilaris debe utilizar
Síndromes periódicos asociados a la criopirina (CAPS)
La dosis de inicio recomendada de Ilaris es en función del peso corporal:
- Adultos y niños de 4años o más
- 150 mg para pacientes que pesan más de 40 kg
- 2 mg/kg para pacientes que pesan entre 15 kg y 40 kg
- 4 mg/kg para pacientes que pesan entre 7,5 kg y menos de 15 kg
- Niños de2 o 3años
- 4 mg/kg para pacientes cuyo peso corporal sea de 7,5 kg o más
Ilaris se inyecta cada 8 semanas como una inyección única.
- Si no responde lo suficiente al tratamiento a los 7 días, su médico puede darle otra dosis de 150 mg o 2 mg/kg.
- Si responde lo suficiente a la segunda dosis, su tratamiento continuará con 300 mg o 4 mg/kg cada 8 semanas.
- Si no responde lo suficiente a la segunda dosis, se puede administrar una tercera dosis de Ilaris a 300 mg o 4 mg/kg.
- Si responde lo suficiente a la tercera dosis, su tratamiento continuará con 600 mg o 8 mg/kg cada 8 semanas.
En niños que han iniciado con una dosis inicial de 4 mg/kg y que no han respondido lo suficiente después de 7 días, el médico puede darle una segunda dosis de 4 mg/kg. Si el niño responde lo suficiente a ésta, se puede continuar el tratamiento con una dosis de 8 mg/kg cada 8 semanas.
Síndrome periódico asociado al receptor del factor de necrosis tumoral (TRAPS), síndrome de hiperinmunoglobulina D (HIDS)/deficiencia de mevalonato quinasa (MKD) y fiebre Mediterránea familiar (FMF)
La dosis de inicio recomendada de Ilaris es, en función del peso corporal:
- Adultos y niños de 2años o más
- 150 mg para pacientes que pesan más de 40 kg
- 2 mg/kg para pacientes que pesan entre 7,5 kg y menos de 40 kg
Ilaris se inyecta cada 4 semanas como una inyección única.
- Si no responde lo suficiente al tratamiento a los 7 días, su médico puede darle otra dosis de 150 mg o 2 mg/kg.
- Si responde lo suficiente a ésta, su tratamiento continuará con 300 mg o 4 mg/kg cada 4 semanas.
Enfermedad de Still (AIJS y ESA)
La dosis recomendada de Ilaris para pacientes con enfermedad de Still cuyo peso corporal sea de 7,5 kg o más es de 4 mg/kg (hasta un máximo de 300 mg). Ilaris se inyecta cada 4 semanas como una dosis única.
Gota artrítica
Su médico comentará con usted la necesidad de empezar o ajustar un tratamiento con reductores de urato para disminuir el nivel de ácido úrico de su sangre.
La dosis recomendada para Ilaris en pacientes adultos con gota es 150 mg administrada como una única dosis durante un ataque de gota artrítica.
Si necesita otro tratamiento con Ilaris, y con la última dosis obtuvo alivio, debe esperar un mínimo de 12 semanas antes de una siguiente dosis.
Autoinyección de Ilaris o inyección de Ilaris a un paciente
Si es un paciente con CAPS, TRAPS, HIDS/MKD, FMF o enfermedad de Still (ESA o AIJS), o un cuidador de un paciente con una de estas enfermedades, puede administrar usted mismo las inyecciones de Ilaris después de recibir una formación adecuada en relación con la técnica de inyección.
- El paciente o cuidador y el médico decidirán quién pondrá las inyecciones de Ilaris.
- Su médico o enfermero le enseñarán cómo poner las inyecciones de Ilaris.
- No debe tratar de ponerse una inyección si no ha recibido la formación necesaria o no está seguro de cómo hacerlo.
- Ilaris 150 mg/ml solución inyectable se suministra en un vial de un solo uso para uso individual.
- No reutilice la solución sobrante.
Para tener más información sobre cómo poner las inyecciones de Ilaris, consulte la sección «Instrucciones de uso» al final de este prospecto. Si tiene dudas, hable con su médico, farmacéutico o enfermero.
Duración del tratamiento con Ilaris
- CAPS,TRAPS, HIDS/MKD, FMFo enfermedad de Still (ESA o AIJS):debe continuar utilizando Ilaris durante el tiempo que su médico le aconseje.
- Gota artrítica:si tiene un ataque de gota artrítica, le administrarán una única dosis de Ilaris. Si experimenta un nuevo ataque, su médico puede considerar administrarle una nueva dosis de Ilaris pero no antes de las 12 semanas de haberle administrado la dosis previa.
Si usa más Ilaris del que debe
Si se inyecta accidentalmente más Ilaris de la dosis recomendada, no es probable que sea grave pero debe informar a su médico, farmacéutico o enfermero lo antes posible.
Si olvidó usar Ilaris
Si tiene CAPS, TRAPS, HIDS/MKD o FMF o enfermedad de Still (ESA o AIJS) y ha olvidado inyectarse una dosis de Ilaris, la dosis siguiente debe inyectarse tan pronto como lo recuerde. Entonces hable con el médico para acordar cuándo debe inyectare la dosis siguiente. A continuación, debe seguirse con la inyección a los intervalos recomendados como antes.
Si interrumpe el tratamiento con Ilaris
La interrupción de su tratamiento con Ilaris puede causar un empeoramiento de su enfermedad. No interrumpa el tratamiento con Ilaris a no ser que se lo indique su médico.
Si tiene cualquier otra duda sobre el uso de este medicamento, pregunte a su médico, farmacéutico o enfermero.
4. Posibles efectos adversos
Al igual que todos los medicamentos, este medicamento puede producir efectos adversos, aunque no todas las personas los sufran.
Algunos efectos adversos pueden ser graves. Informe a su médico inmediatamente, si experimenta cualquiera de los siguientes efectos adversos:
- Fiebre que se prolongue más de 3 días o cualquier síntoma que pueda sugerir una infección grave. Esto incluye temblores, escalofríos, malestar general, pérdida de apetito, dolores en el cuerpo, por lo general relacionado con la aparición repentina de la enfermedad, dolor de garganta o úlceras en la boca, tos, flema, dolor en el pecho, dificultad para respirar, dolor de oído, dolor de cabeza prolongado y enrojecimiento, calor e hinchazón localizadas en la piel o inflamación del tejido conectivo (celulitis). Estos síntomas pueden deberse a una infección grave, una infección inusual (infección oportunista) o estar relacionada con niveles bajos de glóbulos blancos (denominado leucopenia y neutropenia). Si lo considera necesario su médico puede hacerle análisis de sangre de forma regular.
- Reacciones alérgicas con sarpullido y picor y posiblemente también urticaria, dificultad para respirar o tragar, mareo, conciencia inusual del latido del corazón (palpitaciones) y tensión arterial baja.
Otros efectos adversos de Ilaris incluyen:
Muy frecuentes(pueden afectar a más de 1 de cada 10 personas):
- Infecciones de cualquier clase. Estas pueden incluir:
- Infecciones respiratorias tales como infección en el pecho, gripe, inflamación de garganta, secreción nasal, nariz taponada, estornudos, sensación de presión o dolor en las mejillas o en la frente con o sin fiebre (neumonía, bronquitis, síntomas gripales, sinusitis, rinitis, faringitis, tonsilitis (dolor de garganta), nasofaringitis, infección de las vías respiratorias superiores).
- Otras infecciones como infección de oido, infección de piel (celulitis), dolor de estómago y gastroenteritis y dolor y necesidad de orinar frecuentemente con o sin fiebre (infección del tracto urinario).
- Dolor abdominal superior.
- Dolor en articulaciones (artralgia).
- Descenso en los niveles de glóbulos blancos (leucopenia).
- Resultados anormales de la función renal (disminución del aclaramiento renal, proteinuria).
- Reacciones en el lugar de inyección (tales como enrojecimiento, hinchazón, calor y picor).
Frecuentes(pueden afectar hasta 1 de cada 10 personas):
- Candida – infección vaginal por hongos (candidiasis vulvovaginal).
- Sentirse mareado, sensación que todo le da vueltas (mareo o vértigo).
- Dolor en la espalda o músculos.
- Sensación de debilidad o muy cansado (fatiga, astenia).
- Descenso en los niveles de glóbulos blancos los cuales ayudan a prevenir la infección (neutropenia).
- Niveles anómalos de triglicéridos en su sangre (trastorno del metabolismo lipídico).
- Resultados anómalos de la prueba de la función hepática (transaminasas aumentadas) o nivel elevado de bilirrubina en la sangre, con o sin amarilleamiento de la piel y ojos (hiperbilirrubinemia).
Poco frecuentes(pueden afectar hasta 1 de cada 100 personas):
- Ardor (enfermedad de reflujo gastroesofágico).
- Descenso en los niveles de las células sanguíneas que ayudan a prevenir las hemorragias (plaquetas).
Informe inmediatamente a su médico o al médico de su hijo si nota alguno de estos síntomas.
Comunicación de efectos adversos
Si experimenta cualquier tipo de efecto adverso, consulte a su médico, farmacéutico o enfermero, incluso si se trata de posibles efectos adversos que no aparecen en este prospecto. También puede comunicarlos directamente a través del sistema nacional de notificación incluido en el Apéndice V. Mediante la comunicación de efectos adversos usted puede contribuir a proporcionar más información sobre la seguridad de este medicamento.
5. Conservación de Ilaris
- Mantener este medicamento fuera de la vista y del alcance de los niños.
- No utilice este medicamento después de la fecha de caducidad que aparece en la etiqueta y la caja después de CAD. La fecha de caducidad es el último día del mes que se indica.
- Conservar en nevera (entre entre 2 °C y 8 °C). No congelar.
- Mantener el vial en el estuche para protegerlo de la luz.
- La solución debe utilizarse inmediatamente después de la primera perforación del tapón del vial para preparar la inyección.
- No utilice este medicamento si nota que la solución no es de transparente a opalescente o contiene partículas.
- Todo medicamento no utilizado se debe desechar después de inyectar la dosis.
Los medicamentos no se deben tirar por los desagües ni a la basura. Pregunte a su farmacéutico cómo deshacerse de los envases y de los medicamentos que ya no necesita. De esta forma, ayudará a proteger el medio ambiente.
6. Contenido del envase e información adicional
Composición de Ilaris
- El principio activo es canakinumab. Cada vial contiene 150 mg de canakinumab en 1 ml de solución.
- Los demás componentes son manitol, histidina, histidina hidrocloruro monohidrato, polisorbato 80 (ver sección 2), agua para preparaciones inyectables.
Aspecto del producto y contenido del envase
- Ilaris se presenta en forma de solución inyectable dentro de un vial de vidrio de 2 ml.
- La solución es un líquido de transparente a opalescente y de incolora a ligeramente amarillo pardusco. No la utilice si el líquido contiene partículas fácilmente visibles, está turbio o se aprecia un color marrón.
- Ilaris está disponible en envases que contienen un vial.
Titular de la autorización de comercialización
Novartis Europharm Limited
Vista Building
Elm Park, Merrion Road
Dublín 4
Irlanda
Responsable de la fabricación
Novartis Farmacéutica, S.A.
Gran Vía de les Corts Catalanes, 764
08013 Barcelona
España
Novartis Pharma GmbH
Roonstrasse 25
90429 Nuremberg
Alemania
Lek Pharmaceuticals d.d.
Verovskova Ulica 57
1526 Ljubljana
Eslovenia
Novartis Pharma GmbH
Sophie-Germain-Strasse 10
90443 Nürnberg
Alemania
Pueden solicitar más información respecto a este medicamento dirigiéndose al representante local del titular de la autorización de comercialización:
België/Belgique/Belgien Novartis Pharma N.V. Tél/Tel: +32 2 246 16 11 | Lietuva SIA Novartis Baltics Lietuvos filialas Tel: +370 5 269 16 50 |
???????? Novartis Bulgaria EOOD ???.: +359 2 489 98 28 | Luxembourg/Luxemburg Novartis Pharma N.V. Tél/Tel: +32 2 246 16 11 |
Ceská republika Novartis s.r.o. Tel: +420 225 775 111 | Magyarország Novartis Hungária Kft. Tel.: +36 1 457 65 00 |
Danmark Novartis Healthcare A/S Tlf: +45 39 16 84 00 | Malta Novartis Pharma Services Inc. Tel: +356 2122 2872 |
Deutschland Novartis Pharma GmbH Tel: +49 911 273 0 | Nederland Novartis Pharma B.V. Tel: +31 88 04 52 111 |
Eesti SIA Novartis Baltics Eesti filiaal Tel: +372 66 30 810 | Norge Novartis Norge AS Tlf: +47 23 05 20 00 |
Ελλ?δα Novartis (Hellas) A.E.B.E. Τηλ: +30 210 281 17 12 | Österreich Novartis Pharma GmbH Tel: +43 1 86 6570 |
España Novartis Farmacéutica, S.A. Tel: +34 93 306 42 00 | Polska Novartis Poland Sp. z o.o. Tel.: +48 22 375 4888 |
France Novartis Pharma S.A.S. Tél: +33 1 55 47 66 00 | Portugal Novartis Farma - Produtos Farmacêuticos, S.A. Tel: +351 21 000 8600 |
Hrvatska Novartis Hrvatska d.o.o. Tel. +385 1 6274 220 | România Novartis Pharma Services Romania SRL Tel: +40 21 31299 01 |
Ireland Novartis Ireland Limited Tel: +353 1 260 12 55 | Slovenija Novartis Pharma Services Inc. Tel: +386 1 300 75 50 |
Ísland Vistor hf. Sími: +354 535 7000 | Slovenská republika Novartis Slovakia s.r.o. Tel: +421 2 5542 5439 |
Italia Novartis Farma S.p.A. Tel: +39 02 96 54 1 | Suomi/Finland Novartis Finland Oy Puh/Tel: +358 (0)10 6133 200 |
Κ?προς Novartis Pharma Services Inc. Τηλ: +357 22 690 690 | Sverige Novartis Sverige AB Tel: +46 8 732 32 00 |
Latvija SIA Novartis Baltics Tel: +371 67 887 070 |
Fecha de la última revisión de este prospecto:
Otras fuentes de información
La información detallada de este medicamento está disponible en la página web de la Agencia Europea de Medicamentos: https://www.ema.europa.eu
Instrucciones de uso de Ilaris solución inyectable
Lea estas instrucciones por completo antes de inyectar.
- Es importante que no intente inyectársela usted mismo hasta que no haya sido instruido por su profesional sanitario.
- Consulte asimismo la sección 3, «Autoinyección de Ilaris o inyección de Ilaris en un paciente».
Preparativos esenciales:
- Encuentre un sitio limpio en el que preparar y administrarse usted mismo la inyección.
- Lávese las manos con agua y jabón, posteriormente séquelas con una toalla limpia.
- Después de retirar el vial de la nevera, compruebe la fecha de caducidad del vial. No los utilice después de la fecha de caducidad que aparece en la etiqueta y el envase. La fecha de caducidad es el último día del mes que se indica.
- Deje el vial sin abrir durante 10 minutos para llevar el contenido a temperatura ambiente. No intente calentar el vial. Deje que se atempere por si mismo.
- Utilice siempre jeringas y agujas nuevas que estén en envases cerrados. No toque las agujas o el tapón del vial.
Reúna todos los elementos que precisa:
Incluidos en el envase
- un vial de Ilaris solución inyectable (mantener en la nevera).
No incluidos en el envase
- una jeringa de 1,0 ml
- una aguja (como la de 18 G o 21 G x 2 pulgadas o similar, según disponibilidad en el mercado) para extraer la solución del vial (“aguja de extracción”).
- una aguja de 27 G x 0,5 pulgadas (o similar, según disponibilidad en el mercado) para la inyección («aguja de inyección»)
- toallitas con alcohol
- algodón seco y limpio
- una tirita adhesiva
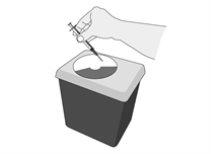
- un contenedor apropiado para depositar las agujas, jeringa y el vial utilizados (contenedor de material de desecho)
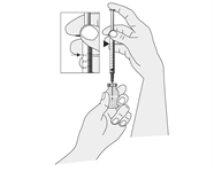
Preparación de la inyección
|
Abrir los envoltorios que contienen la jeringa y la aguja de extracción.
|
|
NOTA: La cantidad necesaria depende de la dosis que deba administrarse. Su profesional sanitario le mostrará la cantidad que ha de inyectarse.
|
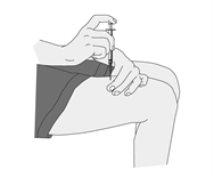
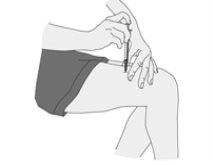
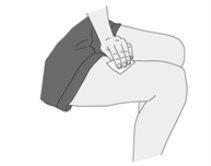
Administración de la inyección
|
|
|
|
Después de la inyección
|
|
|
Mantener el contenedor de material de desecho fuera de la vista y del alcance de los niños. Eliminarlo de acuerdo con las instrucciones recibidas del profesional sanitario o farmacéutico. |
- País de registro
- Principio activo
- Requiere recetaSí
- Fabricante
- Esta información es de carácter general y no sustituye la consulta con un profesional sanitario.
- Alternativas a ILARIS 150 MG/ML SOLUCION INYECTABLEForma farmacéutica: INYECTABLE, 150 mg/ml de canakinumabPrincipio activo: CanakinumabFabricante: Novartis Europharm LimitedRequiere recetaForma farmacéutica: INYECTABLE PERFUSION, 130 mgPrincipio activo: UstekinumabFabricante: Accord Healthcare S.L.U.Requiere recetaForma farmacéutica: INYECTABLE, 45 mgPrincipio activo: UstekinumabFabricante: Accord Healthcare S.L.U.Requiere receta
Médicos online para ILARIS 150 MG/ML SOLUCION INYECTABLE
Comenta la dosis, los posibles efectos secundarios, interacciones, contraindicaciones o la revisión de receta de ILARIS 150 MG/ML SOLUCION INYECTABLE, sujeto a valoración médica y a la normativa local.
Preguntas frecuentes