EVRA 203 MICROGRAMOS/24 HORAS + 33,9 MICROGRAMOS/24 HORAS PARCHE TRANSDERMICO

Cómo usar EVRA 203 MICROGRAMOS/24 HORAS + 33,9 MICROGRAMOS/24 HORAS PARCHE TRANSDERMICO
Traducción generada por IA
Este contenido ha sido traducido automáticamente y se ofrece solo con fines informativos. No sustituye la consulta con un profesional sanitario.
Ver originalContenido del prospecto
Introducción
Prospecto: información para el usuario
EVRA 203 microgramos/24 horas + 33,9 microgramos/24 horas parche transdérmiconorelgestromina/etinilestradiol
Cosas importantes que debe saber acerca de los anticonceptivos hormonales combinados (AHCs):
- Son uno de los métodos anticonceptivos reversibles más fiables si se utilizan correctamente.
- Aumentan ligeramente el riesgo de sufrir un coágulo de sangre en las venas y en las arterias especialmente en el primer año o cuando se reinicia el uso de un anticonceptivo hormonal combinado tras una pausa de 4 semanas o más.
- Esté alerta y consulte a su médico si cree que puede tener síntomas de un coágulo de sangre (ver sección 2 “Coágulos de sangre”).
Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene información importante para usted.
- Conserve este prospecto, ya que puede tener que volver a leerlo.
- Si tiene alguna duda, consulte a su médico, farmacéutico o enfermero.
- Este medicamento se le ha recetado solamente a usted y no debe dárselo a otras personas ya que puede perjudicarles.
- Si experimenta efectos adversos, consulte a su médico, farmacéutico o enfermero, incluso si se trata de efectos adversos que no aparecen en este prospecto. Ver sección 4.
Contenido del prospecto
- Qué es EVRA y para qué se utiliza
- Qué necesita saber antes de empezar a usar EVRA
- Cómo usar EVRA
- Posibles efectos adversos
- Conservación de EVRA
- Contenido del envase e información adicional
1. Qué es EVRA y para qué se utiliza
EVRA contiene dos tipos de hormonas sexuales, un progestágeno llamado norelgestromina y un estrógeno llamado etinilestradiol.
Como contiene dos hormonas, EVRA se considera un “anticonceptivo hormonal combinado”.
Se utiliza para prevenir el embarazo.
2. Qué necesita saber antes de empezar a usar EVRA
Consideraciones generales
Antes de empezar a usar EVRA debe leer la información acerca de los coágulos de sangre en la sección 2. Es particularmente importante que lea los síntomas de un coágulo de sangre (ver sección 2 “Coágulos de sangre”).
Cuando no debe usar EVRA
No debe usar EVRA si tiene alguna de las afecciones enumeradas a continuación. Si tiene alguna de las afecciones enumeradas a continuación, debe informar a su médico. Su médico comentará con usted qué otra forma de anticoncepción sería más adecuada.
- si tiene (o ha tenido alguna vez) un coágulo de sangre en un vaso sanguíneo de las piernas (trombosis venosa profunda, TVP), en los pulmones (embolia pulmonar, EP) o en otros órganos;
- si sabe que padece un trastorno que afecta a la coagulación de la sangre: por ejemplo, deficiencia de proteína C, deficiencia de proteína S, deficiencia de antitrombina III, factor V Leiden o anticuerpos antifosfolipídicos;
- si necesita una operación o si pasa mucho tiempo sin ponerse de pie (ver sección “Coágulos de sangre”);
- si ha sufrido alguna vez un ataque cardíaco o un ictus;
- si tiene (o ha tenido alguna vez) una angina de pecho (una afección que provoca fuerte dolor en el pecho y puede ser el primer signo de un ataque al corazón) o un accidente isquémico transitorio (AIT, síntomas temporales de ictus);
- si tiene alguna de las siguientes enfermedades que pueden aumentar su riesgo de formación de un coágulo en las arterias:
- diabetes grave con lesión de los vasos sanguíneos
- tensión arterial muy alta
- niveles muy altos de grasa en la sangre (colesterol o triglicéridos)
- una afección llamada hiperhomocisteinemia
- si tiene (o ha tenido alguna vez) un tipo de migraña llamada “migraña con aura”;
- si es alérgico a norelgestromina, etinilestradiol o a cualquiera de los demás componentes de este medicamento (incluidos en la sección 6);
- si alguna vez le han dicho que puede tener cáncer de mama o cáncer de útero, cérvix (cuello del útero) o de vagina;
- si ha tenido alguna vez un tumor en el hígado o una enfermedad del hígado por la cual su hígado no funciona correctamente;
- si tiene hemorragia vaginal sin causa aparente.
- si tiene hepatitis C y está en tratamiento con medicamentos que contienen ombitasvir/ paritaprevir/ ritonavir y dasabuvir (ver también sección “Otros medicamentos y EVRA”).
No debe utilizar este medicamento si padece alguna de las afecciones anteriormente mencionadas. Si no está segura, consulte con su médico, farmacéutico o enfermero antes de usar este medicamento.
Cuándo debe tener especial cuidado con EVRA
¿Cuándo debe consultar a su médico? Busque asistencia médica urgente
“Coágulo de sangre [trombosis]” a continuación). Para obtener una descripción de los síntomas de estos efectos adversos graves, consulte “Cómo reconocer un coágulo de sangre” |
Advertencias y precauciones
Antes de usar este medicamento es necesario que su médico le realice una revisión médica.
Informe a su médico si sufre cualquiera de las siguientes afecciones.
Si la afección se desarrolla o empeora mientras está usando EVRA, también debe informar a su médico.
- si padece enfermedad de Crohn o colitis ulcerosa (enfermedad inflamatoria intestinal crónica);
- si padece lupus eritematoso sistémico (LES, una enfermedad que afecta a su sistema natural de defensa);
- si padece síndrome urémico hemolítico (SUH, un trastorno de la coagulación de la sangre que provoca insuficiencia en los riñones);si padece anemia drepanocítica (una enfermedad hereditaria de los glóbulos rojos);
- si tiene niveles elevados de grasa en la sangre (hipertrigliceridemia) o antecedentes familiares positivos de esta afección. La hipertrigliceridemia se ha asociado a un mayor riesgo de padecer pancreatitis (inflamación del páncreas);
- si necesita una operación o pasa mucho tiempo sin ponerse de pie (ver sección 2 “Coágulos de sangre”);
- si acaba de dar a luz corre mayor riesgo de sufrir coágulos de sangre. Debe preguntar a su médico cuánto tiempo después del parto puede empezar a tomar EVRA;
- si tiene una inflamación de las venas que hay debajo de la piel (tromboflebitis superficial)
- si tiene varices;
COÁGULOS DE SANGRE
El uso de un anticonceptivo hormonal combinado como EVRA aumenta su riesgo de sufrir un coágulo
de sangre en comparación con no usarlo. En raras ocasiones un coágulo de sangre puede bloquear
vasos sanguíneos y provocar problemas graves.
Se pueden formar coágulos de sangre:
- en las venas (lo que se llama “trombosis venosa”, “tromboembolismo venoso” o TEV)
- en las arterias (lo que se llama “trombosis arterial”, “tromboembolismo arterial” o TEA)
La recuperación de los coágulos de sangre no es siempre completa. En raras ocasiones puede haber efectos graves duraderos o, muy raramente, pueden ser mortales.
Es importante recordar que el riesgo global de un coágulo de sangre perjudicialdebido a EVRA es pequeño.
CÓMO RECONOCER UN COÁGULO DE SANGRE
Busque asistencia médica urgente si nota alguno de los siguientes signos o síntomas.
¿Experimenta alguno de estos signos? | ¿Qué es posible que esté | |||
sufriendo? | ||||
? | hinchazón de una pierna o pie o a lo largo de una vena de la | Trombosis venosa profunda | ||
pierna o pie, especialmente cuando va acompañada de: | ||||
- | dolor o sensibilidad en la pierna, que tal vez se | |||
advierta sólo al ponerse de pie o al caminar; | ||||
- | aumento de la temperatura en la pierna afectada; | |||
- | cambio de color de la piel de la pierna, p. ej. si se | |||
pone pálida, roja o azul. | ||||
? | falta de aliento repentina sin causa conocida o respiración | Embolia pulmonar | ||
? | rápida; | |||
tos repentina sin una causa clara, que puede arrastrar sangre; | ||||
? | dolor en el pecho agudo que puede aumentar al respirar | |||
? | hondo; | |||
aturdimiento intenso o mareo; | ||||
? | latidos del corazón acelerados o irregulares; | |||
? | dolor de estómago intenso. | |||
Si no está segura, consulte a un médico, ya que algunos de estos | ||||
síntomas como la tos o la falta de aliento se pueden confundir con | ||||
una afección más leve como una infección respiratoria (p. ej. un | ||||
“catarro común”) | ||||
Síntomas que se producen con más frecuencia en un ojo: | Trombosis de las venas | |||
? | pérdida inmediata de la visión, o bien, | retinianas (coágulo de sangre | ||
? | visión borrosa indolora, que puede evolucionar hasta | en el ojo) | ||
pérdida de la visión. |
? | dolor, molestias, presión, pesadez en el pecho; | Ataque al corazón |
? | sensación de opresión o plenitud en el pecho, brazo o debajo | |
? | del esternón; | |
sensación de plenitud, indigestión o ahogo; | ||
? | malestar de la parte superior del cuerpo que irradia a la | |
? | espalda, la mandíbula, la garganta, el brazo y el estómago; | |
sudoración, náuseas, vómitos o mareo; | ||
? | debilidad extrema, ansiedad o falta de aliento; | |
? | latidos del corazón acelerados o irregulares. | |
? | debilidad o entumecimiento repentino de la cara, brazo o | Ictus |
? | pierna, especialmente en un lado del cuerpo; | |
confusión repentina, dificultad para hablar o para | ||
? | comprender; | |
dificultad repentina de visión en un ojo o en ambos; | ||
? | dificultad repentina para caminar, mareo, pérdida del | |
? | equilibrio o de la coordinación; | |
dolor de cabeza repentino, intenso y prolongado sin causa | ||
? | conocida; | |
pérdida del conocimiento o desmayo, con o sin | ||
convulsiones. | ||
A veces los síntomas de ictus pueden ser breves, con una | ||
recuperación casi inmediata y completa, pero de todos modos debe | ||
buscar asistencia médica urgente ya que puede correr riesgo de | ||
sufrir otro ictus. | ||
? | hinchazón y ligera coloración azul de una extremidad; | Coágulos de sangre que |
? | dolor de estómago intenso (abdomen agudo). | bloquean otros vasos |
sanguíneos | ||
COÁGULOS DE SANGRE EN UNA VENA |
¿Qué puede ocurrir si se forma un coágulo de sangre en una vena?
- El uso de anticonceptivos hormonales combinados se ha relacionado con un aumento del riesgo de coágulos de sangre en las venas (trombosis venosa). No obstante, estos efectos adversos son raros. Se producen con más frecuencia en el primer año de uso de un anticonceptivo hormonal combinado.
- Si se forma un coágulo de sangre en una vena de la pierna o del pie, puede provocar trombosis venosa profunda (TVP).
- Si un coágulo de sangre se desplaza desde la pierna y se aloja en el pulmón puede provocar una embolia pulmonar.
- En muy raras ocasiones se puede formar un coágulo en una vena de otro órgano como el ojo (trombosis de las venas retinianas).
¿Cuándo es mayor el riesgo de presentar un coágulo de sangre en una vena?
El riesgo de presentar un coágulo de sangre en una vena es mayor durante el primer año de tomar un anticonceptivo hormonal combinado por primera vez. El riesgo puede ser mayor también si vuelve a empezar a tomar un anticonceptivo hormonal combinado (el mismo medicamento o un medicamento diferente) después de una interrupción de 4 semanas o más.
Después del primer año, el riesgo disminuye, pero siempre es algo mayor que si no estuviera tomando un anticonceptivo hormonal combinado.
Cuando deja de tomar EVRA, su riesgo de presentar un coágulo de sangre regresa a la normalidad en pocas semanas.
¿Cuál es el riesgo de presentar un coágulo de sangre?
El riesgo depende de su riesgo natural de TEV y del tipo de anticonceptivo hormonal combinado que esté tomando.
El riesgo global de presentar un coágulo de sangre en la pierna o en el pulmón (TVP o EP) con EVRA es pequeño.
- De cada 10.000 mujeres que no usan ningún anticonceptivo hormonal combinado y no están embarazadas, unas 2 pueden presentar un coágulo de sangre en un año.
- De cada 10.000 mujeres que usan un anticonceptivo hormonal combinado que contiene levonorgestrel, noretisterona o norgestimato, unas 5-7 presentarán un coágulo de sangre en un año.
- De cada 10.000 mujeres que usan un anticonceptivo hormonal combinado que contiene etonogestrel o norelgestromina como EVRA, entre unas 6 y 12 mujeres presentarán un coágulo de sangre en un año.
- El riesgo de tener un coágulo de sangre variará en función de sus antecedentes médicos personales (ver “Factores que aumentan su riesgo de un coágulo de sangre” a continuación).
Riesgo de presentar un coágulo de | |
sangre en un año | |
Mujeres que no utilizanun parche/comprimido/anillo | Unas 2 de cada 10.000 mujeres |
vaginal hormonal combinado y que no están embarazadas | |
Mujeres que utilizan una píldora anticonceptiva hormonal | Unas 5-7 de cada 10.000 mujeres |
combinada que contiene levonorgestrel, noretisterona o | |
norgestimato | |
Mujeres que utilizan EVRA | Unas 6-12 de cada 10.000 mujeres |
Factores que aumentan su riesgo de un coágulo de sangre en una vena
El riesgo de tener coágulo de sangre con EVRA es pequeño, pero algunas afecciones aumentan el riesgo. Su riesgo es mayor:
- si tiene exceso de peso (índice de masa corporal o IMC superior a 30 kg/m2);
- si alguno de sus parientes próximos ha tenido un coágulo de sangre en la pierna, pulmón u otro órgano a una edad temprana (es decir, antes de los 50 años aproximadamente). En este caso podría tener un trastorno hereditario de la coagulación de la sangre;
- si necesita operarse o si pasa mucho tiempo sin ponerse de pie debido a una lesión o enfermedad, o si tiene la pierna escayolada. Tal vez haya que interrumpir el uso de EVRA varias semanas antes de la intervención quirúrgica o mientras tenga menos movilidad. Si necesita interrumpir el uso de EVRA debe preguntar a su médico cuándo puede empezar a usarlo de nuevo;
- al aumentar la edad (en especial por encima de unos 35 años);
- si ha dado a luz hace menos de unas semanas.
El riesgo de presentar un coágulo de sangre aumenta cuantas más afecciones tenga.
Los viajes en avión (>4 horas) pueden aumentar temporalmente el riesgo de un coágulo de sangre, en especial si tiene alguno de los demás factores de riesgo enumerados.
Es importante informar a su médico si sufre cualquiera de las afecciones anteriores, aunque no esté segura. Su médico puede decidir que hay que interrumpir el uso de EVRA.
Si alguna de las afecciones anteriores cambia mientras está utilizando EVRA, por ejemplo un pariente próximo experimenta una trombosis sin causa conocida, o usted aumenta mucho de peso, informe a su médico.
COÁGULOS DE SANGRE EN UNA ARTERIA
¿Qué puede ocurrir si se forma un coágulo de sangre en una arteria?
Al igual que un coágulo de sangre en una vena, un coágulo en una arteria puede provocar problemas graves. Por ejemplo, puede provocar un ataque al corazón o un ictus.
Factores que aumentan su riesgo de un coágulo de sangre en una arteria
Es importante señalar que el riesgo de un ataque al corazón o un ictus por utilizar EVRA es muy pequeño, pero puede aumentar:
- con la edad (por encima de unos 35 años);
- si fuma. Cuando utiliza un anticonceptivo hormonal combinado como EVRA se le aconseja que deje de fumar. Si no es capaz de dejar de fumar y tiene más de 35 años, su médico puede aconsejarle que utilice un tipo de anticonceptivo diferente;
- si tiene sobrepeso;
- si tiene la tensión arterial alta;
- si algún pariente próximo ha sufrido un ataque al corazón o un ictus a una edad temprana (menos de unos 50 años). En este caso usted también podría tener mayor riesgo de sufrir un ataque cardíaco o una apoplejía;
- si usted o alguno de sus parientes próximos tiene un nivel elevado de grasa en la sangre (colesterol o triglicéridos);
- si padece migrañas, especialmente migrañas con aura;
- si tiene un problema de corazón (trastorno de las válvulas, una alteración del ritmo del corazón llamada fibrilación auricular);
- si tiene diabetes.
Si tiene una o más de estas afecciones o si alguna de ellas es especialmente grave, el riesgo de presentar un coágulo de sangre se puede ver incrementado aún más.
Si alguna de las afecciones anteriores cambia mientras está utilizando EVRA, por ejemplo empieza a fumar, un pariente próximo experimenta una trombosis sin causa conocida, o usted aumenta mucho de peso, informe a su médico.
Trastornos psiquiátricos:
Alguna mujeres que utilizan anticonceptivos hormonales como EVRA han notificado depresión o un estado de ánimo deprimido. La depresión puede ser grave y a veces puede inducir pensamiento suicidas. Si experimenta alteraciones del estado de ánimo y síntomas depresivos, póngase en contacto con su médico para obtener asesoramiento médico adicional lo antes posible.
Además consulte a su médico, farmacéutico o enfermero antes de empezar a usar EVRA si tiene o ha tenido cualquiera de las siguientes afecciones, o si aparecen o empeoran durante el tratamiento con EVRA:
- Cree que puede estar embarazada;
- Tiene dolores de cabeza que empeoran o aparecen con más frecuencia;
- Pesa 90 kg o más; (equivalente a 14 st y 2 lb o más)
- Tiene la tensión arterial alta o que tiende a aumentar;
- Tiene alguna enfermedad de la vesicular biliar incluyendo cáculos biliares o inflamación de la vesícula biliar;
- Tiene una alteración en la sangre llamada porfiria;
- Tiene un trastorno nervioso en el que se producen movimientos repentinos del cuerpo llamado “corea de Sydenham”;
- Tuvo erupciones en la piel con ampollas durante el embarazo (“herpes gestacional”);
- Tiene pérdida de audición;
- Tiene diabetes;
- Tiene depresión;
- Tiene epilepsia o cualquier otro problema que cause convulsiones;
- Tiene alteraciones del hígado, incluyendo color amarillento de la piel y del blanco del ojo (ictericia);
- Tiene o ha tenido “manchas del embarazo”. Éstas son puntos o manchas marrones amarillentas de la piel, especialmente en la cara (llamadas “cloasma”). Puede que estas manchas no
desaparezcan completamente, incluso después de dejar de utilizar EVRA. Proteja su piel del sol o de las radiaciones ultravioletas. Esto puede ayudar a prevenir que aparezcan estas manchas o a que no empeoren.
- Tiene problemas de riñón.
Si no está segura si padece alguna de las afecciones anteriores, consulte con su médico o farmacéutico antes de usar EVRA.
Enfermedades de transmisión sexual
Este medicamento no le protege frente a la infección por VIH (SIDA) o frente a cualquier otra enfermedad de transmisión sexual. Esto incluye clamidia, herpes genital, verrugas genitales, gonorrea, hepatitis B, sífilis. Utilice siempre preservativos para protegerse frente a estas enfermedades.
Pruebas analíticas
- Si necesita que le hagan un análisis de sangre o de orina, informe a su médico o al personal del laboratorio que está utilizando EVRA, ya que los anticonceptivos hormonales pueden alterar algunos resultados analíticos.
Niños y adolescentes
No se ha estudiado EVRA en niñas y adolescentes menores de 18 años. No se debe utilizar EVRA en niñas y adolescentes que no hayan tenido todavía su primer periodo menstrual.
Otros medicamentos y EVRA
Informe a su médico o farmacéutico si está utilizando, ha utilizado recientemente o podría tener que utilizar cualquier otro medicamento.
No utilice EVRA si tiene hepatitis C y está tomando medicamentos que contienen ombitasvir/ paritaprevir/ ritonavir y dasabuvir, ya que puede causar en análisis de sangre un aumento en los resultados función hepática (aumento de la enzima ALT hepática). Su médico le recetará otro tipo de método anticonceptivo antes de iniciar el tratamiento con estos medicamentos. EVRA se puede reiniciar, aproximadamente, 2 semanas después de finalizar este tratamiento. Ver sección “ Cuando no debe usar EVRA”.
Ciertos medicamentos y plantas medicinales pueden impedir el funcionamiento adecuado de EVRA.
Si esto sucediera, usted se puede quedar embarazada, o puede experimentar sangrado inesperado.
Estos incluyen medicamentos empleados para el tratamiento de:
- algunos antirretrovirales usados para tratar infecciones por VIH/SIDA y virus de la Hepatitis C (denominados inhibidores de la proteasa e inhibidores no nucleosídicos de la transcriptasa inversa como ritonavir, nevirapina, efavirenz)
- medicamentos para las infecciones (como rifampicina y griseofulvina)
- medicamentos anticonvulsivantes (como barbitúricos, topiramato, fenitoína, carbamazepina, primidona, oxcarbazepina y felbamato)
- bosentán (un medicamento usado para tratar la tensión arterial alta en los vasos sanguíneos de los pulmones)
- hierba de San Juan o hipérico, (una planta medicinal usada para la depresión).
Si está utilizando algunos de los medicamentos mencionados anteriormente, debe usar otro método anticonceptivo (como preservativo, diafragma o espuma). El efecto de alguno de estos medicamentos puede durar hasta 28 días después de haber interrumpido su uso. Consulte con su médico o farmacéutico sobre la utilización de otro método anticonceptivo si está utilizando EVRA junto con cualquiera de los medicamentos arriba mencionados.
EVRA puede reducir el efecto de algunos medicamentos, como:
- medicamentos que contienen ciclosporina
- lamotrigina utilizado para la epilepsia [Esto puede aumentar el riesgo de las crisis (convulsiones)].
Puede que su médico necesite ajustar la dosis del otro medicamento. Consulte a su médico o farmacéutico antes de tomar cualquier medicamento.
Embarazo y lactancia
- No utilice este medicamento si está embarazada o si cree que pudiera estarlo.
- Deje de utilizar este medicamento inmediatamente si se queda embarazada.
- No utilice este medicamento si está dando el pecho o planea dar el pecho.
Si cree que puede estar embarazada o tiene intención de quedarse embarazada, consulte a su médico o farmacéutico antes de utilizar este medicamento.
Conducción y uso de máquinas
Puede conducir o utilizar máquinas mientras usa este medicamento.
Riesgos del uso de anticonceptivos hormonales combinados
La siguiente información se basa en información sobre los comprimidos anticonceptivos combinados. Puesto que el parche transdérmico EVRA contiene hormonas similares a las que se usan en los comprimidos anticonceptivos combinados, es probable que tenga los mismos riesgos. El uso de cualquier comprimido anticonceptivo combinado implica riesgos, los cuales podrían dar lugar a discapacidad o muerte.
No se ha demostrado que un parche transdérmico como EVRA sea más seguro que un comprimido anticonceptivo combinado administrado por vía oral.
Anticonceptivos hormonales combinados y el cáncer
Cáncer de cérvix (cuello del útero)
El cáncer de cérvix (cuello del útero) también se detecta con más frecuencia en mujeres que usan anticonceptivos hormonales combinados. Sin embargo, se puede deber a otras causas incluyendo las enfermedades de transmisión sexual.
Cáncer de mama
Se han detectado casos de cáncer de mama más frecuentemente en mujeres que utilizan anticonceptivos hormonales combinados. Sin embargo, es posible que los anticonceptivos hormonales combinados no sean la causa de que más mujeres tengan cáncer de mama. Esto se puede deber a que las mujeres que utilizan anticonceptivos hormonales combinados son examinadas más frecuentemente. Esto significaría que hay más posibilidades de que el cáncer de mama sea detectado. El aumento del riesgo de tener cáncer de mama disminuye gradualmente después de interrumpir el tratamiento con los anticonceptivos hormonales combinados. Después de diez años, el riesgo se iguala al de las mujeres que nunca han usado anticonceptivos hormonales combinados.
Cáncer de hígado
Se han hallado casos raros de tumores no cancerígenos en el hígado en mujeres que toman anticonceptivos hormonales combinados. Aún más raramente se han encontrado tumores cancerígenos en el hígado. Esto puede producir sangrados dentro del cuerpo con un dolor muy fuerte en la zona del estómago. Si sufre este síntoma, debe contactar inmediatamente con su médico.
3. Cómo usar EVRA
Siga exactamente las instrucciones de administración de este medicamento indicadas por su médico o farmacéutico.
En caso contrario podría aumentar el riesgo de quedarse embarazada.
- Consulte a su médico o farmacéutico si tiene dudas.
- Debe disponer de métodos anticonceptivos no hormonales (como preservativo, diafragma o espuma) de reserva en caso de que cometiera algún error al usar el parche.
Cuántos parches hay que usar
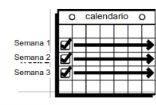
- Semanas 1, 2 y 3: Colocar un parche y dejarlo durante 7 días exactamente.
- Semana 4:No se coloque un parche esta semana.
Si no ha utilizado un método anticonceptivo hormonal durante el ciclo anterior
- Puede empezar a utilizar este medicamento el primer día de su próximo periodo.
- Si han pasado uno o más días desde el comienzo de su periodo, consulte a su médico sobre la utilización temporal de un método anticonceptivo no hormonal.
Si cambia del comprimido anticonceptivo oral a EVRA
Si pasa del comprimido anticonceptivo oral a este medicamento:
- Espere hasta que tenga la menstruación.
- Colóquese el primer parche durante las primeras 24 horas del periodo.
Si se coloca el parche después del Día 1 del periodo, debe:
- Utilizar simultáneamente un método anticonceptivo no hormonal hasta el Día 8 , momento de cambio de parche.
Si no tiene la menstruación en los 5 días posteriores a la toma del último comprimido anticonceptivo, consulte a su médico antes de empezar a usar este medicamento.
Si cambia del comprimido anticonceptivo basado sólo en progestágenos, de un implante o de un inyectable a EVRA
- Puede empezar el tratamiento con este medicamento cualquier día después de dejar de tomar el comprimido anticonceptivo basado sólo en progestágenos, o en el día de extracción del implante o en el día que le toque la siguiente inyección.
- Colóquese el parche al día siguiente de dejar de tomar el comprimido anticonceptivo basado sólo en progestágenos, el día de extracción del implante o cuando le toque la siguiente inyección.
- Debe utilizar simultáneamente un método anticonceptivo no hormonal hasta el Día 8, momento de cambio de parche.
Después de un aborto espontáneo o provocadoantesde 20 semanas de gestación
- Consulte a su médico.
- Puede empezar a utilizar este medicamento de forma inmediata.
Si cuando comienza a utilizar este medicamento, han pasado uno o más días desde el aborto espontáneo o provocado, consulte a su médico sobre la utilización temporal de un método anticonceptivo no hormonal.
Después de un aborto espontáneo o provocadodespuésde 20 semanas de gestación
- Consulte a su médico.
Puede comenzar con este medicamento a los 21 días después del aborto provocado o espontáneo o el primer día del siguiente periodo, lo que primero suceda.
Después del parto
- Consulte a su médico.
- Si ha dado a luz y no está dando el pecho, no debe empezar a utilizar este medicamento antes de 4 semanas después del parto.
- Si comienza a utilizarlo más tarde de 4 semanas después del parto, utilice simultáneamente un método anticonceptivo no hormonal durante los primeros 7 días.
Si ha mantenido relaciones sexuales desde el parto, espere a tener su primera menstruación o consulte a su médico para asegurarse de que no está embarazada antes de empezar a utilizar este medicamento.
Si está dando el pecho
- Consulte a su médico.
- No utilice este medicamento si está dando el pecho o planeando dar el pecho (ver también sección 2, Embarazo y lactancia).
Información importante que debe seguir mientras utilice el parche
- Cámbiese el parche EVRA el mismo día de cada semana, ya que está diseñado para que actúe durante 7 días.
- Nunca deje de llevar el parche más de 7 días seguidos.
- Los parches deben llevarse sólo de uno en uno.
- No corte ni manipule el parche de ninguna forma.
- Evite poner el parche sobre una zona de la piel que esté roja, irritada o cortada.
- El parche se debe pegar bien sobre la piel para que funcione correctamente.
- Hay que presionar bien sobre el parche hasta que los bordes estén bien pegados.
- No se deben aplicar cremas, aceites, lociones, polvos o maquillaje en la zona de la piel donde vaya a pegar el parche o cerca de la zona donde lleve el parche. Esto podría hacer que el parche se despegara.
- No ponga un parche nuevo en la misma zona de la que se acaba de quitar el parche anterior. Si lo hace, es más probable que le produzca irritación.
- Compruebe cada día que no se haya caído el parche.
- No deje de utilizar los parches incluso si no mantiene relaciones sexuales con frecuencia.
Cómo usar el parche:
Si es la primera vez que utiliza EVRA, espere hasta el día en que tenga el periodo menstrual.
- Colóquese el primer parche durante las primeras 24 horas del periodo
- Si se coloca el parche después del primer día del periodo, debe utilizar un método anticonceptivo no hormonal hasta el Día 8, cuando cambie de parche
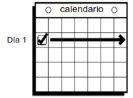
- El día que se ponga el primer parche será el Día 1. El “Día de Cambio del Parche” será este día de cada semana.
Elija un lugar en el cuerpo para ponerse el parche.
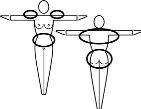
- Póngase siempre el parche sobre piel limpia, seca y sin vello
- Colóqueselo en el glúteo, abdomen, exterior del brazo o parte superior de la espalda, en un lugar donde no roce con las prendas ajustadas
- Nunca se ponga el parche en las mamas.
| Usando los dedos, abra el sobre de aluminio.
Evite el contacto con la superficie adhesiva. |
| Póngase el parche en la piel.
|
| Lleve el parche puesto durante 7 días (una semana).
|
|
Póngase un nuevo parche. Esto hace un total de tres semanas usando parches. A fin de evitar irritaciones, no se ponga el parche nuevo exactamente en el mismo sitio que el anterior. |
| No se ponga ningún parche en la Semana 4 (Día 22 a Día 28).
|
| En su próximo ciclo de cuatro semanas.
|
Si quiere modificar el “Día de Cambio del Parche” a un día diferente de la semana, consulte a su médico. Debe completar el ciclo actual, y quitarse el tercer parche el día correcto. Durante la semana 4, puede elegir un Día de Cambio nuevo y colocarse el primer parche en ese día elegido. En ningún caso deben transcurrir más de 7 días consecutivos sin parche.
Si quiere retrasar su periodo, colóquese un parche al inicio de la semana 4 (Día 22) sin respetar, por lo tanto, la semana de descanso. Puede experimentar una hemorragia ligera o un sangrado intermenstrual. No utilice más de 6 parches consecutivos (por lo tanto no más de 6 semanas). Cuando haya utilizado 6 parches consecutivos (durante 6 semanas consecutivas), no se ponga otro parche en la semana 7. Después de 7 días sin llevar parche, colóquese un nuevo parche y comience el ciclo utilizando éste como Día 1. Consulte con su médico antes de decidir retrasar su periodo.
Actividades diarias mientras utiliza los parches
- Las actividades normales como baños, duchas, sauna y ejercicio no deberían afectar al rendimiento del parche.
- El parche está diseñado para que permanezca en su sitio durante este tipo de actividades.
- Sin embargo, se recomienda que compruebe que el parche no se haya desprendido después de realizar estas actividades.
Si necesita ponerse el parche en una zona nueva del cuerpo en un día diferente a su “Día de Cambio del Parche”
Si le resulta incómodo el parche que lleva o le produce irritación:
- Puede despegárselo y ponerse otro nuevo en una zona diferente del cuerpo hasta el próximo “Día de Cambio del Parche”
- Sólo debe llevar un único parche.
Si le resulta difícil recordar el cambio de parche
- Consulte a su médico, farmacéutico o enfermero sobre cómo hacer que el cambio de parche sea más fácil. También pueden aconsejarle el uso de otro método anticonceptivo.
Si el parche comienza a despegarse, se levantan los bordes o se cae
Menos de un día(hasta 24 horas):
- Intente volver a ponerse el parche o póngase de inmediato un nuevo parche.
- No es necesario tomar otras medidas anticonceptivas.
- El “Día de Cambio del Parche” debe seguir siendo el mismo.
- No intente volver a pegarse un parche si:
- el adhesivo no pega
- se ha pegado a sí mismo o a otra superficie
- tiene alguna partícula pegada
- se ha despegado o caído por segunda vez.
- No debe utilizar ningún tipo de adhesivo o venda para sujetar el parche en su sitio.
- Si no puede volver a pegarse un parche, se debe poner otro parche nuevo de inmediato.
Más de un día(24 horas o más) o si no sabe cuánto tiempo:
- Comience inmediatamente un nuevo ciclo de cuatro semanas colocándose un parche nuevo.
- A partir de ahora habrá un nuevo Día 1 y un nuevo “Día de Cambio del Parche”.
- Debe utilizar anticonceptivos no hormonales adicionales durante la primera semana del nuevo ciclo.
Se puede quedar embarazada si no sigue estas instrucciones.
Si olvida cambiar el parche transdérmico
Al comienzo de cualquier ciclo de parche (Semana 1 (Día 1)):
Si olvida ponerse el parche, podría correr un riesgo muy alto de quedarse embarazada.
- Debe utilizar anticonceptivos no hormonales adicionales durante una semana.
- Póngase el primer parche del nuevo ciclo en cuanto se dé cuenta.
- Ahora tiene un nuevo “Día de Cambio del Parche” y un nuevo Día 1.
En la mitad del ciclo (Semana 2 ó 3):
Si olvida cambiarse el parche durante uno o dos días (hasta 48 horas):
- Póngase un nuevo parche en cuanto se dé cuenta.
- El siguiente parche se pondrá el “Día de Cambio del Parche” habitual.
No es necesario tomar otras medidas anticonceptivas.
Durante más de 2 días(48 horas o más):
- Si olvida cambiarse el parche durante más de 2 días puede quedarse embarazada.
- Comience un nuevo ciclo de cuatro semanas en cuanto se acuerde, colocándose un nuevo parche.
- A partir de ahora habrá un nuevo “Día de Cambio del Parche” y un nuevo Día 1.
- Debe utilizar anticonceptivos adicionales durante la primera semana del nuevo ciclo.
Al final del ciclo con parche (Semana 4):
Si olvida quitarse el parche:
- Quíteselo en cuanto se acuerde.
- Comience el nuevo ciclo el “Día de Cambio del Parche” habitual, el día después del Día 28.
No es necesario el uso de anticonceptivos adicionales.
Si tiene ausencia o irregularidades en el sangrado con EVRA
Este medicamento puede causar sangrado vaginal inesperado o pérdidas (manchado) durante las semanas de uso del parche.
- Normalmente esto deja de ocurrir después de los primeros ciclos.
- Los errores en el uso de los parches también pueden causar manchado y hemorragia ligera.
- Continúe usando este medicamento y si persiste el sangrado en ciclos posteriores a los tres primeros, consulte a su médico o farmacéutico.
Aunque no tenga el periodo durante la semana sin el parche de EVRA (Semana 4), se debe poner un nuevo parche el “Día de Cambio de Parche” habitual.
- Si ha utilizado este medicamento correctamente y no le viene el periodo, no quiere decir necesariamente que esté embarazada.
- Sin embargo, si tiene dos faltas consecutivas, consulte a su médico o farmacéutico, ya que podría estar embarazada.
Si utiliza más EVRA del que debe (más de un parche de EVRA a la vez)
Quítese los parches y consulte a su médico inmediatamente.
El uso de demasiados parches puede ser causa de:
- Sentirse enferma (náuseas) y estar enferma (vómitos)
- Sangrado vaginal.
Si interrumpe el tratamiento con EVRA
Puede tener una menstruación irregular, ligera o ausencia. Esto normalmente ocurre en los 3 primeros meses, especialmente si sus periodos no eran regulares antes de empezar a utilizar este medicamento.
Si tiene cualquier otra duda sobre el uso de este medicamento, pregunte a su médico, farmacéutico o enfermero.
4. Posibles efectos adversos
Al igual que todos los medicamentos, este medicamento puede producir efectos adversos, aunque no todas las personas los sufran. Si sufre cualquier efecto adverso, especialmente si es grave y persistente, o tiene algún cambio de salud que cree que puede deberse a EVRA, consulte a su médico.
Todas las mujeres que toman anticonceptivos hormonales combinados corren mayor riesgo de presentar coágulos de sangre en las venas [tromboembolismo venoso (TEV)] o coágulos de sangre en las arterias (tromboembolismo arterial [TEA]). Para obtener información más detallada sobre los diferentes riesgos de tomar anticonceptivos hormonales combinados, ver sección 2 “Qué necesita saber antes de empezar a usar EVRA”.
Efectos adversos muy frecuentes (pueden afectar a más de 1 de cada 10 mujeres):
- Dolor de cabeza
- Náuseas
- Sensibilidad en las mamas.
Efectos adversos frecuentes (pueden afectar hasta 1 de cada 10 mujeres):
- Infección vaginal por hongos, algunas veces llamada candidiasis
- Alteraciones del estado de ánimo tales como depresión, cambios de humor u oscilaciones en el estado de ánimo, ansiedad, lloros
- Mareos
- Migraña
- Dolor o hinchazón abdominal
- Vómitos o diarrea
- Acné, erupción de la piel, picor de la piel o irritación de la piel
- Espasmos musculares
- Problemas en el pecho tales como dolor, aumento del tamaño o bultos en el pecho
- Cambios en el patrón del sangrado menstrual, calambres uterinos, periodos dolorosos, secreción vaginal
- Problemas donde el parche ha estado en contacto con la piel tales como enrojecimiento, irritación, picor o erupción
- Sensación de cansancio o de malestar
- Aumento de peso.
Efectos adversos poco frecuentes (pueden afectar hasta 1 de cada 100 mujeres):
- Reacción alérgica, ronchas
- Hinchazón debida a la retención de agua en el cuerpo
- Niveles altos de grasas en la sangre (como colesterol o triglicéridos)
- Problemas de sueño (insomnio)
- Disminución del deseo sexual
- Eccema, enrojecimiento de la piel
- Producción anormal de leche en la mama
- Síndrome premenstrual
- Sequedad vaginal
- Otros problemas donde el parche ha estado en contacto con la piel
- Hinchazón
- Presión sanguínea alta o aumento de la presión sanguínea.
- Aumento de apetito
- Pérdida de pelo
- Sensibilidad a la luz del sol.
Efectos adversos raros (pueden afectar hasta 1 de cada 1.000 mujeres):
Coágulos de sangre perjudiciales en una vena o arteria, por ejemplo:
- en una pierna o pie (es decir, TVP)
- en un pulmón (es decir, EP)
- ataque al corazón
- ictus
- mini-ictus o síntomas temporales similares a los de un ictus, lo que se llama accidente isquémico transitorio (AIT)
- coágulos de sangre en el hígado, estómago/intestino, riñones u ojo.
Las posibilidades de tener un coágulo de sangre pueden ser mayores si tiene cualquier otra afección que aumente este riesgo (ver sección 2 para obtener más información sobre las afecciones que aumentan el riesgo de padecer coágulos de sangre y los síntomas de un coágulo de sangre).
- Cáncer de mama, de cuello del útero o hígado
- Problemas en las zonas de la piel donde se ha puesto el parche como erupción con ampollas o úlceras
- Tumores no cancerosos (benignos) en las mamas o el hígado
- Mioma uterino
- Furia o sentirse frustrada
- Aumento del deseo sexual
- Alteración del gusto
- Problemas con el uso de lentillas
- Aumento brusco repentino de la presión arterial (crisis hipertensiva)
- Inflamación de la vesícula biliar o del colon
- Células anormales en el cuello del útero
- Puntos o manchas marrones en la cara
- Cálculos biliares o bloqueo de los conductos biliares
- La piel y la parte blanca de los ojos amarillean
- Niveles de azúcar o insulina en sangre anormales
- Hinchazón de la cara, boca, garganta o lengua
- Erupción cutánea con nódulos rojos dolorosos en las espinillas y en las piernas
- Picor en la piel
- Piel áspera, descamada, con picor y enrojecimiento
- Supresión de la lactancia
- Secreción vaginal
- Retención de líquidos en las piernas
- Retención de líquidos
- Hinchazón en los brazos, las manos, las piernas o los pies.
Si tiene molestias de estómago
- La cantidad de hormonas que obtiene de EVRA no se ve afectada por estar enferma (vómitos) o diarrea.
- No necesita utilizar medidas anticonceptivas adicionales si tiene molestias de estómago.
Puede tener manchado o hemorragia ligera o sensibilidad en las mamas o puede sentir malestar durante los primeros 3 ciclos. Normalmente estos síntomas desaparecen pero si no es así, consulte a su médico o farmacéutico.
Comunicación de efectos adversos
Si experimenta cualquier tipo de efecto adverso, consulte a su médico, farmacéutico o enfermero, incluso si se trata de posibles efectos adversos que no aparecen en este prospecto. También puede comunicarlos directamente a través del sistema nacional de notificación incluido en el Apéndice V. Mediante la comunicación de efectos adversos usted puede contribuir a proporcionar más información sobre la seguridad de este medicamento.
5. Conservación de EVRA
Mantener este medicamento fuera de la vista y del alcance de los niños.
No utilice este medicamento después de la fecha de caducidad que aparece en la etiqueta después de “CAD”. La fecha de caducidad es el último día del mes que se indica.
Conservar en el embalaje original para protegerlo de la luz y la humedad.
No refrigerar o congelar.
Los parches usados todavía contienen algunas hormonas activas. Para proteger el medio ambiente, deben eliminarse con cuidado. Para desechar el parche usado, debe:
- Despegar la etiqueta destinada a desechar el parche de la parte exterior del sobre.
- Coloque el parche usado en la etiqueta, de manera que la parte adhesiva cubra la zona sombreada.
- Cierre la etiqueta dejando en su interior el parche y tírela, manténgala fuera del alcance de los niños.
Los medicamentos no se deben tirar por los desagües ni a la basura. Pregunte a su farmacéutico cómo deshacerse de los envases y de los medicamentos que ya no necesita. De esta forma ayudará a proteger el medio ambiente.
6. Contenido del envase e información adicional
Composición de EVRA
Los principios activos son norelgestromina y etinilestradiol. Cada parche transdérmico de 20 cm2 contiene 6 mg de norelgestromina y 600 microgramos de etinilestradiol.
Los principios activos se liberan durante 7 días, liberándose cada 24 horas una media de 203 microgramos de norelgestromina y 34 microgramos de etinilestradiol.
Los demás componentes son: capa exterior: capa externa de polietileno pigmentado de baja densidad,
capa interna de poliéster; capa intermedia: adhesivo de poliisobutileno/polibuteno, crospovidona, material de poliéster sin tejer, lauril lactato; tercera capa: película de tereftalato de polietileno (PET), recubrimiento de polidimetilsiloxano.
Aspecto del producto y contenido del envase
EVRA es un parche transdérmico plástico, fino, de color beige que lleva grabado “EVRA”. La capa adhesiva se pega sobre la piel después de quitar la capa protectora de plástico transparente.
EVRA se presenta en los siguientes tamaños de envase: Cajas de 3, 9 ó 18 parches en sobres individuales forrados, envueltos de tres en tres, con una lámina transparente de plástico perforada.
Puede que solamente estén comercializados algunos tamaños de envases.
Titular de la autorización de comercialización y responsable de la fabricación
Titular de la autorización de comercialización: Janssen-Cilag International NV Turnhoutseweg, 30, B-2340 Beerse, Bélgica.
Responsable de la fabricación: Janssen-Pharmaceutica NV, Turnhoutseweg 30, B-2340 Beerse, Bélgica.
Pueden solicitar más información respecto a este medicamento dirigiéndose al representante local del titular de la autorización de comercialización:
België/Belgique/Belgien Janssen-Cilag NV Antwerpseweg 15-17 B-2340 Beerse Tel/Tél: + 32 14 64 94 11 | Lietuva UAB "JOHNSON & JOHNSON" Konstitucijos pr. 21C LT-08130 Vilnius Tel: +370 5 278 68 88 |
???????? „??????? & ??????? ????????” ???? ?.?. ??????? 4 ?????? ???? ?????, ?????? 4 ????? 1766 ???.: +359 2 489 94 00 | Luxembourg/Luxemburg Janssen-Cilag NV Antwerpseweg 15-17 B-2340 Beerse Belgique/Belgien Tél/Tel: + 32 14 64 94 11 |
Ceská republikaJanssen-Cilag s.r.o. Walterovo námestí 329/1 CZ-158 00 Praha 5 – Jinonice Tel: +420 227 012 227 | Magyarország Janssen-Cilag Kft. Nagyenyed u. 8-14 H-Budapest, 1123 Tel: +36 1 884 2858 |
Danmark Janssen-Cilag A/S Bregnerødvej 133 DK-3460 Birkerød Tlf: +45 45 94 82 82 | Malta AM.MANGION LTD Mangion Building, Triq Gdida fi Triq Valletta MT-Hal-Luqa LQA 6000 Tel:+356 2397 6000 |
Deutschland Janssen-Cilag GmbH Johnson & Johnson Platz 1 D-41470 Neuss Tel: +49 2137 955 955 | Nederland Janssen-Cilag B.V. Graaf Engelbertlaan 75 NL-4837 DS Breda Tel: +31 76 711 1111 |
Eesti UAB "JOHNSON & JOHNSON" Eesti filiaal Lõõtsa 2 EE-11415 Tallinn Tel: +372 617 7410 | Norge Janssen-Cilag AS Postboks 144 NO-1325-Lysaker Tlf: + 47 24 12 65 00 |
Ελλ?δα Janssen-Cilag Φαρμακευτικ? Α.Ε.Β.Ε. Λεωφ?ρος Ειρ?νης 56 GR-151 21 Πε?κη, Αθ?να Tηλ: +30 210 80 90 000 | Österreich Janssen-Cilag Pharma GmbH. Vorgartenstraße 206B A-1020 Wien Tel:+43 1 610 300 |
España Janssen-Cilag, S.A. Paseo de las Doce Estrellas, 5-7 E-28042 Madrid Tel: +34 91 722 81 00 | Polska Janssen-Cilag Polska Sp. z o.o. ul. Ilzecka 24 PL-02-135 Warszawa Tel.: + 48 22 237 60 00 |
France Janssen-Cilag 1, rue Camille Desmoulins, TSA 91003 F-92787 Issy Les Moulineaux, Cedex 9 Tél: 0800 25 50 75 / + 33 1 55 00 40 03 | Portugal Janssen-Cilag Farmacêutica, Lda. Lagoas Park, Edifício 9 PT-2740-262 Porto Salvo Tel: +351 214 368 600 |
Hrvatska Johnson & Johnson S.E. d.o.o. Oreškoviceva 6h 10010 Zagreb Tel: +385 1 6610 700 | România Johnson & Johnson România SRL Str. Tipografilor nr.11 – 15 Cladirea S-Park, Corp B3-B4, Etaj 3 013714 Bucuresti, ROMÂNIA Tel: +40 21 207 18 00 |
Ireland Janssen Sciences Ireland UC Barnahely Ringaskiddy IRL – Co. Cork P43 FA46 Tel: +353 1 800 709 122 | Slovenija Johnson & Johnson d.o.o. Šmartinska cesta 53 SI-1000, Ljubljana Tel. + 386 1 401 18 00 |
Ísland Janssen-Cilag AB c/o Vistor hf. Hörgatúni 2 IS-210 Garðabær Simi: (+354) 535 7000 | Slovenskárepublika Janssen, Johnson & Johnson, s.r.o. CBC III, Karadžicova 12 SK-821 08 Bratislava Tel. +421 232 408 400 |
Italia Janssen-Cilag SpA Via M.Buonarroti, 23 I-20093 Cologno Monzese MI Tel: +39 02 2510 1 | Suomi/Finland Janssen-Cilag Oy Vaisalantie/Vaisalavägen 2 FI-02130 Espoo/Esbo Puh/Tel: +358 207 531 300 |
Κ?προς Βαρν?βας Χατζηπαναγ?ς Λτδ Λεωφ?ρος Γι?ννου Κρανιδι?τη 226 Λατσι? CY-2234 Λευκωσ?α Τηλ: +357 22 207 700 | Sverige Janssen-Cilag AB Box 4042 SE-16904 Solna Tel: +46 8 626 50 00 |
Latvija UAB "JOHNSON & JOHNSON" filiale Latvija Mukusalas iela 101 Riga, LV-1004 Tel: +371 678 93561 | United Kingdom Janssen-Cilag Ltd. 50-100 Holmers Farm Way High Wycombe Buckinghamshire HP12 4EG - UK Tel: +44 1 494 567 444 |
Fecha de la última revisión de este prospecto:
Otras fuentes de información
La información detallada de este medicamento está disponible en la página web de la Agencia Europea de Medicamentos: http://www.ema.europa.eu .
- País de registro
- Principio activo
- Requiere recetaSí
- Fabricante
- Esta información es de carácter general y no sustituye la consulta con un profesional sanitario.
- Alternativas a EVRA 203 MICROGRAMOS/24 HORAS + 33,9 MICROGRAMOS/24 HORAS PARCHE TRANSDERMICOForma farmacéutica: PARCHE TRANSDERMICO, 203 microgramos/24 h + 33,9 microgramos/24 hPrincipio activo: norelgestromin and ethinylestradiolFabricante: Gedeon Richter Plc.Requiere recetaForma farmacéutica: PARCHE TRANSDERMICO, 203 microgramos/24 h + 33,9 microgramos/24 hPrincipio activo: norelgestromin and ethinylestradiolFabricante: Gedeon Richter Plc.Requiere recetaForma farmacéutica: COMPRIMIDO, 2 mg/0.03 mgPrincipio activo: dienogest and ethinylestradiolFabricante: Laboratorios Cinfa S.A.Requiere receta
Médicos online para EVRA 203 MICROGRAMOS/24 HORAS + 33,9 MICROGRAMOS/24 HORAS PARCHE TRANSDERMICO
Comenta la dosis, los posibles efectos secundarios, interacciones, contraindicaciones o la revisión de receta de EVRA 203 MICROGRAMOS/24 HORAS + 33,9 MICROGRAMOS/24 HORAS PARCHE TRANSDERMICO, sujeto a valoración médica y a la normativa local.
Preguntas frecuentes