
BROMURO DE IPRATROPIO/SALBUTAMOL GENETIC 0,5 MG/2,5 MG SOLUCION PARA INHALACION POR NEBULIZADOR


Cómo usar BROMURO DE IPRATROPIO/SALBUTAMOL GENETIC 0,5 MG/2,5 MG SOLUCION PARA INHALACION POR NEBULIZADOR
Traducción generada por IA
Este contenido ha sido traducido automáticamente y se ofrece solo con fines informativos. No sustituye la consulta con un profesional sanitario.
Ver originalContenido del prospecto
- Introducción
- Qué es Bromuro de ipratropio/Salbutamol Genetic y para qué se utiliza
- Qué necesita saber antes de empezar a usar Bromuro de ipratropio/Salbutamol Genetic
- Cómo usar Bromuro de ipratropio/Salbutamol Genetic
- Posibles efectos adversos
- Conservación de Bromuro de ipratropio/Salbutamol Genetic
- Contenido del envase e información adicional
Introducción
Prospecto: información para el paciente
Bromuro de ipratropio/Salbutamol Genetic 0,5 mg/2,5 mg solución para inhalación por nebulizador
bromuro de ipratropio/salbutamol
Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene información importante para usted.
- Conserve este prospecto, ya que puede tener que volver a leerlo.
- Si tiene alguna duda, consulte a su médico o farmacéutico.
- Este medicamento se le ha recetado solamente a usted, y no debe dárselo a otras personas aunque tengan los mismos síntomas que usted, ya que puede perjudicarles.
- Si experimenta efectos adversos, consulte a su médico o farmacéutico, incluso si se trata de efectos adversos que no aparecen en este prospecto. Ver sección 4.
Contenido del prospecto
- Qué es Bromuro de ipratropio/Salbutamol Genetic y para qué se utiliza
- Qué necesita saber antes de empezar a usar Bromuro de ipratropio/Salbutamol Genetic
- Cómo usar Bromuro de ipratropio/Salbutamol Genetic
- Posibles efectos adversos
- Conservación de Bromuro de ipratropio/Salbutamol Genetic
- Contenido del envase e información adicional
1. Qué es Bromuro de ipratropio/Salbutamol Genetic y para qué se utiliza
Este medicamento se llama Bromuro de ipratropio/Salbutamol Genetic 0,5 mg/2,5 mg solución para inhalación por nebulizador. Se usa con un dispositivo llamado ‘nebulizador’.
Los principios activos son bromuro de ipratropio y salbutamol. Bromuro de ipratropio y salbutamol pertenecen a un grupo de medicamentos llamados broncodilatadores, que ayudan a mejorar la respiración abriendo las vías respiratorias.
Lo hacen evitando la contracción de los músculos lisos que rodean las vías respiratorias, de modo que éstas permanecen abiertas.
Bromuro de ipratropio actúa bloqueando las señales nerviosas dirigidas a los músculos que rodean las vías respiratorias, y salbutamol actúa estimulando los receptores β2 en los músculos.
Bromuro de ipratropio/salbutamol se usa para facilitar la respiración en una enfermedad conocida como enfermedad pulmonar obstructiva crónica o EPOC en pacientes mayores de 12 años. bromuro de ipratropio/salbutamol aliviará las sibilancias, la dificultad para respirar y la opresión en el pecho.
2. Qué necesita saber antes de empezar a usar Bromuro de ipratropio/Salbutamol Genetic
No use Bromuro de ipratropio/Salbutamol Genetic
- si es alérgico a ipratropio o salbutamol o a alguno de los demás componentes de este medicamento (incluidos en la sección 6);
- si es alérgico a medicamentos similares que contengan atropina o medicamentos como atropina;
- si padece ritmo cardíaco rápido (taquicardias);
- si padece cardiomegalia (corazón agrandado) o una enfermedad llamada miocardiopatía hipertrófica obstructiva o MHO, en la que se produce un engrosamiento de las paredes del corazón que dificulta el flujo sanguíneo.
No lo utilice si alguna de las situaciones anteriores le aplica a usted.
Si no está seguro, consulte a su médico o farmacéutico antes de usar bromuro de ipratropio/salbutamol.
Advertencias y precauciones
Consulte a su médico antes de empezar a usar este medicamento:
- si padece o cree que podría padecer una afección ocular denominada glaucoma (aumento de la presión en los ojos) o cualquier otra afección ocular. Su médico quizá le aconseje que se proteja los ojos cuando utilice las ampollas de bromuro de ipratropio/salbutamol;
- si es un hombre y tiene una hipertrofia prostática o problemas para orinar;
- si ha tenido un ataque al corazón (infarto de miocardio) recientemente; si sufre problemas arteriales o dolor en las piernas cuando camina.;
- si tiene antecedentes de enfermedad cardíaca, ritmo cardíaco irregular o angina de pecho (por favor informe a su médico antes de comenzar a utilizar este medicamento);
- si padece diabetes;
- si tiene una glándula tiroides hiperactiva;
- si padece fibrosis quística;
- si le han comunicado que tiene un tumor en la glándula suprarrenal. (no maligno) llamado feocromocitoma. El uso del inhalador puede empeorar los síntomas del mismo.
- Si está embarazada, o tiene intención de quedarse embarazada o en periodo de lactancia. (Ver sección “Embarazo y Lactancia”).
Informe a su médico antes de empezar a usar bromuro de ipratropio/salbutamol si presenta alguna de las condiciones anteriores.
Se ha observado acidosis láctica asociada a altas dosis terapéuticas de salbutamol, principalmente en pacientes tratados con un broncoespasmo agudo (ver las secciones 3 y 4). El aumento en los niveles de lactato puede dar lugar a la falta de respiración e hiperventilación. Hable inmediatamente con su médico si usted siente que el medicamento no está funcionando como habitualmente y necesita usar el nebulizador más veces de las que su médico le ha recomendado.
Consulte a su médico en caso de empeoramiento repentino de sus trastornos respiratorios o si la dosis prescrita no da un resultado normal. No aumente la dosis sin consultar al médico. (Ver sección: “Cómo usar Bromuro de ipratropio/Salbutamol Genetic”).
Si utiliza dosis elevadas de Bromuro de ipratropio/salbutamol durante mucho tiempo, se debe vigilar la cantidad de potasio en sangre, especialmente si está tomando otros medicamentos al mismo tiempo, por ejemplo: esteroides (corticoesteroides), medicamentos que aumentan la producción de orina (diuréticos) u otros medicamentos que abran las vías respiratorias, como teofilina (xantinas). (Ver sección: “Posibles efectos adversos”).
Otros medicamentosy Bromuro de ipratropio/Salbutamol Genetic
Informe a su médico o farmacéutico si está tomando, ha tomado recientemente o pudiera tener que tomar cualquier otro medicamento.
Determinados medicamentos pueden interactuar con bromuro de ipratropio/salbutamol y empeorar los efectos adversos o reducir el efecto de bromuro de ipratropio/salbutamol. Informe siempre a su médico si está tomando alguno de los siguientes medicamentos:
- diuréticos (para incrementar la eliminación de orina)
- comprimidos esteroideos (medicamentos que reducen la inflamación como la prednisolona). Estos medicamentos incrementan el riesgo de niveles bajos de potasio;
- determinados medicamentos para tratar la depresión (como los “antidepresivos”, que son medicamentos prescritos para pacientes con depresión y ansiedad). En esta clase de medicamentos se incluyen los inhibidores de la monoaminooxidasa (p. ej., fenelzina) o los antidepresivos tricíclicos (p. ej., amitriptilina);
- otros medicamentos que ayudan a respirar, como salbutamol y preventivos como dipropionato de beclometasona. Estos pueden aumentar el efecto de bromuro de ipratropio/salbutamol e incrementar la intensidad de los efectos adversos;
- ‘anticolinérgicos’. Se emplean para tratar el dolor cólico, la enfermedad de Parkinson, los problemas para orinar o la incontinencia urinaria o fecal;
- betabloqueantes, es decir, medicamentos utilizados a menudo para tratar afecciones cardíacas, como el dolor en el pecho que se produce durante el esfuerzo (llamado angina de pecho), los latidos cardíacos irregulares (o arritmias) y la presión arterial alta (llamada hipertensión). Se incluyen medicamentos como propranolol. Estos medicamentos se oponen al efecto de ‘apertura de las vías respiratorias’ de bromuro de ipratropio/salbutamol;
- medicamentos llamados ‘beta miméticos’ como fenoterol para problemas respiratorios;
- digoxina (para problemas del corazón) puede causar problemas del ritmo cardíaco cuando se administra junto con bromuro de ipratropio/salbutamol;
- los anestésicos pueden aumentar la propensión a padecer los efectos adversos de salbutamol sobre el corazón. Su médico le supervisará estrechamente o quizá su médico, dentista o anestesista decida interrumpir el tratamiento con bromuro de ipratropio/salbutamol si le van a operar.
Si no está seguro de si alguno de los puntos anteriores le aplica a usted, consulte a su médico o farmacéutico antes de empezar a usar bromuro de ipratropio/salbutamol.
Niños y adolescentes
Bromuro de ipratropio/salbutamol no debe usarse en niños menores de 12 años.
Pruebas de laboratorio
Si tiene que proporcionar una muestra de orina como parte de un control rutinario de drogas en el deporte, dígale a la persona que le haga la prueba que está tomando bromuro de ipratropio/salbutamol porque contiene salbutamol, que puede dar un resultado positivo en la prueba.
Uso de Bromuro de ipratropio/Salbutamol Genetic con alimentos y bebidas
Los alimentos y las bebidas no ejercen ninguna influencia sobre bromuro de ipratropio/salbutamol.
Embarazo y lactancia
Si está embarazada o en periodo de lactancia, cree que podría estar embarazada o tiene intención de quedarse embarazada, consulte a su médico o farmacéutico antes de utilizar este medicamento.
No use bromuro de ipratropio/salbutamol si está embarazada, tiene intención de quedarse embarazada o está en periodo de lactancia a menos que su médico decida que el beneficio para usted es superior al riesgo para su hijo.
Conducción y uso de máquinas
Si padece efectos adversos como mareos, dificultad para enfocar la vista y visión borrosa durante el tratamiento con bromuro de ipratropio/salbutamol debe evitar conducir o utilizar máquinas.
3. Cómo usar Bromuro de ipratropio/Salbutamol Genetic
Siga exactamente las instrucciones de administración de este medicamento indicadas por su médico. En caso de duda, pregunte a su médico o farmacéutico.
Bromuro de ipratropio/salbutamol es para uso por inhalación. La solución es para inhalación oral tras la nebulización.
La dosis recomendada para adultos y niños mayores de 12 años es de 1 ampolla, de tres a cuatro veces al día.
Los pacientes de edad avanzada deben tomar la dosis habitual de adultos.
Uso en niños
Bromuro de ipratropio/salbutamol no se recomienda en niños menores de 12 años.
Bromuro de ipratropio/salbutamol no ha sido estudiado en pacientes con insuficiencia renal o hepática, por lo que debería usarse con precaución en estas poblaciones de pacientes.
No utilice una cantidad de medicamento superior a la indicada por su médico. Informe a su médico si sus problemas respiratorios empeoran, si el medicamento no le alivia los problemas para respirar tanto como antes o si está utilizando el inhalador azul «de rescate» de acción corta (de alivio rápido) con más frecuencia de lo habitual.
Instrucciones de uso
Lea las instrucciones primero antes de empezar a usar el nebulizador.
- Prepare el nebulizador siguiendo las instrucciones del fabricante y el consejo de su médico.
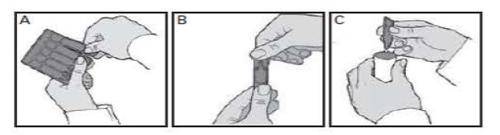
- Separe con cuidado una ampolla de la tira etiquetada girando y tirando. No utilice nunca una ampolla que ya haya sido abierta o si la solución para inhalación por nebulizador está descolorida (imagen A).
- Mantenga la ampolla en posición vertical y ábrala girando la parte superior (imagen B).
- Transfiera todo el contenido a la cámara del nebulizador apretando la ampolla (imagen C).
- Ensamble el nebulizador y úselo siguiendo las instrucciones del fabricante y las indicaciones de su médico.
- Después de utilizar el nebulizador, deseche toda la solución que haya quedado en la cámara. Si queda solución para inhalación por nebulizador en la ampolla, también debe desecharse.
- Limpie bien el nebulizador siguiendo las instrucciones del fabricante. Es importante que el nebulizador se mantenga limpio.
No diluya la solución para inhalación por nebulizador ni la mezcle con otros medicamentos, a menos que se lo indique su médico.
Las ampollas unidosis de bromuro de ipratropio/salbutamol no contienen conservantes y, por ello, es importante que el contenido se utilice inmediatamente después de la apertura. Debe utilizar una ampolla nueva para cada administración de bromuro de ipratropio/salbutamol con el nebulizador.
Deben desecharse las ampollas parcialmente utilizadas, abiertas o dañadas. No debe utilizar nunca una ampolla que ya haya sido abierta.
Es importante que siga estas instrucciones para evitar la contaminación de la solución para inhalación por nebulizador contenida en las ampollas.
No tragar o administrar este medicamento mediante inyección. No permita que la solución para inhalación por nebulizador o el vapor entre en contacto con los ojos. Si alguno de los líquidos o el vapor le entra en los ojos accidentalmente, es posible que le duelan, le escuezan o se le pongan rojos, que se le dilaten las pupilas, tenga visión borrosa o vea colores o luces. Si le sucediera, consulte a su médico. Si tiene problemas en los ojos en cualquier otro momento, consulte a su médico.
Si usa más Bromuro de ipratropio/Salbutamol Geneticdel que debe
Si ha tomado una dosis ligeramente superior a la habitual, quizá note un latido cardíaco más rápido (palpitaciones) o temblores. Otros síntomas pueden ser dolor en el pecho, cambios en la presión arterial, sofoco, inquietud o mareos. Estos efectos suelen desaparecer en unas pocas horas. Es posible que descienda la cantidad de potasio en su sangre; su médico quizá desee vigilar su nivel de potasio haciéndole un análisis de sangre de vez en cuando. Informe a su médico si le preocupa alguno de estos síntomas o si estos persisten.
Si utiliza más cantidad de este medicamento de la que debe, informe a su médico de inmediato o acuda al hospital más cercano. Si decide acudir a un médico o al hospital, debe llevar todos sus medicamentos, incluidos los adquiridos sin receta médica; llévelos en su embalaje original si es posible. Lleve también este prospecto para mostrárselo al médico.
En caso de sobredosis o ingestión accidental, consulte inmediatamente a su médico o farmacéutico o llame al Servicio de Información Toxicológica, teléfono 91 562 04 20, indicando el medicamento y la cantidad ingerida.
Si olvidó usar Bromuro de ipratropio/Salbutamol Genetic
Si olvidó tomar una dosis a la hora adecuada, tómela en cuanto se acuerde.
No tome una dosis doble para compensar las dosis olvidadas.
Si interrumpe el tratamiento con Bromuro de ipratropio/Salbutamol Genetic
No debe interrumpir el tratamiento con bromuro de ipratropio/salbutamol sin consultar antes con su médico.
Si tiene cualquier otra duda sobre el uso de este medicamento, pregunte a su médico o farmacéutico.
4. Posibles efectos adversos
Al igual que todos los medicamentos, este medicamento puede producir efectos adversos, aunque no todas las personas los sufran.
Algunos efectos adversos pueden ser graves y requerir intervención médica.
Informe a su médico inmediatamente si nota alguno de los siguientes efectos adversos graves - puede necesitar tratamiento médico urgente:
Si su problema respiratorio o sus sibilancias empeoran inmediatamente después de inhalar bromuro de ipratropio/salbutamol, o le cuesta respirar y se queda sin aliento, no tome más bromuro de ipratropio/salbutamol, utilice en seguida su inhalador de alivio inmediato de acción corta. Debe dejar de utilizar bromuro de ipratropio/salbutamol y ponerse en contacto con su médico cuanto antes. Es posible que su médico le prescriba otro tratamiento alternativo para su afección.
Si cree que es alérgico a bromuro de ipratropio/salbutamol o que está teniendo una reacción alérgica a la solución para inhalación por nebulizador (que incluyen hinchazón de la lengua, los labios y la cara), deje de usar bromuro de ipratropio/salbutamol y contacte con su médico inmediatamente.
Vea a su médico si presenta alguno de estos efectos adversos.
Si experimenta dolor ocular o molestias en los ojos, visión borrosa u ojos rojos, o si ve halos o manchas de color, debe ponerse en contacto con su médico inmediatamente, ya que puede ser necesario un tratamiento para estos síntomas.
Una reducción de la cantidad de potasio en la sangre (hipopotasemia) debida al salbutamol de este medicamento es más probable si está utilizando bromuro de ipratropio/salbutamol junto con otros tratamientos para el asma, junto con corticoesteroides inhalados o en comprimidos (como la prednisona), o junto con diuréticos (para incrementar la eliminación de orina). Un nivel bajo de potasio en sangre puede causar debilidad muscular, contracciones musculares o anomalías del ritmo cardíaco. Es posible que su médico le haga un análisis de sangre para medir la cantidad de potasio de vez en cuando.
También puede producirse el siguiente efecto secundario, pero su frecuencia no es conocida:
Una condición conocida como acidosis láctica que puede causar dolor de estómago, hiperventilación, dificultad respiratoria, a pesar de que pueda haber una mejora en sus sibilancias, pies y manos frías, latidos irregulares del corazón o sed.
Índices de frecuencia de los efectos adversos
Poco frecuentes(puede afectar hasta 1 de cada 100 personas)
- Sentirse nervioso, tembloroso o mareado
- Boca seca
- Tos, dolor de cabeza
- Sensación de malestar (náuseas)
- Irritación de la garganta
- Aumento de la presión arterial
- Aumento del ritmo cardíaco o latidos irregulares (palpitaciones)
- Problemas del habla (‘disfonía’)
- Reacciones cutáneas
Raros(puede afectar hasta 1 de cada 1.000 personas)
- Ritmo cardíaco irregular
- Frecuencia cardíaca regular pero anormalmente rápida (taquicardia supraventricular)
- Dolor en el pecho (debido a problemas cardíacos como la angina de pecho). Informe a su médico o farmacéutico si esto ocurre, pero no deje de tomar este medicamento a menos que se lo indiquen
- Visión borrosa, pupilas dilatadas, glaucoma, dolor, escozor o enrojecimiento de los ojos, hinchazón de los ojos, ver colores o luces
- Aumento de la sudoración
- Opresión inesperada en el pecho inmediatamente después de inhalar el medicamento
- Sequedad de garganta, hinchazón de la garganta
- Dificultad para respirar o hablar debido a un breve espasmo de los músculos vocales
- Diarrea, estreñimiento, náuseas (vómitos) u otros problemas del sistema digestivo
- Inflamación de la boca
- Calambres, debilidad y dolor muscular
- Dificultad para orinar
- Sensación de debilidad
- Descenso de la presión arterial
- Cambios de humor
También puede tener niveles inusualmente bajos de potasio en la sangre (lo que se denomina "hipopotasemia"). Si esto ocurre, su médico seguirá comprobando sus niveles de potasio.
Aunque no se sabe con exactitud con qué frecuencia ocurre esto, algunas personas pueden experimentar dolor en el pecho (debido a problemas como la angina de pecho).
Informe a su médico lo antes posible si desarrolla estos síntomas mientras recibe tratamiento con bromuro de ipratropio/salbutamol, pero no deje de usar este medicamento a menos que se lo indiquen.
Si el líquido o el vapor entra accidentalmente en sus ojos, puede sentir dolor, escozor o enrojecimiento de los ojos, dilatación de las pupilas, visión borrosa, ver colores o luces. Si esto ocurre, hable con su médico para que le aconseje. Si tiene problemas con los ojos en cualquier otro momento, hable con su médico para que le aconseje.
Comunicación de efectos adversos
Si experimenta cualquier tipo de efecto adverso, consulte a su médico o farmacéutico, incluso si se trata de posibles efectos adversos que no aparecen en este prospecto. También puede comunicarlos directamente a través del Sistema Español de Farmacovigilancia de Medicamentos de Uso Humano: www.notificaRAM.es. Mediante la comunicación de efectos adversos usted puede contribuir a proporcionar más información sobre la seguridad de este medicamento.
5. Conservación de Bromuro de ipratropio/Salbutamol Genetic
Mantener este medicamento fuera de la vista y del alcance de los niños.
No utilice este medicamento después de la fecha de caducidad que aparece en la etiqueta del cartón, del sobre y de la ampolla después de CAD. La fecha de caducidad es el último día del mes que se indica.
- Para un solo uso. Utilizar inmediatamente después de abrir la ampolla por primera vez. Desechar inmediatamente después del primer uso.
- La eliminación de las ampollas parcialmente utilizadas, abiertas o dañadas se realizará de acuerdo con la normativa local.
No congelar.
Tras la apertura de la bolsa, utilizar en un plazo de 7 días.
No utilice este medicamento si observa que la solución para inhalación por nebulizador está turbia.
Los medicamentos no se deben tirar por los desagües, ni a la basura. Deposite los envases y los medicamentos que no necesita en el Punto Sigre de la farmacia. En caso de duda, pregunte a su farmacéutico cómo deshacerse de los envases y de los medicamentos que ya no necesita. De esta forma, ayudará a proteger el medio ambiente.
6. Contenido del envase e información adicional
Composición de Bromuro de ipratropio/Salbutamol Genetic
- Los principios activos son bromuro de ipratropio y salbutamol. Cada ampolla unidosis (dosis de 2,5 ml) contiene 0,5 mg de bromuro de ipratropio (como monohidrato) y 2,5 mg de salbutamol (como sulfato).
- Los demás excipientes son cloruro sódico, agua para preparaciones inyectables y ácido hidroclorhídrico (para el ajuste del pH).
Aspecto del producto y contenido del envase
20 o 30 ampollas unidosis de LDPE etiquetadas, divididas en tiras de 5 ampollas, en un envoltorio de PET/Al/PE (1 tira en cada envoltorio) y envasadas en un estuche adecuado, junto con el prospecto.
Envases de 20 y 30 viales.
Puede que solamente estén comercializados algunos tamaños de envases.
Titular de la autorización de comercialización
Genetic S.p.A.
Via Giuseppe Della Monica 26
Castel San Giorgio (SALERNO)
84083 Italia
Responsable de la fabricación
Genetic S.p.A.
Contrada Canfora,
Fisciano, Salerno
84083 Italia
Representante local
Mabo-Farma S.A.
Calle Vía de los Poblados 3, Edificio 6,
28033 Madrid,
España.
Este medicamento está autorizado en los estados miembros del Espacio Económico Europeo con los siguientes nombres:
País | Nombre del medicamento |
Portugal: | Respito |
España: | Bromuro de ipratropio/Salbutamol Genetic 0,5 mg/2,5 mg solución para inhalación por nebulizador |
Fecha de la última revisión de este prospecto: 04/2022
La información detallada y actualizada de este medicamento está disponible en la página web de la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) (http://www.aemps.gob.es/)
- País de registro
- Principio activo
- Requiere recetaSí
- Fabricante
- Esta información es de carácter general y no sustituye la consulta con un profesional sanitario.
- Alternativas a BROMURO DE IPRATROPIO/SALBUTAMOL GENETIC 0,5 MG/2,5 MG SOLUCION PARA INHALACION POR NEBULIZADORForma farmacéutica: INHALACIÓN PULMONAR, 0,5 mg/2,5 mgPrincipio activo: salbutamol and ipratropium bromideFabricante: Neutec Inhaler Ireland LimitedRequiere recetaForma farmacéutica: INHALACIÓN PULMONAR, 0,5 mg/2,5 mgPrincipio activo: salbutamol and ipratropium bromideFabricante: Laboratorio Aldo Union S.L.Requiere recetaForma farmacéutica: INHALACIÓN PULMONAR, 0,5 mg/2,5 mgPrincipio activo: salbutamol and ipratropium bromideFabricante: Cipla EuropeRequiere receta
Médicos online para BROMURO DE IPRATROPIO/SALBUTAMOL GENETIC 0,5 MG/2,5 MG SOLUCION PARA INHALACION POR NEBULIZADOR
Comenta la dosis, los posibles efectos secundarios, interacciones, contraindicaciones o la revisión de receta de BROMURO DE IPRATROPIO/SALBUTAMOL GENETIC 0,5 MG/2,5 MG SOLUCION PARA INHALACION POR NEBULIZADOR, sujeto a valoración médica y a la normativa local.
Preguntas frecuentes















