
Rymphysia

Zapytaj lekarza o receptę na Rymphysia

Jak stosować Rymphysia
Ulotka dołączona do opakowania: informacja dla użytkownika
Rymphysia, 500 mg, proszek i rozpuszczalnik do sporządzania roztworu do infuzji
Rymphysia, 1000 mg, proszek i rozpuszczalnik do sporządzania roztworu do infuzji
ludzki inhibitor alfa1-proteinazy
Niniejszy produkt leczniczy będzie dodatkowo monitorowany. Umożliwi to szybkie
zidentyfikowanie nowych informacji o bezpieczeństwie. Użytkownik leku też może w tym pomóc,
zgłaszając wszelkie działania niepożądane, które wystąpiły po zastosowaniu leku. Aby dowiedzieć się,
jak zgłaszać działania niepożądane – patrz punkt 4.
Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje ważne dla pacjenta.
- Należy zachować tę ulotkę, aby w razie potrzeby móc ją ponownie przeczytać.
- W razie jakichkolwiek wątpliwości należy zwrócić się do lekarza lub fachowego personelu medycznego.
- Lek ten przepisano ściśle określonej osobie. Nie należy go przekazywać innym. Lek może zaszkodzić innej osobie, nawet jeśli objawy jej choroby są takie same.
- Jeśli u pacjenta wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie objawy niepożądane niewymienione w tej ulotce, należy powiedzieć o tym lekarzowi lub innej osoby należącej do fachowego personelu medycznego. Patrz punkt 4.
Spis treści ulotki
- 1. Co to jest lek Rymphysia i w jakim celu się go stosuje
- 2. Informacje ważne przed zastosowaniem leku Rymphysia
- 3. Jak stosować lek Rymphysia
- 4. Możliwe działania niepożądane
- 5. Jak przechowywać lek Rymphysia
- 6. Zawartość opakowania i inne informacje
1. Co to jest lek Rymphysia i w jakim celu się go stosuje
Co to jest lek Rymphysia
Lek ten zawiera substancję czynną o nazwie „ ludzki inhibitor alfa1-proteinazy”, który jest normalnym
składnikiem krwi i występuje w płucach. Jego główną funkcją w płucach jest ochrona tkanki płucnej
przez hamowanie działania pewnego enzymu, zwanego elastazą neutrofilową. Elastaza neutrofilowa
może powodować uszkodzenia, jeśli jej działanie nie jest kontrolowane (na przykład, jeśli pacjent ma
niedobór inhibitora alfa1-proteinazy).
W jakim celu stosuje się lek Rymphysia
Lek ten stosuje się u dorosłych z rozpoznanym ciężkim niedoborem inhibitora alfa1-proteinazy
(zwanym też niedoborem alfa1-antytrypsyny), u których doszło do choroby płuc zwanej rozedmą płuc.
Rozedma płuc występuje, gdy brak inhibitora alfa1-proteinazy prowadzi do stanu, w którym elastaza
neutrofilowa nie jest właściwie kontrolowana, powodując uszkodzenie drobnych pęcherzyków
w płucach, przez które tlen przenika do organizmu. Z powodu takiego uszkodzenia płuca nie działają
prawidłowo.
Regularne stosowanie tego leku zwiększa stężenie inhibitora alfa1-proteinazy we krwi i w płucach,
dzięki czemu chroni płuca, ograniczając działanie elastazy neutrofilowej i w ten sposób spowalnia
rozwój rozedmy płuc. Nie należy się spodziewać, że lek spowoduje cofnięcie uszkodzeń, które już
wystąpiły.
2. Informacje ważne przed zastosowaniem leku Rymphysia
Kiedy nie stosować leku Rymphysia
- jeśli pacjent ma uczulenie na „ludzki inhibitor alfa1-proteinazy” lub którykolwiek z pozostałych składników tego leku (wymienionych w punkcie 6).
- jeśli u pacjenta stwierdzono we krwi niedobór białek zwanych immunoglobulinami typu A (IgA) i występują u niego przeciwciała przeciwko tym immunoglobulinom.
Jeśli którekolwiek z powyższych dotyczy pacjenta, nie należy stosować leku Rymphysia.
Ostrzeżenia i środki ostrożności
Przed rozpoczęciem stosowania leku Rymphysia należy omówić to z lekarzem lub inną osobą
należącą do fachowego personelu medycznego.
Informacje na temat reakcji alergicznych
Pacjent może mieć uczulenie na lek Rymphysia, nawet jeśli otrzymywał wcześniej podobne leki
i dobrze je tolerował.
- W niektórych przypadkach może wystąpić ciężka reakcja alergiczna.
- Pacjent zostanie poinformowany przez lekarza, jakie są objawy reakcji alergicznych (na przykład dreszcze, uderzenia gorąca, szybsze bicie serca, spadek ciśnienia krwi, odczuwanie oszołomienia, wysypka, pokrzywka, swędzenie, trudności w oddychaniu lub przełykaniu, jak również obrzęk dłoni, twarzy lub jamy ustnej) - patrz także „Reakcje alergiczne” w punkcie 4.
- Jeśli reakcja jest ciężka, lekarz może zdecydować o zmniejszeniu szybkości lub całkowitym przerwaniu infuzji. Następnie może zastosować odpowiednie leczenie objawów reakcji alergicznej.
Należy niezwłocznie powiedzieć lekarzowi lub innej osobie należącej do fachowego personelu
medycznego, jeśli zaobserwuje się wymienione powyżej reakcje w czasie infuzji. W razie leczenia
w warunkach domowych i (lub) samodzielnego podawania, należy natychmiast przerwać infuzję
i skontaktować się z lekarzem lub inną osobą należącą do fachowego personelu medycznego.
Możliwość zakażenia
Lek Rymphysia jest wytwarzany z osocza ludzkiej krwi (jest to płynny składnik krwi, z której
usunięto krwinki).
Gdy leki wytwarzane są z ludzkiej krwi lub osocza, podejmowane są określone środki ostrożności, aby
zapobiec przeniesieniu zakażeń na pacjentów. Obejmują one:
- staranną selekcję dawców krwi i osocza, aby zapewnić wykluczenie dawców mogących być nosicielami zakażeń,
- badanie każdej oddanej próbki oraz pul osocza w celu wykrycia śladów obecności wirusów/zakażeń,
- włączenie do procesu przetwarzania krwi lub osocza etapów mających na celu inaktywację lub usunięcie wirusów.
Jednakże, mimo tych środków ostrożności w przypadku podawania leków przygotowanych z ludzkiej
krwi lub osocza nie można całkowicie wykluczyć możliwości przeniesienia zakażenia. Dotyczy to
również wszelkich nieznanych lub nowych wirusów lub innych rodzajów zakażeń.
Podejmowane środki są uważane za skuteczne wobec wirusów otoczkowych, takich jak wirus
ludzkiego niedoboru odporności (HIV), wirus zapalenia wątroby typu B i wirus zapalenia wątroby
typu C, jak również bezotoczkowego wirusa zapalenia wątroby typu A i parwowirusa B19.
W celu poprawienia identyfikowalności biologicznych produktów leczniczych należy czytelnie
zapisać nazwę i numer serii podawanego produktu.
Jeśli pacjent otrzymuje regularnie/wielokrotnie inhibitory proteinazy pochodzące z ludzkiego osocza,
lekarz może zalecić pacjentowi rozważenie szczepienia przeciwko wirusowemu zapaleniu wątroby
typu A i B.
Palenie tytoniu
Dym tytoniowy jest ważnym czynnikiem ryzyka wystąpienia i rozwoju rozedmy płuc, dlatego
zdecydowanie zaleca się rzucenie palenia i unikanie biernego palenia.
Dzieci i młodzież
Ten lek nie jest przeznaczony do stosowania u dzieci i młodzieży w wieku poniżej 18 lat.
Lek Rymphysia a inne leki
Należy powiedzieć lekarzowi lub innej osobie należącej do fachowego personelu medycznego
o wszystkich lekach przyjmowanych przez pacjenta obecnie lub ostatnio, a także o lekach, które
pacjent planuje przyjmować. Dotyczy to również leków wydawanych bez recepty oraz leków
roślinnych.
Jest to konieczne, gdyż lek Rymphysia może wpływać na działanie niektórych innych leków. Ponadto
niektóre leki mogą wpływać na działanie leku Rymphysia.
Ciąża, karmienie piersią i wpływ na płodność
Jeśli pacjentka jest w ciąży lub karmi piersią, przypuszcza że może być w ciąży lub gdy planuje mieć
dziecko, powinna poradzić się lekarza lub innej osoby należącej do fachowego personelu medycznego
przed zastosowaniem tego leku.
Ze względu na to, że inhibitor alfa1-proteinazy jest normalnym składnikiem krwi ludzkiej, nie
oczekuje się by zalecana dawka tego leku wywierała szkodliwe działanie na rozwijający się płód.
Jednakże, ze względu na brak dostępnych danych na temat bezpieczeństwa stosowania leku
Rymphysia w okresie ciąży, jeżeli pacjentka jest w ciąży, lek ten należy stosować wyłącznie
z zachowaniem ostrożności.
Nie wiadomo, czy lek Rymphysia przenika do mleka ludzkiego. Jeżeli pacjentka karmi piersią, lekarz
omówi z nią ryzyka i korzyści związane ze stosowaniem tego leku.
Nie ma danych dotyczących wpływu na płodność, jednak ze względu na to, że inhibitor
alfa1-proteinazy jest normalnym składnikiem krwi ludzkiej nie oczekuje się żadnego niepożądanego
wpływu na płodność w przypadku stosowania leku Rymphysia w zalecanej dawce.
Prowadzenie pojazdów i obsługiwanie maszyn
Lek Rymphysia może wywierać niewielki wpływ na zdolność prowadzenia pojazdów i obsługiwania
narzędzi lub maszyn. Jeśli u pacjenta wystąpią zawroty głowy lub objawy zmęczenia, nie powinien
prowadzić pojazdów ani obsługiwać narzędzi lub maszyn.
Lek Rymphysia zawiera sód
Rymphysia, 500 mg, proszek i rozpuszczalnik do sporządzania roztworu do infuzji:
- Lek zawiera 108 mg sodu (głównego składnika soli kuchennej) w każdej fiolce z 25 ml roztworu. Odpowiada to 5,4% maksymalnej zalecanej dobowej dawki sodu w diecie u osób dorosłych.
Rymphysia, 1000 mg, proszek i rozpuszczalnik do sporządzania roztworu do infuzji:
- Lek zawiera 216 mg sodu (głównego składnika soli kuchennej) w każdej fiolce z 50 ml roztworu. Odpowiada to 10,8% maksymalnej zalecanej dobowej dawki sodu w diecie u osób dorosłych.
3. Jak stosować lek Rymphysia
Lek Rymphysia jest podawany w infuzji dożylnej. Pierwsze infuzje leku będą nadzorowane przez
fachowy personel medyczny z doświadczeniem w leczeniu niedoboru inhibitora alfa1-proteinazy.
Leczenie w warunkach domowych i (lub) samodzielne podawanie przez pacjenta
Po przeprowadzeniu pierwszych infuzji lek Rymphysia może być podawany samodzielnie przez
pacjenta lub jego opiekuna, jednakże dopiero po przejściu odpowiedniego szkolenia. Jeżeli lekarz
uzna, że pacjent może stosować leczenie w warunkach domowych i (lub) samodzielnie podawać lek,
przeszkoli pacjenta lub opiekuna w następujących kwestiach:
- jak przygotować i podawać ten lek (patrz instrukcja na końcu tej ulotki),
- jak zachować lek w stanie jałowym (zasady przeprowadzania infuzji w warunkach aseptycznych),
- jak prowadzić dzienniczek leczenia,
- jak rozpoznawać działania niepożądane, w tym objawy reakcji alergicznych oraz środki, jakie należy zastosować w razie wystąpienia takich działań (patrz także punkt 2 i punkt 4).
Lekarz prowadzący lub inna osoba należąca do fachowego personelu medycznego będzie regularnie
kontrolować technikę podawania infuzji przez pacjenta i (lub) opiekuna pacjenta, aby upewnić się, że
lek jest zawsze prawidłowo przygotowywany i podawany.
Dawka
Dawka leku Rymphysia podawana pacjentowi zależy od jego masy ciała. Zalecana dawka to 60 mg na
kg masy ciała; dawka taka powinna być podawana raz na tydzień. Infuzja będzie trwać około
15-30 minut. Lekarz określi odpowiednią dawkę i szybkość podawania infuzji biorąc pod uwagę masę
ciała pacjenta oraz tolerancję infuzji.
Zastosowanie większej niż zalecana dawki leku Rymphysia
Jeśli pacjent uzna, że zastosował zbyt dużą dawkę leku Rymphysia, należy skontaktować się
z lekarzem lub inną osobą należącą do fachowego personelu medycznego, która podejmie decyzję na
temat odpowiedniego działania. Następstwa przedawkowania są nieznane.
Pominięcie zastosowania leku Rymphysia
W przypadku pominięcia infuzji należy natychmiast przyjąć kolejną dawkę i kontynuować podawanie
leku w regularnych odstępach zaleconych przez lekarza lub inną osobę należącą do fachowego
personelu medycznego.
Nie należy stosować dawki podwójnej w celu uzupełnienia pominiętej dawki.
Przerwanie stosowania leku Rymphysia
Nie należy przerywać stosowania tego leku bez konsultacji z lekarzem lub inną osobą należącą do
fachowego personelu medycznego. W razie przerwania leczenia lekiem Rymphysia stan pacjenta
może się pogorszyć.
4. Możliwe działania niepożądane
Jak każdy lek, lek ten może powodować działania niepożądane, chociaż nie u każdego one wystąpią.
Takie działania niepożądane mogą wystąpić nawet, jeśli pacjent otrzymywał uprzednio leki podobne
do Rymphysia i dobrze je tolerował. W przypadku tego leku mogą występować następujące działania
niepożądane:
Reakcje alergiczne
Należy natychmiast powiedzieć lekarzowi lub innej osobie należącej do fachowego personelu
medycznego, jeśli podczas podawania leku Rymphysia zauważy się którekolwiek z poniższych
ciężkich działań niepożądanych, gdyż pacjent może wymagać natychmiastowej pomocy medycznej:
- dreszcze lub uderzenia gorąca,
- szybsze bicie serca, spadek ciśnienia krwi lub odczuwanie oszołomienia,
- wysypka, pokrzywka lub swędzenie,
- trudności w oddychaniu lub przełykaniu, jak również obrzęk dłoni, twarzy lub jamy ustnej.
Należy natychmiast poinformować lekarza lub inną osobę należącą do fachowego personelu
medycznego, jeśli zauważy się którekolwiek z powyższych ciężkich działań niepożądanych.
Jeśli reakcja jest ciężka, lekarz lub inna osoba należąca do fachowego personelu medycznego może
zdecydować o zmniejszeniu szybkości lub całkowitym przerwaniu infuzji. Następnie może zastosować
odpowiednie leczenie objawów reakcji alergicznej.
W przypadku leczenia w warunkach domowych i (lub) samodzielnego podawania, należy natychmiast
przerwać infuzję i skontaktować się z lekarzem lub inną osobą należącą do fachowego personelu
medycznego.
- Reakcje alergiczne są niezbyt częstei mogą występować u nie więcej niż 1 na 100 pacjentów.
- Ciężkie reakcje alergiczne są bardzo rzadkiei mogą występować u nie więcej niż 1 na 10 000 pacjentów.
- Reakcje alergiczne mogą wystąpić nawet w sytuacji, gdy przy poprzednich infuzjach nie pojawiały się żadne objawy alergii.
Inne działania niepożądane
Należy natychmiast poinformować lekarza lub inną osobę należącą do fachowego personelu
medycznego, jeśli zauważy się którekolwiek z poniższych działań niepożądanych:
Bardzo często:mogą występować u więcej niż 1 na 10 pacjentów
- zapalenie oskrzeli (utrzymujący się kaszel, który może powodować produkcję śluzu, świszczący oddech, trudności z oddychaniem);
- zakażenie górnych dróg oddechowych (przeziębienie, choroba grypopodobna);
- ból głowy;
- kaszel;
- ból gardła (ból gardła i krtani);
Często:mogą występować u nie więcej niż 1 na 10 pacjentów
- zmienione odczuwanie smaków (zaburzenie smaku);
- dyskomfort w obrębie głowy, migrena;
- senność;
- zaburzenia oka (zapalenie spojówek, podrażnienie oczu i zaburzenia widzenia);
- katar (nieżyt nosa);
- podrażnienie gardła;
- wzdęcia, biegunka, owrzodzenia jamy ustnej, wymioty;
- ból lub dyskomfort w klatce piersiowej;
- gorączka i złe samopoczucie (choroba grypopodobna);
- ból i zasinienie w miejscu infuzji;
- uczucie dużego zmęczenia i senności;
- dyskomfort, ból lub bolesność mięśni (ból mięśniowy);
- ogólne uczucie dyskomfortu, choroby lub rozbicia - bez wyraźnej przyczyny (złe samopoczucie);
Częstość nieznana:częstość nie może być określona na podstawie dostępnych danych
- uczucie osłabienia;
- samopoczucie inne niż normalne;
- reakcja w miejscu infuzji, taka jak zasinienie, ból i wysypka;
Zgłaszanie działań niepożądanych
Jeśli wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie objawy niepożądane niewymienione
w tej ulotce, należy powiedzieć o tym lekarzowi lub innej osoby należącej do fachowego personelu
medycznego. Działania niepożądane można zgłaszać bezpośrednio do Departamentu Monitorowania
Niepożądanych Działań Produktów Leczniczych Urzędu Rejestracji Produktów Leczniczych,
Wyrobów Medycznych i Produktów Biobójczych
Al. Jerozolimskie 181C
02-222 Warszawa
Tel.: + 48 22 49 21 301
Faks: + 48 22 49 21 309
Strona internetowa: https://smz.ezdrowie.gov.pl
Działania niepożądane można zgłaszać również podmiotowi odpowiedzialnemu.
Dzięki zgłaszaniu działań niepożądanych można będzie zgromadzić więcej informacji na temat
bezpieczeństwa stosowania leku.
5. Jak przechowywać lek Rymphysia
Lek należy przechowywać w miejscu niewidocznym i niedostępnym dla dzieci.
Nie stosować tego leku po upływie terminu ważności zamieszczonego na pudełku zewnętrznym i na
etykiecie fiolek po „EXP”. Termin ważności oznacza ostatni dzień podanego miesiąca.
Nie przechowywać w temperaturze powyżej 25°C. Nie zamrażać. Przechowywać w oryginalnym
opakowaniu w celu ochrony przed światłem.
Po rekonstytucji, uzyskany roztwór należy zużyć natychmiast. Jeżeli nie jest to możliwe, roztwór
można przechowywać w temperaturze pokojowej (do 25°C) przez okres do 3 godzin. Nie wolno
zamrażać przygotowanego roztworu.
6. Zawartość opakowania i inne informacje
Co zawiera lek Rymphysia
- Substancją czynnąjest ludzki inhibitor alfa1-proteinazy. Jedna fiolka zawiera około 500 mg lub 1000 mg ludzkiego inhibitora alfa1-proteinazy.
- Pozostałe składnikito: sodu chlorek, sodu diwodorofosforan jednowodny i sodu wodorotlenek.
- Rozpuszczalnik: jałowa woda do wstrzykiwań.
Jak wygląda lek Rymphysia i co zawiera opakowanie
Proszek i rozpuszczalnik do sporządzania roztworu do infuzji.
Lek ten ma postać proszku w kolorze białym lub białawym do lekko żółto-zielonego lub żółtym.
Po rekonstytucji przy użyciu wody do wstrzykiwań roztwór powinien być przezroczysty, bezbarwny
lub lekko żółty do żółto-zielonego i nie powinien zawierać widocznych cząstek stałych.
Jedno opakowanie zawiera:
Rymphysia, 500 mg, proszek i rozpuszczalnik do sporządzania roztworu do infuzji:
- Jedną fiolkę z proszkiem Rymphysia 500 mg
- Jedną fiolkę z rozpuszczalnikiem z 25 ml jałowej wody do wstrzykiwań
- Jedną jałową dwustronną igłę do przenoszenia
- Jeden jałowy filtr o średnicy porów 20 mikronów
Rymphysia, 1000 mg, proszek i rozpuszczalnik do sporządzania roztworu do infuzji:
- Jedną fiolkę z proszkiem Rymphysia 1000 mg
- Jedną fiolkę z rozpuszczalnikiem z 50 ml jałowej wody do wstrzykiwań
- Jedną jałową dwustronną igłę do przenoszenia
- Jeden jałowy filtr o średnicy porów 20 mikronów
Podmiot odpowiedzialny
Takeda Pharma Sp. z o.o.
ul. Prosta 68
00-838 Warszawa
Tel.: +48 22 306 24 47
[email protected]
Wytwórca
Takeda Manufacturing Austria AG
Industriestrasse 67
1221 Wiedeń
Austria
Ten produkt leczniczy jest dopuszczony do obrotu w krajach członkowskich Europejskiego
Obszaru Gospodarczego pod następującymi nazwami:
Austria, Belgia, Czechy, Dania, Finlandia, Francja, Niemcy, Włochy, Łotwa, Luksemburg, Norwegia,
Polska, Portugalia, Rumunia, Hiszpania, Szwecja: Rymphysia
Data ostatniej aktualizacji ulotki: 02/2023.
Informacje przeznaczone dla fachowego personelu medycznego oraz przeszkolonych opiekunów i (lub) pacjentów:
Ogólne instrukcje
- Lek Rymphysia jest przeznaczony wyłącznie do stosowania dożylnego.
- Rekonstytucję, podawanie i wszelkie czynności z produktem należy przeprowadzać z ostrożnością i zachowaniem zasad aseptyki, aby zachować jałowość produktu.
- Przed rekonstytucją pozostawić lek Rymphysia i rozpuszczalnik, aby osiągnęły temperaturę pokojową.
- Lek Rymphysia po rekonstytucji należy przechowywać w temperaturze pokojowej i podać w ciągu trzech (3) godzin od rekonstytucji. Fiolki zużyte częściowo należy wyrzucić i nie pozostawiać do użycia w przyszłości. Roztwór nie zawiera żadnego środka konserwującego.
- Wszelkie niewykorzystane resztki produktu leczniczego lub jego odpady należy usunąć zgodnie z lokalnymi przepisami.
Rekonstytucja
- 1. Zdjąć wieczka z fiolek z rozpuszczalnikiem i produktem.
- 2. Przetrzeć odsłonięte powierzchnie korków alkoholem.
- 3. Zdjąć osłonę z jednego końca dwustronnej igły do przenoszenia. Wprowadzić odsłonięty koniec igły przez środek korka fiolki z rozpuszczalnikiem.
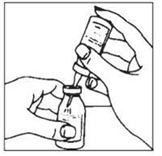
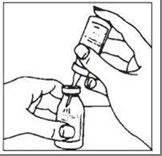
- 4. Zdjąć plastikową osłonę z drugiego końca dwustronnej igły do przenoszenia, która jest osadzona w korku fiolki z rozpuszczalnikiem. Aby zmniejszyć pienienie, należy odwrócić fiolkę z rozpuszczalnikiem i wprowadzić odsłonięty koniec igły przez środek korka fiolki z produktem pod kątem, upewniając się, że fiolka z rozpuszczalnikiem znajduje się zawsze powyżej fiolki z produktem. Wprowadzenie pod kątem powoduje skierowanie strumienia rozpuszczalnika na ściankę fiolki z produktem. Patrz: rysunek poniżej. Podciśnienie w fiolce jest wystarczające do przeniesienia całego rozpuszczalnika.
- 5. Rozłączyć obie fiolki, zdejmując fiolkę z rozpuszczalnikiem z igły do przenoszenia. Dzięki temu jakiekolwiek niskie ciśnienie powstałe w fiolce z produktem zostanie wyrównane. Następnie wyjąć dwustronną igłę do przenoszenia z fiolki z produktem i wyrzucić igłę do odpowiednio zabezpieczonego pojemnika.
- 6. Postawić fiolkę i pozostawić do czasu, aż większość zawartości znajdzie się w roztworze, następnie DELIKATNIE obracać fiolką do całkowitego rozpuszczenia proszku. Rekonstytucja trwa nie dłużej niż pięć (5) minut w przypadku fiolki z 500 mg i nie dłużej niż dziesięć (10) minut w przypadku fiolki z 1000 mg. Uwaga: Nie wstrząsać zawartością fiolki. Fiolki nie należy odwracać do czasu, gdy wszystko będzie przygotowane w celu pobrania zawartości.
- 7. Produkt po rekonstytucji jest bezbarwny lub lekko żółty do żółto-zielonego.
- 8. Sporadycznie w produkcie po rekonstytucji może zostać kilka niewielkich widocznych cząstek. Zostaną one usunięte przez jałowy filtr o średnicy porów 20 mikronów dostarczony z produktem.
Podawanie
- 1. Przed podaniem sprawdzić produkt po rekonstytucji pod względem obecności cząstek stałych i przebarwień.
- 2. Zawartość kilku fiolek można przenieść do pustego, jałowego pojemnika na roztwory dożylne. W tym celu należy stosować technikę aseptyczną i jałową igłę, która nie jest dostarczana z produktem.
- 3. Aby zmniejszyć ryzyko rozwoju szkodliwych drobnoustrojów, lek Rymphysia należy podać w ciągu trzech (3) godzin od rekonstytucji. Niezużytą zawartość należy wyrzucić.
- 4. Lek Rymphysia należy podawać oddzielnie, nie mieszając go z żadnymi innymi środkami ani roztworami rozcieńczającymi.
Szybkość podawania infuzji
- Zalecana szybkość podawania infuzji wynosi 0,08 ml/kg masy ciała na minutę. Szybkość podawania infuzji można dostosować w zależności od odpowiedzi klinicznej i tolerancji przez pacjenta, jednak nie powinna przekraczać 0,2 ml/kg masy ciała na minutę.
- W razie wystąpienia działań niepożądanych należy zmniejszyć szybkość podawania infuzji albo zatrzymać infuzję. Po ustaniu objawów wznowić infuzję z szybkością tolerowaną przez pacjenta.
- Kraj rejestracji
- Substancja czynna
- Wymaga receptyTak
- Producent
- ImporterTakeda Manufacturing Austria AG
- Te informacje mają charakter wyłącznie poglądowy i nie stanowią porady medycznej. Przed zastosowaniem jakiegokolwiek leku zawsze skonsultuj się z lekarzem. Oladoctor nie ponosi odpowiedzialności za decyzje medyczne podjęte na podstawie tych treści.
- Zamienniki RymphysiaPostać farmaceutyczna: Proszek, 500 mgSubstancja czynna: alfa1 antitrypsinProducent: Takeda Manufacturing Austria AGWymaga receptyPostać farmaceutyczna: Roztwór, 277,8 j. Ph. Eur. (500 000 KIU)Substancja czynna: aprotininBez receptyPostać farmaceutyczna: Tabletki, 500 mgSubstancja czynna: tranexamic acidWymaga recepty
Odpowiedniki Rymphysia w innych krajach
Najlepsze odpowiedniki z tą samą substancją czynną i działaniem terapeutycznym.
Odpowiednik Rymphysia – Hiszpania
Odpowiednik Rymphysia – Ukraina
Lekarze online w sprawie Rymphysia
Konsultacja w sprawie dawkowania, działań niepożądanych, interakcji, przeciwwskazań i odnowienia recepty na Rymphysia – decyzja należy do lekarza, zgodnie z lokalnymi przepisami.














