
Maxitrol

Zapytaj lekarza o receptę na Maxitrol

Jak stosować Maxitrol
Ulotka dołączona do opakowania: informacja dla pacjenta
Uwaga! Należy zachować ulotkę. Informacja na opakowaniu bezpośrednim w obcym języku.
Maxitrol (Maxidrol)
(1 mg + 3500 j.m. + 6000 j.m.)/ml, krople do oczu
Dexamethasonum + Neomycini sulfas + Polymyxini B sulfas
Maxitrol i Maxidrol są różnymi nazwami handlowymi tego samego leku.
Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje ważne dla pacjenta.
- Należy zachować tę ulotkę, aby w razie potrzeby móc ją ponownie przeczytać.
- W razie jakichkolwiek wątpliwości należy zwrócić się do lekarza, farmaceuty lub pielęgniarki.
- Lek ten przepisano ściśle określonej osobie. Nie należy go przekazywać innym. Lek może zaszkodzić innej osobie, nawet jeśli objawy jej choroby są takie same.
- Jeśli u pacjenta wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie objawy niepożądane niewymienione w tej ulotce, należy powiedzieć o tym lekarzowi, farmaceucie lub pielęgniarce. Patrz punkt 4.
Spis treści ulotki:
- 1. Co to jest lek Maxitrol i w jakim celu się go stosuje
- 2. Informacje ważne przed zastosowaniem leku Maxitrol
- 3. Jak stosować lek Maxitrol
- 4. Możliwe działania niepożądane
- 5. Jak przechowywać lek Maxitrol
- 6. Zawartość opakowania i inne informacje
1. Co to jest lek Maxitrol i w jakim celu się go stosuje
Lek Maxitrol stosuje się do leczenia chorób zapalnych oczu, którym może towarzyszyć zakażenie.
Stan zapalny oka może być spowodowany zakażeniem lub innymi czynnikami wnikającymi do oka
lub urazami oka.
Lek Maxitrol jest lekiem złożonym zawierającym składniki przeciwbakteryjne i kortykosteroid.
Kortykosteroidy (w tym przypadku deksametazon) są stosowane w zapobieganiu i zmniejszaniu stanów
zapalnych oka. Leki przeciwbakteryjne zawarte w kroplach (w tym przypadku neomycyny siarczan i
polimyksyny B siarczan) są aktywne wobec większości bakterii chorobotwórczych powodujących
zakażenia oka.
2. Informacje ważne przed zastosowaniem leku Maxitrol
Kiedy nie stosować leku Maxitrol
- jeśli pacjent ma uczuleniena neomycyny siarczan, polimyksyny B siarczan, deksametazon lub na którykolwiek z pozostałych składników tego leku (wymienionych w punkcie 6),
- jeśli u pacjenta występuje:
- opryszczkowe zapalenie rogówki, krowianka, ospa wietrzna lub jakiekolwiek inne wirusowe zakażenie oka,
- grzybicze zakażenie oka,
- nieleczone zakażenia pasożytnicze oka,
- prątkowe zakażenie oka,
Strona 1 z 6
- nieleczone ropne zakażenie oka.
Ostrzeżenia i środki ostrożności
Do stosowania wyłącznie do oczu.
- U niektórych pacjentów może wystąpić nadwrażliwość na stosowane miejscowo antybiotyki aminoglikozydowe, jak neomycyna. W przypadku wystąpienia objawów nadwrażliwości, należy zaprzestać stosowania leku i niezwłocznie skontaktować się z lekarzem (patrz pkt. 4). Reakcje nadwrażliwości mogą występować w postaci miejscowego świądu lub zaczerwienienia skóry ciężkich reakcji uczuleniowych (reakcji anafilaktycznej) lub ciężkich reakcji skórnych. Takie reakcje skórne mogą wystąpić w czasie stosowania innych miejscowych lub układowych antybiotyków z tej samej rodziny (aminoglikozydów).
- Dodatkowo, miejscowe stosowanie neomycyny może prowadzić do wystąpienia zaczerwienienia, podrażnienia i uczucia dyskomfortu skóry.
- U pacjentów, u których wystąpiły objawy nadwrażliwości na stosowaną miejscowo neomycynę może też wystąpić nadwrażliwość na inne antybiotyki.
- Jeśli w czasie leczenia lekiem Maxitrol pacjent stosuje inne antybiotyki, powinien zasięgnąć porady lekarza, gdyż jednoczesne stosowanie leku Maxitrol z innymi antybiotykami może powodować poważne działania niepożądane.
- U pacjentów stosujących długotrwale kortykosteroidy do oczu może występować:
- podwyższone ciśnienie oczne. Należy regularnie kontrolować ciśnienie w oku w czasie stosowania tego leku. Jest to szczególnie ważne u pacjentów pediatrycznych, ponieważ spowodowane przez kortykosteroidy podwyższenie ciśnienia ocznego może być u dzieci większe i występować wcześniej niż u dorosłych. Należy poprosić lekarza o poradę szczególnie w przypadku dzieci. Ryzyko podwyższenia ciśnienia ocznego i (lub) zaćmy jest też wyższe u pacjentów predysponowanych (np. chorych na cukrzycę).
- rozwój zespołu Cushinga spowodowanego przez lek dostający się do krwi. Należy zwrócić się do lekarza, jeśli u pacjenta wystąpi obrzęk oraz zwiększenie masy ciała, widoczne szczególnie na tułowiu i twarzy, ponieważ są to zazwyczaj pierwsze objawy choroby nazywanej zespołem Cushinga. Zahamowanie czynności nadnerczy może wystąpić w wyniku przerwania długotrwałego lub intensywnego stosowania leku Maxitrol. Należy zwrócić się do lekarza, zanim pacjent zdecyduje o przerwaniu leczenia. Ryzyko to jest szczególnie istotne u dzieci oraz u pacjentów leczonych rytonawirem lub kobicystatem.
- W przypadku wystąpienia lub nasilenia się objawów infekcji oka należy natychmiast skontaktować się z lekarzem. Pacjenci stosujący lek Maxitrol mogą mieć zmniejszoną odporność na infekcje oczu, w tym zakażenia bakteryjne i grzybicze odporne na leczenie antybiotykami.
- U pacjentów stosujących jednocześnie kortykosteroidy i niesteroidowe leki przeciwzapalne mogą wystąpić problemy z gojeniem się uszkodzeń powierzchni oka.
- Jeśli u pacjenta występują choroby prowadzące do ścieńczenia rogówki lub twardówki powinien powiedzieć o tym lekarzowi.
Jeśli u pacjenta wystąpi nieostre widzenie lub inne zaburzenia widzenia, należy skontaktować się z
lekarzem.
Jeśli pacjent choruje na jaskrę, czas leczenia powinien być ograniczony do dwóch tygodni, o ile lekarz nie
zaleci inaczej.
Lek należy stosować tak długo, jak zalecił to lekarz. Jeżeli objawy choroby nasilą się lub nie ustępują,
należy skonsultować się z lekarzem.
Dzieci
Nie udokumentowano bezpieczeństwa stosowania i skuteczności leku Maxitrol u dzieci, dlatego nie zaleca
się stosowania w tej grupie wiekowej.
Strona 2 z 6
Lek Maxitrol a inne leki
Należy powiedzieć lekarzowi lub farmaceucie o wszystkich lekach stosowanych przez pacjenta obecnie
lub ostatnio, a także o lekach, które pacjent planuje stosować, w tym o lekach wydawanych bez recepty.
Należy szczególnie poinformować lekarza, jeśli pacjent przyjmuje:
- miejscowo działające niesteroidowe leki przeciwzapalne. Jednoczesne miejscowe stosowanie leku steroidowego oraz niesteroidowego leku przeciwzapalnego może powodować wystąpienie problemów z gojeniem się zranień oka;
- rytonawir lub kobicystat, ponieważ mogą one zwiększać zawartość deksametazonu we krwi. Jeśli pacjent stosuje jednocześnie inne krople lub maści podawane do oczu, należy zachować co najmniej 5 minut przerwy pomiędzy podaniami kolejnych leków. Maści do oczu należy stosować na końcu.
Ciąża, karmienie piersią i wpływ na płodność
Jeśli pacjentka jest w ciąży lub karmi piersią, przypuszcza, że może być w ciąży lub gdy planuje mieć
dziecko, powinna poradzić się lekarza lub farmaceuty przed zastosowaniem tego leku.
Lek nie jest zalecany w czasie ciąży lub karmienia piersią.
Prowadzenie pojazdów i obsługiwanie maszyn
Lek Maxitrol nie ma wpływu lub wywiera niewielki wpływ na zdolność prowadzenia pojazdów
i obsługiwania maszyn.
Przez pewien czas po podaniu leku Maxitrol widzenie może być niewyraźne. Nie należy prowadzić
pojazdów ani obsługiwać maszyn do czasu ustąpienia tego objawu.
Lek Maxitrol krople do oczu zawiera benzalkoniowy chlorek
Lek zawiera 0,04 mg benzalkoniowego chlorku w każdym mililitrze (0,04 mg/ml).
Benzalkoniowy chlorek może być absorbowany przez miękkie soczewki kontaktowe i zmieniać ich
zabarwienie. Należy usunąć soczewki kontaktowe przed zakropleniem i odczekać co najmniej 15 minut
przed ponownym założeniem.
Benzalkoniowy chlorek może powodować także podrażnienie oczu, zwłaszcza u osób z zespołem suchego
oka lub zaburzeniami dotyczącymi rogówki (przezroczystej warstwy z przodu oka). W razie wystąpienia
nieprawidłowych odczuć w obrębie oka, kłucia lub bólu w oku po zastosowaniu leku, należy
skontaktować się z lekarzem.
3. Jak stosować lek Maxitrol
Lek Maxitrol należy zawsze stosować zgodnie z zaleceniami lekarza. W razie wątpliwości należy zwrócić
się do lekarza lub farmaceuty.
Lek Maxitrol przeznaczony jest wyłączniedo zakraplania oczu; z jednego opakowania leku powinien
korzystać tylkojeden pacjent.
Jeśli po zdjęciu zakrętki kołnierz zabezpieczający jest poluzowany, należy go usunąć przed
zastosowaniem leku.
Zaleca się zamknięcie powieki i jednoczesne delikatne uciśnięcie palcem przewodu nosowo-łzowego
(kanału łzowego). Dzięki temu można zmniejszyć przedostawanie się do krwi leku po zastosowaniu w
postaci kropli do oczu.
Zalecana dawka
W chorobach o łagodnym przebiegu stosuje się jedną do dwóch kropli do worka (worków) spojówkowego
(spojówkowych) do czterech – sześciu razy na dobę.
Strona 3 z 6
W ciężkich przypadkach stosuje się jedną do dwóch kropli, co godzinę. Stopniowo lek stosuje się w coraz
mniejszej dawce a po ustąpieniu objawów zapalenia przerywa się jego stosowanie.
Lekarz określi czas stosowania leku. Nie należy przedwcześnie przerywać leczenia.
- 1. Przygotować butelkę z lekiem Maxitrol i lustro.
- 2. Umyć ręce.
- 3. Wstrząsnąć butelkę.
- 4. Odkręcić zakrętkę.
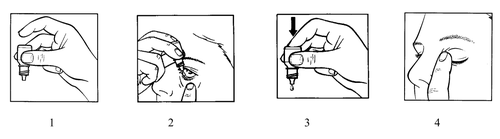
- 5. Wziąć butelkę do ręki i skierować ją do góry dnem, trzymając kciukiem i palcem środkowym (rycina 1).
- 6. Odchylić głowę do tyłu. Powiekę dolną odchylić czystym palcem ku dołowi, tak aby utworzyła się „kieszonka” pomiędzy powieką i gałką oczną; do niej powinna trafić kropla (rycina 2).
- 7. Przybliżyć końcówkę butelki do oka. Dla ułatwienia można posłużyć się lustrem.
- 8.
Nie dotykać końcówką zakraplacza oka, powieki, okolic oka ani innych powierzchni.
Nieprzestrzeganie tego zalecenia może spowodować zakażenie kropli.
- 9. Lekko nacisnąć dno butelki, aby spowodować wypłynięcie pojedynczej kropli leku Maxitrol (rycina 3).
- 10. Po zakropleniu leku Maxitrol zdjąć palec, którym trzymało się dolną powiekę. Zamknąć oko i ucisnąć palcem kącik oka w okolicy nosa (rycina 4). Pomoże to zapobiec przedostawaniu się leku do całego organizmu.
- 11. Jeżeli konieczne jest podawanie kropli do obu oczu, należy powtórzyć czynności wymienione powyżej w stosunku do drugiego oka.
- 12. Bezpośrednio po użyciu leku zakręcić butelkę.
- 13. W tym samym czasie należy korzystać z jednej butelki z lekiem.
Jeżeli kropla nie trafi do okanależy powtórzyć próbę prawidłowego zakroplenia.
Zastosowanie większej niż zalecana dawki leku Maxitrol
W razie miejscowego przedawkowania leku Maxitrol należy przepłukać oko (oczy) letnią wodą.
Nie należy stosować kropli do czasu planowego przyjęcia kolejnej dawki.
Pominięcie zastosowania leku Maxitrol
W przypadku pominięcia dawki leku należy przyjąć kolejną planową dawkę. Jeśli jednak do przyjęcia
kolejnej dawki leku pozostało niewiele czasu, pominiętą dawkę należy opuścić i powrócić do normalnego
schematu podawania. Nie należyprzyjmować dawki podwójnej w celu uzupełnienia pominiętej dawki.
W razie jakichkolwiek dalszych wątpliwości związanych ze stosowaniem tego leku należy zwrócić się do
lekarza lub farmaceuty.
4. Możliwe działania niepożądane
Jak każdy lek, lek ten może spowodować działania niepożądane, chociaż nie u każdego one wystąpią.
Strona 4 z 6
Jeśli u pacjenta wystąpią reakcje alergiczne, w tym wysypka, obrzęk twarzy, warg, języka i
(lub) gardła, co może powodować trudności w oddychaniu lub połykaniu, lub wystąpią inne ciężkie
działania niepożądane, należy przerwać stosowanie leku Maxitrol i natychmiast skontaktować się z
lekarzem lub Oddziałem Ratunkowym najbliższego szpitala.
W czasie stosowania leku Maxitrol obserwowano występowanie następujących działań niepożądanych:
Niezbyt często( może wystąpić nie częściej niż u 1 na 1000 pacjentów): zapalenie rogówki, zwiększenie
ciśnienia wewnątrzgałkowego, świąd oka, uczucie dyskomfortu w oku, podrażnienie oka.
Częstość nieznana( częstość nie może być określona na podstawie dostępnych danych): nadwrażliwość,
ból głowy, wrzodziejące zapalenie rogówki, niewyraźne widzenie, nadwrażliwość na światło,
powiększenie źrenicy, opadanie powieki, ból oka, obrzęk oka, uczucie ciała obcego w oku, przekrwienie
oka, nasilone łzawienie, ciężkie reakcje skórne (zespół Stevensa-Johnsona), nieostre widzenie, nasilony
wzrost owłosienia na ciele (szczególnie u kobiet), osłabienie mięśni oraz utrata masy mięśniowej,
fioletowe rozstępy na skórze, zwiększone ciśnienie krwi, nieregularne miesiączki lub brak miesiączki,
zmiany ilości białka i wapnia w organizmie, zahamowanie wzrostu u dzieci i młodzieży oraz obrzęk i
zwiększenie masy ciała, widoczne szczególnie na tułowiu i twarzy (choroba nazywana zespołem
Cushinga) (patrz punkt 2 „Ostrzeżenia i środki ostrożności”).
Zgłaszanie działań niepożądanych
Jeśli wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie objawy niepożądane niewymienione
w ulotce, należy powiedzieć o tym lekarzowi, farmaceucie lub pielęgniarce. Działania niepożądane można
zgłaszać bezpośrednio do Departamentu Monitorowania Niepożądanych Działań Produktów Leczniczych
Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych,
Al. Jerozolimskie 181C, 02-222 Warszawa, tel.: + 48 22 49 21 301, faks: + 48 22 49 21 309, strona
internetowa: https://smz.ezdrowie.gov.pl
Dzięki zgłaszaniu działań niepożądanych można będzie zgromadzić więcej informacji na temat
bezpieczeństwa stosowania leku.
W przypadku nasilenia się któregokolwiek z objawów lub w przypadku wystąpienia innych objawów
niepożądanych, niewymienionych w tej ulotce, należy poinformować o nich lekarza.
5. Jak przechowywać lek Maxitrol
Aby uniknąć zakażenia kropli butelkę należy wyrzucić po upływie 15 dni od pierwszego otwarcia.
Datę otwarcia butelki należy zapisać w miejscu zaznaczonym poniżej.
Data pierwszego otwarcia:……….
Lek należy przechowywać w miejscu niewidocznym i niedostępnym dla dzieci.
Nie przechowywać w temperaturze powyżej 25℃. Nie przechowywać w lodówce.
Przechowywać butelkę w pozycji pionowej.
Przechowywać opakowanie szczelnie zamknięte.
Nie należy stosować tego leku po upływie terminu ważności zamieszczonego na opakowaniu.
Termin ważności oznacza ostatni dzień podanego miesiąca.
Leków nie należy wyrzucać do kanalizacji ani domowych pojemników na odpadki. Należy zapytać
farmaceutę, jak usunąć leki, których się już nie używa. Takie postępowanie pomoże chronić środowisko.
Strona 5 z 6
6. Zawartość opakowania i inne informacje
Co zawiera lek Maxitrol
Substancjami czynnymi leku są:
Deksametazon 1 mg/ml
Neomycyny siarczan 3500 j.m./ml
Polimyksyny B siarczan 6000 j.m./ml
Substancje pomocnicze to:
sodu chlorek, polisorbat 20, benzalkoniowy chlorek, hypromeloza, woda oczyszczona.
Do leku dodaje się minimalne ilości kwasu solnego rozcieńczonego i (lub) sodu wodorotlenku w celu
utrzymania w normie jego kwasowości (wartości pH).
Jak wygląda lek i co zawiera opakowanie
Lek Maxitrol krople do oczu ma postać nieprzezroczystych kropli w kolorze od białego do jasnożółtego.
Dostępny jest w butelce z PE o pojemności 3 ml, w tekturowym pudełku
W celu uzyskania bardziej szczegółowych informacji należy zwrócić się do podmiotu odpowiedzialnego
lub importera równoległego.
Podmiot odpowiedzialny we Francji, kraju eksportu:
Novartis Pharma S.A.S., 8-10, rue Henri Sainte-Claire Deville, 92500 Rueil-Malmaison, Francja
Wytwórca:
Siegfried El Masnou, S.A., Camil Fabra, 58, 08320 El Masnou, Barcelona, Hiszpania
S.A. ALCON-COUVREUR N.V., Rijksweg 14, 2870 Puurs, Belgia
Novartis Pharma GmbH, Roonstrasse 25, 90429 Nuremberg, Niemcy
Novartis Farmaceutica, S.A., Gran Via de les Corts Catalanes, 764, 08013 Barcelona, Hiszpania
Importer równoległy:
Delfarma Sp. z o.o., ul. Św. Teresy od Dzieciątka Jezus 111, 91-222 Łódź
Przepakowano w:
Delfarma Sp. z o.o., ul. Św. Teresy od Dzieciątka Jezus 111, 91-222 Łódź
Nr pozwolenia we Francji, kraju eksportu: 34009 306 525 3 4
Nr pozwolenia na import równoległy: 184/22 Data zatwierdzenia ulotki:29.04.2022 r.
[Informacja o zastrzeżonym znaku towarowym]
Strona 6 z 6
- Kraj rejestracji
- Substancja czynna
- Wymaga receptyTak
- Podmiot odpowiedzialny (MAH)Novartis Pharma S.A.S.
- Te informacje mają charakter wyłącznie poglądowy i nie stanowią porady medycznej. Przed zastosowaniem jakiegokolwiek leku zawsze skonsultuj się z lekarzem. Oladoctor nie ponosi odpowiedzialności za decyzje medyczne podjęte na podstawie tych treści.
- Zamienniki MaxitrolPostać farmaceutyczna: Krople, (3 mg + 1 mg)/mlSubstancja czynna: dexamethasone and antiinfectivesProducent: Rafarm S.A.Wymaga receptyPostać farmaceutyczna: Krople, (5 mg + 1 mg)/mlSubstancja czynna: dexamethasone and antiinfectivesProducent: Dr. Gerhard Mann Chem. - Pharm. Fabrik GmbHWymaga receptyPostać farmaceutyczna: Maść, (5 mg + 0,3 mg)/gSubstancja czynna: dexamethasone and antiinfectivesProducent: Dr. Gerhard Mann Chem. - Pharm. Fabrik GmbHWymaga recepty
Odpowiedniki Maxitrol w innych krajach
Najlepsze odpowiedniki z tą samą substancją czynną i działaniem terapeutycznym.
Odpowiednik Maxitrol – Украина
Odpowiednik Maxitrol – Испания
Lekarze online w sprawie Maxitrol
Konsultacja w sprawie dawkowania, działań niepożądanych, interakcji, przeciwwskazań i odnowienia recepty na Maxitrol – decyzja należy do lekarza, zgodnie z lokalnymi przepisami.














