
Icatibant Fresenius

Zapytaj lekarza o receptę na Icatibant Fresenius

Jak stosować Icatibant Fresenius
Ulotka dołączona do opakowania: informacja dla użytkownika
Icatibant Fresenius, 30 mg, roztwór do wstrzykiwań w ampułko-strzykawce
Icatibantum
Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje ważne dla pacjenta.
- Należy zachować tę ulotkę, aby w razie potrzeby móc ją ponownie przeczytać.
- W razie jakichkolwiek wątpliwości należy zwrócić się do lekarza lub farmaceuty.
- Lek ten przepisano ściśle określonej osobie. Nie należy go przekazywać innym. Lek może zaszkodzić innej osobie, nawet jeśli objawy jej choroby są takie same.
- Jeśli u pacjenta wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie objawy niepożądane niewymienione w tej ulotce, należy powiedzieć o tym lekarzowi lub farmaceucie. Patrz punkt 4.
Spis treści ulotki
- 1. Co to jest Icatibant Fresenius i w jakim celu się go stosuje
- 2. Informacje ważne przed zastosowaniem leku Icatibant Fresenius
- 3. Jak stosować Icatibant Fresenius
- 4. Możliwe działania niepożądane
- 5. Jak przechowywać Icatibant Fresenius
- 6. Zawartość opakowania i inne informacje
1. Co to jest Icatibant Fresenius i w jakim celu się go stosuje
Icatibant Fresenius zawiera substancję czynną ikatybant.
Icatibant Fresenius jest przeznaczony do leczenia objawów dziedzicznego obrzęku
naczynioruchowego (HAE, ang. Hereditary Angioedema) u pacjentów dorosłych oraz młodzieży
i dzieci w wieku 2 lat i starszych.
W przebiegu HAE dochodzi do zwiększenia stężenia we krwi substancji o nazwie bradykinina, co
prowadzi do wystąpienia objawów takich jak obrzęk, ból, nudności i biegunka.
Icatibant Fresenius blokuje aktywność bradykininy, w związku z czym przerywa rozwój objawów
napadu HAE.
2. Informacje ważne przed zastosowaniem leku Icatibant Fresenius
Kiedy nie stosować leku Icatibant Fresenius:
- jeśli pacjent ma uczulenie na ikatybant lub którykolwiek z pozostałych składników tego leku (wymienionych w punkcie 6).
Ostrzeżenia i środki ostrożności
Przed rozpoczęciem stosowania leku Icatibant Fresenius należy omówić to z lekarzem:
- jeśli u pacjenta występuje dusznica bolesna (zmniejszony dopływ krwi do mięśnia sercowego);
- jeśli u pacjenta niedawno wystąpił udar.
Niektóre z działań niepożądanych związanych ze stosowaniem leku Icatibant Fresenius są podobne do
objawów choroby.
W przypadku zauważenia nasilenia objawów napadu po otrzymaniu leku Icatibant Fresenius, należy
natychmiast powiadomić lekarza.
Ponadto:
- Przed samodzielnym wstrzyknięciem leku Icatibant Fresenius lub przed podaniem leku Icatibant Fresenius przez opiekuna, pacjent lub opiekun powinien być przeszkolony w wykonywaniu wstrzyknięć podskórnych.
- Pacjent z napadem w obrębie krtani (niedrożność górnych dróg oddechowych), który sam wstrzykuje sobie Icatibant Fresenius lub któremu opiekun wstrzykuje Icatibant Fresenius, powinien niezwłocznie zgłosić się po pomoc lekarską do fachowej placówki medycznej.
- Jeśli po jednorazowym samodzielnym wstrzyknięciu leku Icatibant Fresenius lub jednorazowym podaniu leku Icatibant Fresenius przez opiekuna objawy nie ustąpiły, pacjent powinien zgłosić się lub opiekun powinien zgłosić pacjenta do lekarza celem wykonania następnego wstrzyknięcia leku Icatibant Fresenius. Dorosłym pacjentom nie należy podawać więcej niż dwa dodatkowe wstrzyknięcia w ciągu 24 godzin.
Dzieci i młodzież
Nie zaleca się stosowania leku Icatibant Fresenius u dzieci w wieku poniżej 2 lat lub ważących mniej
niż 12 kg, ponieważ nie przebadano go w tej grupie wiekowej.
Icatibant Fresenius a inne leki
Należy powiedzieć lekarzowi o wszystkich lekach stosowanych przez pacjenta obecnie lub ostatnio,
a także o lekach, które pacjent planuje stosować.
Nie są znane interakcje leku Icatibant Fresenius z innymi lekami. Jeżeli pacjent stosuje lek określany
jako inhibitor konwertazy (inhibitor ACE) (np. kaptopril, enalapril, ramipril, chinapril, lizynopril),
w celu obniżenia ciśnienia tętniczego lub z jakiegokolwiek innego powodu, przed zastosowaniem leku
Icatibant Fresenius należy poinformować o tym lekarza.
Ciąża i karmienie piersią
Jeśli pacjentka jest w ciąży lub karmi piersią, przypuszcza, że może być w ciąży, lub gdy planuje mieć
dziecko, powinna poradzić się lekarza przed rozpoczęciem stosowania tego leku.
Pacjentka nie powinna karmić piersią przez 12 godzin po zastosowaniu leku Icatibant Fresenius.
Prowadzenie pojazdów i obsługiwanie maszyn
Nie należy prowadzić pojazdów ani obsługiwać maszyn, jeśli u pacjenta występuje uczucie zmęczenia
lub zawroty głowy w wyniku napadu HAE lub po zastosowaniu leku Icatibant Fresenius.
Icatibant Fresenius zawiera sód
Lek zawiera mniej niż 1 mmol (23 mg) sodu na dawkę, to znaczy lek uznaje się za „wolny od sodu”.
3. Jak stosować Icatibant Fresenius
Ten lek należy zawsze stosować zgodnie z zaleceniami lekarza. W razie wątpliwości należy zwrócić
się do lekarza.
Jeśli pacjent otrzymuje Icatibant Fresenius po raz pierwszy, pierwszą dawkę leku zawsze podaje
lekarz lub pielęgniarka. Lekarz powie pacjentowi, kiedy może on bezpiecznie wrócić do domu. Po
rozmowie z lekarzem lub pielęgniarką i przeszkoleniu w wykonywaniu wstrzyknięć podskórnych,
pacjent może sam wstrzykiwać sobie Icatibant Fresenius lub opiekun może wstrzykiwać pacjentowi
Icatibant Fresenius, jeśli u pacjenta wystąpi napad dziedzicznego obrzęku naczynioruchowego (HAE).
Ważne jest wstrzyknięcie podskórne leku Icatibant Fresenius jak najszybciej po zauważeniu napadu
obrzęku naczynioruchowego. Lekarz prowadzący nauczy pacjenta i jego opiekuna, jak bezpiecznie
wstrzykiwać Icatibant Fresenius, zgodnie z instrukcjami podanymi w ulotce dla pacjenta.
Kiedy i jak często należy stosować Icatibant Fresenius
Lekarz określi dokładną dawkę leku Icatibant Fresenius i powie pacjentowi, jak często należy go
stosować.
Dorośli
- Zalecana dawka leku Icatibant Fresenius to jedno wstrzyknięcie (3 ml, 30 mg), podawane podskórnie niezwłocznie po zauważeniu napadu obrzęku naczynioruchowego (np. nasilony obrzęk skóry, szczególnie w obrębie twarzy i szyi, nasilenie bólu brzucha).
- Jeżeli po 6 godzinach objawy nie ustąpią, należy zwrócić się do lekarza w celu wykonania następnego wstrzyknięcia leku Icatibant Fresenius. Dorosłym pacjentom nie należy podawać więcej niż dwa dodatkowe wstrzyknięcia w ciągu 24 godzin.
- Nie należy przyjmować więcej niż 3 wstrzyknięcia w ciągu 24 godzin. Jeśli pacjent wymagawięcej niż 8 wstrzyknięć w miesiącu, należy skontaktować się z lekarzem.
Dzieci i młodzież w wieku od 2 do 17 lat
- Zalecana dawka leku Icatibant Fresenius to jedno wstrzyknięcie 1 ml do maksymalnie 3 ml, w zależności od masy ciała, podawane podskórnie niezwłocznie po zauważeniu objawów napadu obrzęku naczynioruchowego (np. nasilony obrzęk skóry, szczególnie w obrębie twarzy i szyi, nasilenie bólu brzucha).
- Więcej informacji dotyczących podawania dawki, patrz „Szczegółowa instrukcja wstrzykiwania”.
- Jeżeli pacjent nie wie, jaką dawkę podać, należy zwrócić się do lekarza, farmaceuty lub pielęgniarki.
- Jeśli objawy nasilą się lub nie ustąpią, należy niezwłocznie zasięgnąć pomocy lekarskiej.
Jak podawać Icatibant Fresenius
Icatibant Fresenius jest przeznaczony do podawania podskórnego. Każdą ampułko-strzykawkę należy
użyć wyłącznie jeden raz.
Icatibant Fresenius wstrzykuje się za pomocą krótkiej igły do tkanki tłuszczowej pod skórą brzucha.
W razie jakichkolwiek dalszych wątpliwości związanych ze stosowaniem tego leku, należy zwrócić
się do lekarza lub farmaceuty.
Poniższa szczegółowa instrukcja dotyczy:
- podawania samodzielnego (dorośli);
- podawania przez opiekuna lub fachowy personel medyczny dorosłym, młodzieży i dzieciomw wieku powyżej 2 lat (o masie ciała nie mniejszej niż 12 kg).
Instrukcja obejmuje następujące główne kroki:
- 1) Informacje ogólne 2a) Przygotowanie ampułko-strzykawki dla dzieci i młodzieży (w wieku od 2 do 17 lat) o masie ciała 65 kg lub mniejszej 2b) Przygotowanie ampułko-strzykawki i igły do wstrzyknięcia (wszyscy pacjenci)
- 3) Przygotowanie miejsca wstrzyknięcia
- 4) Wstrzyknięcie roztworu
- 5) Usuwanie sprzętu do wstrzykiwań
Szczegółowa instrukcja wstrzykiwania
- 1) Informacje ogólne
- Przed rozpoczęciem pracy należy oczyścić używaną powierzchnię.
- Umyć ręce wodą i mydłem.
- Otworzyć opakowanie, odrywając warstwę uszczelniającą.
- Wyjąć ampułko-strzykawkę z opakowania.
- Odkręcić i zdjąć zakrętkę z końcówki ampułko-strzykawki.
- Po odkręceniu zakrętki odłożyć ampułko-strzykawkę.
2a) Przygotowanie ampułko-strzykawki dla dzieci i młodzieży (w wieku od 2 do 17 lat) o masie ciała 65 kg lub mniejszej
Ważne informacje dla fachowego personelu medycznego i opiekunów:
W przypadku gdy dawka jest mniejsza niż 30 mg (3 ml), do uzyskania odpowiedniej dawki
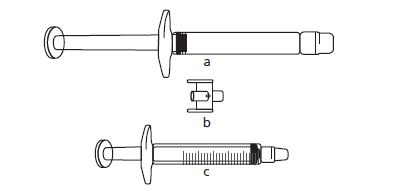
z ampułko-strzykawki potrzebne będą (patrz poniżej):
a) ampułko-strzykawka z lekiem Icatibant Fresenius (zawierającym roztwór ikatybantu),
b) adapter (łącznik),
c) strzykawka 3 ml z podziałką.
Potrzebną objętość roztworu w mililitrach należy pobrać do pustej strzykawki o pojemności 3 ml
z podziałką (patrz tabela poniżej).
Tabela 1. Schemat podawania dla dzieci i młodzieży
Masa ciała Objętość roztworu
12 kg do 25 kg
1,0 ml
26 kg do 40 kg
1,5 ml
41 kg do 50 kg
2,0 ml
51 kg do 65 kg
2,5 ml
Pacjentom o masie ciała powyżej 65 kgpodaje się całą zawartość ampułko-strzykawki (3 ml).
Jeśli pacjent nie ma pewności, jaką objętość roztworu pobrać, należy zwrócić się do lekarza, farmaceuty lub pielęgniarki.
- 1) Zdjąć zakrętki po obydwu stronach adaptera.

Należy unikać dotykania końcówki i czubka adaptera oraz strzykawki, aby zapobiec skażeniu.
- 2) Przykręcić adapter do ampułko-strzykawki.

- 3) Przymocować strzykawkę z podziałką do drugiego końca adaptera tak, aby obie końcówki były ściśle połączone.
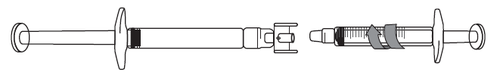
Pobieranie roztworu ikatybantu do strzykawki z podziałką:
- 1) Aby rozpocząć pobieranie roztworu ikatybantu, należy wcisnąć tłok ampułko-strzykawki (po lewej na ilustracji poniżej).
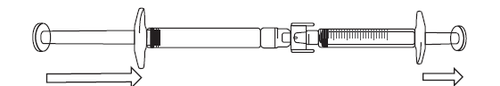
- 2) Jeżeli roztwór ikatybantu nie zaczął przepływać do strzykawki z podziałką, należy delikatnie ciągnąć tłok strzykawki, aż roztwór ikatybantu zacznie do niej napływać (patrz ilustracja poniżej).
- 3) Należy kontynuować wciskanie tłoka ampułko-strzykawki, aż wymagana objętość roztworu do wstrzyknięcia (dawka) przepłynie do strzykawki z podziałką. Informacje dotyczące dawkowania znajdują się w tabeli 1.
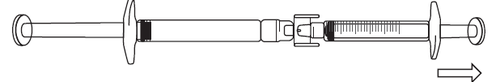
Jeżeli w strzykawce z podziałką znajduje się powietrze, należy:
- Obrócić połączone ze sobą strzykawki tak, aby ampułko-strzykawka znalazła się na górze (patrz ilustracja).
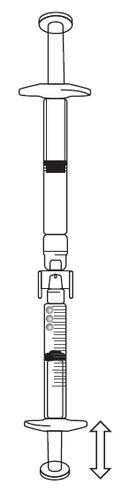
- Wcisnąć tłok strzykawki z podziałką tak, aby powietrze wróciło do ampułko-strzykawki (może być konieczne powtórzenie tego kroku kilka razy).
- Pobrać potrzebną objętość roztworu ikatybantu.
- 4) Odłączyć ampułko-strzykawkę z adapterem od strzykawki z podziałką.
- 5) Umieścić ampułko-strzykawkę z adapterem w specjalnym pojemniku na ostre narzędzia.
2b) Przygotowanie ampułko-strzykawki i igły do wstrzyknięcia
Wszyscy pacjenci (dorośli, młodzież i dzieci)
- Wyjąć z opakowania igłę z zabezpieczeniem.
- Zdjąć warstwę uszczelniającą z igły (igła nadal powinna pozostawać w osłonce).
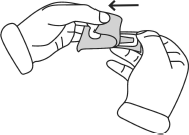
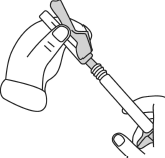
- Chwycić pewnie strzykawkę. Ostrożnie założyć igłę na strzykawkę, zawierającą bezbarwny roztwór. Wcisnąć mocno przekręcając strzykawkę zgodnie z ruchem wskazówek zegara.
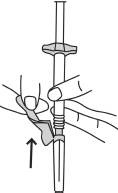
- Odciągnąć zabezpieczenie igły w kierunku strzykawki, z dala od igły.
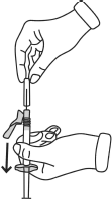
- Wyjąć igłę z osłonki, pociągając za korpus strzykawki. Nie ciągnąć za tłok strzykawki.
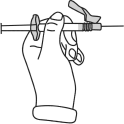
- Strzykawka jest już gotowa do wstrzyknięcia.
- 3) Przygotowanie miejsca wstrzyknięcia
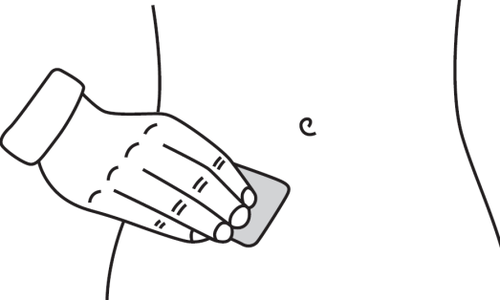
- Wybrać miejsce wstrzyknięcia. Miejscem wstrzyknięcia powinien być fałd skóry na brzuchu, około 5-10 cm poniżej pępka, po dowolnej stronie. Ten obszar skóry powinien znajdować się w odległości co najmniej 5 cm od jakichkolwiek blizn. Nie wybierać do wstrzyknięcia powierzchni skóry z wybroczynami, obrzękami lub bolesnej.
- Oczyścić miejsce wstrzyknięcia, przecierając je płatkiem gazy nasączonym alkoholem i pozostawić do wyschnięcia.
- 4)Wstrzyknięcie roztworu
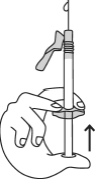
- Strzykawkę należy trzymać jedną ręką, pomiędzy dwoma palcami, z kciukiem na końcówce tłoka.
- Upewnić się, że w strzykawce nie ma pęcherzyków powietrza, poprzez naciśnięcie tłoka do pojawienia się pierwszej kropli na końcu igły.
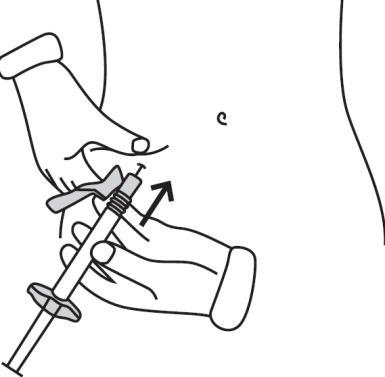
- Trzymać strzykawkę pod kątem 45-90 stopni do skóry, z igłą skierowaną do skóry.
- Trzymając strzykawkę jedną ręką, drugą ręką chwycić delikatnie fałd skóry pomiędzy kciuk i palce w miejscu, które zostało wcześniej zdezynfekowane.
- Przytrzymać fałd skóry, zbliżyć strzykawkę do skóry i szybko wkłuć igłę w fałd skóry.
- Powoli wciskać tłok strzykawki trzymając rękę nieruchomo, aż do wstrzyknięcia całego płynu do skóry i całkowitego opróżnienia strzykawki.
- Tłok wciskać powoli, przez około 30 sekund.
- Puścić fałd skóry i delikatnie wyciągnąć igłę.
- 5) Usuwanie sprzętu do wstrzykiwań
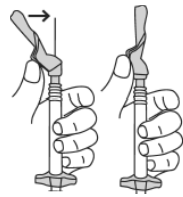
- Przesuwać zabezpieczenie igły do przodu, na igłę, do momentu usłyszenia i poczucia zablokowania.
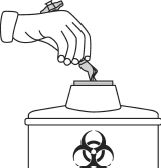
- Umieścić strzykawkę, igłę i osłonkę igły w pojemniku na ostre przedmioty, przeznaczonym do usuwania odpadów, które mogą powodować skaleczenia.
4. Możliwe działania niepożądane
Jak każdy lek, lek ten może powodować działania niepożądane, chociaż nie u każdego one wystąpią.
Niemal u wszystkich pacjentów otrzymujących Icatibant Fresenius występuje reakcja w miejscu
wstrzyknięcia (podrażnienie, obrzęk, ból, świąd, zaczerwienienie skóry i uczucie pieczenia). Działania
te są zwykle łagodne i ustępują bez konieczności stosowania dodatkowego leczenia.
Bardzo często (mogą dotyczyć więcej niż 1 na 10 pacjentów):
Dodatkowe reakcje w miejscu wstrzyknięcia (uczucie ucisku, zasinienie, upośledzenie czucia i (lub)
drętwienie, wypukła, swędząca wysypka na skórze oraz uczucie ciepła).
Często (może dotyczyć nie więcej niż 1 na 10 pacjentów):
- nudności;
- bóle głowy;
- zawroty głowy;
- gorączka;
- świąd;
- wysypka;
- zaczerwienienie skóry;
- nieprawidłowy wynik testów wątrobowych.
Częstość nieznana (nie może być określona na podstawie dostępnych danych):
- pokrzywka.
Należy niezwłocznie powiadomić lekarza, jeśli pacjent zauważy nasilenie objawów lub zaostrzenie
napadu choroby po zastosowaniu leku Icatibant Fresenius.
Jeśli wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie możliwe objawy niepożądane
niewymienione w tej ulotce, należy zwrócić się do lekarza.
Zgłaszanie działań niepożądanych
Jeśli wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie objawy niepożądane niewymienione
w tej ulotce, należy powiedzieć o tym lekarzowi lub farmaceucie, lub pielęgniarce. Działania
niepożądane można zgłaszać bezpośrednio do Departamentu Monitorowania Niepożądanych Działań
Produktów Leczniczych Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych
i Produktów Biobójczych
Al. Jerozolimskie 181C
02-222 Warszawa
tel.: + 48 22 49 21 301
faks: + 48 22 49 21 309
strona internetowa: https://smz.ezdrowie.gov.pl
Działania niepożądane można zgłaszać również podmiotowi odpowiedzialnemu.
Dzięki zgłaszaniu działań niepożądanych można będzie zgromadzić więcej informacji na temat
bezpieczeństwa stosowania leku.
5. Jak przechowywać Icatibant Fresenius
Lek należy przechowywać w miejscu niewidocznym i niedostępnym dla dzieci.
Nie stosować tego leku po upływie terminu ważności zamieszczonego na pudełku i ampułko-
strzykawce po: EXP. Termin ważności oznacza ostatni dzień podanego miesiąca.
Nie przechowywać w temperaturze powyżej 30°C. Nie zamrażać.
Zużyć natychmiast po otwarciu i stosować tylko nieuszkodzone opakowania.
Wyłącznie do jednorazowego użycia.
Nie stosować tego leku, jeśli ampułko-strzykawka lub opakowanie igły są uszkodzone, lub gdy
występują jakiekolwiek widoczne oznaki zepsucia, na przykład jeżeli roztwór jest mętny, występują
w nim cząstki stałe lub gdy jego zabarwienie ulegnie zmianie.
Leków nie należy wyrzucać do kanalizacji ani domowych pojemników na odpadki. Należy zapytać
farmaceutę, jak usunąć leki, których się już nie używa. Takie postępowanie pomoże chronić
środowisko.
6. Zawartość opakowania i inne informacje
Co zawiera Icatibant Fresenius
- Substancją czynną jest ikatybant. Każda ampułko-strzykawka zawiera 30 mg ikatybantu (w postaci octanu). Każdy ml roztworu zawiera 10 mg ikatybantu.
- Pozostałe składniki to: sodu chlorek, kwas octowy lodowaty (do ustalenia pH), sodu wodorotlenek (do ustalenia pH) i woda do wstrzykiwań.
Jak wygląda Icatibant Fresenius i co zawiera opakowanie
Icatibant Fresenius jest przezroczystym, bezbarwnym roztworem do wstrzykiwań
w ampułko-strzykawce (z bezbarwnego szkła typu I) o pojemności 3 ml z tłokiem zakończonym
korkiem bromobutylowym powlekanym polimerem fluorowęglowym, w tekturowym pudełku.
Do opakowania dołączona jest igła podskórna z zabezpieczeniem (25G; 16 mm).
Icatibant Fresenius jest dostępny w opakowaniu zawierającym jedną ampułko-strzykawkę z jedną igłą
z zabezpieczeniem lub trzy ampułko-strzykawki z trzema igłami z zabezpieczeniem.
Nie wszystkie wielkości opakowań muszą znajdować się w obrocie.
Podmiot odpowiedzialny
Fresenius Kabi Polska Sp. z o.o.
Al. Jerozolimskie 134
02-305 Warszawa
Wytwórca
Fresenius Kabi Austria GmbH
Hafnerstraße 36
A-8055 Graz
Austria
W celu uzyskania bardziej szczegółowych informacji należy zwrócić się do podmiotu
odpowiedzialnego:
Fresenius Kabi Polska Sp. z o.o.
Al. Jerozolimskie 134
02-305 Warszawa
tel.: +48 22 345 67 89
Ten lek jest dopuszczony do obrotu w krajach członkowskich Europejskiego Obszaru
Gospodarczego i w Zjednoczonym Królestwie (Irlandii Północnej) pod następującymi nazwami:
| Nazwa Państwa Członkowskiego | Nazwa leku |
| Austria | Icatibant Fresenius 30 mg Injektionslösung in einer Fertigspritze |
| Belgia | Icatibant Fresenius 30 mg oplossing voor injectie in een voorgevulde spuit, solution injectable en seringue pré-remplie, Injektionslösung in einer Fertigspritze |
| Chorwacja | Ikatibant Fresenius 30 mg otopina za injekciju u napunjenoj štrcaljki |
| Czechy | Icatibant Fresenius |
| Dania | Icatibant Fresenius |
| Estonia | Icatibant Fresenius |
| Finlandia | Icatibant Fresenius 30 mg injektioneste, liuos, esitäytetty ruisku |
| Francja | ICATIBANT FRESENIUS 30 mg, solution injectable en seringue préremplie |
| Niemcy | Icatibant Fresenius 30 mg Injektionslösung in einer Fertigspritze |
| Węgry | Icatibant Fresenius 30 mg oldatos injekció előretöltött fecskendőben |
| Irlandia | Icatibant 30 mg solution for injection in pre-filled syringe |
| Włochy | Icatibant Fresenius |
| Łotwa | Icatibant Fresenius 30 mg šķīdums injekcijām pilnšļircē |
| Litwa | Icatibant Fresenius 30 mg injekcinis tirpalas užpildytame švirkšte |
| Holandia | Icatibant Fresenius 30 mg, oplossing voor injectie in een voorgevulde spuit |
| Norwegia | Icatibant Fresenius |
| Polska | Icatibant Fresenius |
| Portugalia | Icatibant Fresenius |
| Słowacja | Icatibant Fresenius 30 mg |
| Hiszpania | Icatibanto Fresenius 30 mg solución inyectable en jeringa precargada EFG |
| Szwecja | Icatibant Fresenius 30 mg injektionsvätska, lösning i förfylld spruta |
| Zjednoczone Królestwo (Irlandia Pólnocna) | Icatibant 30 mg solution for injection in pre-filled syringe |
Data ostatniej aktualizacji ulotki:15.04.2024 r.
- Kraj rejestracji
- Substancja czynna
- Wymaga receptyTak
- Producent
- ImporterFresenius Kabi Austria GmbH
- Te informacje mają charakter wyłącznie poglądowy i nie stanowią porady medycznej. Przed zastosowaniem jakiegokolwiek leku zawsze skonsultuj się z lekarzem. Oladoctor nie ponosi odpowiedzialności za decyzje medyczne podjęte na podstawie tych treści.
- Zamienniki Icatibant FreseniusPostać farmaceutyczna: Roztwór, 30 mgSubstancja czynna: icatibantProducent: Universal Farma, S.L.Wymaga receptyPostać farmaceutyczna: Roztwór, 30 mgSubstancja czynna: icatibantProducent: Universal Farma, S.L.Wymaga receptyPostać farmaceutyczna: Roztwór, 30 mgSubstancja czynna: icatibantWymaga recepty
Odpowiedniki Icatibant Fresenius w innych krajach
Najlepsze odpowiedniki z tą samą substancją czynną i działaniem terapeutycznym.
Odpowiednik Icatibant Fresenius – Spain
Odpowiednik Icatibant Fresenius – Ukraine
Lekarze online w sprawie Icatibant Fresenius
Konsultacja w sprawie dawkowania, działań niepożądanych, interakcji, przeciwwskazań i odnowienia recepty na Icatibant Fresenius – decyzja należy do lekarza, zgodnie z lokalnymi przepisami.














