

Atmina

Zapytaj lekarza o receptę na Atmina

Jak stosować Atmina
Ulotka dołączona do opakowania: informacja dla pacjenta
Atmina, 4,6 mg/24 h, system transdermalny, plaster
Atmina, 9,5 mg/24 h, system transdermalny, plaster
Rivastigminum
Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje ważne dla pacjenta.
- Należy zachować tę ulotkę, aby w razie potrzeby móc ją ponownie przeczytać.
- W razie jakichkolwiek wątpliwości należy zwrócić się do lekarza lub farmaceuty.
- Lek ten przepisano ściśle określonej osobie. Nie należy go przekazywać innym. Lek może zaszkodzić innej osobie, nawet jeśli objawy jej choroby są takie same.
- Jeśli u pacjenta wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie objawy niepożądane niewymienione w tej ulotce, należy powiedzieć o tym lekarzowi lub farmaceucie. Patrz punkt 4.
Spis treści ulotki
- 1. Co to jest lek Atmina i w jakim celu się go stosuje
- 2. Informacje ważne przed zastosowaniem leku Atmina
- 3. Jak stosować lek Atmina
- 4. Możliwe działania niepożądane
- 5. Jak przechowywać lek Atmina
- 6. Zawartość opakowania i inne informacje
1. Co to jest lek Atmina i w jakim celu się go stosuje
Substancją czynną leku Atmina jest rywastygmina.
Rywastygmina należy do grupy substancji zwanych inhibitorami cholinesterazy. U pacjentów
z otępieniem typu alzheimerowskiego dochodzi do obumarcia pewnych komórek nerwowych w mózgu,
co powoduje zmniejszenie stężenia neuroprzekaźnika acetylocholiny (substancja umożliwiająca
komunikowanie się komórek nerwowych między sobą). Działanie rywastygminy polega na blokowaniu
enzymów powodujących rozpad acetylocholiny: acetylocholinesterazy i butyrylocholinesterazy.
Blokując działanie tych enzymów, rywastygmina umożliwia zwiększenie stężenia acetylocholiny
w mózgu, co pomaga w łagodzeniu objawów choroby Alzheimera.
Lek Atmina jest stosowany w leczeniu dorosłych pacjentów z otępieniem typu alzheimerowskiego
o nasileniu łagodnym do umiarkowanie ciężkiego, które jest postępującą chorobą mózgu, która powoduje
stopniowe zaburzenia pamięci, zdolności intelektualnych i zachowania.
2. Informacje ważne przed zastosowaniem leku Atmina
Kiedy nie stosować leku Atmina
- jeśli pacjent ma uczulenie na rywastygminę (substancja czynna leku Atmina) lub którykolwiek z pozostałych składników tego leku (wymienionych w punkcie 6);
- jeśli u pacjenta kiedykolwiek wystąpiła reakcja alergiczna na podobne leki (pochodne karbaminianu);
- jeśli u pacjenta występuje reakcja skórna wykraczająca poza obszar skóry zajmowany przez plaster, jeśli nasiliła się reakcja miejscowa (np. wystąpiły pęcherze, zaostrzenie stanu zapalnego skóry, opuchnięcie) lub jeśli zmiany te nie ustąpiły w ciągu 48 godzin po usunięciu plastra. Jeśli taka sytuacja dotyczy pacjenta, należy poinformować o tym lekarza i nie naklejać plastra Atmina.
Ostrzeżenia i środki ostrożności
Przed rozpoczęciem stosowania leku Atmina należy omówić to z lekarzem lub farmaceutą:
- jeśli u pacjenta występują lub kiedykolwiek występowały choroby serca takie, jak nieregularny lub
wolny rytm pracy serca, wydłużenie odstępu QT, wydłużenie odstępu QT stwierdzane w rodzinie,
torsade de pointeslub małe stężenie potasu lub magnezu we krwi;
- jeśli u pacjenta występuje lub kiedykolwiek występował czynny wrzód żołądka;
- jeśli u pacjenta występują lub kiedykolwiek występowały trudności w oddawaniu moczu;
- jeśli u pacjenta występują lub kiedykolwiek występowały napady padaczkowe;
- jeśli u pacjenta występuje lub kiedykolwiek występowała astma lub ciężka choroba układu oddechowego;
- jeśli u pacjenta występuje drżenie mięśniowe;
- jeśli pacjent ma małą masę ciała;
- jeśli u pacjenta występują reakcje ze strony żołądka i jelit, takie jak nudności (mdłości), wymioty i biegunka. Pacjent może się odwodnić (tracąc zbyt dużo płynu), jeśli wymioty czy biegunka utrzymują się przez dłuższy czas;
- jeśli u pacjenta występują zaburzenia czynności wątroby.
Jeśli którakolwiek z tych sytuacji dotyczy pacjenta, lekarz może prowadzić dokładniejszą obserwację
pacjenta w czasie stosowania tego leku.
Jeśli pacjent nie naklejał plastra przez dłużej niż trzy dni, nie powinien naklejać kolejnego plastra zanim
nie porozmawia o tym z lekarzem.
Należy ostrożnie usunąć wszystkie naklejone plastry przed naklejeniem nowego. Nie należy naklejać
więcej niż jednego plastra w tym samym czasie. Naklejenie kilku (lub więcej niż jednego) plastrów na
skórę może narazić pacjenta na przyjęcie nadmiernej ilości leku.
Dzieci i młodzież
Stosowanie leku Atmina u dzieci i młodzieży w leczeniu choroby Alzheimera nie jest właściwe.
Lek Atmina a inne leki
Należy powiedzieć lekarzowi lub farmaceucie o wszystkich lekach przyjmowanych przez pacjenta
obecnie lub ostatnio, a także o lekach, które pacjent planuje przyjmować.
Lek Atmina może wpływać na działanie leków przeciwcholinergicznych, z których niektóre są
stosowane w łagodzeniu skurczów żołądka (np. dicyklomina), w leczeniu choroby Parkinsona
(np. amantadyna) lub w zapobieganiu chorobie lokomocyjnej (np. difenhydramina, skopolamina lub
meklizyna).
Leku Atmina, system transdermalny w postaci plastra, nie należy stosować jednocześnie
z metoklopramidem (lek stosowany w łagodzeniu lub zapobieganiu nudnościom i wymiotom).
Jednoczesne stosowanie tych dwóch leków może spowodować takie zaburzenia, jak sztywność kończyn
i drżenie dłoni.
Jeśli pacjent ma być poddany operacji w czasie stosowania leku Atmina, system transdermalny w postaci
plastra, powinien powiedzieć lekarzowi o jego stosowaniu, ponieważ może on nasilać działanie
niektórych środków zwiotczających mięśnie, podawanych w trakcie znieczulenia.
Należy zachować ostrożność, gdy lek Atmina, system transdermalny w postaci plastra jest stosowany
razem z lekami beta-adrenolitycznymi (leki, takie jak atenolol, stosowane w leczeniu nadciśnienia
tętniczego, dławicy piersiowej i innych chorób serca). Jednoczesne przyjmowanie tych dwóch leków
może spowodować takie zaburzenia, jak spowolnienie pracy serca (bradykardia), prowadzące do
omdlenia lub utraty przytomności.
Należy zachować ostrożność, gdy lek Atmina jest stosowany razem z innymi lekami, które mogą
wpływać na rytm serca lub układ przewodzący serca (wydłużenie odstępu QT).
Ciąża, karmienie piersią i wpływ na płodność
Jeśli pacjentka jest w ciąży lub karmi piersią, przypuszcza, że może być w ciąży lub gdy planuje mieć
dziecko, powinna poradzić się lekarza lub farmaceuty przed zastosowaniem tego leku.
Jeśli pacjentka jest w ciąży, należy dokonać oceny korzyści ze stosowania leku Atmina względem
możliwych działań leku na nienarodzone dziecko. Lek Atmina nie powinien być stosowany w czasie
ciąży, jeśli nie jest to bezwzględnie konieczne.
Nie należy karmić piersią podczas stosowania leku Atmina.
Prowadzenie pojazdów i obsługiwanie maszyn
Lekarz poinformuje pacjenta, czy jego stan pozwala na bezpieczne prowadzenie pojazdów
i obsługiwanie maszyn. Lek Atmina, system transdermalny w postaci plastra, może powodować
omdlenia lub silne splątanie. Jeśli pacjent czuje się słabo lub jest zdezorientowany, nie wolno pacjentowi
prowadzić pojazdów, obsługiwać maszyn ani wykonywać innych zadań wymagających koncentracji.
3. Jak stosować lek Atmina
Ten lek należy zawsze stosować dokładnie tak, jak zalecił lekarz. W razie wątpliwości należy zwrócić się
do lekarza lub farmaceuty.
Jak rozpoczynać leczenie
Lekarz poinformuje pacjenta, który plaster leku Atmina jest najlepszy w danym przypadku.
- Leczenie zazwyczaj rozpoczyna się od leku Atmina 4,6 mg/24 h.
- Zalecana, zazwyczaj stosowana dawka dobowa leku Atmina to 9,5 mg/24 h. Jeśli dawka ta jest dobrze tolerowana, lekarz może rozważyć zwiększenie dawki do 13,3 mg/24 h. Nie można uzyskać dawki 13,3 mg/24 h z lekiem Atmina. W przypadku chorób wymagających zastosowania takiej dawki, dostępne są inne systemy transdermalne zawierające rywastygminę o mocy 13,3 mg/24 h.
- Należy naklejać tylko jedenprostokątny plaster i jedną owalną, samoprzylepną osłonę ochronną na raz (jak szczegółowo opisano poniżej) i należy zmieniać je na nowe dwa razy w tygodniu,najpóźniej po 4 dniach. Plastry należy zmieniać w dwóch ustalonych dniach:
W każdy
Poniedziałek i piątek LUB
Wtorek i sobotę LUB
Środę i niedzielę LUB
Czwartek i poniedziałek LUB
Piątek i wtorek LUB
Sobotę i środę LUB
Niedzielę i czwartek.
Należy zawsze naklejać nowy plaster o tej samej porze dnia. W celu ułatwienia zapamiętania, należy
zanotować dni i godzinę zmiany plastra.
Podczas leczenia lekarz może dostosować dawkę leku do potrzeb danego pacjenta.
Jeśli pacjent nie nakleił plastra przez więcej niż trzy dni, nie powinien naklejać kolejnego plastra zanim
nie porozmawia o tym z lekarzem. Leczenie plastrami można wznowić stosując tę samą dawkę, jeśli
przerwa w leczeniu nie przekraczała trzech dni. W przeciwnym razie lekarz zaleci wznowienie leczenia
dawką 4,6 mg/24 h leku Atmina.
Lek Atmina można stosować z jedzeniem, piciem i alkoholem.
Gdzie naklejać lek Atmina, system transdermalny w postaci plastra
Przed naklejeniem plastra należy upewnić się, że skóra w miejscu planowanego naklejenia jest czysta,
sucha i nieowłosiona, oczyszczona z pudru, olejków, kremów nawilżających lub płynów, które mogłyby
uniemożliwiać właściwe przyklejenie plastra, wolna od skaleczeń, wysypki i (lub) podrażnień.
- Należy ostrożnie usunąć wszystkie naklejone plastry przed naklejeniem nowego.Naklejenie kilku plastrów na skórę może narazić pacjenta na przyjęcie nadmiernej ilości leku, co może okazać się niebezpieczne.
- Należy naklejać JEDENprostokątny plaster razem z jedną samoprzylepną osłoną ochronną na TYLKO JEDNOz następujących miejsc, jak pokazano na poniższych rysunkach:
- górna część lewego ramienia lubgórna część prawego ramienia
- górna część klatki piersiowej po lewej stronie lubpo prawej stronie (należy unikaćnaklejania plastrów na piersi)
- górna część pleców po lewej stronie lubpo prawej stronie
- dolna część pleców po lewej stronie lubpo prawej stronie.
Najpóźniej po 4 dniach należy zdjąć poprzedni plaster przed przyklejeniem JEDNEGO nowego plastra i jednej samoprzylepnej osłony ochronnej na TYLKO JEDNO z następujących, możliwych miejsc.
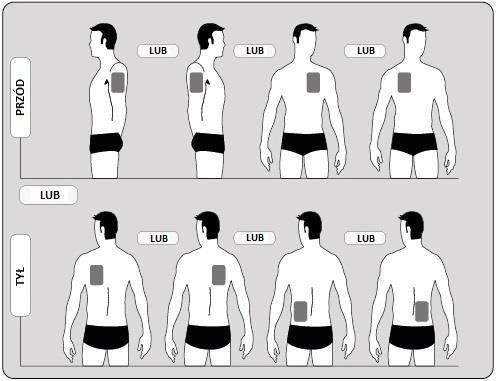
Zmieniając plaster, należy usunąć poprzedni plaster, zanim naklei się nowy plaster w innym miejscu
(na przykład na 4 dni po prawej stronie ciała, następnie po lewej stornie na 3 dni, i na górze na 4 dni,
a następnie na dole na kolejne 3 dni). Nie należy naklejać plastra w tym samym miejscu w ciągu 14 dni.
Jak pacjent powinien przyklejać lek Atmina, system transdermalny w postaci plastra
Lek Atmina przeznaczony jest do stosowania przezskórnego.
Lek Atmina składa się z dwóch części:
- jeden prostokątny, półprzezroczysty plaster zawierający substancję czynną (system transdermalny), który znajduje się w szczelnie zamkniętej saszetce i
- jeden owalny, beżowy plaster z tkaniny niezawierający substancji czynnej (samoprzylepna osłona ochronna), który również znajduje się w szczelnie zamkniętej saszetce. Ta saszetka jest większa niż saszetka zawierająca system transdermalny w postaci plastra.
 |  |
| System transdermalny w postaci plastra zawierający substancję czynną | Plaster z tkaniny niezawierający substancji czynnej (do umocowania) |
Nie należy otwierać saszetki ani wyjmować plastra z saszetki, aż do chwili jego przyklejenia na skórę.
Jako pierwszy należy zawszenałożyć prostokątnysystem transdermalny, plaster.
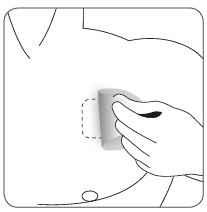 | Ostrożnie zdjąć poprzedni plaster przed naklejeniem nowego. Pacjenci rozpoczynający leczenie (po raz pierwszy) oraz pacjenci wznawiający leczenie rywastygminą po przerwie, powinni rozpoczynać od czynności pokazanych na drugim rysunku. |
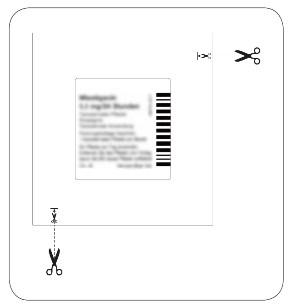 | Każdy plaster znajduje się w osobnej, szczelnie zamkniętej saszetce. Saszetkę należy otworzyć tuż przed użyciem plastra. Należy przeciąć saszetkę w obu miejscach oznakowanych nożyczkami, lecz nie dalej niż do wskazanej linii. Przedrzeć saszetkę w celu jej otwarcia. Nie przecinać saszetki na całej długości, aby uniknąć uszkodzenia plastra. Wyjąć z saszetki prostokątny, półprzezroczysty system transdermalny w postaci plastra. |
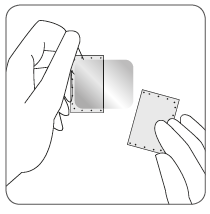 | Warstwa przylepna plastra jest zabezpieczona warstwą ochronną. Należy zdjąć jedną część warstwy ochronnej, nie dotykając palcami powierzchni klejącej plastra. |
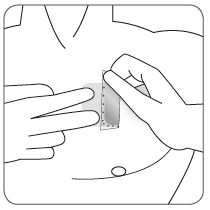 | Przyłożyć klejącą powierzchnię plastra do górnej lub dolnej części pleców, górnej części ramienia lub do klatki piersiowej, a następnie usunąć drugą część warstwy ochronnej. |
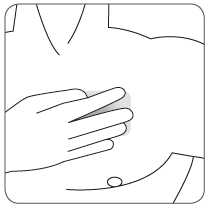 | Przycisnąć plaster mocno dłonią przez około 15 sekund, upewniając się, że jego brzegi dobrze przylegają do skóry. |
Następnie należy nałożyć owalną, samoprzylepną osłonę ochronną.
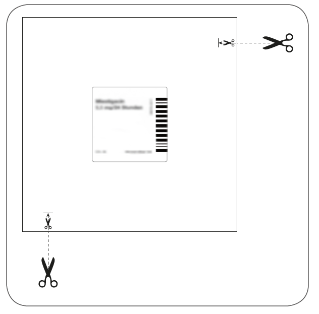 | Należy przeciąć saszetkę w obu miejscach oznakowanych nożyczkami, lecz nie dalej niż do wskazanej linii. Przedrzeć saszetkę w celu jej otwarcia. Nie przecinać saszetki na całej długości, aby uniknąć uszkodzenia samoprzylepnej osłony ochronnej niezawierającej leku. Wyjąć owalną, beżową, samoprzylepną osłonę ochronną z saszetki. |
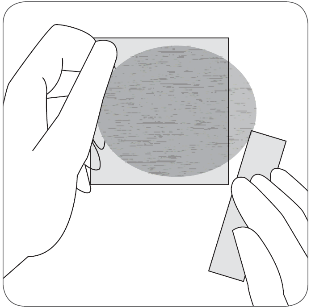 | Warstwa przylepna osłony ochronnej jest zabezpieczona warstwą ochronną. Należy zdjąć mniejszą część warstwy ochronnej, nie dotykając palcami powierzchni klejącej plastra. |
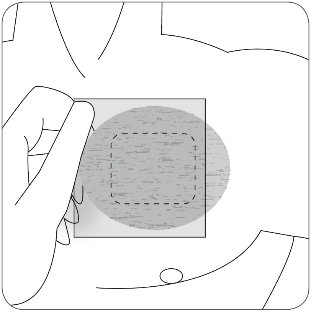 | Przyłożyć klejącą powierzchnię osłony ochronnej na naklejony wcześniej system transdermalny w postaci plastra, tak aby był całkowicie zakryty, a następnie usunąć drugą część warstwy ochronnej. |
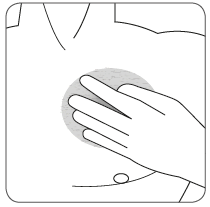 | Przycisnąć plaster mocno dłonią przez co najmniej 30 sekund, upewniając się, że jego brzegi dobrze przylegają do skóry. |
Dla niektórych pacjentów pomocne może być zapisanie cienkim długopisem na osłonie ochronnej
np. dnia tygodnia.
Plaster należy nosić stale, aż do czasu jego zmiany na nowy. Pacjent może wypróbować różne miejsca
przyklejenia nowego plastra, aby wybrać najbardziej dogodne i nie narażone na zdarcie przez odzież.
Jak pacjent powinien zdejmować lek Atmina, system transdermalny w postaci plastra
Należy delikatnie pociągnąć za jeden brzeg samoprzylepnej osłony ochronnej i powoli odkleić ją od
skóry razem z systemem transdermalnym.
Jeśli system transdermalny pozostanie na skórze, należy delikatnie pociągnąć za jeden brzeg i odkleić go
od skóry.
Jeśli na skórze pozostaną resztki kleju, można je usunąć przemywając to miejsce ciepłą wodą i łagodnym
mydłem lub oliwką dla dzieci. Nie należy stosować alkoholu ani innych rozpuszczalników (zmywacza
do paznokci i innych środków).
Po zdjęciu plastra należy umyć ręce wodą z mydłem. W razie kontaktu leku z oczami lub
zaczerwienienia oczu po kontakcie z plastrem, natychmiast należy przemyć oczy dużą ilością wody,
a jeśli objawy nie ustąpią, należy zgłosić się po pomoc medyczną.
Czy pacjent może stosować lek Atmina, system transdermalny w postaci plastra podczas kąpieli, pływania lub na słońcu?
- Kąpiel, pływanie bądź kąpiel pod prysznicem nie powinny mieć wpływu na działanie plastra. Należy upewnić się, że podczas wykonywania tych czynności nie dojdzie do obluzowania się plastra.
- Nie należy narażać plastra na dłuższe działanie wszelkich zewnętrznych źródeł ciepła (np. nadmierne działanie promieni słonecznych, sauna, solarium).
Jak postępować w razie odklejenia się plastra
Jeśli plaster sam się odklei, należy nakleić nowy, a następnie zmienić go o zwykłej porze.
Kiedy i jak długo pacjent powinien stosować lek Atmina, system transdermalny w postaci plastra?
- Aby leczenie przyniosło efekty, należy naklejać nowy plaster dwa razy w tygodniu, najpóźniej po
czterech dniach, najlepiej o tej samej porze dnia.
- Należy naklejać tylko jeden prostokątny system transdermalny w postaci plastra i jedną owalną, samoprzylepną osłonę ochronną na raz i należy zmieniać je na nowe w dwóch ustalonych dniachtygodnia.
Zastosowanie większej niż zalecana dawki leku Atmina
Jeśli pacjent przez przypadek naklei więcej niż jeden prostokątnysystem transdermalnym w postaci
plastra, należy zdjąć wszystkie plastry, a następnie poinformować lekarza o przypadkowym naklejeniu
więcej niż jednego plastra. Pacjent może wymagać pomocy lekarskiej. U niektórych osób, które przez
przypadek zastosowały zbyt dużo rywastygminy, wystąpiły nudności (mdłości), wymioty, biegunka,
wysokie ciśnienie krwi i omamy. Może także wystąpić spowolnienie pracy serca i omdlenie.
Pominięcie zastosowania leku Atmina
Jeśli pacjent stwierdził, że zapomniał nakleić plaster, powinien natychmiast to zrobić, o ile przerwa
w leczeniu nie przekraczała trzech dni.
Następny plaster można nakleić o zwykłej porze w ustalonym dniu, aby powrócić do zwykłego schematu
dawkowania. Nie należy naklejać dwóch plastrów w celu uzupełnienia pominiętego plastra. Jeśli pacjent
nie miał naklejonego plastra przez więcej niż trzy dni, nie powinien naklejać kolejnego plastra zanim nie
porozmawia o tym z lekarzem.
Przerwanie stosowania leku Atmina
W razie przerwania stosowania plastrów, należy poinformować o tym lekarza lub farmaceutę.
W razie jakichkolwiek dalszych wątpliwości związanych ze stosowaniem tego leku, należy zwrócić się
do lekarza lub farmaceuty.
4. Możliwe działania niepożądane
Jak każdy lek, lek ten może powodować działania niepożądane, chociaż nie u każdego one wystąpią.
Działania niepożądane mogą wystąpić częściej w początkowym okresie stosowania leku lub w okresie
zwiększania dawki. Działania niepożądane zazwyczaj powoli ustępują, w miarę, jak organizm
przystosowuje się do leczenia.
W razie wystąpienia jednego z wymienionych działań niepożądanych należy zdjąć plaster i natychmiast powiedzieć o tym lekarzowi, ponieważ działania te mogą być ciężkie:
Często(może wystąpić rzadziej niż u 1 na 10 osób)
- utrata apetytu
- zawroty głowy
- pobudzenie lub senność
- nietrzymanie moczu (niezdolność do właściwego utrzymania moczu).
Niezbyt często(może wystąpić rzadziej niż u 1 na 100 osób)
- zaburzenia rytmu serca, takie jak wolne bicie serca
- widzenie rzeczy, których nie ma (omamy)
- wrzód żołądka
- odwodnienie (utrata zbyt dużej ilości płynu)
- nadmierna ruchliwość (wysoki stopień aktywności, niepokój)
- agresja.
Rzadko(może wystąpić rzadziej niż u 1 na 1000 osób)
- upadki.
Bardzo rzadko(może wystąpić rzadziej niż u 1 na 10 000 osób)
- sztywność ramion lub nóg
- drżenie rąk.
Częstość nieznana(częstość nie może być określona na podstawie dostępnych danych)
- reakcja alergiczna w miejscu naklejenia plastra, taka jak pęcherze lub stan zapalny skóry
- nasilenie objawów choroby Parkinsona - takich, jak drżenie, sztywność lub pociąganie nogami
- zapalenie trzustki - do objawów należy silny ból w górnej części brzucha, często z nudnościami (mdłościami) lub wymiotami
- szybkie lub nierówne bicie serca
- wysokie ciśnienie krwi
- drgawki (napady padaczkowe)
- zaburzenia czynności wątroby (zażółcenie skóry, zażółcenie białkówek oczu, nieprawidłowa ciemna barwa moczu lub niewyjaśnione nudności, wymioty, zmęczenie i utrata apetytu)
- zmiany w wynikach badań czynności wątroby
- niepokój
- koszmary senne
- zespół Piza (stan obejmujący mimowolny skurcz mięśni z nieprawidłowym pochyleniem ciała i głowy na jedną stronę).
W razie wystąpienia jednego z wymienionych działań niepożądanych, należy zdjąć plaster i natychmiast
powiedzieć o tym lekarzowi.
Inne działania niepożądane zgłaszane po zastosowaniu rywastygminy w postaci kapsułek lub roztworu doustnego, które mogą również wystąpić po zastosowaniu plastrów:
Często(może wystąpić rzadziej niż u 1 na 10 osób)
- nadmierne wydzielanie śliny
- utrata apetytu
- niepokój
- ogólne złe samopoczucie
- drżenie lub splątanie
- nasilone pocenie się.
Niezbyt często(może wystąpić rzadziej niż u 1 na 100 osób)
- zaburzenia rytmu serca (np. szybkie bicie serca)
- trudności w zasypianiu
- przypadkowe upadki.
Rzadko(może wystąpić rzadziej niż u 1 na 1000 osób)
- drgawki (napady padaczkowe)
- choroba wrzodowa jelit
- ból w klatce piersiowej - może być spowodowany skurczem serca.
Bardzo rzadko(może wystąpić rzadziej niż u 1 na 10 000 osób)
- wysokie ciśnienie krwi
- zapalenie trzustki - do objawów należy silny ból w górnej części brzucha, często z nudnościami (mdłościami) lub wymiotami
- krwawienia z przewodu pokarmowego - krew w kale lub wymiotach
- widzenie rzeczy, których nie ma (omamy)
- gwałtowne wymioty, które mogą prowadzić do pęknięcia części przewodu pokarmowego łączącego jamę ustną z żołądkiem (przełyku).
Zgłaszanie działań niepożądanych
Jeśli wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie objawy niepożądane niewymienione
w tej ulotce, należy powiedzieć o tym lekarzowi lub farmaceucie. Działania niepożądane można zgłaszać
bezpośrednio do Departamentu Monitorowania Niepożądanych Działań Produktów Leczniczych Urzędu
Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych; Al. Jerozolimskie
181C, 02-222 Warszawa, tel.: + 48 22 49 21 301, faks: + 48 22 49 21 309, strona internetowa:
https://smz.ezdrowie.gov.pl.
Działania niepożądane można zgłaszać również podmiotowi odpowiedzialnemu.
Dzięki zgłaszaniu działań niepożądanych można będzie zgromadzić więcej informacji na temat
bezpieczeństwa stosowania leku.
5. Jak przechowywać lek Atmina
- Lek należy przechowywać w miejscu niewidocznym i niedostępnym dla dzieci.
- Nie stosować tego leku po upływie terminu ważności zamieszczonego na pudełku tekturowym i saszetce po: „Termin ważności (EXP)”. Termin ważności oznacza ostatni dzień podanego miesiąca.
- Brak specjalnych zaleceń dotyczących przechowywania leku.
- Nie należy stosować plastra, który jest uszkodzony lub nosi ślady otwierania.
Po zdjęciu plastra należy złożyć go na pół powierzchnią przylepną do środka i mocno ścisnąć. Należy
włożyć zużyty plaster do saszetki, a następnie wyrzucić w miejsce niedostępne dla dzieci. Leków nie
należy wyrzucać do kanalizacji ani domowych pojemników na odpadki. Należy zapytać farmaceutę, jak
usunąć leki, których się już nie używa. Takie postępowanie pomoże chronić środowisko.
6. Zawartość opakowania i inne informacje
Co zawiera lek Atmina
Substancją czynną leku jest rywastygmina.
Atmina 4,6 mg/24 h, system transdermalny, plaster:
Z każdego systemu transdermalnego, plastra uwalnia się 4,6 mg rywastygminy w ciągu 24 godzin. Każdy
system transdermalny, plaster o powierzchni 10,8 cm zawiera 25,92 mg rywastygminy.
Atmina 9,5 mg/24 h, system transdermalny, plaster:
Z każdego systemu transdermalnego, plastra uwalnia się 9,5 mg rywastygminy w ciągu 24 godzin. Każdy
system transdermalny, plaster o powierzchni 21,6 cm zawiera 51,84 mg rywastygminy.
Pozostałe składniki to:
Warstwa zewnętrzna (pokrywająca): folia z poli(tereftalanu etylenu).
Warstwa aktywna: tokoferol, poli(2-etyloheksylu akrylan, winylu octan) (1:1), butylu akrylanu i butylu
metakrylanu kopolimer.
Membrana przepuszczalna dla substancji czynnej: folia z polietylenu.
Warstwa adhezyjna: poliizobutylen o średniej masie cząsteczkowej, poliizobut yl en o wysokiej masie
cząsteczkowej, polibutylen o wysokiej masie cząsteczkowej.
Warstwa zabezpieczająca (usuwalna): folia z poliestru silikonowanego.
Nadruk: Niebieski tusz.
Jak wygląda lek Atmina i co zawiera opakowanie
Każdy system transdermalny jest cienkim plastrem o prostokątnym kształcie, z zaokrąglonymi rogami.
Plaster jest półprzezroczysty i posiada następujące oznakowanie:
Atmina, 4,6 mg/24 h, system transdermalny, plaster: RID-TDS 4.6 mg/24 h
Atmina, 9,5 mg/24 h, system transdermalny, plaster: RID-TDS 9.5 mg/24 h
Każdy system transdermalny, plaster znajduje się w osobnej, szczelnie zamkniętej saszetce. Saszetki są
oznakowane w następujący sposób:
Atmina, 4,6 mg/24 h, system transdermalny, plaster
Atmina, 9,5 mg/24 h, system transdermalny, plaster
Dodatkowo, w każdym tekturowym pudełku z systemem transdermalnym, plastrem znajduje się osłona
ochronna, służąca do umocowania systemu transdermalnego, plastra.
Każda osłona ochronna to cienki, beżowy plaster o owalnym kształcie.
Osłony ochronne znajdują się w osobnych, szczelnie zamkniętych saszetkach. Saszetki są oznakowane
w następujący sposób:
Samoprzylepna osłona ochronna niezawierająca substancji czynnej.
Całość w tekturowym pudełku.
Atmina, 4,6 mg/24 h, system transdermalny, plasteri Atmina, 9,5 mg/24 h, system transdermalny, plaster
są dostępne w opakowaniach zawierających po 2, 8, 16 lub 24 systemy transdermalne, plastry z
odpowiednio 2, 8, 16 lub 24 samoprzylepnymi osłonami ochronnymi.
Nie wszystkie wielkości opakowań muszą znajdować się w obrocie.
Podmiot odpowiedzialny i wytwórca
Podmiot odpowiedzialny
Exeltis Poland Sp. z o.o.
ul. Szamocka 8
01-748 Warszawa
e-mail: [email protected]
Wytwórca
Luye Pharma AG
Am Windfeld 35
83714 Miesbach
Niemcy
Ten lek jest dopuszczony do obrotu w krajach członkowskich Europejskiego Obszaru
Gospodarczego pod następującymi nazwami:
Hiszpania
Alzerta dos por semana 4.6 mg/24 h parches transdérmicos
Alzerta dos por semana 9.5 mg/24 h parches transdérmicos
Niemcy
Rivez zweimal wöchentlich 4.6 mg/24 Stunden Transdermales Pflaster
Rivez zweimal wöchentlich 9.5 mg/24 Stunden Transdermales Pflaster
Polska
Atmina
Data ostatniej aktualizacji ulotki:06.12.2024 r.
- Kraj rejestracji
- Substancja czynna
- Wymaga receptyTak
- Producent
- ImporterLuye Pharma AG
- Te informacje mają charakter wyłącznie poglądowy i nie stanowią porady medycznej. Przed zastosowaniem jakiegokolwiek leku zawsze skonsultuj się z lekarzem. Oladoctor nie ponosi odpowiedzialności za decyzje medyczne podjęte na podstawie tych treści.
- Zamienniki AtminaPostać farmaceutyczna: System, 4,6 mg/24 hSubstancja czynna: rivastigmineProducent: Luye Pharma AGWymaga receptyPostać farmaceutyczna: System, 4,6 mg/24 hSubstancja czynna: rivastigmineWymaga receptyPostać farmaceutyczna: System, 9,5 mg/24 hSubstancja czynna: rivastigmineProducent: Luye Pharma AG Zentiva SAWymaga recepty
Odpowiedniki Atmina w innych krajach
Najlepsze odpowiedniki z tą samą substancją czynną i działaniem terapeutycznym.
Odpowiednik Atmina – Hiszpania
Odpowiednik Atmina – Ukraina
Lekarze online w sprawie Atmina
Konsultacja w sprawie dawkowania, działań niepożądanych, interakcji, przeciwwskazań i odnowienia recepty na Atmina – decyzja należy do lekarza, zgodnie z lokalnymi przepisami.











