
RETACRIT 4000 UI/0,4 ml SOLUCION INYECTABLE EN JERINGA PRECARGADA

Cómo usar RETACRIT 4000 UI/0,4 ml SOLUCION INYECTABLE EN JERINGA PRECARGADA
Traducción generada por IA
Este contenido ha sido traducido automáticamente y se ofrece solo con fines informativos. No sustituye la consulta con un profesional sanitario.
Ver originalContenido del prospecto
Introducción
Prospecto: información para el usuario
Retacrit 1 000UI/0,3ml solución inyectable en jeringa precargada
Retacrit 2 000UI/0,6ml solución inyectable en jeringa precargada
Retacrit 3 000UI/0,9ml solución inyectable en jeringa precargada
Retacrit 4 000UI/0,4ml solución inyectable en jeringa precargada
Retacrit 5 000UI/0,5ml solución inyectable en jeringa precargada
Retacrit 6 000UI/0,6ml solución inyectable en jeringa precargada
Retacrit 8 000UI/0,8ml solución inyectable en jeringa precargada
Retacrit 10000UI/1ml solución inyectable en jeringa precargada
Retacrit 20000UI/0,5ml solución inyectable en jeringa precargada
Retacrit 30000UI/0,75ml solución inyectable en jeringa precargada
Retacrit 40000UI/1ml solución inyectable en jeringa precargada
epoetina zeta
Lea todo el prospecto detenidamente antes de empezar a usar el medicamento, porque contiene información importante para usted.
- Conserve este prospecto, ya que puede tener que volver a leerlo.
- Si tiene alguna duda, consulte a su médico, farmacéutico o enfermero.
- Este medicamento se le ha recetado solamente a usted, y no debe dárselo a otras personas aunque tengan los mismos síntomas que usted, ya que puede perjudicarles.
- Si experimenta efectos adversos, consulte a su médico, farmacéutico o enfermero, incluso si se trata de efectos adversos que no aparecen en este prospecto. Ver sección 4.
Contenido del prospecto
- Qué es Retacrit y para qué se utiliza
- Que necesita saber antes de empezar a usar Retacrit
- Cómo usar Retacrit
- Posibles efectos adversos
- Conservación de Retacrit
- Contenido del envase e información adicional
1. Qué es Retacrit y para qué se utiliza
Retacrit contiene el principio activo epoetina zeta, una proteína que estimula la médula ósea para la producción de más glóbulos rojos, células que llevan hemoglobina (sustancia que transporta oxígeno). La epoetina zeta es una copia de la proteína humana eritropoyetina y actúa de la misma manera.
- Retacrit está indicado para tratar la anemia sintomática causada por una enfermedad renal
- en niños que se someten a hemodiálisis;
- en adultos que se someten a hemodiálisis o diálisis peritoneal;
- en adultos con anemia grave que aún no se han sometido a diálisis.
Si padece una enfermedad renal, puede que tenga un número bajo de glóbulos rojos si su riñón no produce suficiente eritropoyetina (necesaria para la producción de glóbulos rojos). Retacrit se receta con el fin de estimular a la médula ósea para que produzca más glóbulos rojos.
- Retacrit está indicado para tratar la anemia en adultos que reciben quimioterapia para el tratamiento de tumores sólidos, linfoma maligno o mieloma múltiple (neoplasia de la médula ósea) que pueden necesitar una transfusión sanguínea. Retacrit puede reducir la necesidad de recibir una transfusión sanguínea en estos pacientes.
- Retacrit está indicado en adultos con anemia moderada que van a donar sangre antes desometerse a una operación quirúrgica, de modo que se les pueda readministrar durante o después de la intervención quirúrgica. Dado que Retacrit estimula la producción de glóbulos rojos, los médicos pueden extraer más sangre de estas personas.
- Retacrit está indicado en adultos con anemia moderada a punto de someterse a una cirugía ortopédica mayor programada(por ejemplo, operaciones de reemplazo de cadera o rodilla)para reducir la necesidad potencial de transfusión sanguínea.
- Retacrit está indicado en pacientes adultos con anemia con un trastorno de la médula ósea que provoca una alteración grave en la creación de células sanguíneas (síndromes mielodisplásicos).Retacrit puede reducir la necesidad de una transfusión de sangre.
2. Que necesitas saber antes de empezar a usar Retacrit
No use Retacrit
- Si es alérgicoa la epoetina zeta o a alguno de los demás componentes de este medicamento (incluidos en la sección 6).
- Si le han diagnosticado aplasia eritrocitaria pura(la médula ósea no puede producir suficientes glóbulos rojos) después de un tratamiento previo con cualquier producto que estimule la producción de glóbulos rojos (incluido Retacrit). Ver sección 4.
- Si presenta hipertensión arterialque no se controla adecuadamente con medicamentos.
- Para estimular la producción de glóbulos rojos (de modo que sus médicos le puedan extraer más sangre) si no puede recibir transfusiones de su propia sangredurante la intervención quirúrgica o después de ella.
- Si está a punto de someterse a una cirugía ortopédica mayor programada (tal como una intervención de cadera o rodilla) y usted:
- tiene una enfermedad grave del corazón;
- tiene alteraciones graves en las venas o las arterias;
- ha sufrido recientemente un infarto de miocardio o un derrame cerebral;
- no puede tomar medicamentos para hacer menos espesa la sangre.
Puede que Retacrit no sea adecuado para usted. Hable con su médico. Algunas personas necesitan medicamentos para reducir el riesgo de que se formen coágulos de sangre durante el tratamiento con Retacrit. Si no puede tomar medicamentos para prevenir la formación de coágulos de sangre, no debe tomar Retacrit.
Advertencias y precauciones
Consulte a su médico, farmacéutico o enfermero antes de empezar a usar Retacrit.
Tenga especial cuidado con Retacrit
Retacrit y otros productos que estimulan la producción de glóbulos rojos pueden aumentar el riesgo de formación de coágulos sanguíneos en todos los pacientes. Este riesgo puede ser mayor si usted tiene otros factores de riesgopara la formación de coágulos sanguíneos (por ejemplo, si ha tenido un coágulo sanguíneo en el pasado o tiene sobrepeso, diabetes, padece una enfermedad del corazón o se encuentra postrado durante mucho tiempo debido a una intervención quirúrgica o enfermedad). Informe a su médico acerca de cualquiera de estas cosas. Su médico le ayudará a decidir si Retacrit es adecuado para usted.
Consulte a su médicosi se identifica con alguna de las siguientes situaciones.Es posible que aún pueda usar Retacrit, pero coméntelo antes con su médico.
- Si sabe que padeceo ha padecido:
- hipertensión arterial;
- crisis epilépticas o convulsiones;
- enfermedad del hígado;
- anemia por otras causas;
- porfiria (un trastorno raro de la sangre).
- Si es un paciente con insuficiencia renal crónica, y en especial si no responde bien a Retacrit, su médico comprobará su dosis de Retacrit, porque aumentar repetidamente la dosis de Retacrit si no responde al tratamiento puede aumentar el riesgo de padecer un problema de corazón o de los vasos sanguíneos y podría aumentar el riesgo de infarto de miocardio, ictus y muerte.
- Si es un paciente con cáncer,debe saber que los productos que estimulan la producción de glóbulos rojos (como Retacrit) pueden actuar como un factor de crecimiento y, por tanto, pueden afectar, en teoría, a la progresión del cáncer. Dependiendo de su situación individual, puede ser preferible una transfusión de sangre. Comente esto con su médico.
- Si es un paciente con cáncer,debe saber que el uso de Retacrit puede asociarse a una menor supervivencia y una mayor tasa de mortalidad en pacientes con cáncer de cabeza y cuello y cáncer de mama metastásico que reciben quimioterapia.
- Se han observado reacciones adversas cutáneas gravescomo, por ejemplo, síndrome de Stevens-Johnson (SSJ) y necrólisis epidérmica tóxica (NET) con la administración de epoetinas.
El SSJ/NET pueden aparecer inicialmente como manchas rojizas como dianas o parches circulares, a menudo con ampollas centrales en el tronco. Pueden aparecer también úlceras en la boca, garganta, nariz, genitales y ojos (irritación e hinchazón ocular). Estas erupciones cutáneas graves van precedidas a menudo de fiebre o síntomas de tipo gripal. Las erupciones pueden progresar a descamación generalizada de la piel y a complicaciones potencialmente mortales.
Si presenta una erupción cutánea grave o alguno de estos otros síntomas cutáneos, deje de tomar Retacrit y póngase en contacto con su médico o solicite atención médica de inmediato.
Tenga especial cuidado con otros productos que estimulan la producción de glóbulos rojos de la sangre
Retacrit pertenece a uno de los grupos de productos que estimula la producción de glóbulos rojos de la sangre como hace la proteína de eritropoyetina humana. Su médico debe registrar el nombre exacto del producto que está usando.
Si, durante su tratamiento, se le administra un producto perteneciente a este grupo, distinto a Retacrit, consulte a su médico o farmacéutico antes de usarlo.
Otros medicamentos y Retacrit
Informe a su médico o farmacéutico si está utilizando, ha utilizado recientemente o pudiera tener que utilizar cualquier otro medicamento.
Si está usando Retacrit junto con un medicamento denominado ciclosporina(p. ej., tras un trasplante de riñón), su médico puede solicitar análisis de sangre para controlar el nivel de ciclosporina.
Los complementos de hierro y otros estimulantes sanguíneospueden aumentar la efectividad del Retacrit. Su médico decidirá si le conviene usarlos.
Si visita un hospital, clínica o médico de cabecera, dígales que recibe tratamiento con Retacrit, ya que puede afectar a otros tratamientos o resultados de análisis.
Embarazo, lactancia y fertilidad
Es importante que informe a su médicosi se identifica con alguna de las siguientes situaciones.Es posible que aún pueda usar Retacrit, pero coméntelo antes con su médico.
- Si está embarazada o en periodo de lactancia, cree que podría estar embarazada o tiene intención de quedarse embarazada, consulte a su médico o farmacéutico antes de utilizar este medicamento.
- Si está en periodo de lactancia.
No hay datos disponibles sobre los efectos de la epoetina zeta en la fertilidad.
Conducción y uso de máquinas
La influencia de Retacrit sobre la capacidad para conducir y utilizar máquinas es nula o insignificante.
Retacrit contiene fenilalanina
Retacrit contiene 0,5 mg de fenilalanina por cada ml.
La fenilalanina puede ser perjudicial en caso de padecer fenilcetonuria (FCN), una enfermedad genética rara en la que la fenilalanina se acumula debido a que el organismo no es capaz de eliminarla correctamente sección
Retacrit contiene sodio
Este medicamento contiene menos de 1 mmol de sodio (23 mg) por dosis, esto es, esencialmente “exento de sodio”.
3. Cómo usar Retacrit
Siga exactamente las instrucciones de administración de este medicamento indicadas por su médico.En caso de duda, consulte de nuevo a su médico.
Su médico le ha realizado análisis de sangrey ha decidido que necesita Retacrit.
Retacrit puede administrarse mediante inyección:
- O bienen una vena o a través de un tubo que se introduce en una vena (por vía intravenosa).
- O biendebajo de la piel (por vía subcutánea).
Su médico decidirá de qué modo se inyectará Retacrit. Las inyecciones las realizará habitualmente un médico, un enfermero u otro profesional sanitario. Más adelante y dependiendo del motivo por el que necesiten el tratamiento con Retacrit, algunas personas pueden aprender a inyectarse el medicamento debajo de la piel: ver Instrucciones sobre cómo inyectarse Retacrit.
Retacrit no debe usarse:
- después de la fecha de caducidad de la etiqueta y la caja exterior;
- si usted sabe o cree que puede haberse congelado accidentalmente, o
- si se ha producido una avería en la nevera.
La dosis de Retacrit que recibirá se basa en su peso corporal en kilogramos. La causa de su anemia también es un factor que su médico tendrá en cuenta a la hora de decidir la dosis correcta.
Su médico controlará su tensión arterialperiódicamente mientras se encuentre en tratamiento con Retacrit.
Pacientes con insuficiencia renal
- Su médico mantendrá su nivel de hemoglobina entre 10 y 12 g/dl, ya que un nivel alto de hemoglobina puede aumentar el riesgo de coágulos sanguíneos y de muerte. En niños, el nivel de hemoglobina debe mantenerse entre 9,5 y 11 g/dl.
- La dosis de inicio habitualde Retacrit para adultos y niños es de 50 UI/kg (unidades internacionales por kilogramo) tres veces por semana.
- En los pacientes en diálisis peritoneal, Retacrit se puede administrar dos veces por semana.
- Tanto en los adultos como en los niños, Retacrit se administra en forma de inyección, bien en una vena (vía intravenosa) o bien a través de un tubo que se introduce en una vena. Cuando no se pueda conseguir fácilmente este acceso (a través de una vena o un tubo), su médico puede decidir que Retacrit debe inyectarse bajo la piel (vía subcutánea). Esto incluye a los pacientes en diálisis y los que todavía no lo están.
- Su médico pedirá análisis de sangre periódicos para ver cómo está respondiendo la anemia y podrá ajustar la dosis, generalmente con una frecuencia no superior a cada cuatro semanas. Se debe evitar un aumento de la hemoglobina superior a 2 g/dl durante un periodo de cuatro semanas.
- Una vez corregida la anemia, su médico seguirá realizándole análisis de sangre periódicos. Es posible que le vuelva a ajustar la dosis y frecuencia de administración de Retacrit para mantener su respuesta al tratamiento. Su médico utilizará la mínima dosis eficaz para controlar los síntomas de la anemia.
- Si no responde bien a Retacrit, su médico comprobará su dosis y le informará si necesita modificar la dosis de Retacrit.
- Si recibe un intervalo de dosis mayor (más de una vez por semana) de Retacrit, es posible que no mantenga unos niveles de hemoglobina adecuados y que requiera un aumento de la dosis de Retacrit o de la frecuencia de su administración.
- Puede que se le administren suplementos de hierro antes del tratamiento con Retacrit y durante el mismo a fin de aumentar su eficacia.
- Si en el momento de iniciar el tratamiento con Retacrit se está sometiendo a diálisis, es posible que haya que ajustarle su pauta de diálisis. Su médico decidirá si esto es necesario.
Adultos en quimioterapia
- Su médico puede iniciar el tratamiento con Retacrit si su hemoglobina es igual o inferior a 10 g/dl.
- Su médico mantendrá su concentración de hemoglobina entre 10 y 12 g/dl, ya que una concentración alta de hemoglobina puede aumentar el riesgo de coágulos sanguíneos y de muerte.
- La dosis de inicio es de 150 UI/kg de peso corporal 3 veces por semana o de 450 UI/kg de peso corporal una vez por semana.
- Retacrit se administra por inyección debajo de la piel.
- Su médico solicitará análisis de sangre y puede ajustar la dosis, dependiendo de cómo responda su anemia al tratamiento con Retacrit.
- Puede que se le administren suplementos de hierro antes del tratamiento con Retacrit y durante el mismo a fin de aumentar su eficacia.
- Normalmente seguirá recibiendo el tratamiento con Retacrit durante un mes tras finalizar la quimioterapia.
Adultos donantes de su propia sangre
- La dosis habituales de 600 UI/kg de peso corporal 2 veces por semana.
- Retacrit se administra mediante una inyección en una vena inmediatamente después de haber donado sangre durante tres semanas antes de la cirugía.
- Puede que se le administren suplementos de hierro antes del tratamiento con Retacrit y durante el mismo a fin de aumentar su eficacia.
Adultos programados para una cirugía ortopédica mayor
- La dosis recomendadaes de 600 UI/kg de peso corporal una vez por semana.
- Retacrit se administra mediante una inyección debajo de la piel durante tres semanas antes de la cirugía y el día de la cirugía.
- En casos en los que se necesita reducir el tiempo previo a la operación, se le administrará una dosis diaria de 300 UI/kg durante un máximo de 10 días antes de la cirugía, el día de la cirugía y durante cuatro días inmediatamente después.
- Si los análisis de sangre muestran un nivel de hemoglobina demasiado alto antes de la operación, se interrumpirá el tratamiento.
- Puede que se le administren suplementos de hierro antes del tratamiento con Retacrit y durante el mismo a fin de aumentar su eficacia.
Adultos con síndrome mielodisplásico
- Su médico puede iniciar el tratamiento con Retacrit si su concentración de hemoglobina es igual o inferior a 10 g/dl. El objetivo del tratamiento es mantener el nivel de hemoglobina entre 10 y 12 g/dl ya que un nivel de hemoglobina más alto puede aumentar el riesgo de coágulos sanguíneos y la muerte.
- Retacrit se administra por inyección debajo de la piel.
- La dosis de inicio es de 450 UI por kilogramo de peso corporal una vez a la semana.
- Su médico le pedirá análisis de sangre y puede ajustar la dosis, dependiendo de cómo responda su anemia al tratamiento con Retacrit.
Instrucciones sobre cómo inyectarse Retacrit
Cuando se inicia el tratamiento, el personal médico o de enfermería suele inyectar Retacrit. Más tarde, su médico puede proponer que usted o su cuidador aprendan a inyectar Retacrit bajo la piel (por vía subcutánea) por sí mismos.
- No intente inyectarse a no ser que su médico o enfermero le hayan enseñado cómo hacerlo.
- Siga exactamente las instrucciones de administración de Retacrit indicadas por su médico o enfermero.
- Solo use Retacrit si se ha conservado correctamente; ver sección5,Conservación de Retacrit.
- Antes del uso, deje reposar la jeringa de Retacrit hasta que alcance la temperatura ambiente. Esto suele llevar entre 15 y 30minutos.
Use solo una dosis de Retacrit de cada jeringa.
Si Retacrit se inyecta bajo la piel (vía subcutánea), la cantidad inyectada no es normalmente más de 1 mililitro (1 ml) en una sola inyección. En caso de volúmenes mayores, se debe elegir más de un lugar para la inyección.
Retacrit se administra sólo y no se mezcla con otros líquidos para inyección.
No agite las jeringas de Retacrit.Una agitación vigorosa prolongada puede dañar el producto. Si el producto ha sido sacudido con fuerza, no lo use.
Cómo inyectarse usted mismo utilizando una jeringa precargada
- Saque el envase con la jeringa precargada de la nevera.
- Saque el blíster con la jeringa precargada del envase. Cuando el envase contenga blísteres con más de una jeringa precargada, corte el blíster con una jeringa precargada a lo largo de la parte perforada, devuelva el resto de los blísteres con jeringas precargadas al envase y retorne el envase a la nevera.
- Abra el blister con la jeringa precargada después de sacarlo de la nevera. El líquido debe alcanzar la temperatura ambiente. Noretire la cubierta de la aguja de la jeringa mientras deja que la jeringa precargada alcance la temperatura ambiente.

- Revise la jeringa, para asegurarse de que es la dosis correcta, no ha pasado su fecha de caducidad, no está dañado, y el líquido es claro y sin congelar.
- No utilice la jeringa precargada si:
- El envase está abierto o dañado.
- El medicamento está turbio o ha cambiado de color o el líquido tiene partículas flotando en él.
- Alguna parte de la jeringa precargada aparece agrietada o rota o se ha salido el líquido de la jeringa.
- La jeringa precargada se ha caído. La jeringa precargada puede estar rota incluso si no puede ver la rotura.
- Falta la cubierta de la aguja o no está bien colocada.
- La fecha de caducidad impresa en la etiqueta ha pasado.
En todos los casos anteriores, deseche la jeringa precargada y utilice una jeringa precargada nueva.
- Elija un lugar de inyección. Los buenos sitios son la parte superior del muslo y alrededor de la barriga (abdomen) pero lejos del ombligo. Varíe el sitio día a día.
- Lávese las manos. Use un hisopo de antiséptico en el lugar de la inyección, para desinfectarla.
- Sostenga la jeringa precargada por el cuerpo de la jeringa con la aguja cubierta apuntando hacia arriba.
- Nola sostenga por la cabeza del émbolo, émbolo o cubierta de la aguja.
- Notire del émbolo en ningún momento.
- Noretire la cubierta de la aguja de la jeringa precargada hasta que esté listo para inyectar su medicamento.
- Retire la cubierta de la aguja de la jeringa sosteniendo el cuerpo de la jeringa y tire de la cubierta de la aguja hacia afuera y lejos de su cuerpo con cuidado, sin girarla. Deseche la cubierta de la aguja. Novuelva a tapar la aguja. Noempuje el émbolo, toque la aguja ni agite la jeringa.
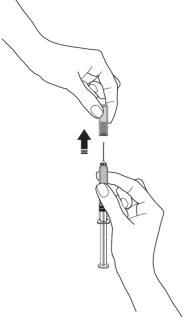
- Pellizque un pliegue de piel entre el pulgar y el dedo índice. Nola comprima.
- Con la otra mano, sostenga la jeringa precargada como si fuera un lápiz. Utilice un movimiento rápido de “dardo” para insertar la aguja en un ángulo aproximado de 45 grados en la piel.
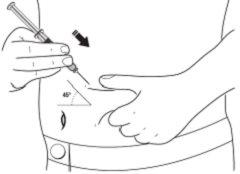
- Introducir la aguja en su totalidad. Su médico o enfermera le han mostrado cómo hacer esto.
- Empuje el émbolo con el pulgar en la medida de lo que pueda para inyectar toda la cantidad de líquido. Empuje lenta y regularmente, manteniendo el pliegue cutáneo pellizcado.
- Cuando el émbolo haya llegado al final, saque la aguja y suelte la piel.
- Cuando la aguja se extrae de la piel, puede haber un poco de sangrado en el sitio de inyección. Esto es normal. Puede presionar un hisopo antiséptico sobre el sitio de la inyección durante unos segundos después de la inyección.
- Nointente volver a colocar la cubierta de la aguja. Deshágase de la jeringa usada en un recipiente para objetos punzocortantes (a prueba de pinchazos).
- Nunca ponga las jeringas usadas en el contenedor de basura doméstica normal
Cómo inyectarse usted mismo utilizando una jeringa precargada conmecanismo de protecciónde la aguja
Su jeringa precargada tiene un mecanismo de protección de la aguja adjunto para protegerle de una herida por pinchazo de la aguja.
- Saque el envase con la jeringa precargada con mecanismo de protección de la aguja de la nevera.
- Saque el blíster con la jeringa precargada del envase. Cuando el envase contenga blísteres con más de una jeringa precargada, corte el blíster con una jeringa precargada a lo largo de la parte perforada, devuelva el resto de los blísteres con jeringas precargadas al envase y retorne el envase a la nevera.
- Abra el blíster con la jeringa precargada quitando la tapa del blíster.
- Saque la jeringa precargada del blíster cogiéndola por el cuerpo de la jeringa.
- Noagarre la cubierta gris de la aguja ni el émbolo.
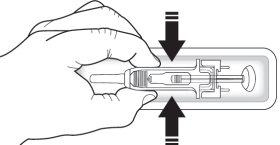
- Verifique la jeringa para asegurarse de que el mecanismo de protección de la aguja cubra el cuerpo de la jeringa precargada. Noempuje el mecanismo de protección de la aguja sobre la cubierta de la aguja antes de la inyección. Esto puede activar o bloquear el mecanismo de protección de la aguja. Si el mecanismo de protección de la aguja cubre la aguja, significa que se ha activado.
- El líquido debe alcanzar la temperatura ambiente. Noretire la cubierta de la aguja de la jeringa mientras deja que la jeringa precargada alcance la temperatura ambiente.
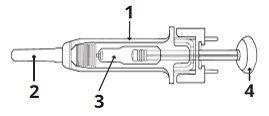
1 | Mecanismo de protección de la aguja |
2 | Cubierta de la aguja |
3 | Medicamento |
4 | Émbolo |
- Revise la jeringa, para asegurarse de que es la dosis correcta, no ha pasado su fecha de caducidad, no está dañado, y el líquido es claro y sin congelar.
- No utilice la jeringa precargada si:
- El envase de cartón está abierto o dañado.
- Falta el mecanismo de protección de la aguja, se ha desprendido o se ha activado.
- El medicamento está turbio o ha cambiado de color o el líquido tiene partículas flotando en él. Noinspeccione el producto a través del plástico del dispositivo de seguridad.
- Alguna parte de la jeringa precargada aparece agrietada o rota o se ha salido líquido de la jeringa.
- La jeringa precargada se ha caído. La jeringa precargada puede estar rota incluso si no puede ver la rotura.
- Falta la cubierta de la aguja o no está bien colocada.
- La fecha de caducidad impresa en la etiqueta ha pasado.
En todos los casos anteriores, deseche la jeringa precargada y utilice una jeringa precargada nueva.
- Elija un lugar de inyección. Los buenos sitios son la parte superior del muslo y alrededor de la barriga (abdomen) pero lejos del ombligo. Varíe el sitio día a día.
- Lávese las manos. Use un hisopo de antiséptico en el lugar de la inyección, para desinfectarla.
- Sostenga la jeringa precargada por el cuerpo del mecanismo de protección de la aguja con la aguja cubierta apuntando hacia arriba.
- Nola sostenga por la cabeza del émbolo, émbolo o cubierta de la aguja.
- Notire del émbolo en ningún momento.
- Noretire la cubierta de la aguja de la jeringa precargada hasta que esté listo para inyectar su medicamento.
- Retire la cubierta de la aguja de la jeringa sosteniendo el cuerpo de la jeringa y tire de la cubierta de la aguja con cuidado, sin girarla. Deseche la cubierta de la aguja. Novuelva a tapar la aguja. Noempuje el émbolo, toque la aguja ni agite la jeringa.
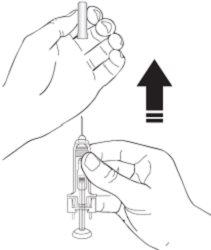
- Pellizque un pliegue de piel entre el pulgar y el dedo índice. Nola comprima.
- Con la otra mano, sostenga la jeringa precargada como si fuera un lápiz. Utilice un movimiento rápido de “dardo” para insertar la aguja en un ángulo aproximado de 45 grados en la piel.
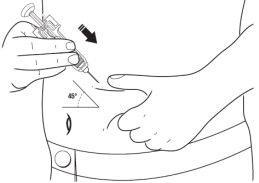
- Introducir la aguja en su totalidad. Su médico o enfermera le han mostrado cómo hacer esto.
- Presionar el émbolo mientras sujeta el collarín con los dedos hasta que se haya administrado la dosis completa. La protección de la aguja NO se activará a menos que la dosis se haya administrado en su TOTALIDAD.
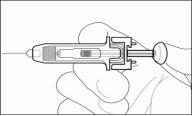 .
.
- Cuando el émbolo haya llegado al final, saque la aguja y suelte la piel.
- Suelte el émbolo y permita a la jeringa que se mueva hacia arriba hasta que toda la aguja esté guardada y bloqueada en su sitio.
- Cuando la aguja se extrae de la piel, puede haber un poco de sangrado en el sitio de inyección. Esto es normal. Puede presionar un hisopo antiséptico sobre el sitio de la inyección durante unos segundos después de la inyección.
- Nointente volver a colocar la cubierta de la aguja. Deshágase de la jeringa usada en un recipiente para objetos punzocortantes (a prueba de pinchazos).
- Nunca ponga las jeringas usadas en el contenedor de basura doméstica normal.
Cómo inyectarse usted mismo utilizando unajeringa precargada con protector para atrapar la aguja (trampa para la aguja)
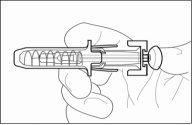
Su jeringa tiene adjunto un protector para atrapar la aguja (trampa para la aguja), que está diseñado específicamente para ayudar a prevenir las lesiones accidentales después de la correcta administración de medicamentos inyectables. Se compone de un dispositivo de plásticoque bloquea la aguja y que está firmemente unido a la etiqueta de la jeringa. Juntos, estos dos componentes, realizan la función detrampa para la aguja (seguridad).
El protector bloqueante de plástico sujeto a la etiqueta de la jeringa requiere acciones específicas por parte del usuario para "activarlo", lo que hará a la aguja inofensiva después de administrar la inyección:
- Saque el envase con la jeringa precargada de la nevera.
- Saque el blíster con la jeringa precargada del envase. Cuando el envase contenga blísteres con más de una jeringa precargada, corte el blíster con una jeringa precargada a lo largo de la parte perforada, devuelva el resto de los blísteres con jeringas precargadas al envase y retorne el envase a la nevera.
- Abra el blíster con la jeringa precargada con trampa para la aguja quitando la cubierta después de sacarla de la nevera.
- Sujete el cuerpo de la jeringa para extraer la jeringa precargada del blíster.
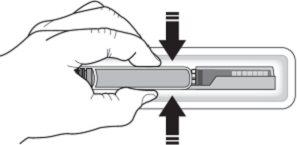
- Noretire la cubierta de la aguja de la jeringa precargada hasta que esté listo para inyectar su medicamento.
- El líquido debe alcanzar la temperatura ambiente. Noretire la cubierta de la aguja de la jeringa mientras deja que la jeringa precargada alcance la temperatura ambiente.
- Revise la jeringa, para asegurarse de que es la dosis correcta, no ha pasado su fecha de caducidad, no está dañado, y el líquido es claro y sin congelar.
- No utilice la jeringa precargada si:
- El envase está abierto o dañado.
- El medicamento está turbio o ha cambiado de color o el líquido tiene partículas flotando en él.
- Alguna parte de la jeringa precargada aparece agrietada o rota o se ha salido líquido de la jeringa.
- La jeringa precargada se ha caído. La jeringa precargada puede estar rota incluso si no puede ver la rotura.
- Falta la cubierta de la aguja o no está bien colocada.
- La fecha de caducidad impresa en la etiqueta ha pasado.
En todos los casos anteriores, deseche la jeringa precargada y utilice una jeringa precargada nueva.
- Elija un lugar de inyección. Los buenos sitios son la parte superior del muslo y alrededor de la barriga (abdomen) pero lejos del ombligo. Varíe el sitio día a día.
- Lávese las manos. Use un hisopo de antiséptico en el lugar de la inyección, para desinfectarla.
- Sostenga la jeringa precargada por el cuerpo de la jeringa con la aguja cubierta apuntando hacia arriba.
- Nola sostenga por la cabeza del émbolo, émbolo o cubierta de la aguja.
- Notire del émbolo en ningún momento.
- Agarre la punta de la aguja de plástico y aléjela de la cubierta de la aguja.

- Noquite la tapa de la aguja de la jeringa precargada hasta que esté listo para inyectarse el medicamento.
- Retire la cubierta de la aguja de la jeringa sosteniendo el cuerpo de la jeringa y tire de la cubierta de la aguja con cuidado, sin girarla. Deseche la cubierta de la aguja. Novuelva a tapar la aguja. Noempuje el émbolo, toque la aguja ni agite la jeringa.
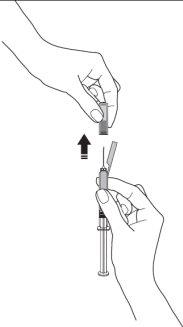
- Pellizque un pliegue de piel entre el pulgar y el dedo índice. Nola comprima.
- Con la otra mano, sostenga la jeringa precargada como si fuera un lápiz. Utilice un movimiento rápido de “dardo” para insertar la aguja en un ángulo aproximado de 45 grados en la piel.
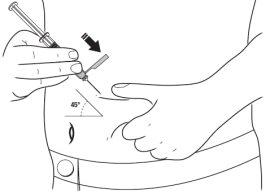
- Introducir la aguja en su totalidad. Su médico o enfermera le han mostrado cómo hacer esto.
- Empuje el émbolo con su dedo pulgar tanto como pueda e inyecte la totalidad del líquido. Empuje suavemente de manera uniforme, manteniendo el pliegue de la piel pellizcada
- Cuando el émbolo no de más de sí, saque la aguja y retírela de la piel.
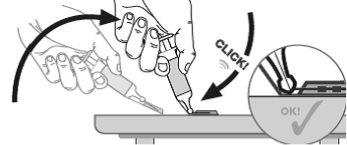
- Colocar trampa para la aguja sobre una superficie dura, estable y con una mano dé un giro del cilindro de la jeringa hacia arriba contra la aguja forzando la aguja hacia la trampa, donde quedará bloqueada (un audible click se escucha cuando la aguja esté bloquada en la trampa). Continuar doblando la aguja de la jeringa hasta que supere un ángulo de 45 grados con la superficie plana para que esté definitivamente fuera de uso.
- Cuando la aguja se extrae de la piel, puede haber un poco de sangrado en el sitio de inyección. Esto es normal. Puede presionar un hisopo antiséptico sobre el sitio de la inyección durante unos segundos después de la inyección.
- Nointente volver a colocar la cubierta de la aguja. Deshágase de la jeringa usada en un recipiente para objetos punzocortantes (a prueba de pinchazos).
- Nunca ponga las jeringas usadas en el contenedor de basura doméstica normal.
Si usa más Retacrit del que debe
Informe inmediatamente al médico o al enfermero si piensa que se le ha inyectado demasiado Retacrit. Es poco probable que se produzcan efectos adversos como consecuencia de una sobredosis de Retacrit.
Si olvidó usar Retacrit
Póngase la siguiente inyección tan pronto como se acuerde. Si queda menos de un día para la siguiente inyección, prescinda de la dosis omitida y continúe con su programa habitual. No duplique las inyecciones para compensar las dosis olvidadas.
Si es un paciente con hepatitisC que recibe interferón y ribavirina
Debe comentarlo con su médico porque, en raras ocasiones, la combinación de epoetina zeta con interferón y ribavirina ha producido una pérdida de efecto y la aparición de una enfermedad denominada aplasia pura de células rojas (APCR), una forma grave de anemia. Retacrit no está aprobado en el tratamiento de la anemia asociada a hepatitis C.
Si tiene cualquier otra duda sobre el uso de este medicamento, pregunte a su médico, farmacéutico o enfermero.
4. Posibles efectos adversos
Al igual que todos los medicamentos, este medicamento puede producir efectos adversos, aunque no todas las personas los sufran.
Informe a su médico o enfermera inmediatamentesi experimenta cualquiera de los efectos mencionados en la siguiente lista.
Se han observado erupciones cutáneas graves, como síndrome de Stevens-Johnson y necrólisis epidérmica tóxica, con la administración de epoetinas. Estas reacciones pueden aparecer como máculas o manchas circulares de color rojo, a menudo con ampollas centrales en el tronco, descamación de la piel y úlceras en la boca, garganta, nariz, genitales y ojos y que pueden ir precedidas de fiebre y síntomas de tipo gripal. Deje de usar Retacrit si presenta estos síntomas y póngase en contacto con su médico o solicite atención médica de inmediato. Ver también la sección 2.
Muy frecuentes: pueden afectar a más de 1 de cada 10 personas.
- Diarrea
- Malestar de estómago
- Vómitos
- Fiebre
- En pacientes con insuficiencia renal que aún no se han sometido a diálisis se ha comunicado congestión en el tracto respiratorio, tales como, congestión nasal y dolor de garganta.
Frecuentes: pueden afectar hasta 1 de cada 10 personas.
- Aumento de la tensión arterial. Los dolores de cabeza, especialmente repentinos, punzantes y de tipo migrañoso, la sensación de confusión o las convulsionespueden ser signos de un aumento repentino de la tensión arterial. Esto necesita tratamiento urgente. Este aumento puede precisar tratamiento con medicamentos (o el ajuste de la dosificación de los medicamentos que ya esté tomando para la hipertensión arterial).
- Coágulos de sangre(incluyendo trombosis venosa profunda y embolia) que pueden necesitar tratamiento urgente. Puede presentar dolor en el pecho, dificultad para respirar e inflamación dolorosa y enrojecimiento, normalmente en una pierna.
- Tos.
- Picores en la piel, que pueden resultar de una reacción alérgica.
- Dolor de huesos o músculos
- Síntomas de tipo gripal, como dolor de cabeza, pinchazos y dolores en las articulaciones, sensación de debilidad, escalofríos, cansancio y mareo. Pueden ser más frecuentes al inicio del tratamiento. Si presenta estos síntomas durante la inyección intravenosa, una administración más lenta de la inyección puede ayudar a evitar que ocurran nuevamente.
- Enrojecimiento, ardor y dolor en el lugar de la inyección
- Hinchazón de los tobillos, los pies o los dedos
- Dolor de brazo o pierna
Poco frecuentes: pueden afectar hasta 1cada 100 personas.
- Niveles altos de potasio en la sangreque pueden causar un ritmo cardíaco anormal (este es un efecto secundario muy común en pacientes en diálisis).
- Temblores
- Congestión de nariz o vía aérea
- Reacción alérgica
- Ronchas cutáneas (habones)
Raros: pueden afectar hasta 1 de cada 1.000 personas.
- Síntomas de aplasia pura de células rojas (APCR).
La APCR es la incapacidad para producir suficientes glóbulos rojos en la médula ósea. La APCR puede provocar una anemia repentina y grave.Los síntomas son:
- Cansancio inusual,
- Sensación de mareo,
- Dificultad para respirar.
Se han notificado casos muy raros de APCR principalmente en pacientes con enfermedad renal después de meses o años de tratamiento con Retacrit y otros productos que estimulan la producción de glóbulos rojos.
- Se puede producir un aumento de la cantidad de unas células sanguíneas pequeñas (llamadas plaquetas) que normalmente participan en la formación de los coágulos de sangre, especialmente cuando se inicia el tratamiento. Su médico lo comprobará.
- Reacciones alérgicas graves que pueden incluir:
- cara, labios, boca, lengua o garganta hinchada;
- dificultad para tragar o respirar;
- erupción con picor (habones).
- Trastorno que afecta a la sangre que puede causar dolor, orina con color oscuro o aumento de la sensibilidad en la piel a la luz solar (porfiria).
Si está recibiendo hemodiálisis:
- Se pueden formar coágulos de sangre(trombosis) en la fístula de la diálisis. Esto es más frecuente si tiene la tensión arterial baja o si su fístula presenta complicaciones.
- También se pueden formar coágulos de sangreen su sistema de hemodiálisis. Su médico puede decidir aumentar su dosis de heparina durante la diálisis.
Si padece alguno de estos efectos o si observa cualquier otro efecto mientras esté en tratamiento con Retacrit, comuníqueselo inmediatamente a su médico o enfermero.
Comunicación de efectos adversos
Si experimenta cualquier tipo de efecto adverso, consulte a su médico, farmacéutico o enfermero, incluso si se trata de posibles efectos adversos que no aparecen en este prospecto. También puede comunicarlos directamente a través del Sistema Español de Farmacovigilancia de Medicamentos de Uso Humano: www.notificaRAM.es. Mediante la comunicación de efectos adversos usted puede contribuir a proporcionar más información sobre la seguridad de este medicamento.
5. Conservación de Retacrit
Mantener este medicamento fuera de la vista y del alcance de los niños.
No utilice este medicamento después de la fecha de caducidad que aparece en la caja y la etiqueta después de “EXP”. La fecha de caducidad es el último día del mes que se indica.
Conservar en nevera (2°C‑8°C). Puede sacar Retacrit de la nevera y mantenerlo a temperatura ambiente (hasta 25 °C) durante un periodo máximo de 3 días. Una vez que una jeringa se haya extraído de la nevera y haya alcanzado la temperatura ambiente (hasta 25 °C), se debe utilizar en un plazo de tres días o desecharse.
No congelar ni agitar.
Conservar en el embalaje exterior para protegerlo de la luz.
No utilice este medicamento si observa que el precinto está roto o si el líquido tiene color o pueden verse partículas flotando en él. Si observa alguna de estas situaciones, deseche el medicamento.
Los medicamentos no se deben tirar por los desagües ni a la basura. Pregunte a su farmacéutico cómo deshacerse de los envases y de los medicamentos que ya no necesita. De esta forma, ayudará a proteger el medio ambiente.
6. Contenido del envase e información adicional
Composición de Retacrit
El principio activo es epoetina zeta (producida mediante tecnología de ADN recombinante en líneas celulares de ovarios de hámster china).
Retacrit 1 000UI/0,3ml solución inyectable en jeringa precargada
1 jeringa precargada con 0,3 ml de solución inyectable contiene 1 000 unidades internacionales (UI) de epoetina zeta (eritropoyetina recombinante humana). La solución contiene 3 333 UI de epoetina zeta por ml.
Retacrit 2 000UI/0,6ml solución inyectable en jeringa precargada
1 jeringa precargada con 0,6 ml de solución inyectable contiene 2 000 unidades internacionales (UI) de epoetina zeta (eritropoyetina recombinante humana). La solución contiene 3 333 UI de epoetina zeta por ml.
Retacrit 3 000UI/0,9ml solución inyectable en jeringa precargada
1 jeringa precargada con 0,9 ml de solución inyectable contiene 3 000 unidades internacionales (UI) de epoetina zeta (eritropoyetina recombinante humana). La solución contiene 3 333 UI de epoetina zeta por ml.
Retacrit 4 000UI/0,4ml solución inyectable en jeringa precargada
1 jeringa precargada con 0,4 ml de solución inyectable contiene 4 000 unidades internacionales (UI) de epoetina zeta (eritropoyetina recombinante humana). La solución contiene 10 000 UI de epoetina zeta por ml.
Retacrit 5 000UI/0,5ml solución inyectable en jeringa precargada
1 jeringa precargada con 0,5 ml de solución inyectable contiene 5 000 unidades internacionales (UI) de epoetina zeta (eritropoyetina recombinante humana). La solución contiene 10 000 UI de epoetina zeta por ml.
Retacrit 6 000UI/0,6ml solución inyectable en jeringa precargada
1 jeringa precargada con 0,6 ml de solución inyectable contiene 6 000 unidades internacionales (UI) de epoetina zeta (eritropoyetina recombinante humana). La solución contiene 10 000 UI de epoetina zeta por ml.
Retacrit 8 000UI/0,8ml solución inyectable en jeringa precargada
1 jeringa precargada con 0,8 ml de solución inyectable contiene 8 000 unidades internacionales (UI) de epoetina zeta (eritropoyetina recombinante humana). La solución contiene 10 000 UI de epoetina zeta por ml.
Retacrit 10000UI/1ml solución inyectable en jeringa precargada
1 jeringa precargada con 1 ml de solución inyectable contiene 10 000 unidades internacionales (UI) de epoetina zeta (eritropoyetina recombinante humana). La solución contiene 10 000 UI de epoetina zeta por ml.
Retacrit 20000UI/0,5ml solución inyectable en jeringa precargada
1 jeringa precargada con 0,5 ml de solución inyectable contiene 20 000 unidades internacionales (UI) de epoetina zeta (eritropoyetina recombinante humana). La solución contiene 40 000 UI de epoetina zeta por ml.
Retacrit 30000UI/0,75ml solución inyectable en jeringa precargada
1 jeringa precargada con 0,75 ml de solución inyectable contiene 30 000 unidades internacionales (UI) de epoetina zeta (eritropoyetina recombinante humana). La solución contiene 40 000 UI de epoetina zeta por ml.
Retacrit 40000UI/1ml solución inyectable en jeringa precargada
1 jeringa precargada con 1 ml de solución inyectable contiene 40 000 unidades internacionales (UI) de epoetina zeta (eritropoyetina recombinante humana). La solución contiene 40 000 UI de epoetina zeta por ml.
Los demás componentes son fosfato dihidrógeno de sodio dihidratado, fosfato de sodio dihidratado, cloruro de sodio (ver sección 2 “Retacrit contiene sodio”), cloruro de calcio dihidratado, polisorbato 20, glicina, leucina, isoleucina, treonina, ácido glutámico, fenilalanina (ver sección 2 “Retacrit contiene fenilalanina”), agua para preparaciones inyectables, hidróxido de sodio (para el ajuste de pH), ácido clorhídrico (para el ajuste de pH).
Aspecto del producto y contenido del envase
Retacrit es una solución inyectable transparente e incolora que se presenta en jeringas de vidrio transparente con una aguja de inyección fija.
Las jeringas precargadas contienen entre 0,3 y 1 ml de solución, dependiendo del contenido de epoetina zeta (ver «Composición de Retacrit»).
Cada paquete incluye 1, 4 o 6 jeringas precargadas con o sin protector de seguridad para la aguja o con protector bloqueante de plástico sujeto a la etiqueta de la jeringa.
Los paquetes multienvases contienen 4 (4 envases de 1) o 6 (6 envases de 1) jeringas precargadas
Titular de la autorización de comercialización
Pfizer Europe MA EEIG
Boulevard de la Plaine 17
1050 Bruxelles
Bélgica
Responsables de la fabricación
Hospira Zagreb d.o.o.
Prudnicka cesta 60
10291 Prigorje Brdovecko
Croacia
Pueden solicitar más información respecto a este medicamento dirigiéndose al representante local del titular de la autorización de comercialización:
España
Pfizer, S.L.
Tel: +34 91 490 99 00
Fecha de la última revisión de este prospecto: 07/2023.
La información detallada de este medicamento está disponible en la página web de la Agencia Europea del Medicamentos: http://www.ema.europa.eu.
- País de registro
- Principio activo
- Requiere recetaSí
- Fabricante
- Esta información es de carácter general y no sustituye la consulta con un profesional sanitario.
- Alternativas a RETACRIT 4000 UI/0,4 ml SOLUCION INYECTABLE EN JERINGA PRECARGADAForma farmacéutica: INYECTABLE, 20000 UIPrincipio activo: erythropoietinFabricante: Sandoz GmbhRequiere recetaForma farmacéutica: INYECTABLE, 20 kilo UIPrincipio activo: erythropoietinFabricante: Sandoz GmbhRequiere recetaForma farmacéutica: INYECTABLE, 40.000 UI/ml de epoyetina alfaPrincipio activo: erythropoietinFabricante: Sandoz GmbhRequiere receta
Médicos online para RETACRIT 4000 UI/0,4 ml SOLUCION INYECTABLE EN JERINGA PRECARGADA
Comenta la dosis, los posibles efectos secundarios, interacciones, contraindicaciones o la revisión de receta de RETACRIT 4000 UI/0,4 ml SOLUCION INYECTABLE EN JERINGA PRECARGADA, sujeto a valoración médica y a la normativa local.
Preguntas frecuentes















