
REFACTO AF 1000 UI POLVO Y DISOLVENTE PARA SOLUCION INYECTABLE EN JERINGA PRECARGADA

Cómo usar REFACTO AF 1000 UI POLVO Y DISOLVENTE PARA SOLUCION INYECTABLE EN JERINGA PRECARGADA
Traducción generada por IA
Este contenido ha sido traducido automáticamente y se ofrece solo con fines informativos. No sustituye la consulta con un profesional sanitario.
Ver originalContenido del prospecto
Introducción
Prospecto: información para el usuario
ReFacto AF 250UI polvo y disolvente para solución inyectable en jeringa precargada
ReFacto AF 500UI polvo y disolvente para solución inyectable en jeringa precargada
ReFacto AF 1000UI polvo y disolvente para solución inyectable en jeringa precargada
ReFacto AF 2000UI polvo y disolvente para solución inyectable en jeringa precargada
ReFacto AF 3000 UI polvo y disolvente para solución inyectable en jeringa precargada
moroctocog alfa (factor de coagulación VIII humano recombinante)
Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene información importante para usted.
- Conserve este prospecto, ya que puede tener que volver a leerlo.
- Si tiene alguna duda, consulte a su médico o farmacéutico.
- Este medicamento se le ha recetado solamente a usted, y no debe dárselo a otras personas aunque tengan los mismos síntomas que usted, ya que puede perjudicarles.
- Si experimenta efectos adversos, consulte a su médico o farmacéutico, incluso si se trata de efectos adversos que no aparecen en este prospecto. Ver sección 4.
Contenido del prospecto:
- Qué es ReFacto AF y para qué se utiliza
- Qué necesita saber antes de empezar a usar ReFacto AF
- Cómo usar ReFacto AF
- Posibles efectos adversos
- Conservación de ReFacto AF
- Contenido del envase e información adicional
1. Qué es ReFacto AF y para qué se utiliza
ReFacto AF contiene el principio activo moroctocog alfa, factor de coagulación VIII humano. El factor VIII es necesario para que la sangre forme coágulos y detenga las hemorragias. En los pacientes con hemofilia A (deficiencia del factor VIII de nacimiento) no está presente o no actúa adecuadamente.
ReFacto AF se utiliza para el tratamiento y la prevención (profilaxis) de episodios hemorrágicos en adultos y niños de todas las edades (incluidos recién nacidos) con hemofilia A.
2. Qué necesita saber antes de empezar a usar ReFacto AF
No use ReFacto AF
- si es alérgico a moroctocog alfa o a alguno de los demás componentes de este medicamento (incluidos en la sección 6);
- si es alérgico a las proteínas de hámster.
Consulte a su médico si tiene dudas.
Advertencias y precauciones
Consulte a su médico o farmacéutico antes de empezar a usar ReFacto AF
- si sufre reacciones alérgicas. Algunos de los signos de las reacciones alérgicas son dificultad para respirar, falta de aliento, hinchazón, urticaria, picores, opresión torácica, silbidos al respirar y tensión arterial baja. La anafilaxia es una reacción alérgica grave que produce dificultad para tragar o para respirar, enrojecimiento o hinchazón de las manos, de la cara o de ambas. Si se presenta alguno de esos síntomas, interrumpa la perfusión inmediatamente y póngase en contacto con su médico o busque asistencia médica de urgencias inmediata. En casos de reacciones alérgicas graves se debe plantear tratamiento alternativo.
- la formación de inhibidores (anticuerpos) es una complicación conocida que puede producirse durante el tratamiento con todos los medicamentos compuestos por factor VIII. Estos inhibidores, especialmente en niveles elevados, impiden que el tratamiento funcione correctamente, por lo que se les supervisará cuidadosamente a usted o a su hijo por si desarrollan dichos inhibidores. Si su hemorragia o la de su hijo no se está controlando con ReFacto AF, consulte a su médico inmediatamente.
- si su hemorragia no se detiene como cabría esperar póngase en contacto con su médico o busque asistencia médica de urgencia inmediatamente.
Otros medicamentos y ReFacto AF
Informe a su médico o farmacéutico si está utilizando, ha utilizado recientemente o pudiera tener que utilizar cualquier otro medicamento.
Embarazo,lactancia y fertilidad
Si está embarazada o en periodo de lactancia, cree que podría estar embarazada o tiene intención de quedarse embarazada, consulte a su médico o farmacéutico antes de utilizar este medicamento
Conducción y uso de máquinas
La influencia de ReFacto AF sobre la capacidad para conducir y utilizar máquinas es nula.
ReFacto AF contiene sodio
Tras la reconstitución, ReFacto AF contiene 1,27 mmol (ó 29 mg) de sodio (componente principal de la sal de mesa/para cocinar) por jeringa precargada. Esto equivale al 1,5% de la ingesta diaria máximo de sodio recomendada para un adulto. Según su peso corporal y su dosis de ReFacto AF, podría recibir múltiples jeringas precargadas. Esto se debe tener en cuenta si usted sigue una dieta baja en sal.
3. Cómo usar ReFacto AF
Siga exactamente las instrucciones de administración de este medicamento indicadas por su médico. En caso de duda, consulte de nuevo a su médico o farmacéutico.
El tratamiento con ReFacto AF debe ser iniciado por un médico con experiencia en el tratamiento de pacientes con hemofilia A. Su médico decidirá la dosis de ReFacto AF que debe recibir. Esta dosis y su duración dependerán de sus necesidades individuales de tratamiento sustitutivo con factor VIII. ReFacto AF se administra mediante inyección en una vena y dicha inyección dura varios minutos. Las inyecciones de ReFacto AF pueden ser administradas por los pacientes o por sus cuidadores, siempre que hayan recibido la formación adecuada.
Durante su tratamiento su médico puede modificar la dosis de ReFacto AF que usted recibe.
Consulte con su médico antes de viajar. Cuando viaje debe llevar su producto de factor VIII en cantidad suficiente para el tratamiento previsto.
Se recomienda que cada vez que se administre ReFacto AF registre el nombre que figura en el envase y el número de lote del producto. Puede pegar una de las etiquetas despegables que se encuentran en la jeringa precargada para documentar el número del lote en su diario o para notificar cualquier efecto secundario.
Reconstitución y administración
Las instrucciones facilitadas a continuación son una guía para la reconstitución y administración de ReFacto AF suministrado en jeringa precargada. Los pacientes deben seguir las instrucciones de reconstitución y administración específicas indicadas por sus médicos.
ReFacto AF se administra por perfusión intravenosa (IV) después de la reconstitución. La jeringa precargada está formada por dos cámaras, una cámara contiene el polvo liofilizado de ReFacto AF y la otra cámara contiene el disolvente [solución de cloruro sódico de 9 mg/ml (0,9%)]. A lo largo de estas instrucciones, se hará referencia a este dispositivo como jeringa precargada.
Para la reconstitución utilice sólo la jeringa precargada que se encuentra en el envase. Para la administración se pueden utilizar otras jeringas estériles desechables.
No se debe mezclar ReFacto AF con otras soluciones de perfusión.
Nota: Si necesita utilizar más de una jeringa precargada de ReFacto AF por perfusión, cada jeringa debe ser reconstituida de acuerdo a las instrucciones específicas. Para sacar el contenido reconstituido de cada jeringa, se puede utilizar una jeringa de 10 cc o una jeringa más grande con cierre luer (no incluida en este kit) (consultar las Instrucciones Adicionales).
Preparación
- Lávese siempre las manos antes de realizar los siguientes procedimientos.
- Durante el procedimiento de reconstitución debe seguirse una técnica aséptica (es decir, limpia y libre de gérmenes).
- Para minimizar la exposición al aire, todos los componentes utilizados en la reconstitución y administración de este producto deben utilizarse lo antes posible después de la apertura del envase estéril.
Reconstitución
- Deje que la jeringa precargada alcance la temperatura ambiente.
- Extraiga los componentes del kit de la jeringa precargada de ReFacto AF y deposítelos en una superficie limpia, y asegúrese de que tiene todos los materiales que va a necesitar.
- Sujete el émbolo como se muestra en el diagrama. Enrosque firmemente el émbolo en la apertura de la jeringa precargada de ReFacto AF, empujando y enroscando en el sentido de las agujas del reloj hasta notar resistencia (aproximadamente 2 giros).
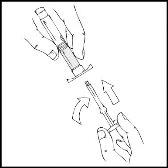
Durante el proceso de reconstitución, es importante mantener la jeringa precargada de ReFacto AF en posición vertical (con el polvo blanco encima de la solución clara) para prevenir posibles fugas.
- Sujetando la jeringa precargada en posición vertical, quite el precinto blanco de seguridad doblando el precinto de izquierda a derecha (o mediante un movimiento cuidadoso de balanceo) para romper la perforación del tapón y dejar descubierto el tapón de goma gris de la jeringa precargada de ReFacto AF.
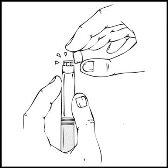
- Retire el tapón azul estéril de ventilación de su envase.
Mientras sujeta la jeringa precargada de ReFacto AF en posición vertical, retire el tapón de goma gris y sustitúyalo con el tapón de protección azul para ventilación. Este tapón de ventilación tiene pequeños orificios que permiten que el aire escape para prevenir un aumento de la presión. Evite tocar la parte final abierta de la jeringa o el tapón de protección azul de ventilación.
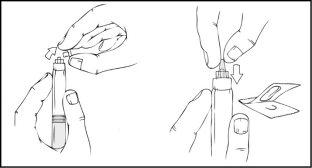
- Empuje el émbolo lenta y cuidadosamentehasta que los dos émbolos de la jeringa precargada choquen, y todo el disolvente sea transferido a la cámara superior que contiene el polvo de ReFacto AF.
Nota: Para prevenir la fuga de fluido de la punta de la jeringa, no empuje el émbolo con excesiva fuerza.
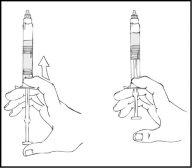
- Con la jeringa precargada de ReFacto AF en posición vertical, agítela cuidadosamentevarias veces hasta que el polvo se disuelva.
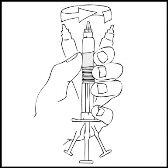
Inspeccione visualmente la solución final en cuanto a la presencia de partículas o decoloración. La solución debe tener un aspecto de transparente a ligeramente opalescente y será incolora. Deseche la jeringa precargada si se observan partículas o decoloración.
- Continuando con la jeringa precargada de ReFacto AF en posición vertical, avance el émbolo hasta que prácticamente se haya eliminado, pero no todo, el aire de la cámara (superior).
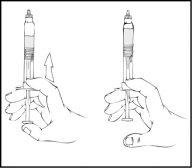
ReFacto AF debe utilizarse en las 3 horas siguientes a su reconstitución o eliminación del tapón gris de la jeringa precargada.
Si no va a utilizar la solución de ReFacto AF inmediatamente, debe guardar la jeringa en posición vertical, con el tapón azul de protección para ventilación en la jeringa precargada hasta que esté listo para la perfusión. La solución reconstituida se puede conservar a temperatura ambiente hasta 3 horas. Si no la ha utilizado en 3 horas, tírela.
Administración (Perfusión intravenosa)
Su médico u otro profesional sanitario le enseñará a realizar la perfusión de ReFacto AF. Una vez que haya aprendido como realizar la auto-perfusión, usted podrá seguir las instrucciones incluidas en este prospecto.
ReFacto AF se administra mediante perfusión intravenosa (IV) después de la reconstitución del polvo con el disolvente (cloruro sódico 0,9%). Una vez reconstituido y antes de la administración, ReFacto AF debe ser inspeccionado visualmente en cuanto a la presencia de partículas o decoloración.
ReFacto AF se debe administrar utilizando el sistema de perfusión incluido en este kit, a no ser que su médico u otro profesional sanitario le haya dado otra recomendación.
- Retire el tapón de protección azul para la ventilación y acople firmemente el dispositivo de perfusión en la jeringa precargada de ReFacto AF.
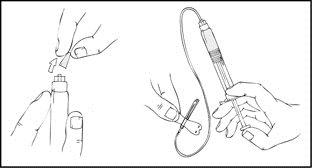
- Aplique un torniquete y prepare el sitio de inyección limpiando bien la piel con una de las toallitas con alcohol que se suministran.
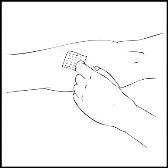
- Retire la tapa protectora de la aguja e inserte la aguja de mariposa del sistema de perfusión en la vena, siguiendo las instrucciones de su médico u otro profesional sanitario. Se debe inyectar por vía intravenosa el producto reconstituido en varios minutos. Su médico puede cambiarle la velocidad de perfusión recomendada para que sea más cómoda. Hable con su médico u otro profesional sanitario sobre el procedimiento de perfusión. No realice auto-perfusión a no ser que esté entrenado debidamente.
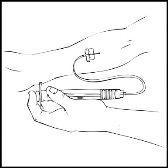
ReFacto AF reconstituido no debe ser administrado en el mismo tubo o envase con otros medicamentos.
- Después de la perfusión de ReFacto AF, retire el sistema de perfusión y deséchelo. La cantidad de medicamento que queda en el sistema de perfusión no afecta a su tratamiento.
Nota: Deseche la solución no utilizada, la jeringa precargada vacía y los materiales médicos utilizados en un recipiente adecuado para eliminar desechos médicos, ya que estos materiales pueden dañar a otros si no se eliminan adecuadamente.
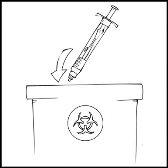
Se recomienda anotar el número de lote que se encuentra en la etiqueta de la jeringa precargada de ReFacto AF cada vez que utilice ReFacto AF. Puede utilizar la etiqueta despegable de la jeringa precargada de ReFacto AF para registrar el número de lote.
Instrucciones adicionales:
Reconstitución múltiple de ReFacto AF en jeringa precargada a una jeringa de 10cc o una jeringa más grande con cierre luer (las jeringas de 10cc o con cierre luer no se proporcionan en el kit).
Las siguientes instrucciones son para el uso de múltiples kits de ReFacto AF en jeringa precargada con una jeringa de 10cc o una jeringa más grande con cierre luer.
- Reconstituya todas las jeringas precargadas de ReFacto AF siguiendo las instrucciones que se muestran más arriba (ver Reconstitución y Administración).
Sujete la jeringa precargada de ReFacto AF en posición vertical, lentamente empuje el émbolo hasta que casi, pero no todo, el aire haya salido de la cámara donde se encuentra el producto.
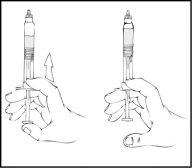
- Retire el conector de la jeringa luer-to-luer del envase (los conectores de jeringa luer-to-luer no están incluidos).
- Conecte una jeringa estéril de 10 cc o una jeringa más grande de cierre luer con el puerto abierto del conector de la jeringa y la jeringa precargada de ReFacto AF con el puerto abierto restante del lado opuesto.
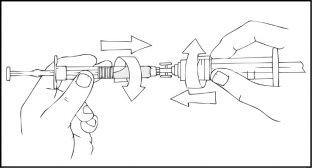
- Con la jeringa precargada de ReFacto AF en la parte de arriba, empuje lentamente el émbolo hasta que el contenido se vacíe dentro de la jeringa de 10 cc o una jeringa más grande de cierre tipo luer.
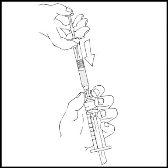
- Retire la jeringa precargada de ReFacto AF y repita los procedimientos 3 y 4 para reconstituciones adicionales de jeringas.
- Retire el conector de jeringa luer-to-luer de la jeringa de 10 cc o de la jeringa más grande de cierre luer y conecte el sistema de perfusión, según se describe más arriba en las instrucciones para la administración de la jeringa precargada [ver Administración (Perfusión intravenosa)].
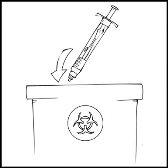
Nota: Deseche la solución no utilizada, la jeringa precargada vacía y los materiales médicos utilizados en un recipiente adecuado para eliminar desechos médicos, ya que estos materiales pueden dañar a otros si no se eliminan adecuadamente.
Si usa más ReFacto AF del que debe
Consulte a su médico o farmacéutico.
Si interrumpe el tratamiento con ReFacto AF
No deje de utilizar ReFacto AF sin consultar con su médico.
Si tiene cualquier otra duda sobre el uso de este medicamento, pregunte a su médico o farmacéutico.
4. Posibles efectos adversos
Al igual que todos los medicamentos, este medicamento puede producir efectos adversos, aunque no todas las personas los sufran.
Reacciones alérgicas
Si aparecen reacciones alérgicas(anafilácticas) súbitas, graves, debe detenerse inmediatamentela infusión. Debe consultar a su médico inmediatamentesi usted presenta alguno de los siguientes síntomas tempranos de reacciones alérgicas:
- erupción, habón urticarial, ronchas, picor generalizado
- hinchazón de labios y lengua
- dificultad para respirar, silbidos al respirar, opresión en el pecho
- sensación general de malestar
- mareo y pérdida de consciencia
Los síntomas graves, como la dificultad para respirar y el desmayo (o el casi desmayo), precisan de un rápido tratamiento de emergencia. Las reacciones alérgicas (anafilácticas) súbitas, graves son poco frecuentes (pueden afectar hasta 1 de cada 100 pacientes)
Desarrollo de inhibidores
En los niños que no han recibido tratamiento previo con medicamentos compuestos por factor VIII, pueden producirse anticuerpos inhibidores (ver sección 2) muy frecuentemente (más de 1 de cada 10 pacientes); sin embargo, en los pacientes que han recibido tratamiento previo con factor VIII (más de 150 días de tratamiento), el riesgo es poco frecuente (menos de 1 de cada 100 pacientes). Si esto sucede, los medicamentos que toman usted o su hijo pueden dejar de funcionar correctamente y usted o su hijo pueden sufrir una hemorragia persistente. En ese caso, contacte con su médico inmediatamente.
Efectos adversos muy frecuentes(pueden afectar a más de 1 de cada 10 pacientes)
- desarrollo de inhibidores en pacientes que nunca habían sido tratados previamente con productos de factor VIII
- dolor de cabeza
- tos
- dolor articular
- fiebre
Efectos adversos frecuentes(pueden afectar hasta 1 de cada 10 pacientes)
- hemorragia
- mareo
- pérdida del apetito, diarrea, vómitos, dolor de estómago, náuseas
- urticaria, erupción cutánea, picor
- dolor muscular
- escalofríos, reacción relacionada con la localización del catéter
- algunos análisis de sangre pueden mostrar un incremento de anticuerpos contra el factor VIII
Efectos adversos poco frecuentes(pueden afectar hasta 1 de cada 100 pacientes)
- desarrollo de inhibidores en paciente que habían sido tratados previamente con productos de factor VIII (menos de 1 de cada 100 pacientes)
- reacción alérgica grave
- entumecimiento, somnolencia, alteración del gusto
- dolor en el pecho, latidos cardíacos rápidos, palpitaciones
- presión arterial baja, dolor y enrojecimiento de las venas relacionado con la presencia de coágulos de sangre, rubefacción
- dificultad para respirar
- sudoración excesiva
- debilidad, reacción en el lugar de la inyección (incluido el dolor)
- ligero aumento de las enzimas cardiacas
- aumento de las enzimas hepáticas, aumento de la bilirrubina
Comunicación de efectos adversos
Si experimenta cualquier tipo de efecto adverso, consulte a su médico o farmacéutico, incluso si se trata de posibles efectos adversos que no aparecen en este prospecto. También puede comunicarlos directamente a través del sistema nacional de notificación incluido en el Apéndice V. Mediante la comunicación de efectos adversos usted puede contribuir a proporcionar más información sobre la seguridad de este medicamento.
5. Conservación de ReFacto AF
Mantener este medicamento fuera de la vista y del alcance de los niños.
No utilice este medicamento después de la fecha de caducidad que aparece en el envase exterior y en la etiqueta de la jeringa precargada después de CAD. La fecha de caducidad es el último día del mes que se indica.
Conservar y transportar refrigerado (entre 2°C y 8°C). No congelar para evitar que se dañe la jeringa precargada.
Para su comodidad, el medicamento se puede retirar de dicho almacenamiento y conservar a temperatura ambiente (hasta 25ºC) durante un único período de 3 meses como máximo. Al final de este periodo de almacenamiento a temperatura ambiente el producto no debe volver a refrigerarse, sino debe ser utilizado o desechado. Anote en el envase exterior la fecha en la que se retira ReFacto AF en jeringa precargada de la nevera y se pone a temperatura ambiente (hasta 25ºC). Mantenga la jeringa precargada dentro del envase exterior para protegerlo de la luz.
El producto reconstituido debe utilizarse en las 3 horas siguientes a la reconstitución o eliminación del tapón gris.
La solución será de clara a ligeramente opalescente e incolora. No utilizar este medicamento si aprecia que es turbia o contiene partículas visibles.
Los medicamentos no se deben tirar por los desagües ni a la basura. Pregunte a su farmacéutico cómo deshacerse de los envases y de los medicamentos que no necesita. De esta forma, ayudará a proteger el medio ambiente.
6. Contenido del envase e información adicional
Composición de ReFacto AF
- El principio activo es moroctocog alfa (factor VIII de coagulación recombinante). Cada jeringa precargada de ReFacto AF contiene nominalmente 250, 500, 1000, 2000 o 3000 UI de moroctocog alfa.
Para la reconstitución de moroctocog alfa, se incluye un disolvente [solución inyectable de cloruro sódico de 9 mg/ml (0,9%)] en la jeringa precargada de ReFacto AF.
- Los demás componentes son sacarosa, dihidrato de cloruro cálcico, L-histidina, polisorbato 80 y cloruro sódico (ver sección 2 “ReFacto AF contiene sodio”).
- Después de la reconstitución con el disolvente [solución de cloruro sódico de 9 mg/ml (0,9%)], la solución para inyección preparada contiene 62,5, 125, 250, 500 o 750 UI de moroctocog alfa por ml, respectivamente (según la potencia de moroctocog alfa, es decir, 250, 500, 1000, 2000 o 3000 UI).
Aspecto del producto y contenido del envase
ReFacto AF es una jeringa precargada con polvo y disolvente para solución inyectable que contiene el polvo de ReFacto AF en la cámara superior y el disolvente [solución inyectable de cloruro sódico de 9 mg/ml (0,9%)] en la cámara inferior.
El contenido del envase es:
- una jeringa precargada contiene 250, 500, 1000, 2000 o 3000 UI de polvo de moroctocog alfa y 4 ml de disolvente estéril de cloruro sódico 9 mg/ml (0,9%) solución para inyección para la reconstitución
- un émbolo
- un tapón protector estéril para la ventilación
- un sistema de perfusión estéril
- dos toallitas con alcohol
- esparadrapo
- una gasa
Titular de la autorización de comercialización
Pfizer Europe MA EEIG
Boulevard de la Plaine 17
1050 Bruxelles
Bélgica
Responsable de la fabricación
Wyeth Farma, S.A.
Autovía del Norte A-1 Km 23
Desvío Algete Km 1
28700 San Sebastián de los Reyes
Madrid
España
Pueden solicitar más información respecto a este medicamento dirigiéndose al representante local del titular de la autorización de comercialización.
België/Belgique/Belgien Luxembourg/Luxemburg Pfizer NV/SA Tél/Tel: +32 (0)2 554 62 11 | Lietuva Pfizer Luxembourg SARL filialas Lietuvoje Tel: +370 5 251 4000 |
???????? ??????? ?????????? ????, ???? ???????? ???.: +359 2 970 4333 | Magyarország Pfizer Kft. Tel.: + 36 1 488 37 00 |
Ceská republika Pfizer, spol. s r.o. Tel: +420 283 004 111 | Malta Vivian Corporation Ltd. Tel: +356 21344610 |
Danmark Pfizer ApS Tlf.: +45 44 20 11 00 | Nederland Pfizer bv Tel: +31 (0)800 63 34 636 |
Deutschland PFIZER PHARMA GmbH Tel: +49 (0)30 550055-51000 | Norge Pfizer AS Tlf: +47 67 52 61 00 |
Eesti Pfizer Luxembourg SARL Eesti filiaal Tel: +372 666 7500 | Österreich Pfizer Corporation Austria Ges.m.b.H. Tel: +43 (0)1 521 15-0 |
Ελλ?δα Pfizer Ελλ?ς Α.Ε Τηλ: +30 210 6785800 | Polska Pfizer Polska Sp. z o.o. Tel.: +48 22 335 61 00 |
España Pfizer S.L. Tel: +34 91 490 99 00 | Portugal Laboratórios Pfizer, Lda. Tel: +351 21 423 5500 |
France Pfizer Tél: +33 (0)1 58 07 34 40 | România Pfizer Romania S.R.L. Tel: +40 (0) 21 207 28 00 |
Hrvatska Pfizer Croatia d.o.o. Tel: + 385 1 3908 777 | Slovenija Pfizer Luxembourg SARL Pfizer, podružnica za svetovanje s podrocja farmacevtske dejavnosti, Ljubljana Tel: + 386 (0) 1 52 11 400 |
Ireland Pfizer Healthcare Ireland Unlimited Company Tel: 1800 633 363 (toll free) Tel: +44 (0)1304 616161 | Slovenská republika Pfizer Luxembourg SARL, organizacná zložka Tel: + 421 2 3355 5500 |
Ísland Icepharma hf. Sími: +354 540 8000 | Suomi/Finland Pfizer Oy Puh/Tel: +358 (0)9 430 040 |
Italia Pfizer S.r.l. Tel: +39 06 33 18 21 | Sverige Pfizer AB Tel: + 46 (0)8 550 520 00 |
Κ?προς Pfizer Ελλ?ς Α.Ε. (Cyprus Branch) Τηλ: +357 22817690 | |
Latvija Pfizer Luxembourg SARL filiale Latvija Tel: +371 670 35 775 |
Fecha de la última revisión de este prospecto: 02/2025.
La información detallada de este medicamento está disponible en la página web de la Agencia Europea de Medicamentos: https://www.ema.europa.eu.
- País de registro
- Principio activo
- Requiere recetaSí
- Fabricante
- Esta información es de carácter general y no sustituye la consulta con un profesional sanitario.
- Alternativas a REFACTO AF 1000 UI POLVO Y DISOLVENTE PARA SOLUCION INYECTABLE EN JERINGA PRECARGADAForma farmacéutica: INYECTABLE, 1.000 UIPrincipio activo: factor de coagulación VIIIFabricante: Takeda Manufacturing Austria AgRequiere recetaForma farmacéutica: INYECTABLE, 1.500 UIPrincipio activo: factor de coagulación VIIIFabricante: Takeda Manufacturing Austria AgRequiere recetaForma farmacéutica: INYECTABLE, 1000 UI - tras reconstitución en 2 ml de agua para inyectables la dosis es de 500 UI/mlPrincipio activo: factor de coagulación VIIIFabricante: Takeda Manufacturing Austria AgRequiere receta
Médicos online para REFACTO AF 1000 UI POLVO Y DISOLVENTE PARA SOLUCION INYECTABLE EN JERINGA PRECARGADA
Comenta la dosis, los posibles efectos secundarios, interacciones, contraindicaciones o la revisión de receta de REFACTO AF 1000 UI POLVO Y DISOLVENTE PARA SOLUCION INYECTABLE EN JERINGA PRECARGADA, sujeto a valoración médica y a la normativa local.
Preguntas frecuentes















